Presente e futuro della terapia di supporto in



































































- Slides: 94

Presente e futuro della terapia di supporto in oncologia Roma 22 -23 giugno 2006 La malattia metastatica ossea: la radioterapia Prof. R. Maurizi Enrici Cattedra di Radioterapia Università “La Sapienza”-Roma

“Dimensioni” del problema alcune premessse… Ottimizzazione terapie oncologiche Aumento aspettativa di vita Incremento tempi di sopravvivenza Aumento incidenza metastasi L’osso è una delle più frequenti sedi di metastatizzazione

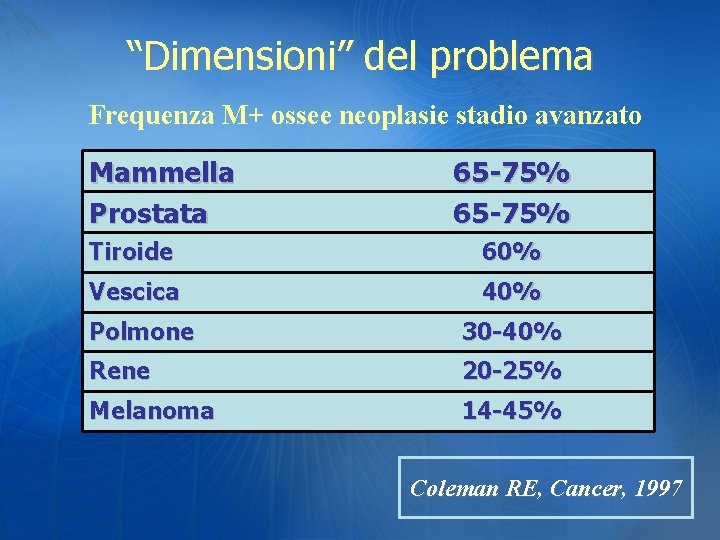
“Dimensioni” del problema Frequenza M+ ossee neoplasie stadio avanzato Mammella Prostata 65 -75% Tiroide 60% Vescica 40% Polmone 30 -40% Rene 20 -25% Melanoma 14 -45% Coleman RE, Cancer, 1997

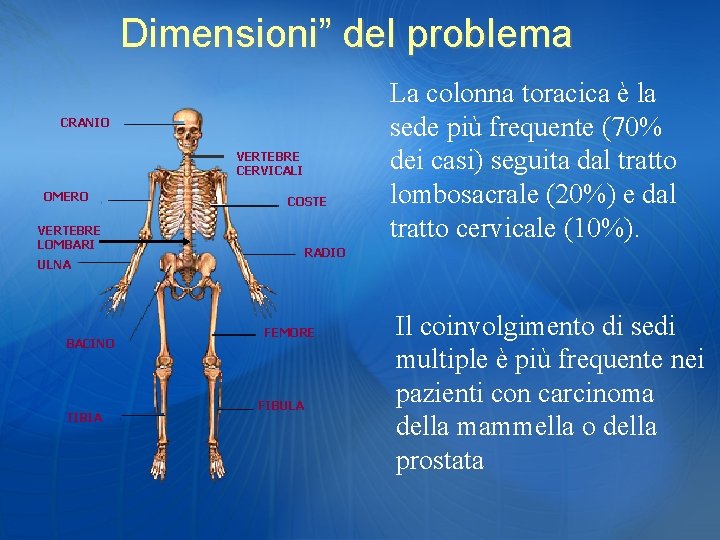
Dimensioni” del problema CRANIO VERTEBRE CERVICALI OMERO COSTE VERTEBRE LOMBARI RADIO ULNA BACINO TIBIA La colonna toracica è la sede più frequente (70% dei casi) seguita dal tratto lombosacrale (20%) e dal tratto cervicale (10%). FEMORE FIBULA Il coinvolgimento di sedi multiple è più frequente nei pazienti con carcinoma della mammella o della prostata

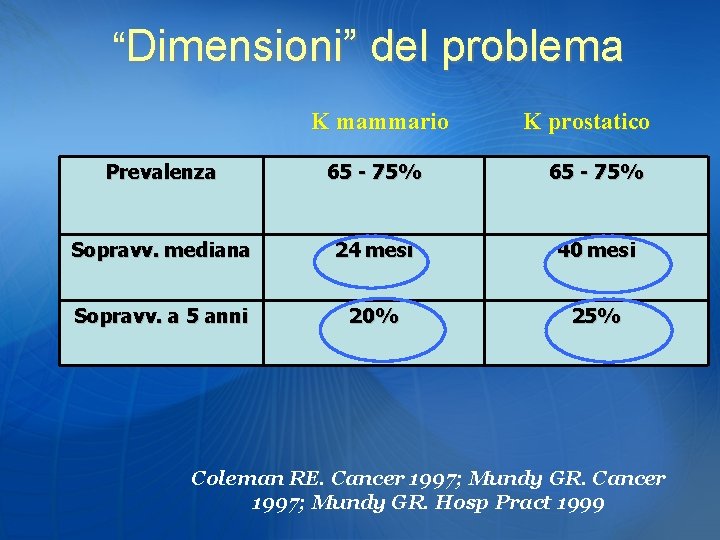
“Dimensioni” del problema K mammario K prostatico Prevalenza 65 - 75% Sopravv. mediana 24 mesi 40 mesi Sopravv. a 5 anni 20% 25% Coleman RE. Cancer 1997; Mundy GR. Hosp Pract 1999

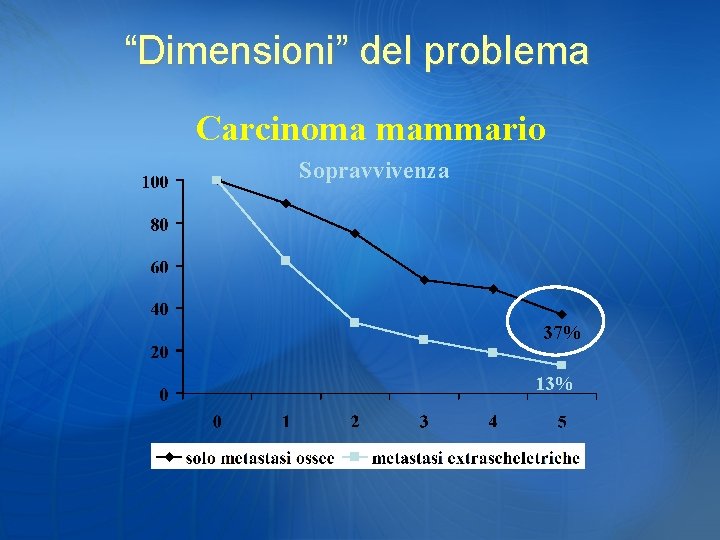
“Dimensioni” del problema Carcinoma mammario Sopravvivenza 37% 13%

“Dimensioni” del problema CENSIMENTO A. I. R. O. 2000 • • 21 Centri di Radioterapia Pazienti trattati 20818 Trattamenti palliativi 6088 (29%) RT metastasi ossee 3386 16% pazienti trattati palliativi 55% trattamenti

“Dimensioni” del problema Questi pazienti possono vivere per molti anni dopo l’esordio della metastasi, per questo è importante la strategia terapeutica da adottare al fine di ridurre le complicanze

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

Dolore osseo

Il dolore è il sintomo più comune della metastasi ossea ed è di solito il primo sintomo avvertito dai pazienti. Inizialmente di tipo transitorio, in seguito tende a peggiorare con esacerbazioni notturne o durante il riposo

Il dolore ü Il dolore osseo è presente nel 28 -45% dei pazienti affetti da cancro e nel 70% di quelli con malattia in fase avanzata. ü La presenza di dolore non è correlata con il tipo di tumore, la sede, il numero e l’entità delle metastasi, il sesso e l’età dei pazienti

Il dolore Caratteristica del dolore vertebrale: ü Presenza di un dolore locale, sordo e continuo aggravato dal movimento ü Dolore muscolare riflesso ü Dolore riferito agli arti

Il dolore di tipo radicolare si sviluppa tardivamente. Quello che origina dalle radici toraciche è spesso bilaterale e viene descritto dai pazienti come una costrizione di tipo acuto irradiata a cintura attorno al torace e all’addome.

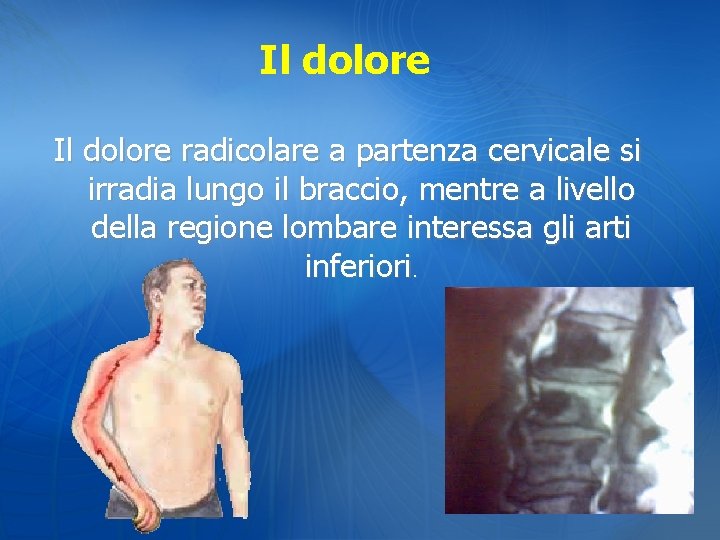
Il dolore radicolare a partenza cervicale si irradia lungo il braccio, mentre a livello della regione lombare interessa gli arti inferiori.

Il dolore A prescindere dalla componente organica, che determina limitazione della mobilità e della autonomia, il dolore cronico è caratterizzato da una forte componente psicologica che porta alla depressione

Il dolore ha un notevole impatto psico-sociale in quanto: ü rendendolo dipendente, priva il paziente della propria autonomia, dignità e del proprio ruolo all’interno del nucleo familiare ü può determinare un danno economico personale, per l’impossibilità a lavorare ü rappresenta un costo per la società per i ripetuti accessi ospedalieri

Il dolore Adeguato trattamento analgesico Buon controllo del dolore

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

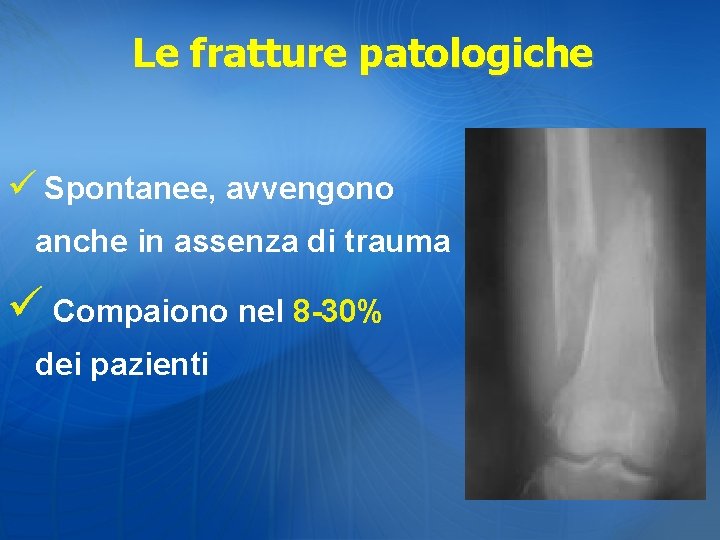
Le fratture patologiche ü Spontanee, avvengono anche in assenza di trauma ü Compaiono nel 8 -30% dei pazienti

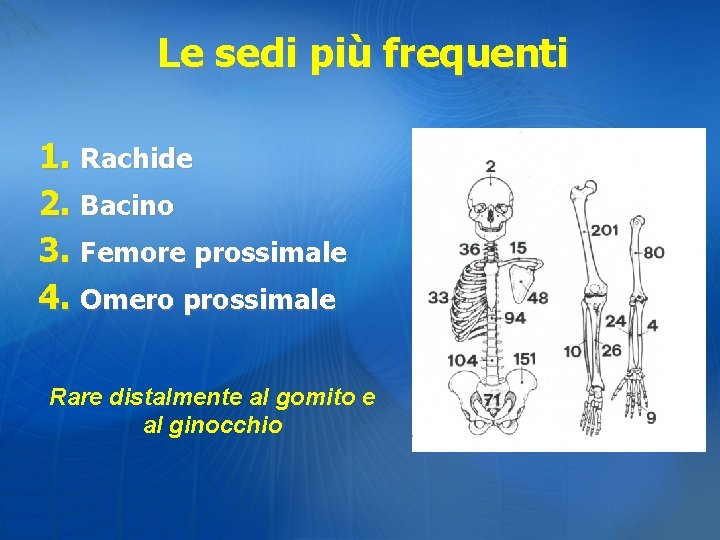
Le sedi più frequenti 1. Rachide 2. Bacino 3. Femore prossimale 4. Omero prossimale Rare distalmente al gomito e al ginocchio

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

COMPRESSIONE MIDOLLARE

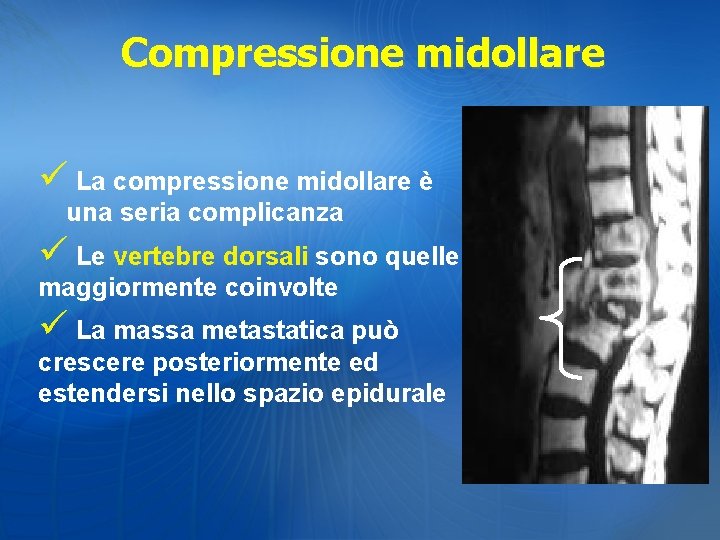
Compressione midollare ü La compressione midollare è una seria complicanza ü Le vertebre dorsali sono quelle maggiormente coinvolte ü La massa metastatica può crescere posteriormente ed estendersi nello spazio epidurale

Compressione midollare ü La pressione trasmessa al midollo induce un danno meccanico, ischemia e stasi venosa e la compressione determina un progressivo deficit neurologico distalmente alla lesione ü L’esordio è subdolo con vaghi dolori, debolezza agli arti e parestesie

Compressione midollare ü A quadro conclamato possono comparire disturbi sfinterici, perdita della sensibilità, sino a paraplegia e tetraplegia ü L’esordio può essere: - Acuto (<48 ore) nel 22% dei casi - Nel 61% dei casi progredisce in 7 -10 giorni verso la paraplegia o tetraplegia - Nell’ 11% dei casi ha un andamento insidioso con durata sino ad 1 mese

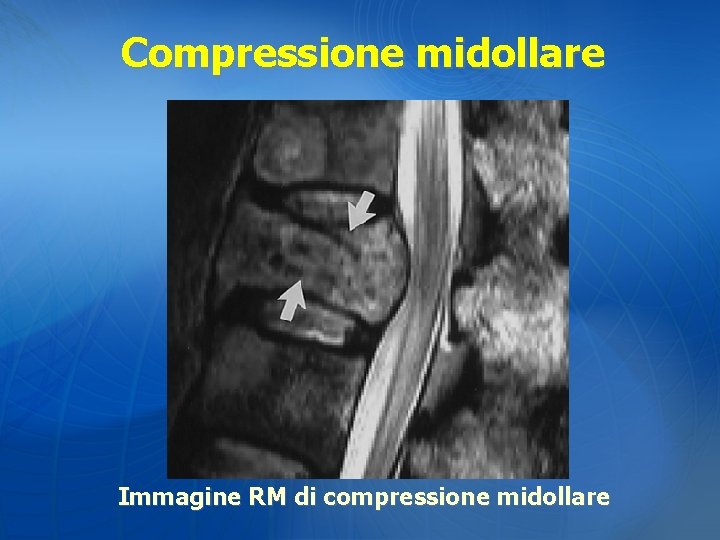
Compressione midollare Immagine RM di compressione midollare

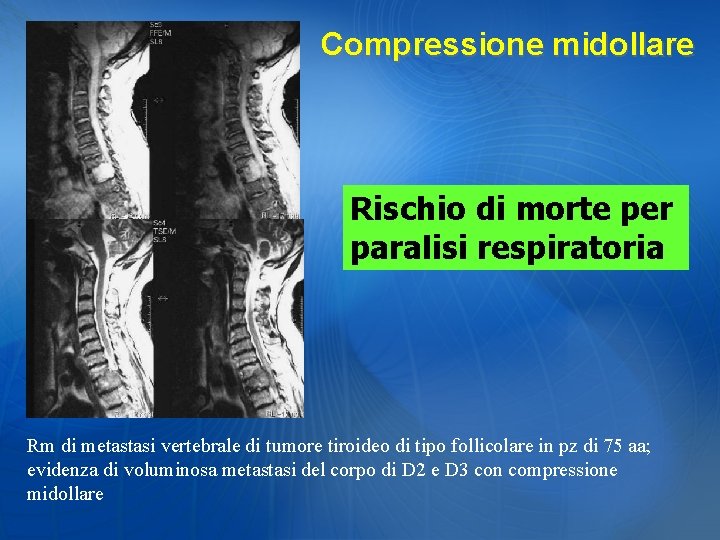
Compressione midollare Rischio di morte per paralisi respiratoria Rm di metastasi vertebrale di tumore tiroideo di tipo follicolare in pz di 75 aa; evidenza di voluminosa metastasi del corpo di D 2 e D 3 con compressione midollare

Compressione midollare La diagnosi deve essere il più TEMPESTIVA possibile per evitare danni irreversibili

Compressione midollare La diagnosi deve essere il più TEMPESTIVA possibile per evitare danni irreversibili Emergenza oncologica

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

La infiltrazione midollare ü In caso di massivo coinvolgimento osseo, con invasione midollare, possono manifestarsi piastrinopenia, anemia e neutropenia ü Sono più frequenti nel carcinoma della mammella, prostata, polmone, surrene, tiroide e rene

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

Le cause dell’ipercalcemia ü In piccola parte è causata dal riassorbimento del calcio dall’osso per azione litica diretta delle cellule metastatiche ü Per la maggior parte dei casi è mediata dai fattori attivanti gli osteoclasti (in primis il paratormone) da parte delle cellule neoplastiche ü La gravità dipende più dalla velocità di aumento del calcio ionizzato che dal suo grado di elevazione

Ipercalcemia üSi manifesta nel 20 - 30 % dei pazienti ü È associata ad una cattiva prognosi ü Talvolta non è correlata alla presenza di metastasi ossee Stewart AF, “Hypercalcemia Associated with Cancer”, N Engl J Med 352; 4, 2005

I sintomi dell’ipercalcemia Generali Disidratazione, perdita di peso, anoressia, prurito, polidipsia Neuromuscolari Affaticabilità, letargia, debolezza muscolare, iporeflessia, stato confusionale, psicosi, convulsioni, coma Gastrointestinali Nausea, vomito, stipsi, ileo paralitico Renali Poliuria, insufficienza renale Cardiaci Bradicardia, allungamento dell’intervallo PR, accorciamento dell’intervallo QT, aritmie atriali o ventricolari

METASTASI OSSEE-COMPLICANZE Qualità di vita • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia

METASTASI OSSEE-COMPLICANZE Qualità di vita QUALITA’ • • Dolore osseo severo Impotenza funzionale Fratture patologiche Compressione midollo spinale o radici nervose • Alterazione ematopoiesi da infiltrazione midollo osseo • Ipercalcemia DI VITA

La “Qualità di vita” Con il termine "qualità d. I vita” ci si riferisce ad un complesso di stati oggettivi e di percezioni soggettive della salute, che sono pertinenti al dominio fisico, psicologico e sociale (inteso come attività di vita quotidiana) di ciascuno

Gli strumenti più usati ü Questionari a risposta multipla autocompilativi ü Strumenti specifici - per malattia (FLIC, EORTC, FACT) - per organo o trattamento (moduli EORTC e FACT) - batterie di sintomi (RSCL, LCSS) FLIC = Functional Living Index-Cancer FACT = Functional Assessment of Cancer Therapy RSCL = Rotterdam Symptoms Checklist LCSS = Lung Cancer Symptom Scale

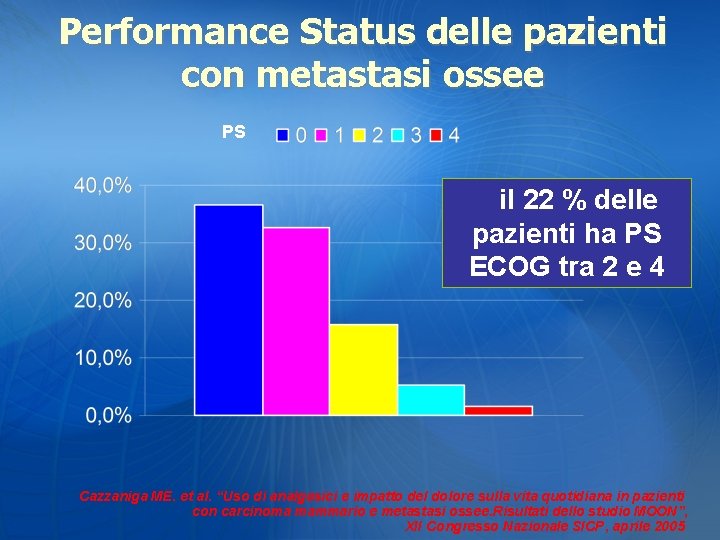
Performance Status delle pazienti con metastasi ossee PS ~ il 22 % delle pazienti ha PS ECOG tra 2 e 4 Cazzaniga ME. et al. “Uso di analgesici e impatto del dolore sulla vita quotidiana in pazienti con carcinoma mammario e metastasi ossee. Risultati dello studio MOON”, XII Congresso Nazionale SICP, aprile 2005

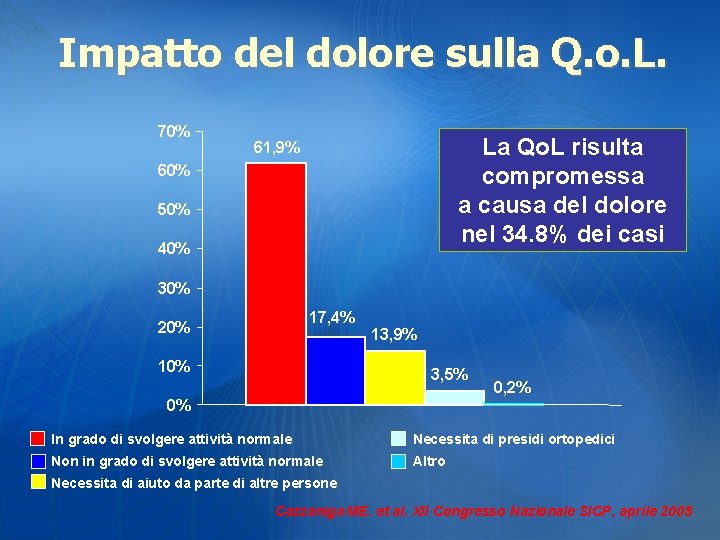
Impatto del dolore sulla Q. o. L. 70% La Qo. L risulta compromessa a causa del dolore nel 34. 8% dei casi 61, 9% 60% 50% 40% 30% 17, 4% 20% 13, 9% 3, 5% 0% 0, 2% In grado di svolgere attività normale Necessita di presidi ortopedici Non in grado di svolgere attività normale Altro Necessita di aiuto da parte di altre persone Cazzaniga ME. et al. XII Congresso Nazionale SICP, aprile 2005

Quality of Life and pain among prostate cancer patients with bone metastases 264 pazienti ü Età mediana 76 anni ü 48% con M+ ossee ü Valutazione - Qo. L (questionari SF-8 e FACT-P) - Dolore - Eventi scheletrici Kurth H. et al. , Abstract 4747, ASCO 2005

I pazienti affetti da M+ ossee presentavano ü Peggiore qualità di vita sia valutata con il SF-8 (p<0. 05) che il FAC-P (p<0. 05) ü Maggiore incidenza di dolore (50% vs 29%; p<0. 001). Kurth H. et al. , Abstract 4747, ASCO 2005

Bisphonates for breast cancer (Cochrane Review) Sono stati identificati 117 reports (papers o abstract) che avevano come end-point primario eventi scheletrici, dolore, qualità di vita e sopravvivenza. Dopo la prima analisi, 37 sono stati valutati in dettaglio e 19 studi randomizzati inclusi nella review. Pavlakis N et al. , The Cochrane Library, Issue 2, 2005

Le conclusioni degli autori L’utilizzo di bifosfonati (ev o per os): l il rischio di eventi scheletrici l l’incidenza di eventi scheletrici l il tempo alla comparsa di eventi scheletrici l il dolore nelle donne con M+ ossee evidenti Pavlakis N et al. , The Cochrane Library, Issue 2, 2005

Radioterapia con fasci esterni INDICAZIONI • Trattamento sintomatico dolore • Prevenzione e terapia fratture patologiche • Sindrome da compressione midollare

Radioterapia con fasci esterni INDICAZIONI La radioterapia è un trattamento eccellente per il dolore osseo da metastasi isolate o multiple con una risposta parziale nell’ 80 -90% dei pazienti, e risposta completa nel 50%.

Radioterapia - Meccanismo d’azione ü Effetto citocida sulle cellule neoplastiche con riduzione dei fenomeni meccanici e biologici coinvolti nel danno osseo ü Apoptosi delle cellule normali radiosensibili con inibizione dei mediatori chimici e riduzione della stimolazione degli osteoclasti

Radioterapia-Obiettivi • Controllo dolore • Diminuzione assunzione analgesici • Controllo progressione malattia

Radioterapia-Obiettivi Un approccio terapeutico di tipo sintomatico deve essere volto a: ü Prevenire l’insorgenza di fratture patologiche ü Migliorare la mobilità e le funzioni del movimento fisico del paziente ü Mantenere un accettabile livello di qualità della vita ü Prolungare la sopravvivenza (quando possibile)

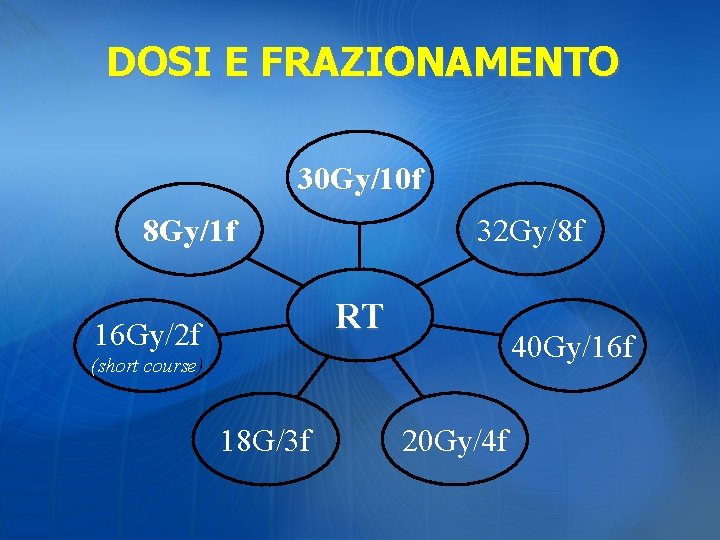
DOSI E FRAZIONAMENTO Il problema più dibattuto, in ambito radioterapico, riguarda la scelta della dose totale e del frazionamento.

DOSI E FRAZIONAMENTO 30 Gy/10 f 32 Gy/8 f 8 Gy/1 f RT 16 Gy/2 f 40 Gy/16 f (short course) 18 G/3 f 20 Gy/4 f

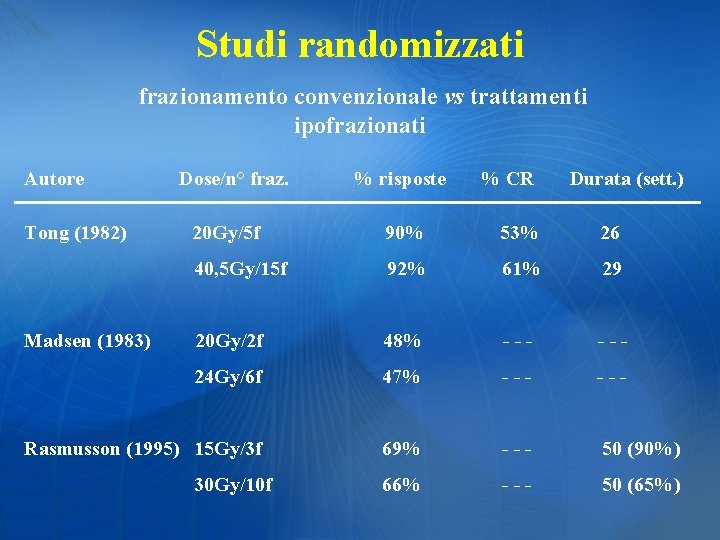
Studi randomizzati frazionamento convenzionale vs trattamenti ipofrazionati Autore Tong (1982) Dose/n° fraz. % risposte % CR Durata (sett. ) 20 Gy/5 f 90% 53% 26 40, 5 Gy/15 f 92% 61% 29 20 Gy/2 f 48% --- 24 Gy/6 f 47% --- Rasmusson (1995) 15 Gy/3 f 69% --- 50 (90%) 66% --- 50 (65%) Madsen (1983) 30 Gy/10 f

Dutch Bone Metastasis Study (1999) 8 Gy/1 f vs 24 Gy/6 f (1171 pazienti) 8 Gy/1 f 24 Gy/6 f Risposta 64% 60% Risposta completa 37% 33% Durata risposta 20 settimane 24 settimane Ritrattamento 25% 7% 4% 2% Fratture

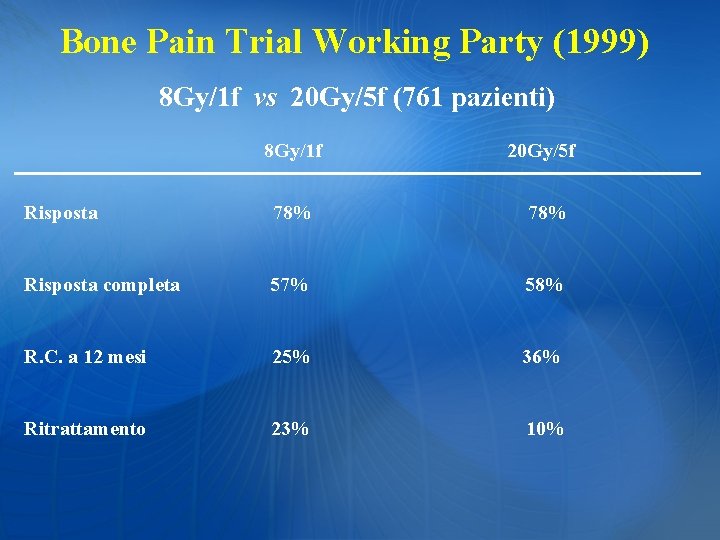
Bone Pain Trial Working Party (1999) 8 Gy/1 f vs 20 Gy/5 f (761 pazienti) 8 Gy/1 f 20 Gy/5 f Risposta 78% Risposta completa 57% 58% R. C. a 12 mesi 25% 36% Ritrattamento 23% 10%

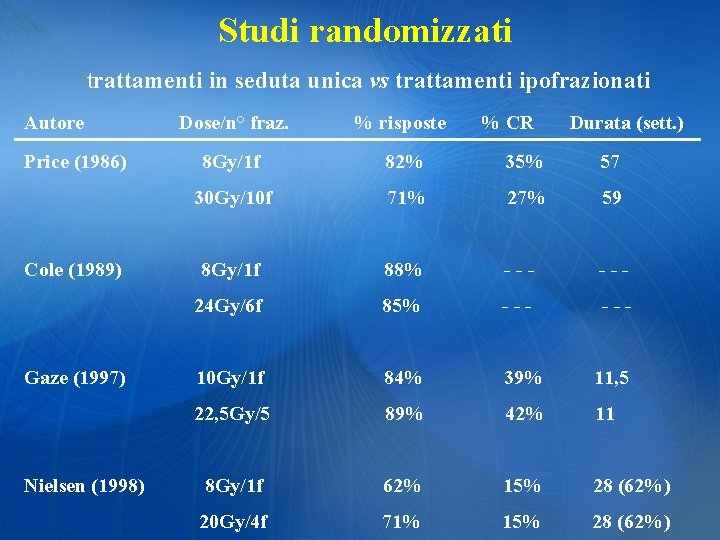
Studi randomizzati trattamenti in seduta unica vs trattamenti ipofrazionati Autore Price (1986) Cole (1989) Gaze (1997) Nielsen (1998) Dose/n° fraz. % risposte % CR Durata (sett. ) 8 Gy/1 f 82% 35% 57 30 Gy/10 f 71% 27% 59 8 Gy/1 f 88% --- 24 Gy/6 f 85% --- 10 Gy/1 f 84% 39% 11, 5 22, 5 Gy/5 89% 42% 11 8 Gy/1 f 62% 15% 28 (62%) 20 Gy/4 f 71% 15% 28 (62%)

RADIOTERAPIA-RISULTATI ü Effetto antalgico/palliativo 75% ü Picco risposta 12 -20 settimane ü Durata risposta 3 -12 mesi ü Ricalcificazione lesioni 25%

RADIOTERAPIA-RISULTATI • Controllo del dolore completo o parziale rispettivamente nel 30 -60% e 70 -80% dei casi (Mc. Quay HJ Clin Oncol 1997; Ratanatharathorn V Int J Radiant Oncol Biol Phis 1999; Saarto T Eur J Pain 2002) • Il controllo del dolore ottenuto già dai primi giorni di trattamento è legato ad una rapida riduzione di mediatori chimici del dolore (Poulsen HS Cancer Treatment Rev 1989; Mercadante S Pain 1997; Saarto T Eur J Pain 2002) • Il controllo del dolore che si ottiene da 2 a 8 settimane dalla fine del trattamento radioterapico coincide con l’inizio del processo di ricalcificazione delle lesioni osteolitiche (Poulsen HS Cancer Treatment Rev 1989; Saarto T Eur J Pain 2002)

RADIOTERAPIA-RISULTATI • Controllo del dolore completo o parziale rispettivamente nel 30 -60% e 70 -80% dei casi (Mc. Quay HJ Clin Oncol 1997; Ratanatharathorn V Int J Radiant Oncol Biol Phis 1999; Saarto T Eur J Pain 2002) • Il controllo del dolore ottenuto già dai primi giorni di trattamento è legato ad una rapida riduzione di mediatori chimici del dolore (Poulsen HS Cancer Treatment Rev 1989; Mercadante S Pain 1997; Saarto T Eur J Pain 2002) • Il controllo del dolore che si ottiene da 2 a 8 settimane dalla fine del trattamento radioterapico coincide con l’inizio del processo di ricalcificazione delle lesioni osteolitiche (Poulsen HS Cancer Treatment Rev 1989; Saarto T Eur J Pain 2002)

Radioterapia Frazionamenti Nonostante i molteplici studi proposti in passato sul frazionamento di dosi, il protocollo convenzionale adottato prevede la somministrazione di 30 Gy in 10 frazioni applicabili in 2 settimane. Pazienti collaboranti, in buone condizioni generali con aspettativa di vita lunga

Radioterapia Frazionamenti In alcune situazioni cliniche può essere opportuno utilizzare trattamenti più brevi che riducono i disagi per il paziente e i suoi familiari Pazienti non collaboranti, in cattive condizioni generali con aspettativa di vita breve

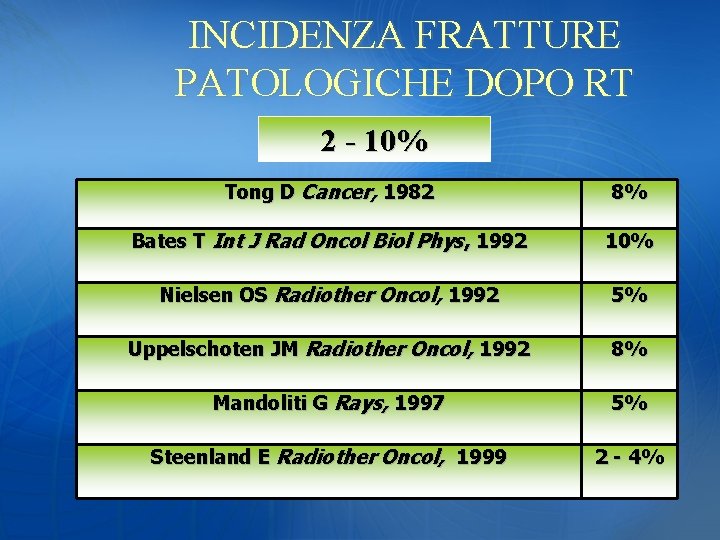
INCIDENZA FRATTURE PATOLOGICHE DOPO RT 2 - 10% Tong D Cancer, 1982 8% Bates T Int J Rad Oncol Biol Phys, 1992 10% Nielsen OS Radiother Oncol, 1992 5% Uppelschoten JM Radiother Oncol, 1992 8% Mandoliti G Rays, 1997 5% Steenland E Radiother Oncol, 1999 2 - 4%

COMPRESSIONE MIDOLLARE

• Compressione/infiltrazione neoplastica midollo spinale, radici nervose e/o cauda equina • 97% dei casi localizzazione extradurale EMERGENZA ONCOLOGICA • Corretta diagnosi dei sintomi precoci • Pronta terapia aggressiva Approccio diagnostico-terapeutico multidisciplinare

• DIAGNOSI PRECOCE • TRATTAMENTO IMMEDIATO Obiettivo • evitare la paraplegia (se presente da più di 24 ore, consente solo ridotte possibilità di recupero neurologico max 10 -13%)

• 85 -90% dei casi coinvolgimento colonna vertebrale • 70% lesioni osteolitiche • • • 10% rachide cervicale 70% rachide dorsale 20% rachide lombo-sacrale Byrne 1992, Siegal 1995, Nelson 2000

INCIDENZA • 20% dei pazienti con metastasi vertebrali presenta compressione midollare (Findlay 1987, Dumm 1980) • frequenza: mammella e polmone; linfoma, mieloma, prostata, sarcoma • U. S. A. 18. 000 - 20. 000 nuovi casi/anno (De Vita 1997) • RT-Perugia 60 pazienti/anno (5% intera casistica) • RT-Rovigo 19 pazienti nel 2004 (16% metastasi ossee)

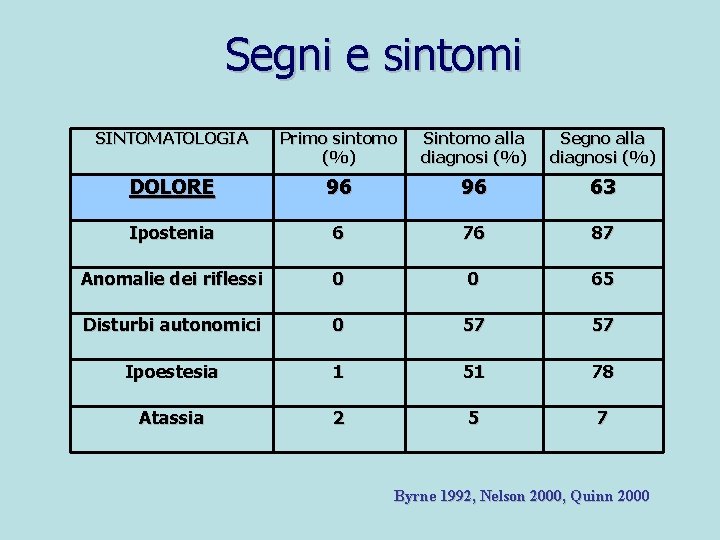
Segni e sintomi SINTOMATOLOGIA Primo sintomo (%) Sintomo alla diagnosi (%) Segno alla diagnosi (%) DOLORE 96 96 63 Ipostenia 6 76 87 Anomalie dei riflessi 0 0 65 Disturbi autonomici 0 57 57 Ipoestesia 1 51 78 Atassia 2 5 7 Byrne 1992, Nelson 2000, Quinn 2000

Fattori prognostici MAGGIORI Diagnosi e terapia precoci Minori Capacità motoria dopo la terapia Istologia Velocità di insorgenza del deficit neurologico • Radiosensibilità • Risposta agli steroidi • Condizioni generali del paziente • • • Katagiri 1998, Rades 1999, Solberg 1999, Rades 2000, Mc Donald 2000

Finalità del trattamento • Controllare il dolore • Preservare o ripristinare le capacità motorie e sfinteriche • Migliorare la qualità di vita • Aumentare la sopravvivenza

Iter terapeutico LINEE GUIDA Ø RADIOTERAPIA + DESAMETAZONE OPZIONE TERAPEUTICA STANDARD Ø CHIRURGIA + RADIOTERAPIA Dubbio diagnostico Instabilità del rachide Compressione da frammenti ossei Pregressa RT o progressione durante la RT

FRAZIONAMENTI “Split-course” 15 Gy/3 f split 4 gg 15 Gy/5 f Accelerato 30 Gy/10 f (3 Gy/seduta) “Short course” 8 Gy split 7 gg 8 Gy

STUDI MULTICENTRICI AIRO FRAZIONAMENTI • • • Accelerato (3 Gyx 10) Split-course (5 Gy x 3; 3 Gy x 5) Short-course (8 Gy x 2) • 275 pz accelerato e split-course (fase II) • 52 pz short-course (fase I-II) • 300 pz short-course vs split-course (fase III)

Radioterapia + Desametasone efficaci nella maggioranza dei casi (diagnosi precoce!) Il frazionamento breve della dose (short-course) efficace quanto il più protratto (split-course) senza tossicità aggiuntiva Chirurgia casi selezionati (5 -10%) laminectomia semplice trattamento inadeguato! (exeresi tumorale con approccio posteriore, anteriore e/o laterale + stabilizzazione del rachide).

RISULTATI • Effetto antalgico 62 -63% • Capacità motoria 71 -74% • Durata mediana risposta 4 mesi • Sopravvivenza mediana 4, 5 mesi • Tossicità grave: nessuna

FRATTURE PATOLOGICHE ü Incidenza 8 -30% ü Mammella, rene, polmone, tiroide 80% Indicazioni RT ü Consolidamento post-chirurgico con metodiche ipofrazionate (30 Gy/10 f) ü Casi non operabili frazioni singole di 8 Gy (ripetibili al momento della riesacerbazione dei sintomi)

Radioterapia Volumi di trattamento ü Local –field (LF): comporta la irradiazione della metastasi radiologicamente evidente e tessuto osseo circostante ü Wide-field (WFRT): comporta la irradiazione della metastasi radiologicamente evidenti e dei segmenti ossei limitrofi dove possono essere localizzate micrometastasi ü Half-Body radiation therapy(HBRT): Comporta la irradiazione di metà del corpo per la palliazione di metastasi osse diffuse

IRRADIAZIONE EMICORPOREA • Indicazioni Metastasi multiple polisintomatiche Frazione unica 6 -8 Gy • Efficacia Rapida palliazione (24 -48 ore) in più del 70% dei pz Completa risoluzione dei sintomi nel 20% • Tossicità acuta Nausea e vomito Manifestazioni pneumonitiche (emisoma superiore) Manifestazioni gastrointestinali (emisoma inferiore)

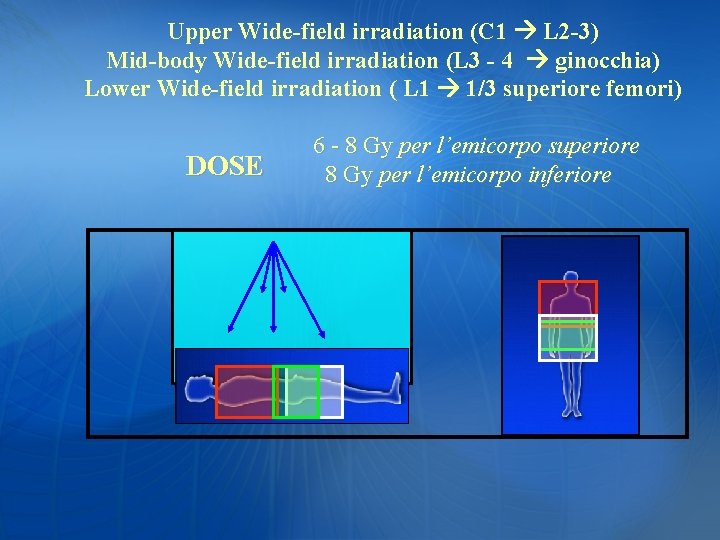
Upper Wide-field irradiation (C 1 L 2 -3) Mid-body Wide-field irradiation (L 3 - 4 ginocchia) Lower Wide-field irradiation ( L 1 1/3 superiore femori) DOSE 6 - 8 Gy per l’emicorpo superiore 8 Gy per l’emicorpo inferiore

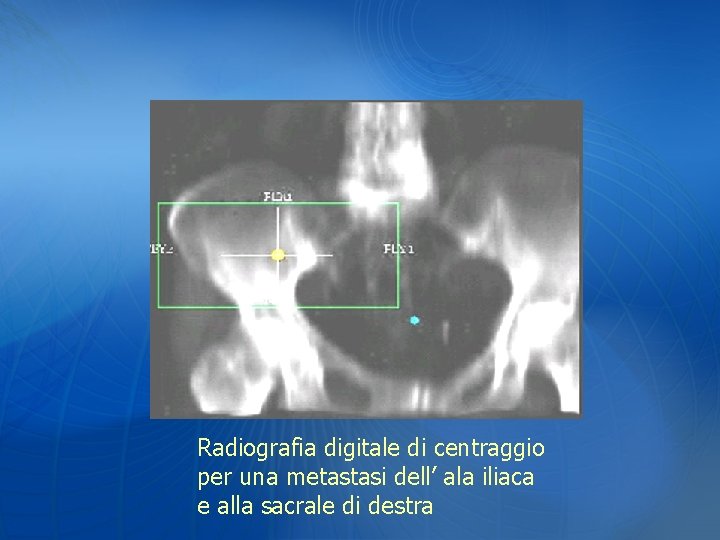
Radiografia digitale di centraggio per una metastasi dell’ ala iliaca e alla sacrale di destra

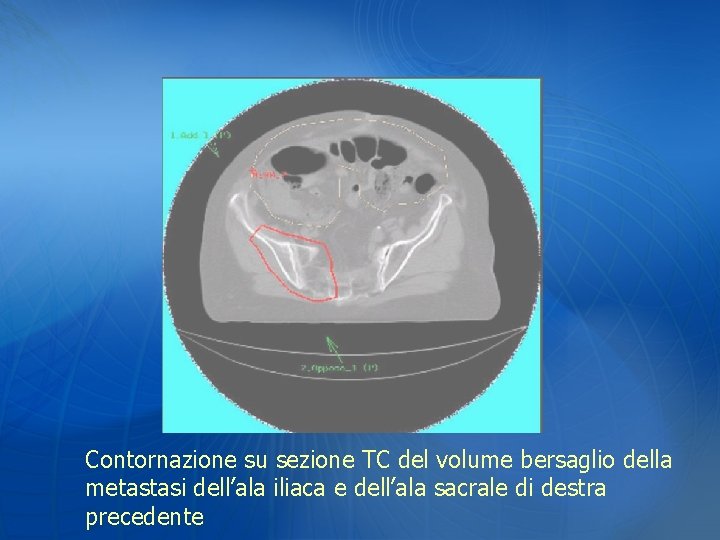
Contornazione su sezione TC del volume bersaglio della metastasi dell’ala iliaca e dell’ala sacrale di destra precedente

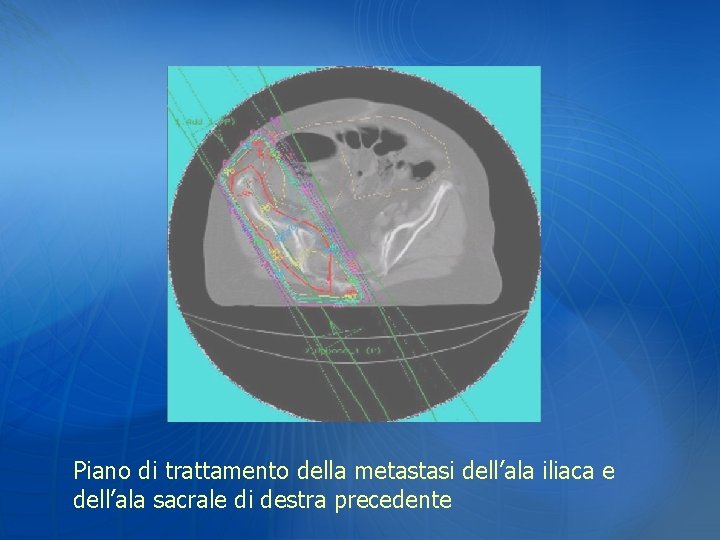
Piano di trattamento della metastasi dell’ala iliaca e dell’ala sacrale di destra precedente

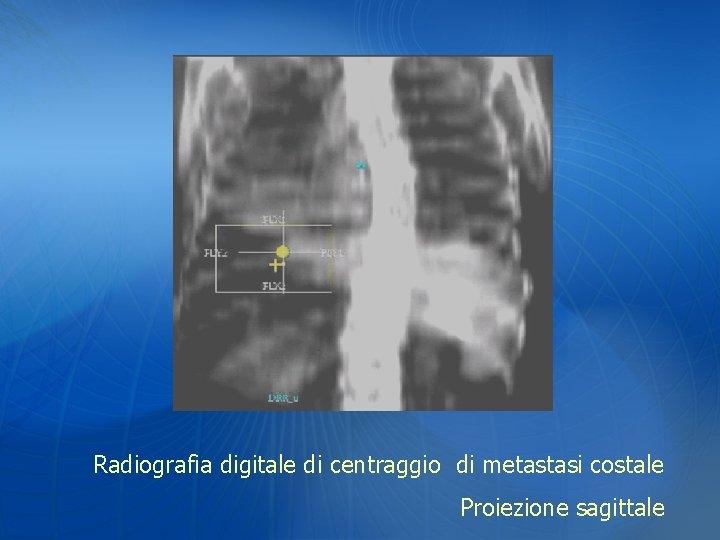
Radiografia digitale di centraggio di metastasi costale Proiezione sagittale

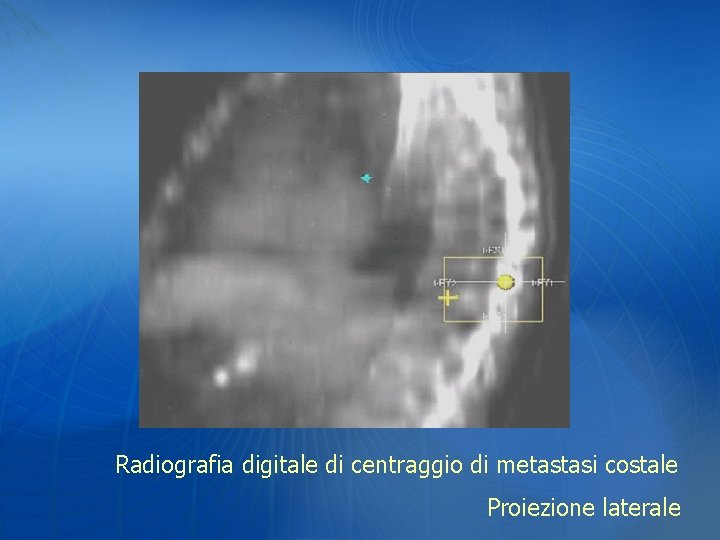
Radiografia digitale di centraggio di metastasi costale Proiezione laterale

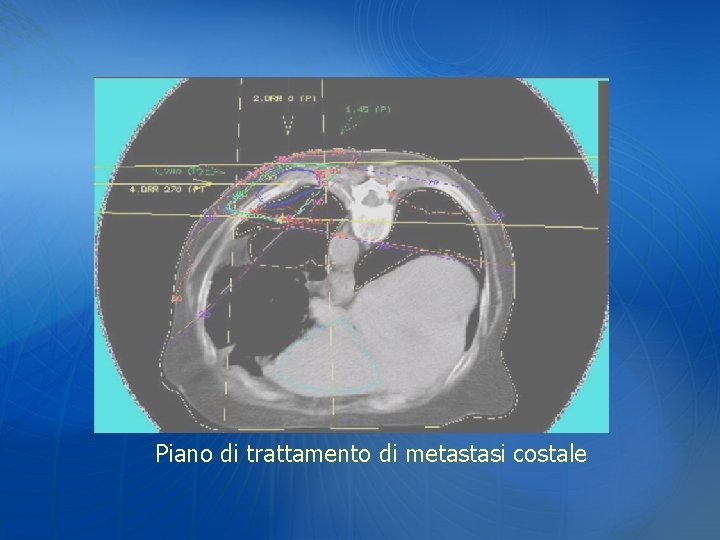
Piano di trattamento di metastasi costale

Conclusioni I pazienti con metastasi ossee hanno spesso un’ aspettativa di vita relativamente lunga ed è per questo che diventa importante la strategia terapeutica da adottare al fine di ridurre le complicanze e di migliorare la qualità della vita.

Conclusioni Le possibilità terapeutiche offerte dalla Radioterapia sono in continua evoluzione. ü Ottimizzazione dei piani di cura ü Miglior distribuzione di dose ü Maggior risparmio dei tessuti sani Aumento del rapporto terapeutico Migliore qualità di vita

GRAZIE Applausi!!

Chirurgia Per evitare un crollo vertebrale o dare struttura all’osso danneggiato dalla metastasi vengono impiantati chirurgicamente aste metalliche, piastre, viti, fili metallici, chiodi o perni. Vertebroplastica percutanea

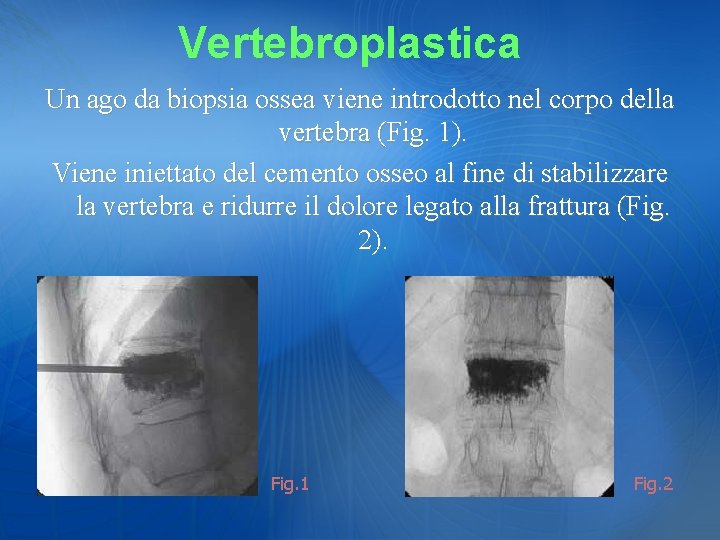
Vertebroplastica La Vertebroplastica Percutanea è una procedura terapeutica mini-invasiva per il trattamento delle fratture vertebrali dolorose che consiste nell’iniezione attraverso un ago metallico appositamente conformato, introdotto sotto guida combinata della TC o Fluoroscopia, di un CEMENTO A BASSA VISCOSITA’: il polimetilmetacrilato (PMMA), il quale si diffonde all’interno del corpo vertebrale fratturato, prevenendo ulteriori cedimenti.

Vertebroplastica Un ago da biopsia ossea viene introdotto nel corpo della vertebra (Fig. 1). Viene iniettato del cemento osseo al fine di stabilizzare la vertebra e ridurre il dolore legato alla frattura (Fig. 2). Fig. 1 Fig. 2

Vertebroplastica Vengono introdotti pochi ml di cemento che determinano il consolidamento dell’osso mentre la temperatura sviluppata durante la polimerizzazione (circa 90°C) causa la necrosi del tessuto tumorale conseguente risoluzione del dolore (il pz. così smettere di indossare il busto, ridurre o sospendere l’assunzione di farmaci analgesici e migliorare la qualità di vita).

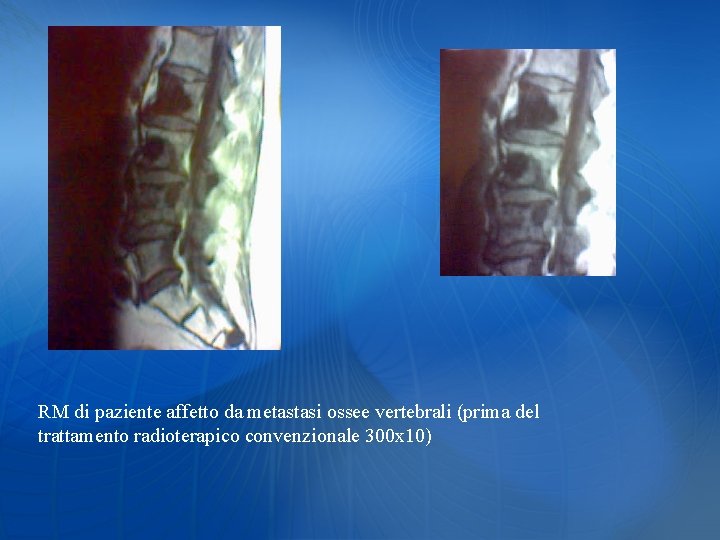
RM di paziente affetto da metastasi ossee vertebrali (prima del trattamento radioterapico convenzionale 300 x 10)