Presentazione dellantigene Antigen processing Antigen presentation MHC di









- Slides: 26

Presentazione dell’antigene • Antigen processing • Antigen presentation

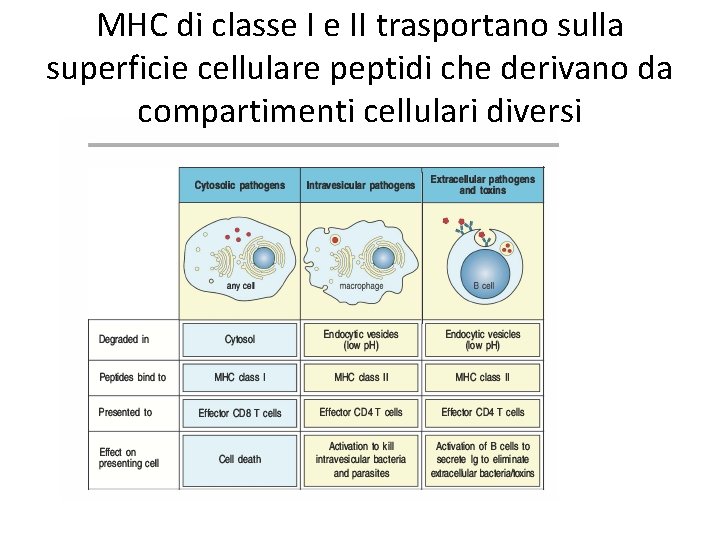
MHC di classe I e II trasportano sulla superficie cellulare peptidi che derivano da compartimenti cellulari diversi • Agenti infettivi possono raggiungere il cytosol o il compartimento vescicolare e quindi il processamento degli antigeni può avvenire in entrambi I compartimenti • MHC di classe I trasportano peptidi che si originano nel cytosol • MHC di classe II trasportano peptidi che si originano nelle vescicole • L’uso di diverse molecole MHC garantisce che sia attivata l’appropriata strategia di eliminazione dell’agente infettivo

MHC di classe I e II trasportano sulla superficie cellulare peptidi che derivano da compartimenti cellulari diversi

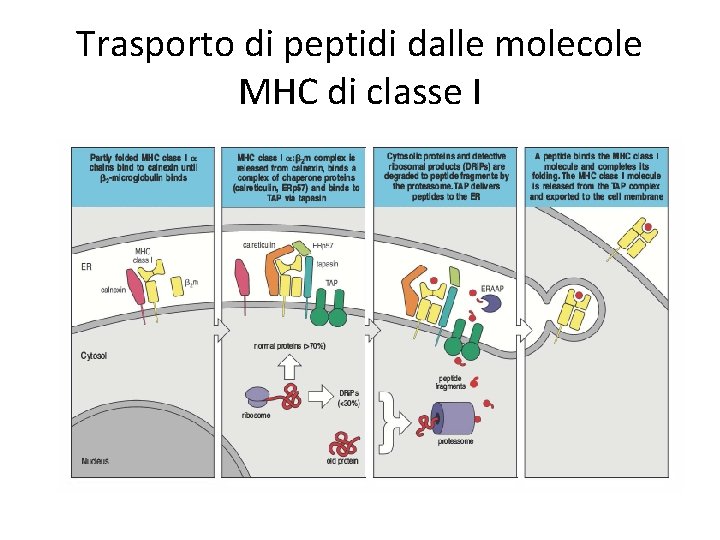
Trasporto di peptidi dalle molecole MHC di classe I

Trasporto di peptidi dalle molecole MHC di classe I • MHC I (catene alfa) si accumulano nel reticolo endoplasmatico dopo la loro sintesi, associate alla calnexina • Una volta che si associa la ß 2 -microglobulina, la calnexina si stacca e la molecola di MHC ancora non completamente “folded” si associa al trasportatore TAP attraverso un adattatore (la tapasina) • Altre molecole sono coinvolte in questa fase: la chaperone ERp 57 e la calreticulina • MHC resta nel reticolo endoplasmatico finchè non è rilasciata dal legame con un peptide che porta al suo “folding” completo • Anche in assenza di infezioni, ci sono continuamente peptidi che si formano per opera del proteasome a partire da: • “defective ribosomal products” (DRi. Ps) • Proteine “vecchie” • Questi peptidi vengono trasportati da TAP, eventualmente “limati” dall’aminopeptidasi ERAAP e poi si associano alla molecola di MHC di classe I, che migra al Golgi e da qui è portata alla membrana cellulare

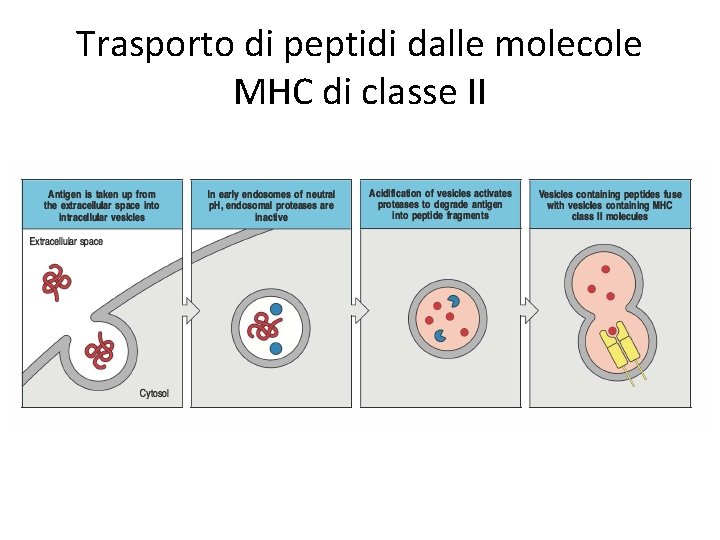
Trasporto di peptidi dalle molecole MHC di classe II

Trasporto di peptidi dalle molecole MHC di classe II • Una Antigen-Presenting-Cell (APC) può inglobare la fonte di antigene dall’esterno, oppure il parassita, batterio o virus possono avere invaso la cellula e replicare all’interno di vescicole intracellulari • Il p. H delle vescicole va progressivamente acidificandosi • La diminuzione del p. H porta all’attivazione di una serie di proteasi vescicolari che processano l’antigene in peptidi • La molecola di MHC di classe II durante la sua maturazione entra nelle vescicole e si associa al ligando peptidico per poterlo poi trasportare alla membrana cellulare

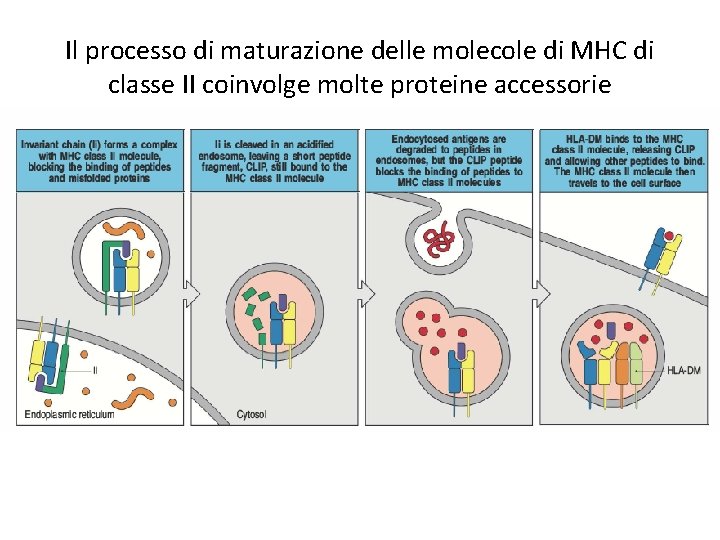
Il processo di maturazione delle molecole di MHC di classe II coinvolge molte proteine accessorie

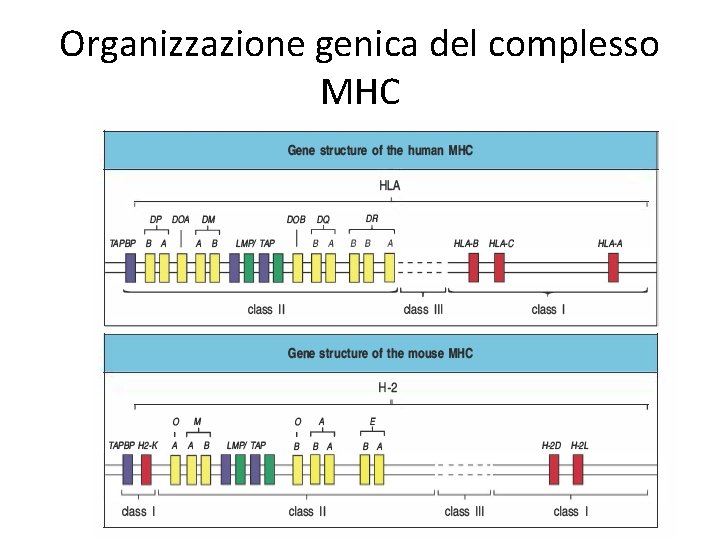
Organizzazione genica del complesso MHC • Il complesso MHC ha due caratteristiche: – Poligenico: ogni individuo ha molti geni per MHC di classe I ed altrettanti per la classe II – Polimorfico: esistono molteplici varianti alleliche per ogni gene nella popolazione (> 800 alleli) • Ogni individuo può esprimere almeno tre molecole di classe I e tre o quattro di classe II in base alla poligenia delle molecole di MHC, e molte di più per il loro polimorfismo

Organizzazione genica del complesso MHC

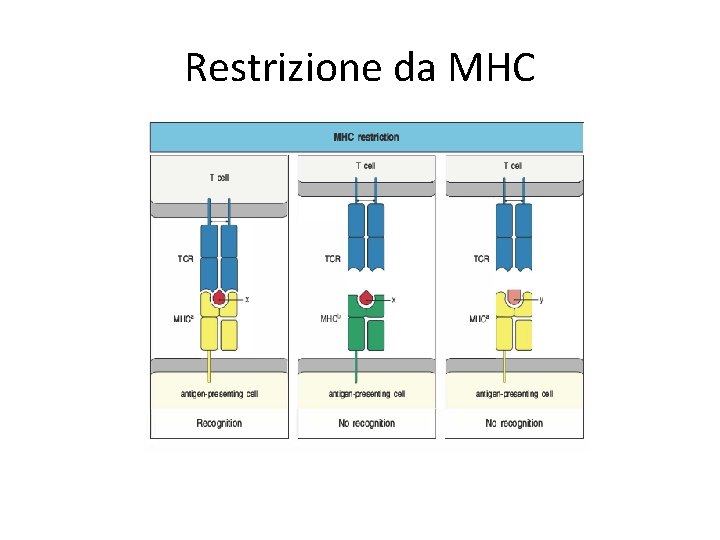
Restrizione da MHC

Trasduzione del segnale ed attivazione linfocitaria

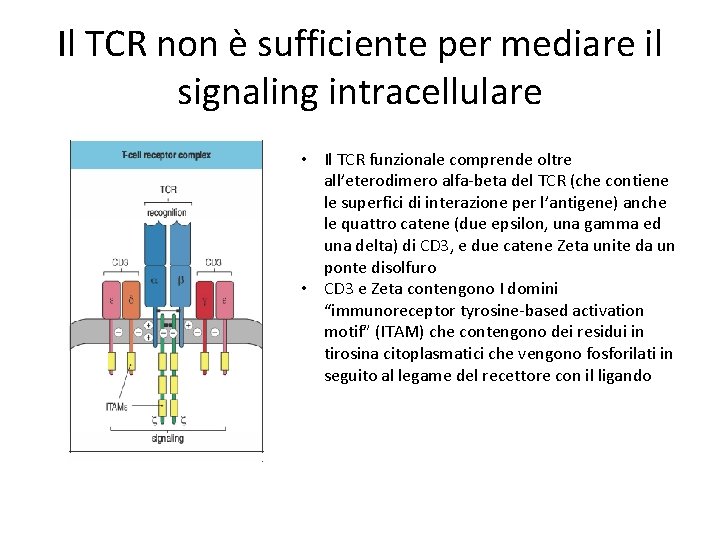
Il TCR non è sufficiente per mediare il signaling intracellulare • Il TCR funzionale comprende oltre all’eterodimero alfa-beta del TCR (che contiene le superfici di interazione per l’antigene) anche le quattro catene (due epsilon, una gamma ed una delta) di CD 3, e due catene Zeta unite da un ponte disolfuro • CD 3 e Zeta contengono I domini “immunoreceptor tyrosine-based activation motif” (ITAM) che contengono dei residui in tirosina citoplasmatici che vengono fosforilati in seguito al legame del recettore con il ligando

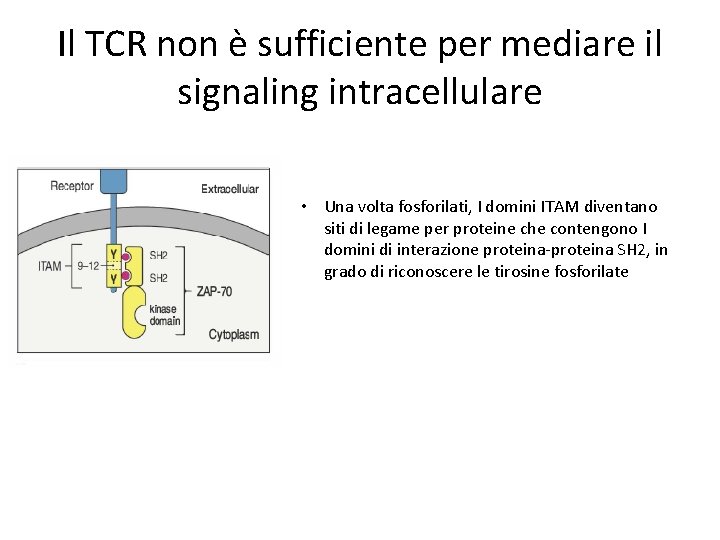
Il TCR non è sufficiente per mediare il signaling intracellulare • Una volta fosforilati, I domini ITAM diventano siti di legame per proteine che contengono I domini di interazione proteina-proteina SH 2, in grado di riconoscere le tirosine fosforilate

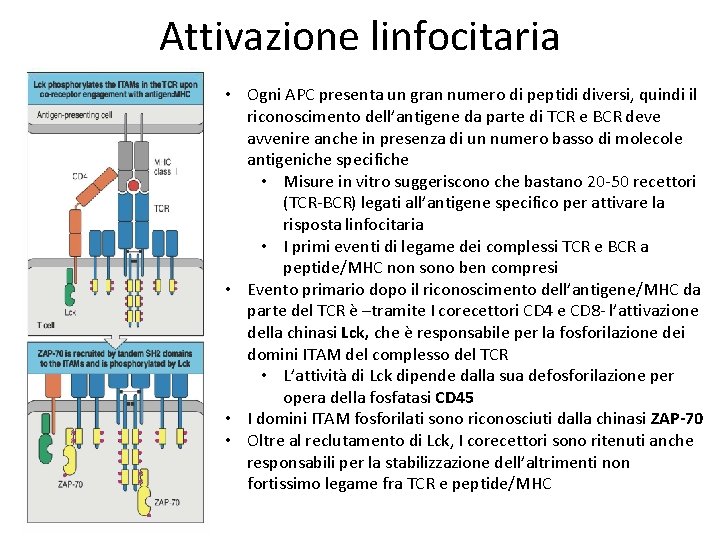
Attivazione linfocitaria • Ogni APC presenta un gran numero di peptidi diversi, quindi il riconoscimento dell’antigene da parte di TCR e BCR deve avvenire anche in presenza di un numero basso di molecole antigeniche specifiche • Misure in vitro suggeriscono che bastano 20 -50 recettori (TCR-BCR) legati all’antigene specifico per attivare la risposta linfocitaria • I primi eventi di legame dei complessi TCR e BCR a peptide/MHC non sono ben compresi • Evento primario dopo il riconoscimento dell’antigene/MHC da parte del TCR è –tramite I corecettori CD 4 e CD 8 - l’attivazione della chinasi Lck, che è responsabile per la fosforilazione dei domini ITAM del complesso del TCR • L’attività di Lck dipende dalla sua defosforilazione per opera della fosfatasi CD 45 • I domini ITAM fosforilati sono riconosciuti dalla chinasi ZAP-70 • Oltre al reclutamento di Lck, I corecettori sono ritenuti anche responsabili per la stabilizzazione dell’altrimenti non fortissimo legame fra TCR e peptide/MHC

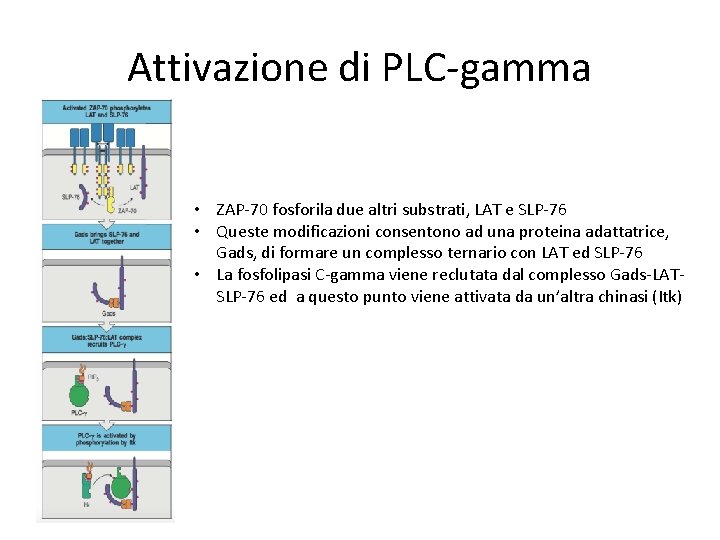
Attivazione di PLC-gamma • ZAP-70 fosforila due altri substrati, LAT e SLP-76 • Queste modificazioni consentono ad una proteina adattatrice, Gads, di formare un complesso ternario con LAT ed SLP-76 • La fosfolipasi C-gamma viene reclutata dal complesso Gads-LATSLP-76 ed a questo punto viene attivata da un’altra chinasi (Itk)

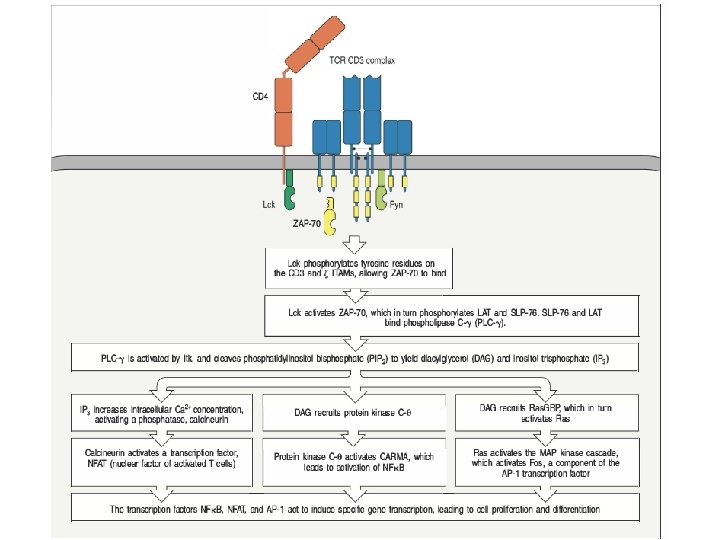
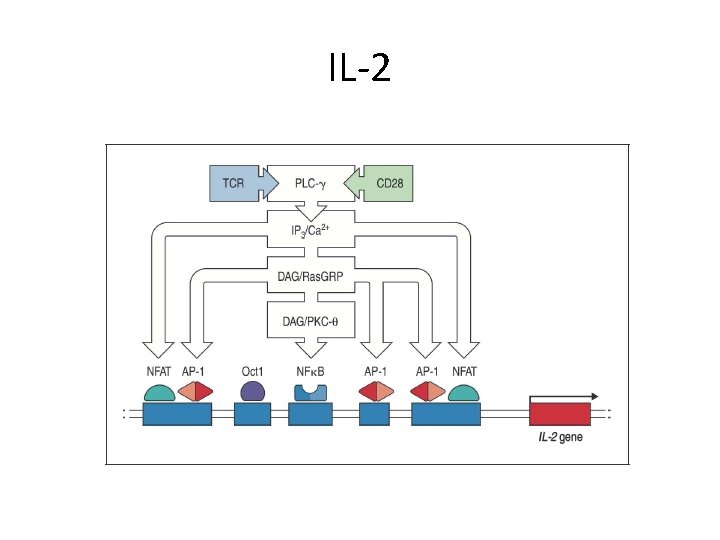
La formazione di “second messengers” • PLC-gamma genera a partire da PIP 2 due lipidi: DAG e IP 3 • IP 3 porta all’efflusso di ioni Calcio dal reticolo endoplasmatico al cytosol, e quindi apertura di canali del calcio (CRAC) di membrana che consentono ulteriore ingresso di Calcio nel cytosol • DAG porta al reclutamento della Proteina chinasi C-delta e di proteine attivanti Ras alla membrana citoplasmatica • Attraverso questi 3 pathways intracellulari • Ioni calcio • PKC-delta • RAS • vengono attivati tre diversi pathway trascrizionali • Ioni Calcio: shuttling nucleare del fattore di trascrizione NFAT • RAS (attraverso una cascata di chinasi intracellulari) porta all’attivazione del fattore di trascrizione AP 1 • PKC-Delta porta all’attivazione di AP 1 e del fattore di trascrizione NF-k. B • Questi pathway trascrizionali hanno numerosi target • IL-2 integra I 3 segnali, dal momento che tutti questi fattori di tarscrizione legano elementi regolatori presenti nel promotore del gene


IL-2

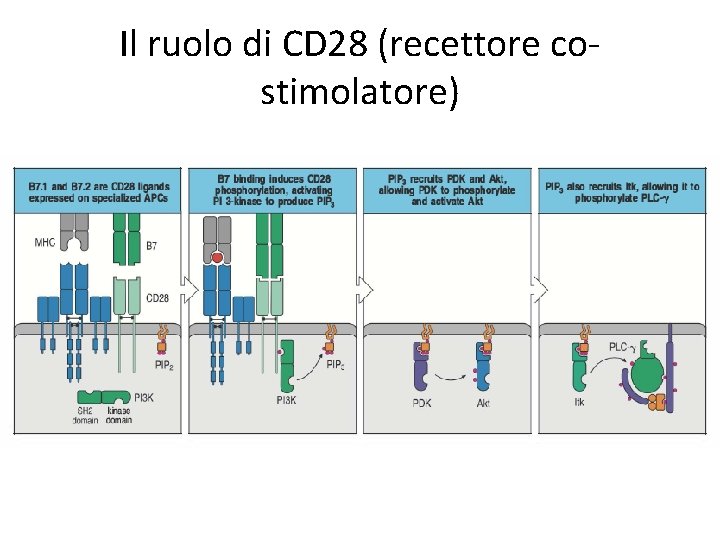
Il ruolo di CD 28 (recettore costimolatore)

Il ruolo di CD 28 (recettore costimolatore) • IL legame dell’antigene al TCR non è sufficiente per l’attivazione linfocitaria delle cellule T naïve • Le APCs esprimono sulla superficie cellulare delle molecole co-stimolatorie • Queste interagiscono con recettori co-stimolatori delle cellule T • Il legame ligando-recettore (insieme con il legame TCR-MHC/antigene) porta all’attivazione linfocitaria • I co-stimolatori attivano un pathway intracellulare parallelo e necessario per l’efficiente trasduzione del segnale mediata da TCR/antigene • Il risultato dell’attivazione di CD 28 è l’attivazione della PI-3 chinasi che porta alla produzione di PIP 3, che porta a sua volta all’attivazione di Itk che attiva PLC-gamma • Anche la chinasi Akt è attivata •

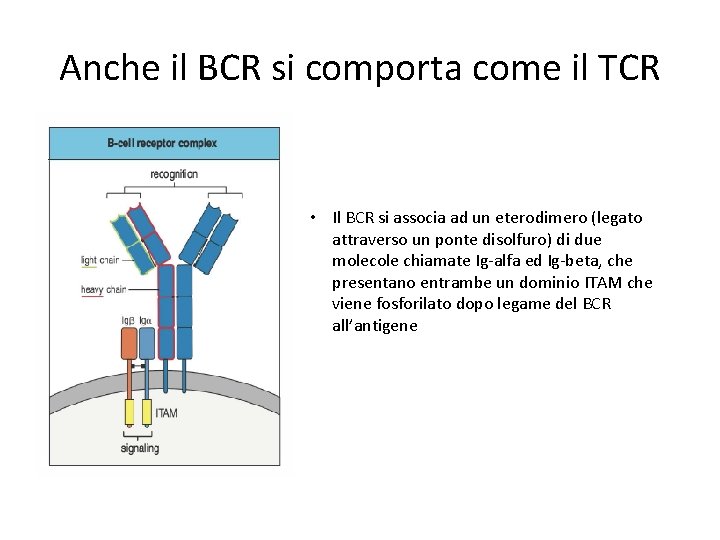
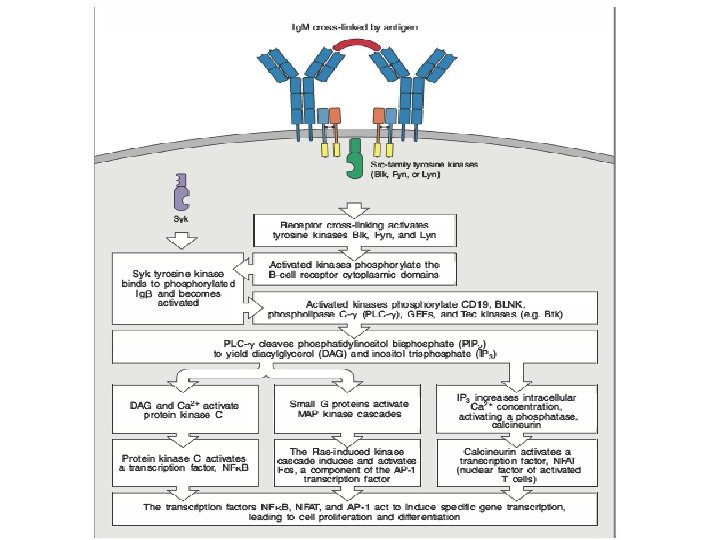
Anche il BCR si comporta come il TCR • Il BCR si associa ad un eterodimero (legato attraverso un ponte disolfuro) di due molecole chiamate Ig-alfa ed Ig-beta, che presentano entrambe un dominio ITAM che viene fosforilato dopo legame del BCR all’antigene

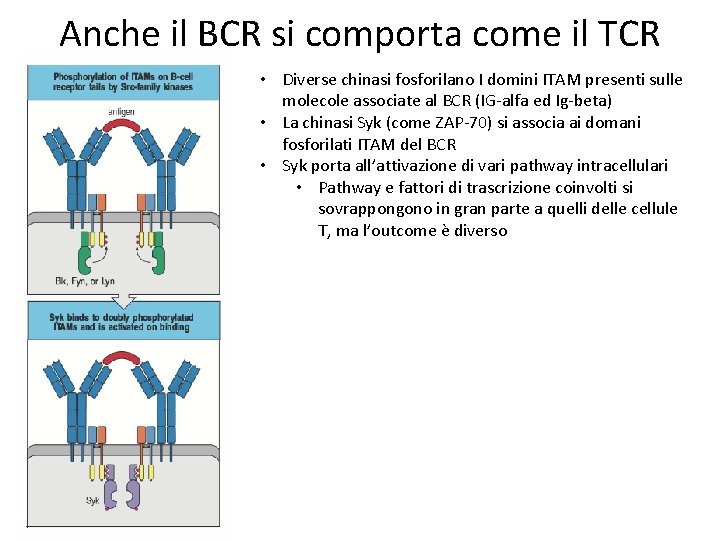
Anche il BCR si comporta come il TCR • Diverse chinasi fosforilano I domini ITAM presenti sulle molecole associate al BCR (IG-alfa ed Ig-beta) • La chinasi Syk (come ZAP-70) si associa ai domani fosforilati ITAM del BCR • Syk porta all’attivazione di vari pathway intracellulari • Pathway e fattori di trascrizione coinvolti si sovrappongono in gran parte a quelli delle cellule T, ma l’outcome è diverso


La risposta immune è regolata da recettori inibitori • Molecole correlate a CD 28 sono espresse dai linfociti T e legano molecole della famiglia di B 7 • Tra queste molecole, alcune hanno attività inibitoria – Cellule T: CTLA-4 e PD-1 – Cellule B/T: BTLA • Modelli animali: topi privi di CTLA-4 hanno proliferazioni linfocitaria incontrollata, a dimostrazione della necessità dei meccanismi di controllo

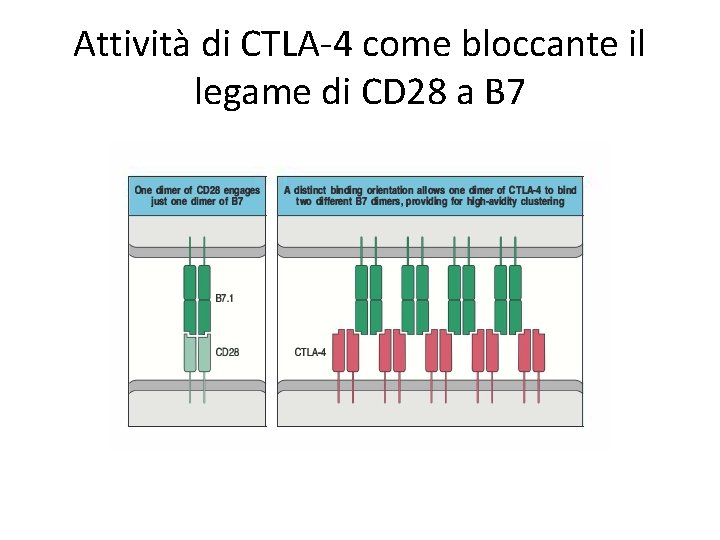
Attività di CTLA-4 come bloccante il legame di CD 28 a B 7