Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 21 Kimia Inti

Reaksi-reaksi Inti Beberapa inti tidak stabil. Inti-inti ini disebut radioaktif dan memancarkan partikel dan biasanya radiasi elektromagnetk energi-tinggi (sinar gamma) pada saat yang bersamaan. Reaksi inti yang lain melibatkan pemboman inti dengan partikel-partikel seperti neutron, proton, atau inti lainnya.
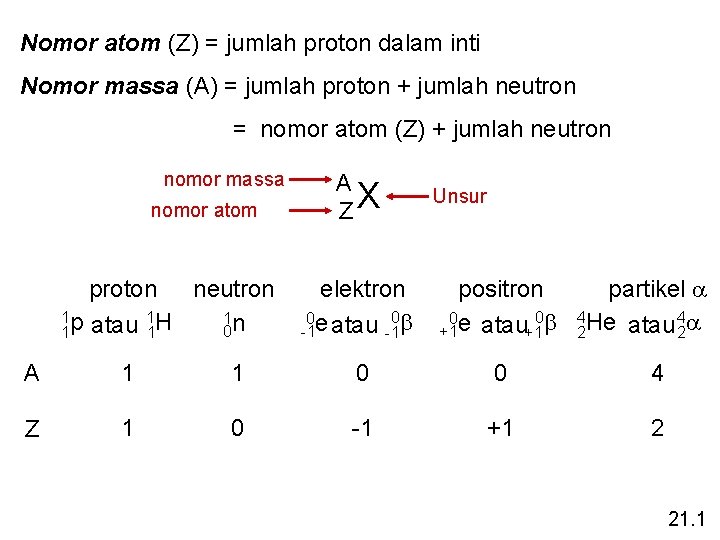
Nomor atom (Z) = jumlah proton dalam inti Nomor massa (A) = jumlah proton + jumlah neutron = nomor atom (Z) + jumlah neutron nomor massa nomor atom proton neutron 1 p 1 H 1 n atau 0 1 1 A ZX Unsur elektron 0 b 0 e atau -1 -1 positron 0 b 0 e atau +1 +1 partikel a 4 He 4 a atau 2 2 A 1 1 0 0 4 Z 1 0 -1 +1 2 21. 1

Menyetarakan Persamaan Inti 1. Kekekalan nomor massa (A). Jumlah proton plus neutron dalam produk harus sama dengan jumlah proton plus neutron dalam reaktan. 235 92 U + 10 n 138 55 Cs + 96 37 Rb + 2 10 n 235 + 1 = 138 + 96 + 2 x 1 2. Kekekalan nomor atom (Z) atau muatan inti. Jumlah muatan inti dalam produk harus sama dengan jumlah muatan inti dalam reaktan. 235 92 U + 10 n 138 55 Cs + 96 37 Rb 92 + 0 = 55 + 37 + 2 x 0 + 2 10 n 21. 1

Peluruhan 212 Po karena emisi alpha. Tulis persamaan inti setimbang untuk peluruhan 212 Po. 4 partikel alpha - 42 He atau 2 a 212 Po 84 4 He 2 + AZX 212 = 4 + A A = 208 84 = 2 + Z Z = 82 212 Po 84 4 He 2 + 208 82 Pb 21. 1

21. 1

Kestabilan Inti dan Peluruhan Radioaktif Peluruhan Beta +-10 b + n 14 C 6 14 N 7 40 K 19 40 Ca 20 jumlah neutron turun 1 + -10 b + n 1 n 0 jumlah proton naik 1 1 p 1 +-10 b + n Peluruhan Positron 11 C 6 11 B 5 38 19 K 38 Ar 18 ++10 b + n jumlah neutron naik 1 ++10 b + n jumlah proton turun 1 1 p 1 1 n 0 ++10 b + n n dan n memiliki A = 0 dan Z = 0 21. 2

Kestabilan Inti dan Peluruhan Radioaktif Penangkapan elektron +n 37 Ar 18 + -10 e 37 Cl 17 55 Fe 26 + -10 e 55 Mn 25 1 p 1 jumlah neutron naik 1 +n jumlah proton turun 1 + -10 e 1 n 0 +n Peluruhan alpha 212 Po 84 4 He 2 + 208 82 Pb jumlah neutron turun 2 jumlah proton turun 2 Fisi spontan 252 Cf 98 1 n 2125 In + 2 49 0 21. 2
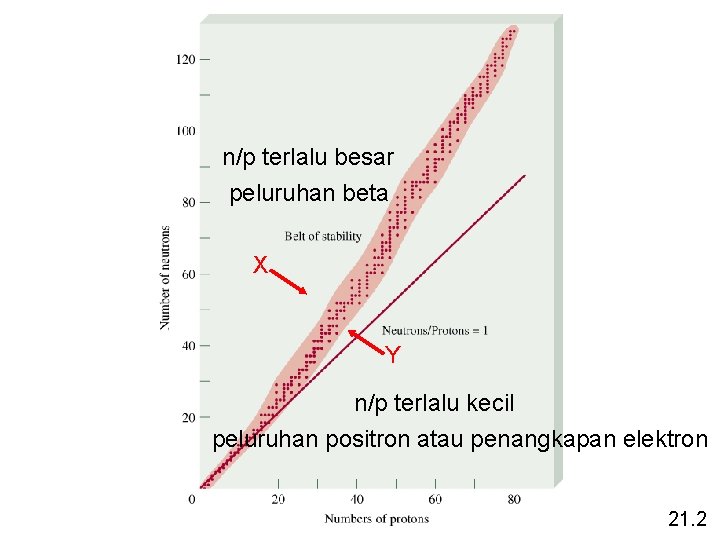
n/p terlalu besar peluruhan beta X Y n/p terlalu kecil peluruhan positron atau penangkapan elektron 21. 2

Kestabilan Inti • Inti yang mengandung proton atau neutron sebanyak 2, 8, 20, 50, 82, atau 126 lebih stabil dibandingkan inti-inti lainnya • Inti yang jumlah proton dan jumlah neutronnya genap lebih stabil dibanding yang ganjil • Semua isotop dari unsur dengan nomor atom lebih dari 83 adalah isotop radioaktif • Semua isotop Tc dan Pm bersifat radioaktif 21. 2

Energi ikatan inti (BE) energi yg dibutuhkan untuk memecah inti menjadi komponen-komponennya, proton dan neutron. BE + 199 F 911 p + 1010 n Δ E = (Δ m)c 2 BE = 9 x (p massa) + 10 x (n massa) – 19 F massa BE (sma) = 9 x 1, 007825 + 10 x 1, 008665 – 18, 9984 BE = 0, 1587 sma 1 sma = 1, 49 x 10 -10 J BE = 2, 37 x 10 -11 J Energi ikatan per nukleon = Jumlah nukleon 2, 37 x 10 -11 J = 1, 25 x 10 -12 J = 19 nukleon 21. 2
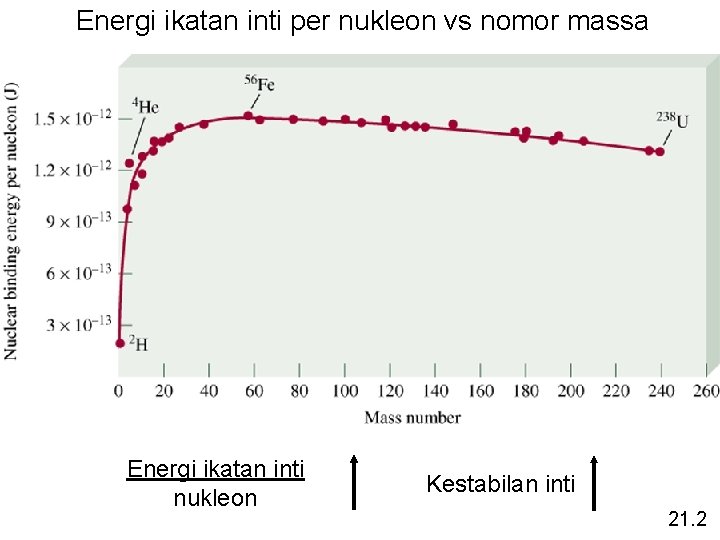
Energi ikatan inti per nukleon vs nomor massa Energi ikatan inti nukleon Kestabilan inti 21. 2
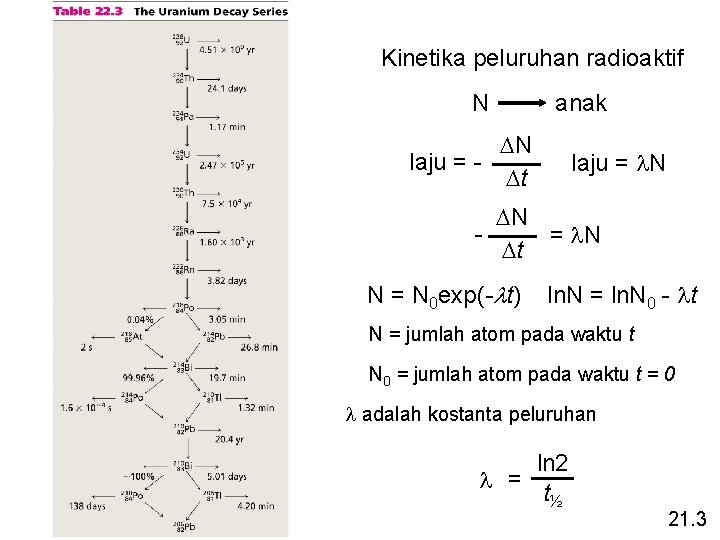
Kinetika peluruhan radioaktif N anak DN laju = Dt laju = l. N DN = l. N Dt N = N 0 exp(-lt) ln. N = ln. N 0 - lt N = jumlah atom pada waktu t N 0 = jumlah atom pada waktu t = 0 l adalah kostanta peluruhan ln 2 l = t½ 21. 3
![Kinetika Peluruhan Radioaktif ln[N] = ln[N]0 - lt ln [N] [N] = [N]0 exp(-lt) Kinetika Peluruhan Radioaktif ln[N] = ln[N]0 - lt ln [N] [N] = [N]0 exp(-lt)](http://slidetodoc.com/presentation_image_h2/6c9b078d6fd83c0a195721f8cb040a18/image-14.jpg)
Kinetika Peluruhan Radioaktif ln[N] = ln[N]0 - lt ln [N] [N] = [N]0 exp(-lt) 21. 3

Penarikan Radiokarbon 14 N 7 14 C 6 + 01 n 14 C 6 14 N 7 + 11 H + -10 b + n t½ = 5730 tahun Isotop C-14 dihasilkan ketika nitrogen atmosfer dibombardir dengan sinar kosmik. Semua makhluk hidup mengandung C-14, namun ketika mati, jumlah C-14 berkurang. 21. 3

Umur batuan K-40 meluruh menjadi Ar-40 dengan waktu -paruh 1, 2 x 109 tahun Penarikhan Uranium-238 238 U 92 206 Pb 82 + 8 24 a + 6 -10 b t½ = 4, 51 x 109 tahun 21. 3
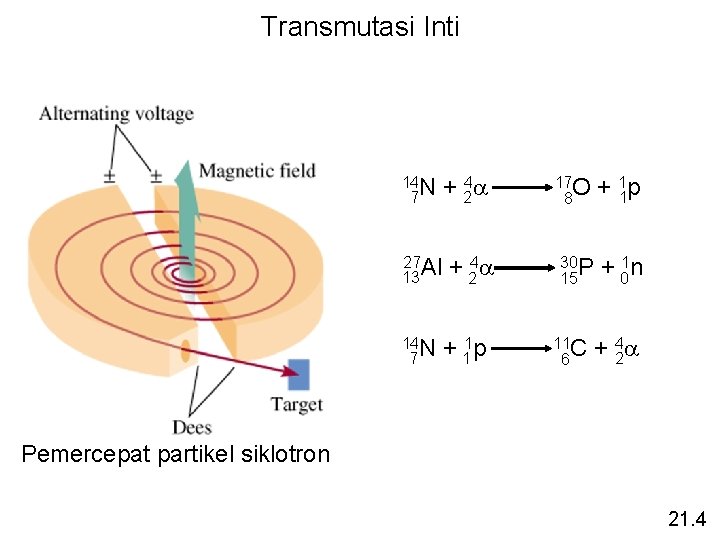
Transmutasi Inti 14 N 7 27 13 Al 14 N 7 + 24 a + 11 p 17 O 8 + 11 p 30 P 15 + 01 n 11 C 6 + 24 a Pemercepat partikel siklotron 21. 4
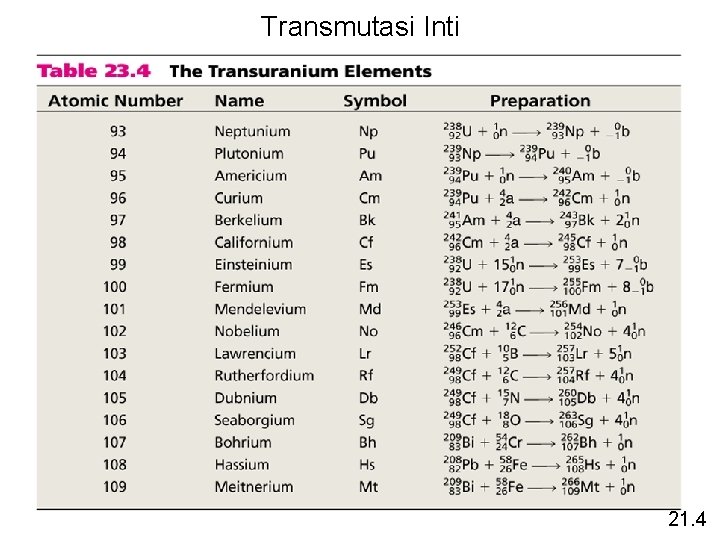
Transmutasi Inti 21. 4
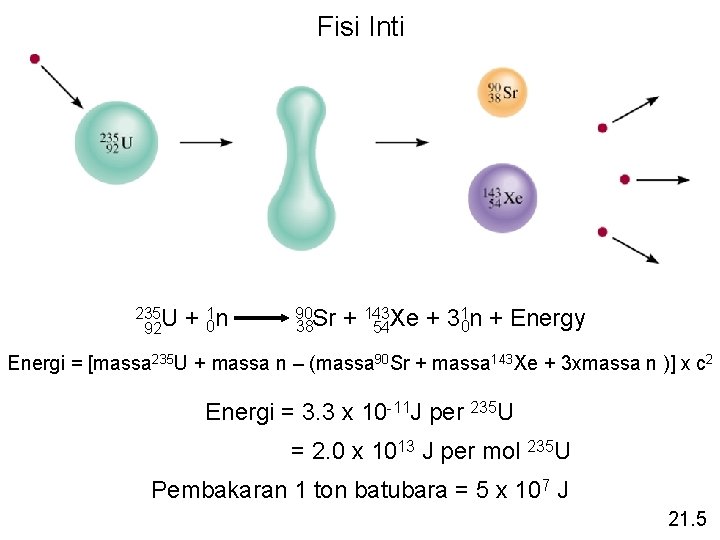
Fisi Inti 235 U 92 + 01 n 90 Sr 38 1 n + Energy + 143 Xe + 3 0 54 Energi = [massa 235 U + massa n – (massa 90 Sr + massa 143 Xe + 3 xmassa n )] x c 2 Energi = 3. 3 x 10 -11 J per 235 U = 2. 0 x 1013 J per mol 235 U Pembakaran 1 ton batubara = 5 x 107 J 21. 5
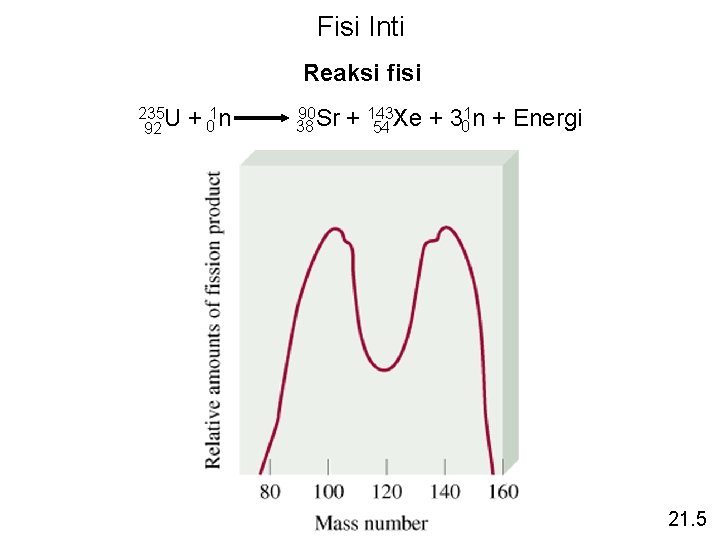
Fisi Inti Reaksi fisi 235 U 92 + 01 n 90 Sr 38 1 n + Energi + 143 Xe + 3 0 54 21. 5
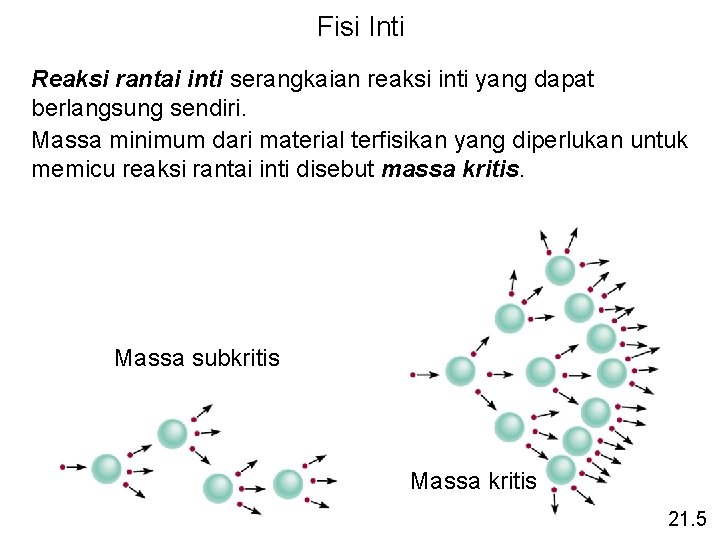
Fisi Inti Reaksi rantai inti serangkaian reaksi inti yang dapat berlangsung sendiri. Massa minimum dari material terfisikan yang diperlukan untuk memicu reaksi rantai inti disebut massa kritis. Massa subkritis Massa kritis 21. 5

The little boy bomb. Bom ini menggunakan U-235

The fat man bomb. Bom ini menggunakan Pu-239

Fig. 21. 9
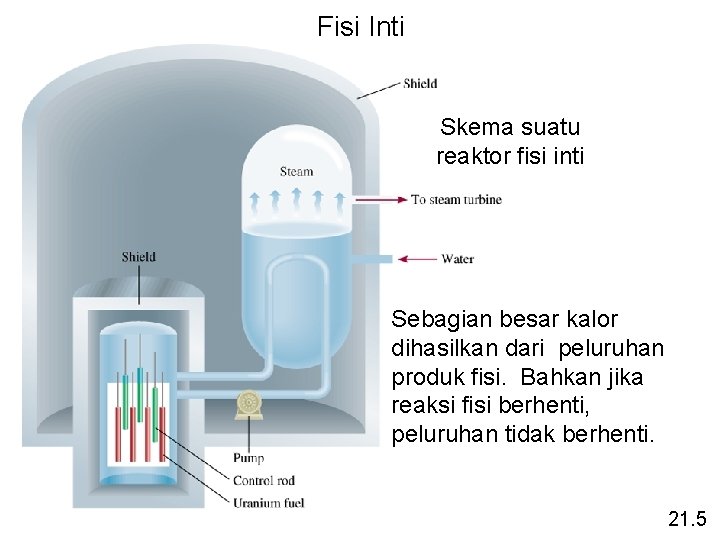
Fisi Inti Skema suatu reaktor fisi inti Sebagian besar kalor dihasilkan dari peluruhan produk fisi. Bahkan jika reaksi fisi berhenti, peluruhan tidak berhenti. 21. 5
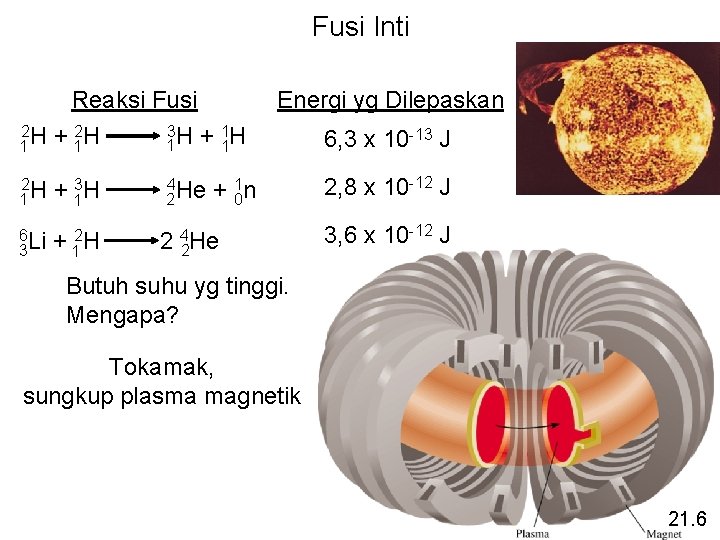
Fusi Inti Reaksi Fusi 2 2 3 1 1 H + 1 H 2 H 1 + 13 H 6 Li 3 + 12 H 4 He 2 2 Energi yg Dilepaskan + 01 n 4 He 2 6, 3 x 10 -13 J 2, 8 x 10 -12 J 3, 6 x 10 -12 J Butuh suhu yg tinggi. Mengapa? Tokamak, sungkup plasma magnetik 21. 6
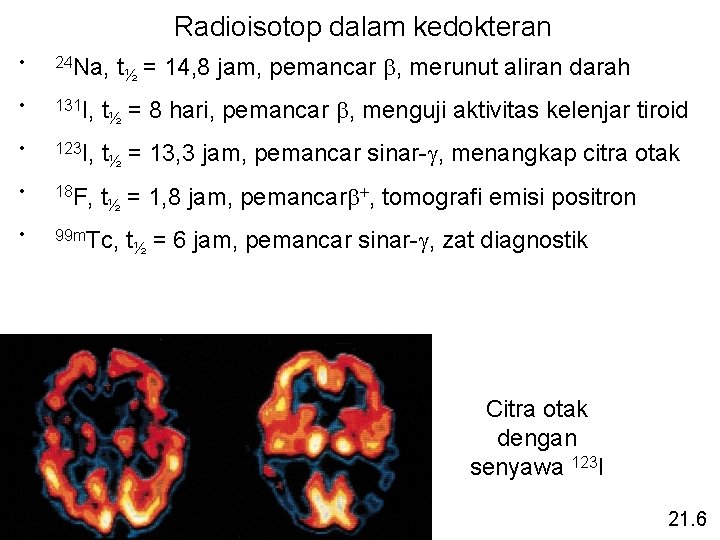
Radioisotop dalam kedokteran t½ = 14, 8 jam, pemancar b, merunut aliran darah • 24 Na, • 131 I, t½ = 8 hari, pemancar b, menguji aktivitas kelenjar tiroid • 123 I, t½ = 13, 3 jam, pemancar sinar-g, menangkap citra otak • 18 F, t½ = 1, 8 jam, pemancarb+, tomografi emisi positron • 99 m. Tc, t½ = 6 jam, pemancar sinar-g, zat diagnostik Citra otak dengan senyawa 123 I 21. 6
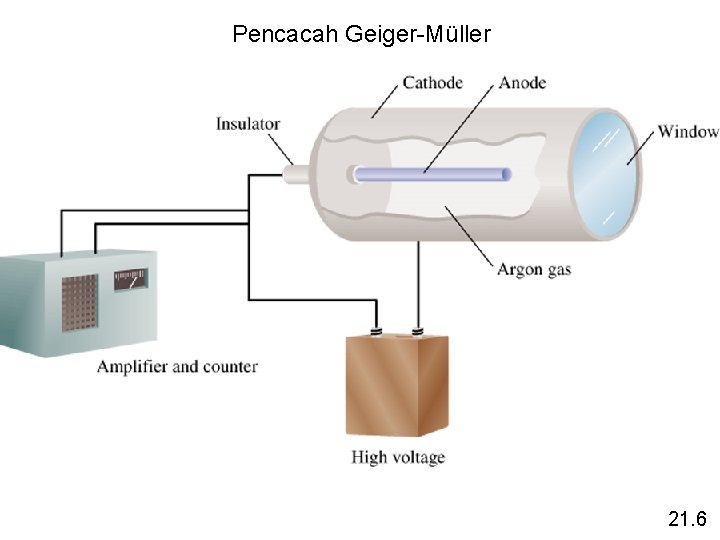
Pencacah Geiger-Müller 21. 6

Dampak biologis dari radiasi radiation absorbed dose (rad) 1 rad = 1 x 10 -5 J/g zat Roentgen equivalent for man (rem) 1 rem = 1 rad x Q Quality Factor g-ray = 1 b=1 a = 20 21. 6
- Slides: 29