Presentaciones adaptadas al texto del libro Temas de

Presentaciones adaptadas al texto del libro: “Temas de química (II) para alumnos de ITOP e ICCP” Tema 11. Fundamentos de la Corrosión Metálica ROCÍO LAPUENTE ARAGÓ Departamento de Ingeniería de la Construcción UNIVERSIDAD DE ALICANTE ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 1

1. La civilización y las superficies ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 2

Una civilización industrial depende de la estabilidad de los metales en atmósferas húmedas Todos los metales son irreversiblemente inestables, excepto los metales nobles “Los tracios”. Bulgaria, SV a. J. C. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 3

2. Las reacciones de transferencia de carga son el origen de la inestabilidad de una superficie ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 4

3. Un metal que sufre de corrosión es análogo a una pila productora de energía en cortocircuito La corrosión puede definirse como la reacción química o electroquímica de un metal o aleación con su medio circundante con el consiguiente deterioro de sus propiedades. La corrosión son reacciones redox en las cuales un metal sufre el ataque de su entorno y se convierte en un producto no deseado. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 5

-Reacciona con su -Deterioro de sus medio circundante. propiedades. METAL -Se convierte en un -Sufre el ataque de producto no deseado. su entorno. N Ó I C C U R T ES D ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 6

¿ PORQUÉ SE PRODUCE LA CORROSIÓN? Normalmente, lo que observamos asociado a la destrucción del metal Oxidación Acepte esos electrones es su oxidación. Pérdida de electrones. Alguna especie. REACCIONES DE OXIDACIÓN-REDUCCIÓN. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 7
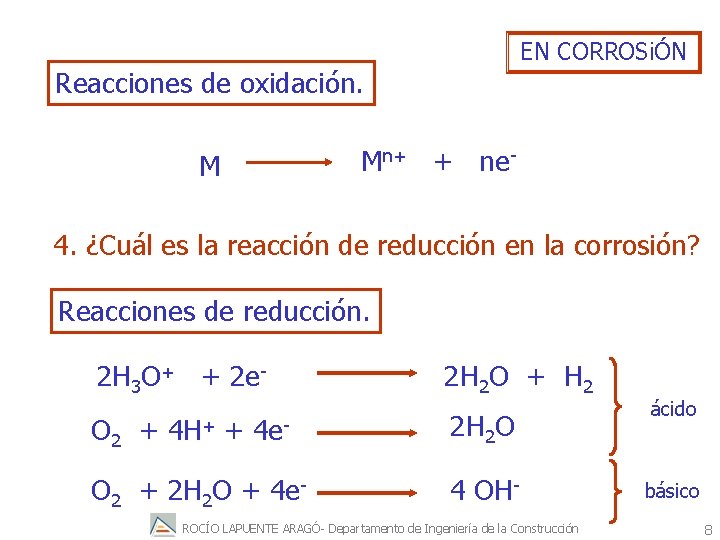
EN CORROSiÓN Reacciones de oxidación. M Mn+ + ne- 4. ¿Cuál es la reacción de reducción en la corrosión? Reacciones de reducción. 2 H 3 O+ + 2 e- 2 H 2 O + H 2 O 2 + 4 H+ + 4 e- 2 H 2 O O 2 + 2 H 2 O + 4 e- 4 OH- ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción ácido básico 8

ANODO CATODO ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 9
Veamos como ocurre la corrosión ¡Aviso! Esto no esta en el libro ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 10
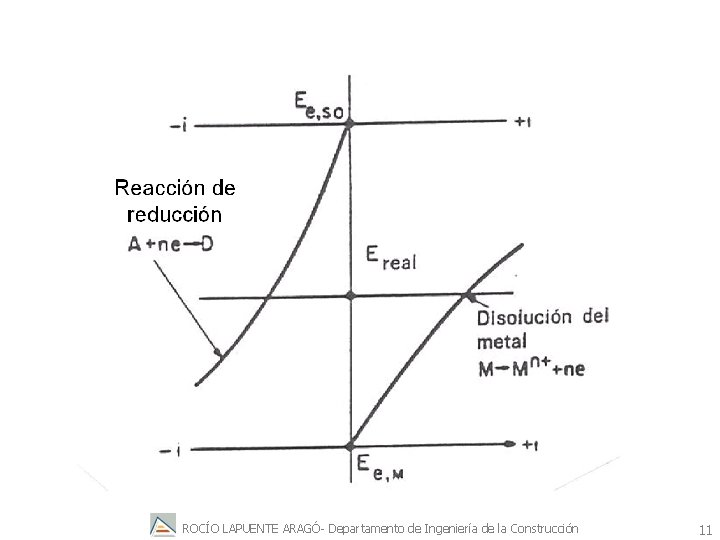
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 11

E = E 0 0, 059 lg Q n Ecuación de Nersnt: Relaciona el potencial con las concentraciones ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 12

Aplicamos la ecuación de Nerst para determinar el valor de EPila Cuál es el valor de EPila para la pila : Pt/ Fe 2+ (0, 10 M), Fe 3+(0, 20 M)// Ag+(1, 0 M)/ Ag(s) E 0 Pila= E 0(Cátodo) - E 0(Anodo) = E 0(Ag +/Ag) - E 0(Fe 3+/Fe 2+) = 0, 800 V – 0, 771 V = 0, 029 V E 0 Pila = 0, 029 V ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 13

Para determinar EPila para la reacción: Fe 2+ (0, 10 M) + Ag+(1, 0 M) Fe 3+(0, 20 M)+ Ag(s) Se sustituye en la ecuación de Nerst los valores adecuados: [Fe 3+] 0, 059 log E=E 0 n [Fe 2+][Ag+] E=0, 029 - 0, 059 log [0, 2] [0, 1][1, 0] = 0, 011 V ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 14
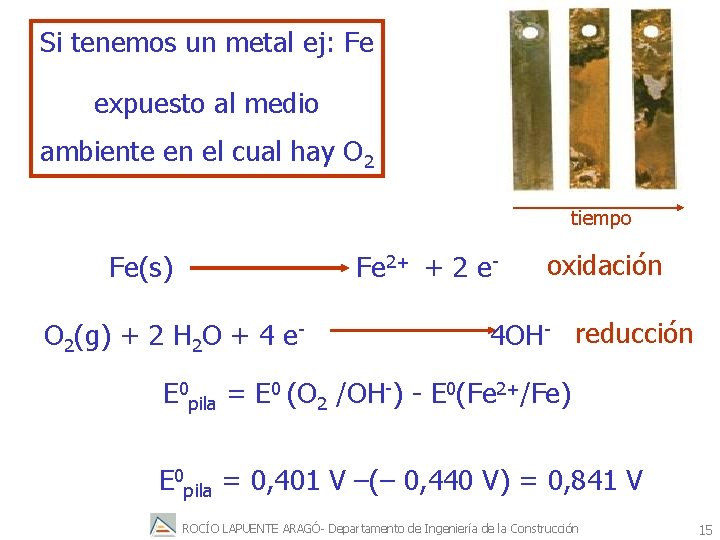
Si tenemos un metal ej: Fe expuesto al medio ambiente en el cual hay O 2 tiempo Fe(s) Fe 2+ + 2 e- O 2(g) + 2 H 2 O + 4 e- oxidación 4 OH- reducción E 0 pila = E 0 (O 2 /OH-) - E 0(Fe 2+/Fe) E 0 pila = 0, 401 V –(– 0, 440 V) = 0, 841 V ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 15

2 Fe(s) + 2 O 2(g) + 2 H 2 O 2 Fe 2+ + 4 OHn=4 E 0 = 0, 841 V 0, 059 log E=E 04 [Fe 2+]2[OH-]4 [Pp. O 2]2 Puesto que Fe 2+ y OH- se generan como resultado del proceso E dependerá de Pp. O 2 ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 16

Veamos lo que ocurre en el caso de tener una superficie de Fe expuesta al aire, en la cual consideramos dos punto con diferente aireación Fe(s) Fe 2+ + 2 e- O 2(g) + 2 H 2 O + 4 e- oxidación 4 OH- reducción ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 17

¿cómo capta los electrones el oxígeno? Necesita un contacto metálico para “cogerlos” Ese contacto es otra zona de la superficie de Fe. En ese punto el O 2 se reduce sobre el Fe y esa zona actúa como cátodo ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 18
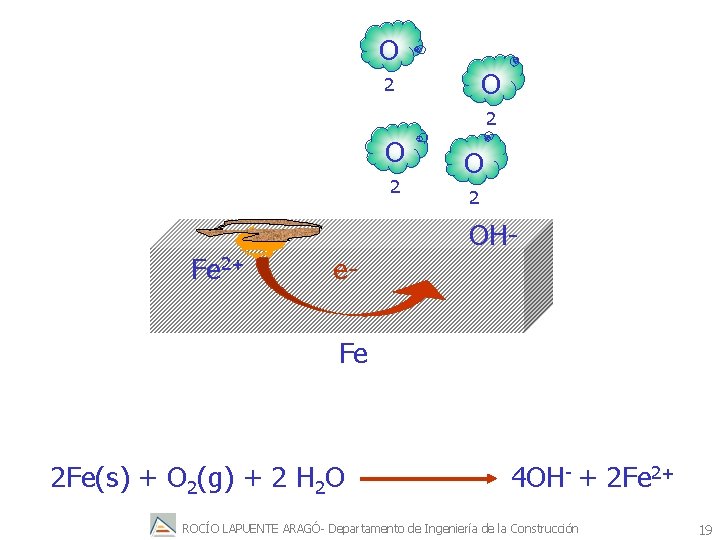
O O 2 2 O 2 OHFe 2+ e. Fe 2 Fe(s) + O 2(g) + 2 H 2 O 4 OH- + 2 Fe 2+ ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 19

E 0 pila = E 0 (catodo) - E 0(anodo) E 0 pila = E 0 (reacción de reducción) - E 0(reacción de oxidación) E 0 pila = E 0 (O 2 /OH-) - E 0(Fe 2+/Fe) E 0 pila = 0, 401 V –(– 0, 440 V) = 0, 841 V ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 20

En una superficie en aparente igualdad de condiciones ¿qué zona actúa como cátodo y que zona actúa como ánodo? E=E 0 - 0, 059 log 4 Si el aire es casi todo O 2 [Fe 2+]2[OH-]4 [Pp. O 2]2 Pp. O 2= 1 atm E=E 0 Pp. O 2>1 atm E>E 0 ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 21
![Cuanto mayor sea el valor de Mayor será el valor de [Pp. O 2]2 Cuanto mayor sea el valor de Mayor será el valor de [Pp. O 2]2](http://slidetodoc.com/presentation_image/49b413fb9bab4c073eb0663f82186bce/image-22.jpg)
Cuanto mayor sea el valor de Mayor será el valor de [Pp. O 2]2 E Lo cual implica que la zona con mayor presión de oxígeno (más aireación) actúa como cátodo Cuanto menor sea el valor de Menor será el valor de [Pp. O 2]2 E Lo cual implica que la zona con menor presión de oxígeno (menos aireación) actúa como ánodo Y tiene lugar la corrosión ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 22
5. Termodinámica y estabilidad de los metales Al elegir un material para construcción nos preguntaremos: ¿Serán capaces de producirse espontáneamente las reacciones de oxidación y reducción, que conjuntamente constituyen el proceso de corrosión? . Respuesta: LA TERMODINÁMICA ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 23

¿Como utilizar la TERMODINÁMICA? comparando DGc= -n. FEC DGA= -n. FEA Si este cambio total de energía libre es negativo, la corrosión del metal tendrá lugar espontáneamente. A E N DGc + DGA Á T N O P <0 ES ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 24
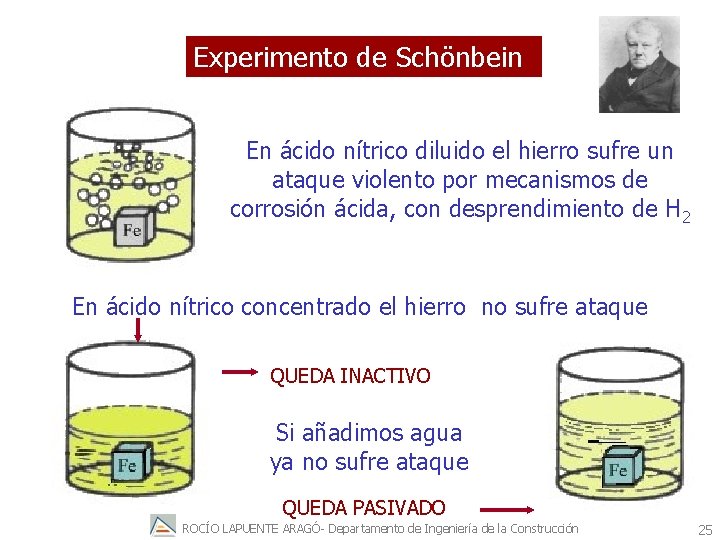
Experimento de Schönbein En ácido nítrico diluido el hierro sufre un ataque violento por mecanismos de corrosión ácida, con desprendimiento de H 2 En ácido nítrico concentrado el hierro no sufre ataque QUEDA INACTIVO Si añadimos agua ya no sufre ataque QUEDA PASIVADO ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 25

CONSIDEREMOS LA SIGUIENTES REACCIONES DEL HIERRO Fe + H 2 O Fe+3 + 3 H 2 O Fe (OH)3 + 3 H+ + 3 e. Fe (OH)3 + 3 H+ Reacción del hierro en contacto con el agua para formar el hidróxido férrico. El equilibrio de esta reacción ya no depende solamente de un potencial eléctrico que haga mover esos tres electrones, sino también del p. H. Aquí no hay transferencia de electrones, es una reacción química, no electroquímica. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 26

Estas reacciones y muchas otras son importantes para saber el estado en que se encontrará una estructura de acero, dependiendo del potencial y de la acidez del medio. Si se contara con los equilibrios de todas las reacciones posibles entre un metal y el agua tendencia que poseería ese metal ante un conjunto dado de condiciones de potencial y de p. H Si formará óxidos o hidróxidos Podríamos decir si tenderá a disolverse completamente o si el metal permanecerá intacto ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 27

En diferentes medios pueden formarse productos sólidos oxidados que pueden influir en la cinética de la corrosión. En ocasiones los productos de la corrosión pueden ser películas protectoras Estas películas son diferentes al variar el p. H Pourbaix tuvo la brillante idea de recopilar estos datos en los llamados: “DIAGRAMAS DE POURBAIX” ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 28

En los procesos de oxidación de los metales podemos encontrarnos con dos situaciones “tipo”: 1º) Mn+ + ne = M no comporta transferencia de protones. Su potencial de equilibrio no depende del p. H. En un diagrama E/p. H se representa como una línea recta paralela al eje del p. H. Fe 2+ + 2 e- Fe(s) 2º) x. A + m. H+ + ne = y. D + z. H 2 O. Incluye transferencia de electrones y también de protones. El potencial de equilibrio variará con el p. H. En un diagrama E/p. H se representa por una línea recta, de pendiente negativa, 2 Fe (OH)3 + 6 H+ + 6 e- 2 Fe + 3 H 2 O ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 29
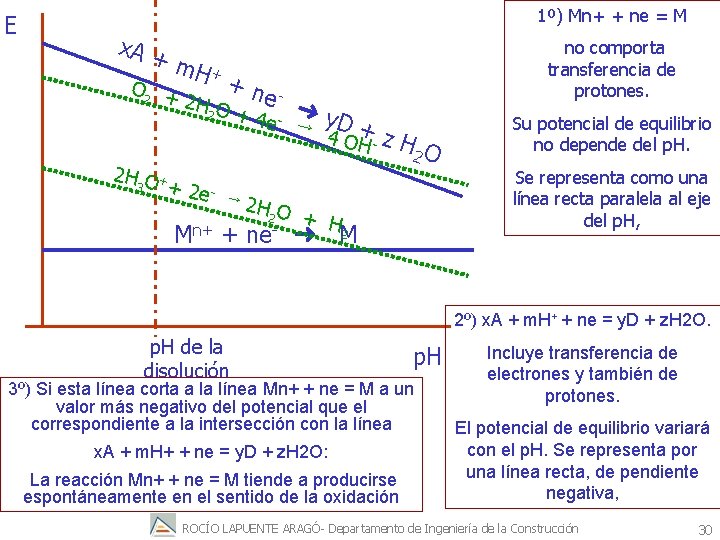
E 1º) Mn+ + ne = M x. A + m. H + +n O 2 + e ➜ 2 H O 2 + 4 e - → y. D +z 4 OH H 2 O 2 H O + 3 + 2 e - → 2 H O 2 + H n+ 2 M + ne ➜ M no comporta transferencia de protones. Su potencial de equilibrio no depende del p. H. Se representa como una línea recta paralela al eje del p. H, 2º) x. A + m. H+ + ne = y. D + z. H 2 O. p. H de la disolución p. H 3º) Si esta línea corta a la línea Mn+ + ne = M a un valor más negativo del potencial que el correspondiente a la intersección con la línea x. A + m. H+ + ne = y. D + z. H 2 O: La reacción Mn+ + ne = M tiende a producirse espontáneamente en el sentido de la oxidación Incluye transferencia de electrones y también de protones. El potencial de equilibrio variará con el p. H. Se representa por una línea recta, de pendiente negativa, ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 30
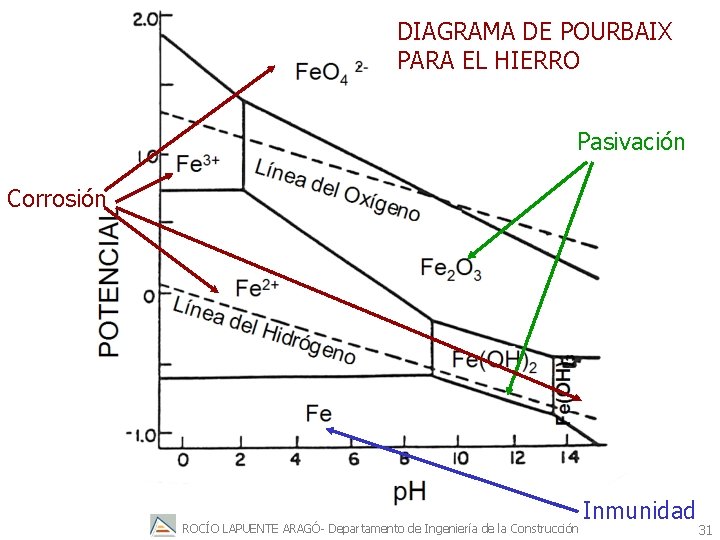
DIAGRAMA DE POURBAIX PARA EL HIERRO Pasivación Corrosión ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción Inmunidad 31

Al utilizar los diagramas potencial-p. H para decidir si un metal se corroerá o no, conviene adoptar un criterio práctico y razonable aún cuando arbitrario: calcular el potencial de equilibrio para la reacción Mn+ + ne- = M para una concentración de ion metálico de 10 -6 Moles litro-1, Esta concentración se considera que comporta una disolución "considerable", es decir que hay corrosión. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 32
Estados del hierro en el diagrama de Pourbaix, dibujado por Pourbaix ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 33
¿QUÉ ES LA PASIVACIÓN? Se entiende por pasividad la propiedad que presentan determinados metales y aleaciones de permanecer inertes en determinados medios en los cuales de acuerdo con la termodinámica deberían de comportarse como metales activos Y disolverse con velocidades altas por corrosión electroquímica. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 34
a) Formación de una capa de productos oxidados de muy pequeño espesor Compacta Adherente Baja porosidad MECANISMO b) Presencia de monocapas de oxígeno absorbidas sobre la (Menos común) superficie metálica ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 35

6. Diagramas potencial-p. H (o de Pourbaix): Usos y abusos. el último producto de una reacción de disolución de un metal puede ser: una especie iónica Fe(s) → Fe 2+ + 2 e 2 Fe + 3 H 2 O → 2 Fe (OH)3 + 6 H+ + 6 eun óxido o hidróxido sólido. Se pueden obtener los valores de. Erev A Partir de para un metal que se encuentre en equilibrio valores de - o con sus iones hidratados simples DG - o con sus productos de hidrólisis solubles - o con su óxido insoluble ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 36
el producto obtenido es aquel que proporciona los valores más negativos del potencial cualquier otro estado que se presente se transformará espontáneamente en el optimo EA menor EPILA mayor Los diagramas potencial-p. H también son útiles en este aspecto DGmás negativo (más favorable) Indican las condiciones de potencial y de p. H en que en un producto sólido es termodinámicamente estable ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 37
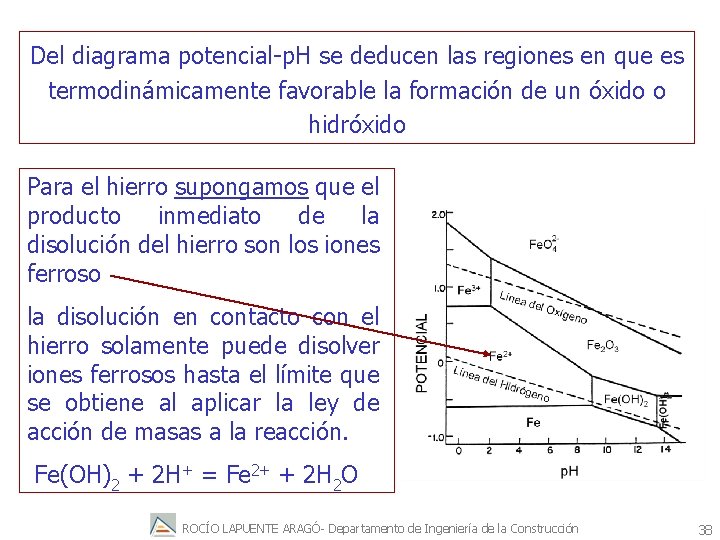
Del diagrama potencial-p. H se deducen las regiones en que es termodinámicamente favorable la formación de un óxido o hidróxido Para el hierro supongamos que el producto inmediato de la disolución del hierro son los iones ferroso la disolución en contacto con el hierro solamente puede disolver iones ferrosos hasta el límite que se obtiene al aplicar la ley de acción de masas a la reacción. Fe(OH)2 + 2 H+ = Fe 2+ + 2 H 2 O ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 38
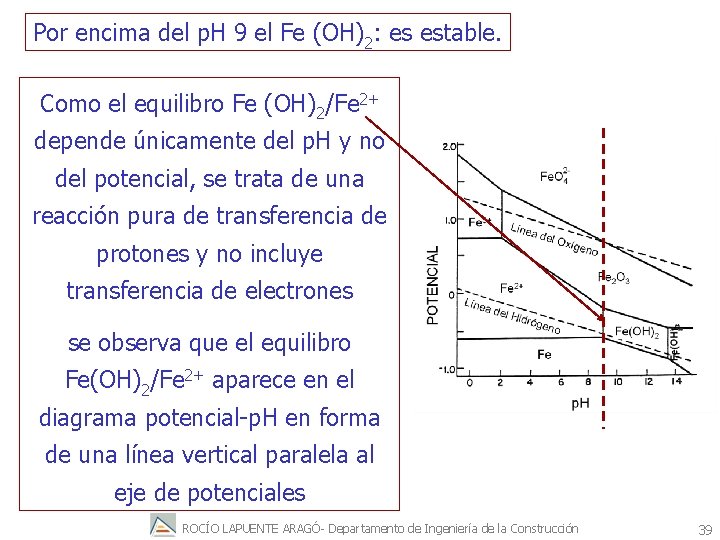
Por encima del p. H 9 el Fe (OH)2: es estable. Como el equilibro Fe (OH)2/Fe 2+ depende únicamente del p. H y no del potencial, se trata de una reacción pura de transferencia de protones y no incluye transferencia de electrones se observa que el equilibro Fe(OH)2/Fe 2+ aparece en el diagrama potencial-p. H en forma de una línea vertical paralela al eje de potenciales ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 39

Los diagramas potencial-p. H -Dan respuestas "si" o "no" acerca de si un determinado proceso de corrosión es termodinámicamente posible o no. -Resumen las reacciones de • transferencia de electrones • transferencia de protones • transferencia de electrones y protones favorecidas, por razones termodinámicas, cuando introduce un metal en una disolución en concreto ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción se 40

¡CUIDADO! Cuando un diagrama potencial-p. H indica que un metal es inmune a la corrosión, lo es siempre que el p. H en la inmediata vecindad de su superficie sea el que se supone que debe ser. Cuando el diagrama indique un determinado proceso de corrosión puede producirse espontáneamente, esto no significa que la corrosión se dé realmente en la práctica. p. H adecuado Si no se cuidan estos detalles se corre el riesgo de cometer graves errores de interpretación. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 41
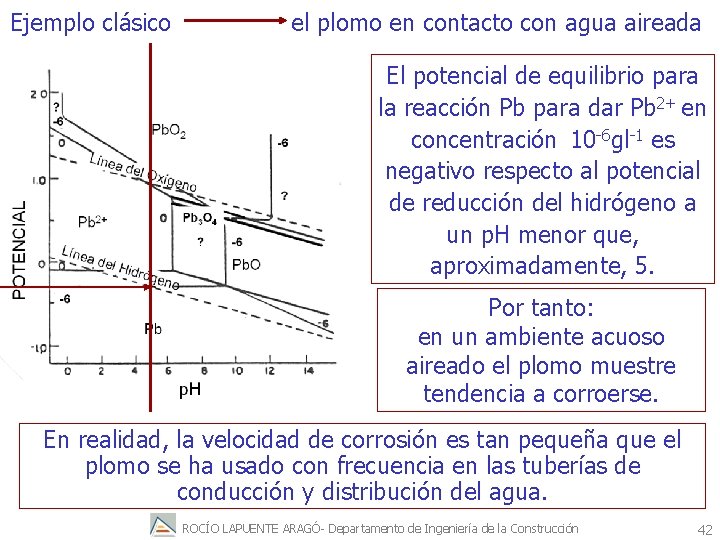
Ejemplo clásico el plomo en contacto con agua aireada El potencial de equilibrio para la reacción Pb para dar Pb 2+ en concentración 10 -6 gl-1 es negativo respecto al potencial de reducción del hidrógeno a un p. H menor que, aproximadamente, 5. Por tanto: en un ambiente acuoso aireado el plomo muestre tendencia a corroerse. En realidad, la velocidad de corrosión es tan pequeña que el plomo se ha usado con frecuencia en las tuberías de conducción y distribución del agua. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 42

La termodinámica -Define una condición la velocidad y el control previa necesaria y de un sistema que se vital para la corrosión Pero corroe sólo puede -Determina el sentido obtenerse a través de un en que una reacción estudio de la cinética general de corrosión electródica de la tenderá a producirse corrosión. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 43
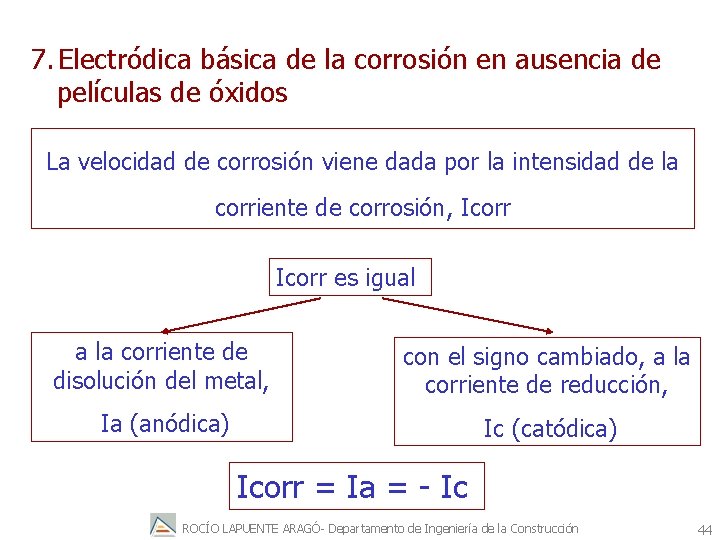
7. Electródica básica de la corrosión en ausencia de películas de óxidos La velocidad de corrosión viene dada por la intensidad de la corriente de corrosión, Icorr es igual a la corriente de disolución del metal, con el signo cambiado, a la corriente de reducción, Ia (anódica) Ic (catódica) Icorr = Ia = - Ic ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 44
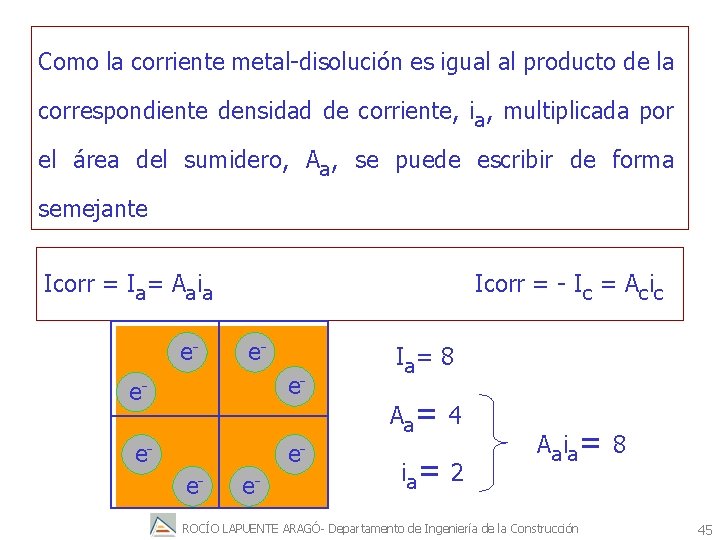
Como la corriente metal-disolución es igual al producto de la correspondiente densidad de corriente, ia, multiplicada por el área del sumidero, Aa, se puede escribir de forma semejante Icorr = Ia= Aaia e- Icorr = - Ic = Acic e- e- ee- e- Ia = 8 Aa = 4 ia = 2 Aa ia = 8 ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 45

Además existe una diferencia de potencial uniforme el potencial de corrosión en toda la superficie del metal que se corroe. Este potencial de corrosión acompaña a las corrientes de disolución del metal y de reducción Ecorr = Ec = Ea ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 46

-Si no forman películas de óxido sobre la superficie del metal que se corroe -y ninguna de las densidades de corriente queda controlada por un transporte de masa, - es decir, si no se presenta ninguna sobrevoltaje de concentración, se puede obtener una ecuación explícita para la corriente de corrosión: Icorr = (Ioa Ioc)1/2 exp F(Eoc – Eoa)/4 RT (condiciones superideales ) ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 47
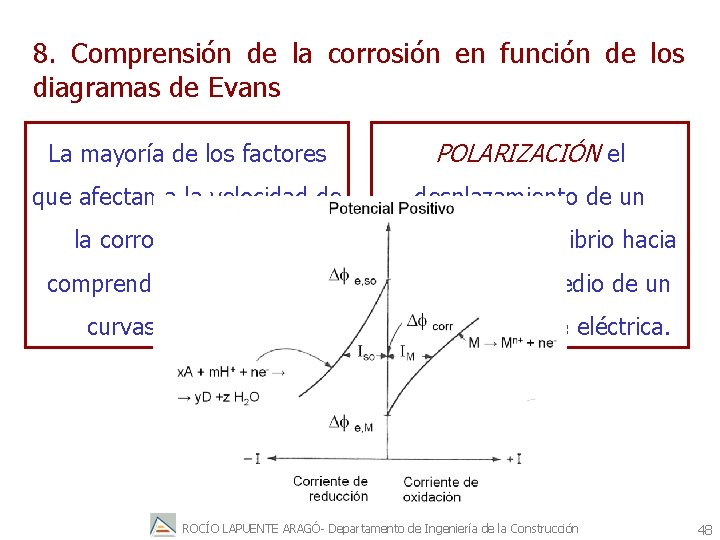
8. Comprensión de la corrosión en función de los diagramas de Evans La mayoría de los factores POLARIZACIÓN el que afectan a la velocidad de desplazamiento de un la corrosión se puede potencial de equilibrio hacia comprender a partir de las otro valor por medio de un curvas polarización flujo de corriente eléctrica. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 48
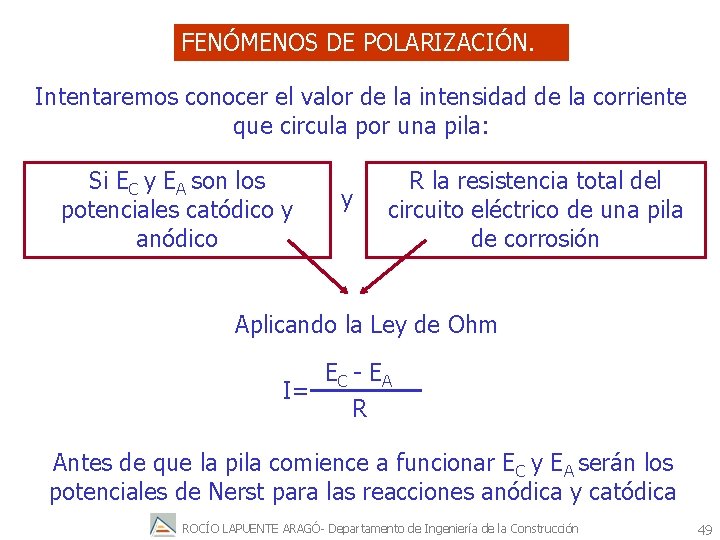
FENÓMENOS DE POLARIZACIÓN. Intentaremos conocer el valor de la intensidad de la corriente que circula por una pila: Si EC y EA son los potenciales catódico y anódico y R la resistencia total del circuito eléctrico de una pila de corrosión Aplicando la Ley de Ohm EC - E A I= R Antes de que la pila comience a funcionar EC y EA serán los potenciales de Nerst para las reacciones anódica y catódica ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 49
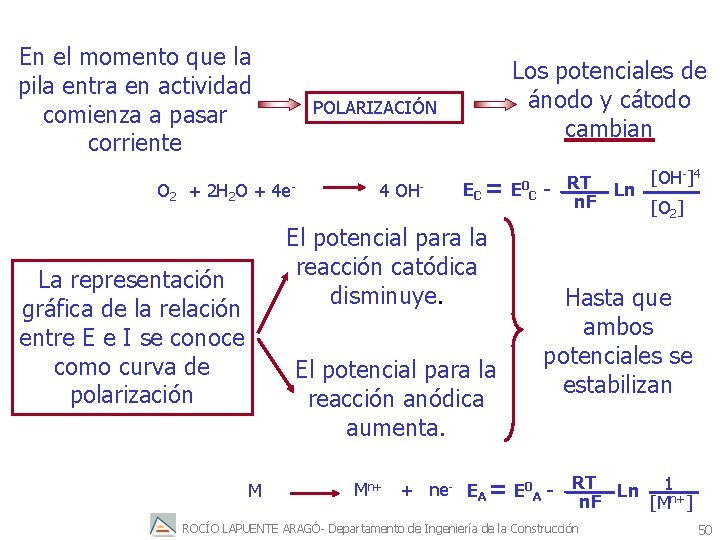
En el momento que la pila entra en actividad comienza a pasar corriente O 2 + 2 H 2 O + Los potenciales de ánodo y cátodo cambian POLARIZACIÓN 4 e- 4 OH- EC = El potencial para la reacción catódica disminuye. La representación gráfica de la relación entre E e I se conoce como curva de polarización El potencial para la reacción anódica aumenta. M E 0 [OH-]4 RT Ln C n. F [O 2] Hasta que ambos potenciales se estabilizan Mn+ + ne- EA = E 0 A - RT Ln 1 n. F [Mn+] ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 50
![EC = E 0 C - - 4 RT Ln [OH ] n. F EC = E 0 C - - 4 RT Ln [OH ] n. F](http://slidetodoc.com/presentation_image/49b413fb9bab4c073eb0663f82186bce/image-51.jpg)
EC = E 0 C - - 4 RT Ln [OH ] n. F [O 2] EA = E 0 A - RT Ln 1 n+ n. F [M ] E EC - 4 OH - - O 2 + 2 H O 2 + 4 e n+ + ne M M EA -I -ICORR +ICORR ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción +I 51

EVANS Se le debe a Evans el método gráfico que permite analizar la relación entre la velocidad de corrosión y la polarización de los electrodos El método es muy sencillo y consiste en la superposición de las dos curvas de polarización (anódica de disolución metálica y catódica de reducción) Para ello los potenciales se representan frente a │I│ ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 52
Doblamos por el eje… ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 53
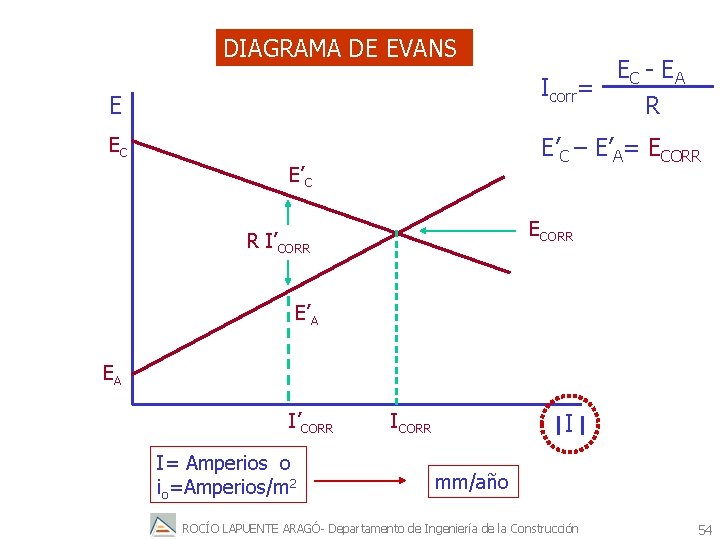
DIAGRAMA DE EVANS E EC - E A Icorr= R EC E’C – E’A= ECORR E’C ECORR R I’CORR E’A EA I’CORR I= Amperios o io=Amperios/m 2 I ICORR mm/año ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 54

Desde un punto de vista cinético, en un sistema cualquiera en el cual tenga lugar el fenómeno de corrosión, existe un balance perfecto entre las reacciones anódicas y catódicas sobre la superficie del metal. Según los diagramas de EVANS ambos potenciales de equilibrio son desplazados a un valor común, el potencial de corrosión, en el cual la velocidad de oxidación del metal (corrosión) es igual a la velocidad de reducción. Por lo general, cuando medimos el potencial de un metal sumergido en un medio agresivo, contra un electrodo de referencia, lo que realmente medimos es el potencial de corrosión mixto, Ecorr. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 55
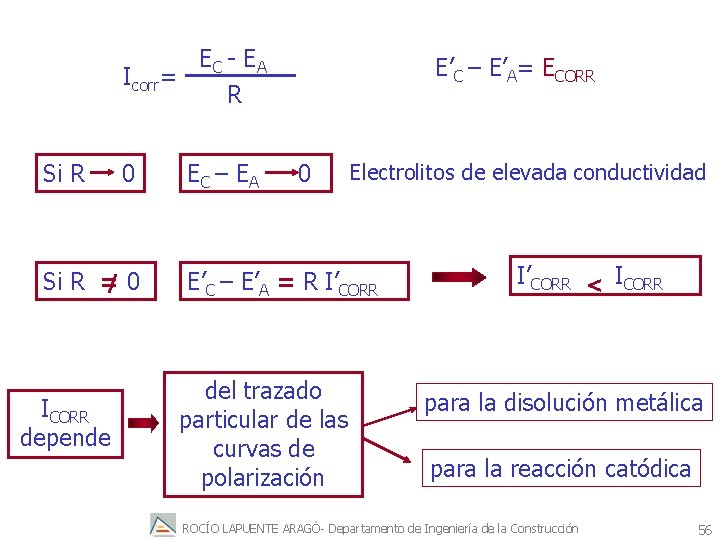
EC - E A Icorr= R Si R 0 Si R = 0 ICORR depende EC – E A E’C – E’A= ECORR 0 Electrolitos de elevada conductividad E’C – E’A = R I’CORR del trazado particular de las curvas de polarización I’CORR < ICORR para la disolución metálica para la reacción catódica ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 56
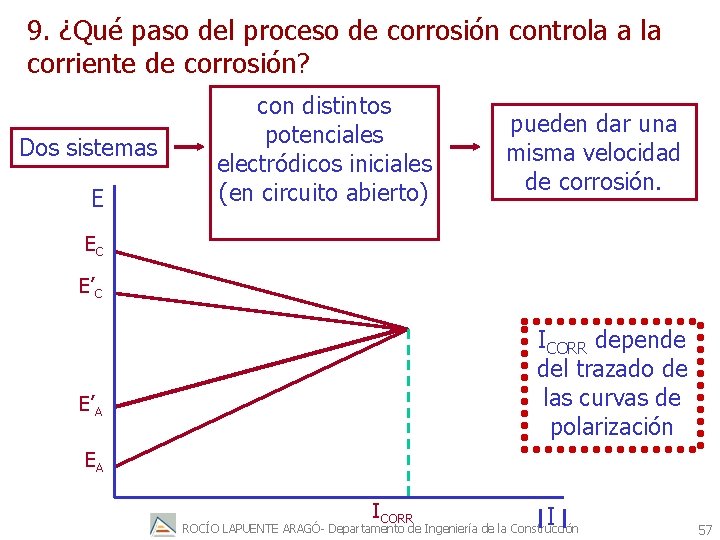
9. ¿Qué paso del proceso de corrosión controla a la corriente de corrosión? Dos sistemas E con distintos potenciales electródicos iniciales (en circuito abierto) pueden dar una misma velocidad de corrosión. EC E’C ICORR depende del trazado de las curvas de polarización E’A EA ICORR I ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 57
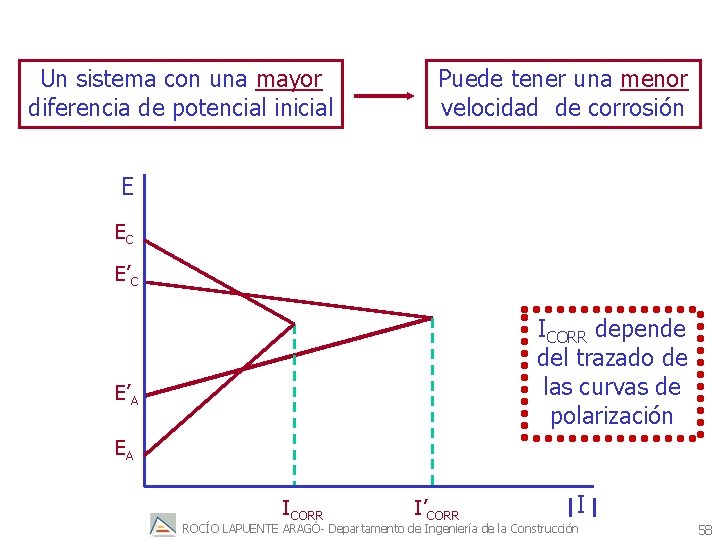
Un sistema con una mayor diferencia de potencial inicial Puede tener una menor velocidad de corrosión E EC E’C ICORR depende del trazado de las curvas de polarización E’A EA ICORR I’CORR I ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 58
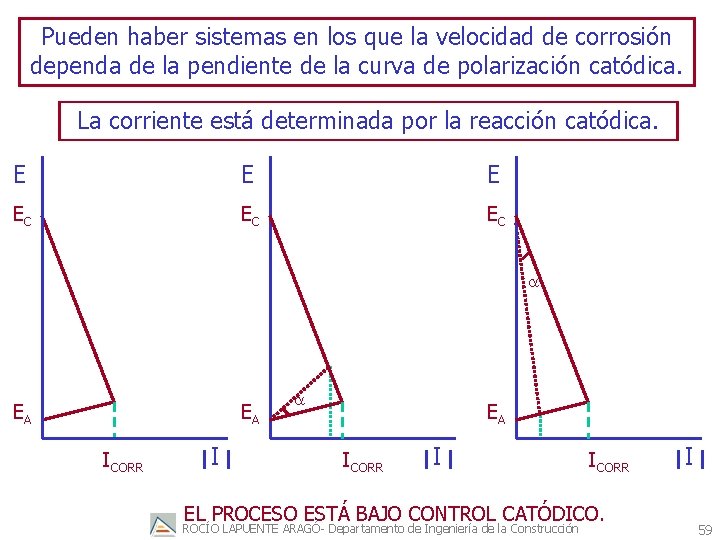
Pueden haber sistemas en los que la velocidad de corrosión dependa de la pendiente de la curva de polarización catódica. La corriente está determinada por la reacción catódica. E EC EC EC a EA EA ICORR I a EA ICORR I ICORR EL PROCESO ESTÁ BAJO CONTROL CATÓDICO. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción I 59
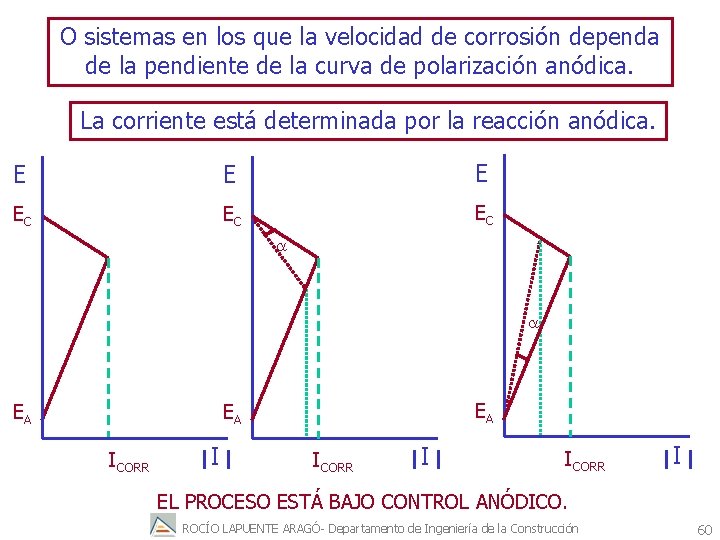
O sistemas en los que la velocidad de corrosión dependa de la pendiente de la curva de polarización anódica. La corriente está determinada por la reacción anódica. E EC EC EC a a EA EA EA ICORR I EL PROCESO ESTÁ BAJO CONTROL ANÓDICO. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 60
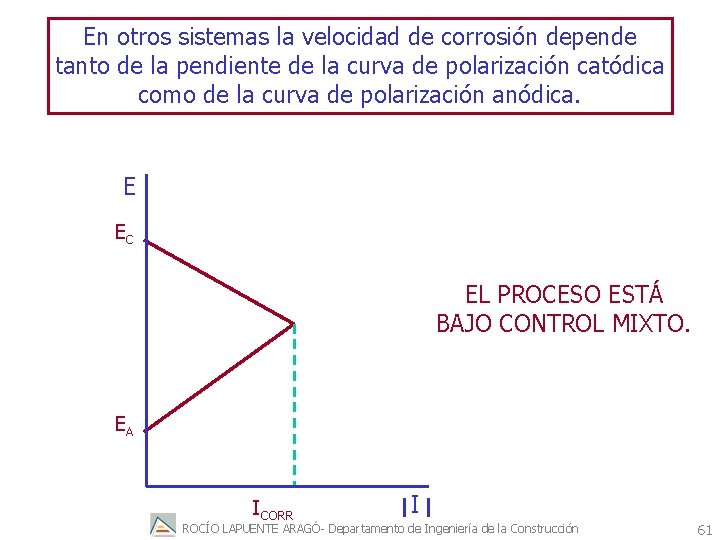
En otros sistemas la velocidad de corrosión depende tanto de la pendiente de la curva de polarización catódica como de la curva de polarización anódica. E EC EL PROCESO ESTÁ BAJO CONTROL MIXTO. EA ICORR I ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 61
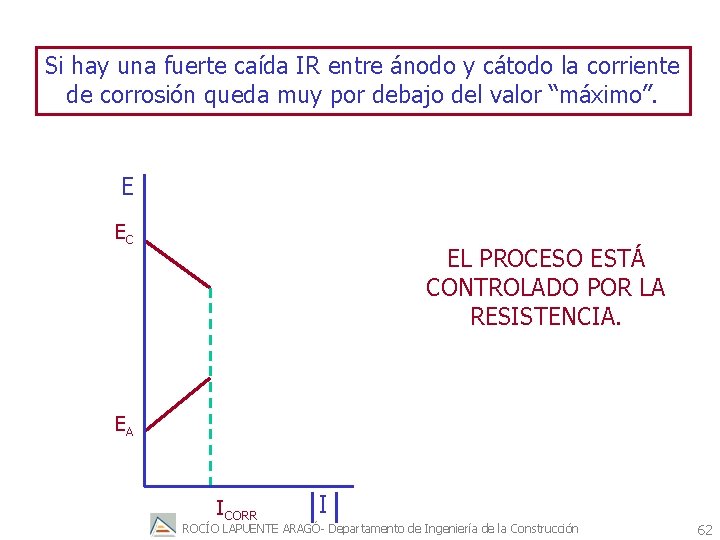
Si hay una fuerte caída IR entre ánodo y cátodo la corriente de corrosión queda muy por debajo del valor “máximo”. E EC EL PROCESO ESTÁ CONTROLADO POR LA RESISTENCIA. EA ICORR I ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 62

CURVA “REAL” DE POLARIZACIÓN ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 63
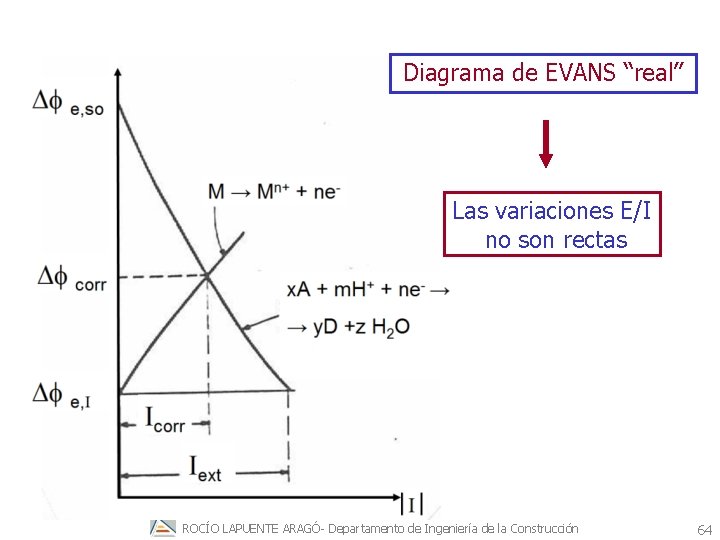
Diagrama de EVANS “real” Las variaciones E/I no son rectas ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 64
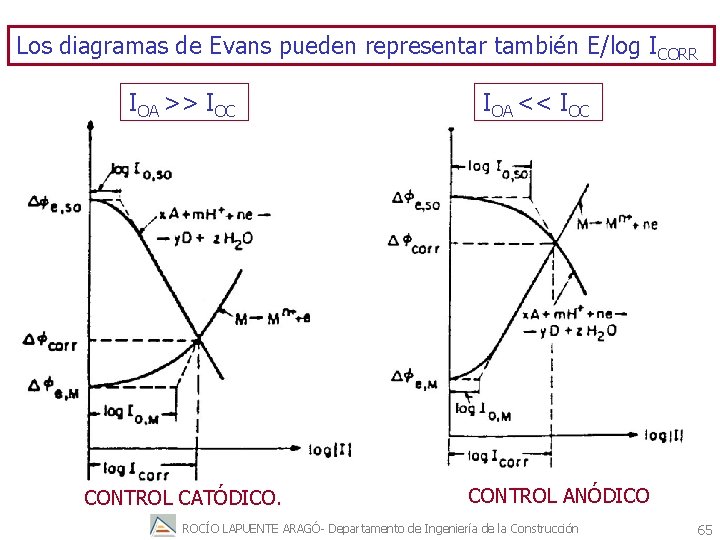
Los diagramas de Evans pueden representar también E/log ICORR IOA >> IOC CONTROL CATÓDICO. IOA << IOC CONTROL ANÓDICO ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 65
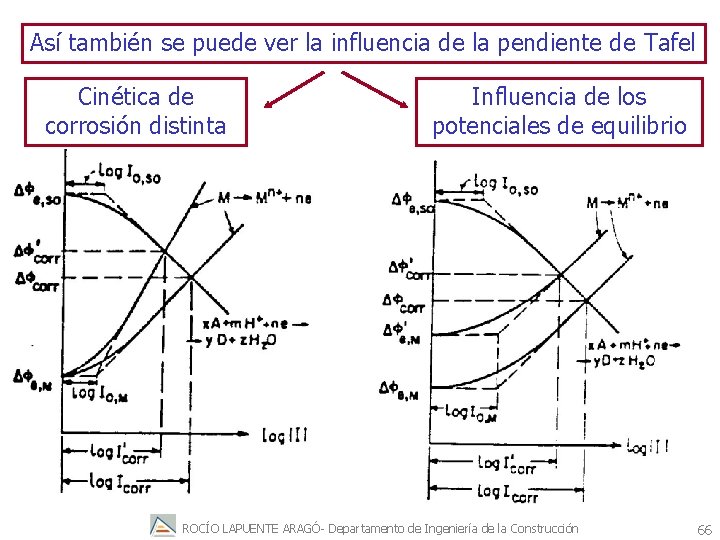
Así también se puede ver la influencia de la pendiente de Tafel Cinética de corrosión distinta Influencia de los potenciales de equilibrio ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 66
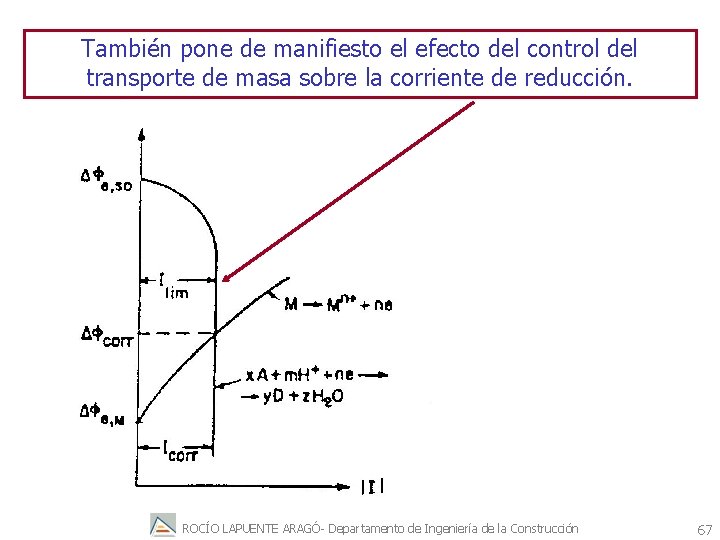
También pone de manifiesto el efecto del control del transporte de masa sobre la corriente de reducción. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 67

10. Algunos ejemplos comunes de corrosión. En la carrocería de los coches… El centro es el cátodo y lo que lo rodea es el ánodo. Por eso aumenta la zona dañada CORROSIÓN POR AIREACIÓN DIFERENCIAL ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 68
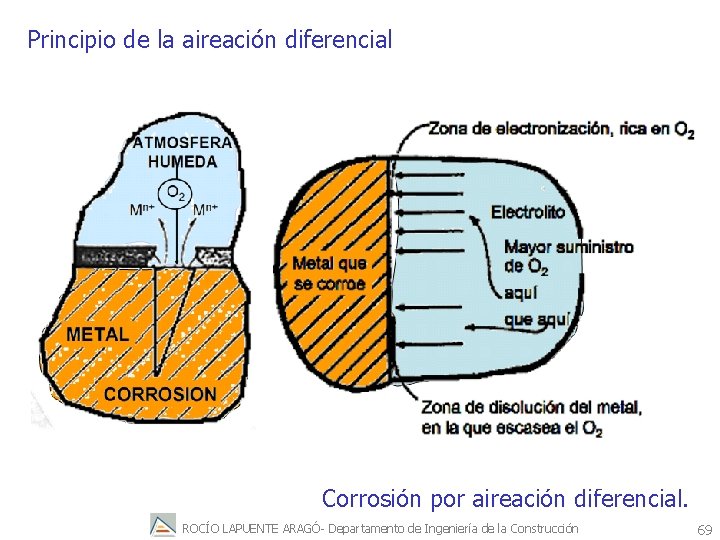
Principio de la aireación diferencial Corrosión por aireación diferencial. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 69
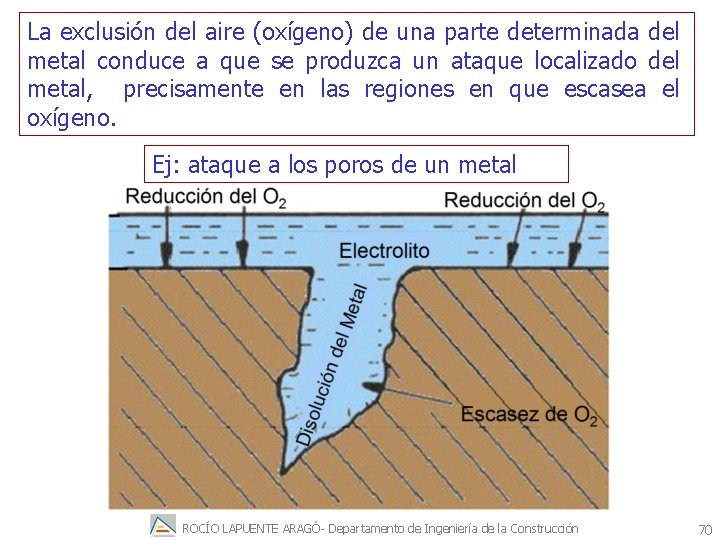
La exclusión del aire (oxígeno) de una parte determinada del metal conduce a que se produzca un ataque localizado del metal, precisamente en las regiones en que escasea el oxígeno. Ej: ataque a los poros de un metal ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 70
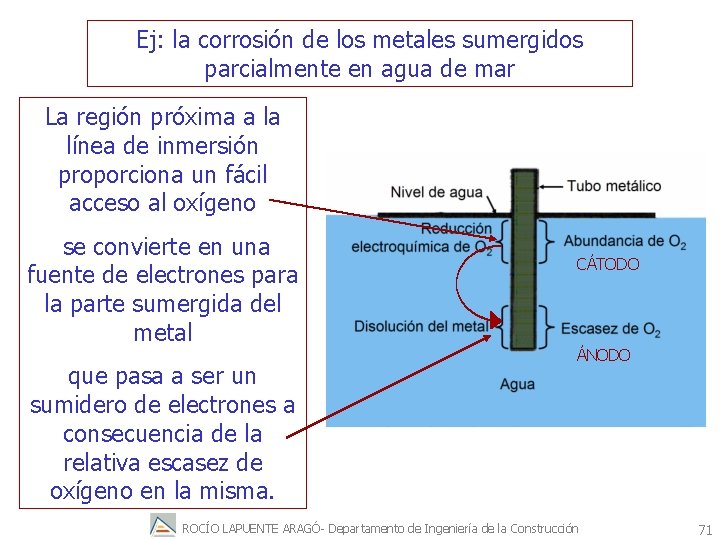
Ej: la corrosión de los metales sumergidos parcialmente en agua de mar La región próxima a la línea de inmersión proporciona un fácil acceso al oxígeno se convierte en una fuente de electrones para la parte sumergida del metal que pasa a ser un sumidero de electrones a consecuencia de la relativa escasez de oxígeno en la misma. CÁTODO ÁNODO ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 71
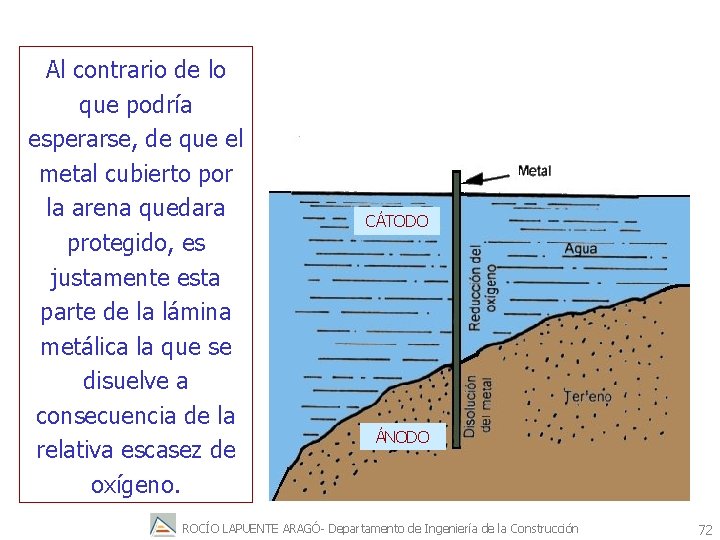
Al contrario de lo que podría esperarse, de que el metal cubierto por la arena quedara protegido, es justamente esta parte de la lámina metálica la que se disuelve a consecuencia de la relativa escasez de oxígeno. CÁTODO ÁNODO ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 72
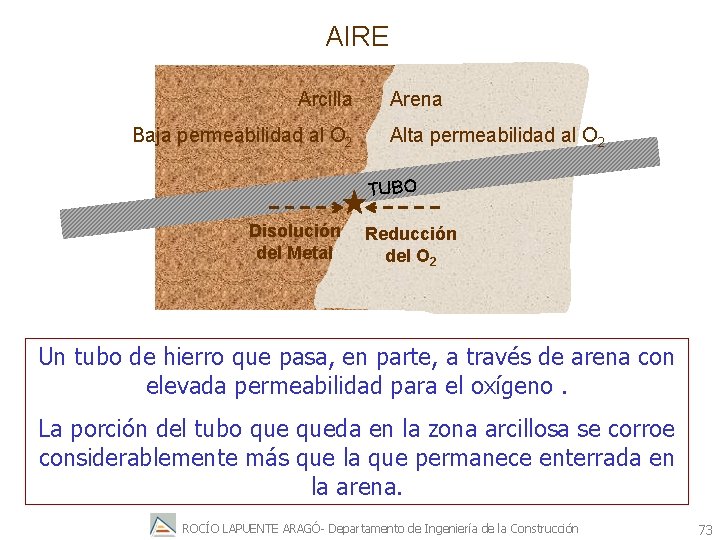
AIRE Arcilla Baja permeabilidad al O 2 Arena Alta permeabilidad al O 2 TUBO Disolución del Metal Reducción del O 2 Un tubo de hierro que pasa, en parte, a través de arena con elevada permeabilidad para el oxígeno. La porción del tubo queda en la zona arcillosa se corroe considerablemente más que la que permanece enterrada en la arena. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 73
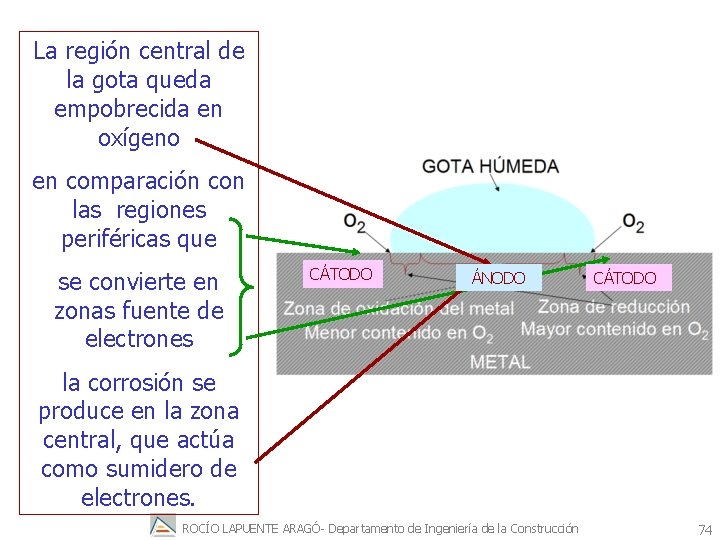
La región central de la gota queda empobrecida en oxígeno en comparación con las regiones periféricas que se convierte en zonas fuente de electrones CÁTODO ÁNODO CÁTODO la corrosión se produce en la zona central, que actúa como sumidero de electrones. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 74
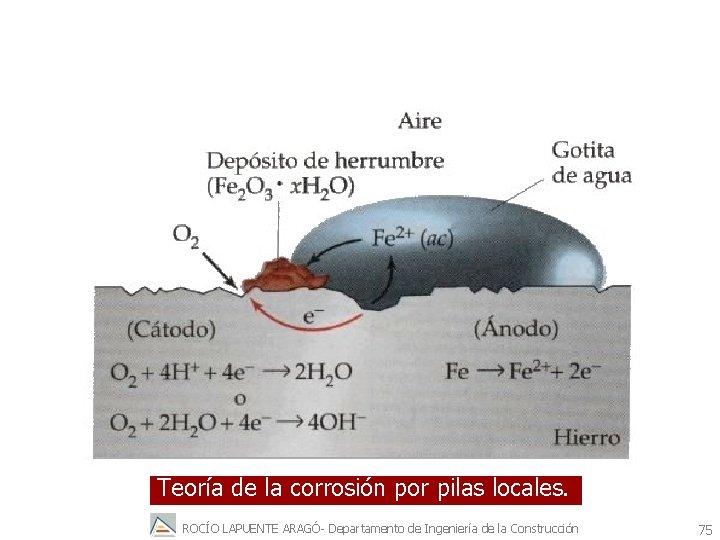
Teoría de la corrosión por pilas locales. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 75

CORROSIÓN GALVÁNICA. La corrosión también puede ser debida al contacto de dos metales diferentes al tener diferentes potenciales de equilibrio aparecen en posiciones diferenciadas en la serie electroquímica presentan una diferente velocidad de corrosión en un ambiente dado aluminio y cobre ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 76
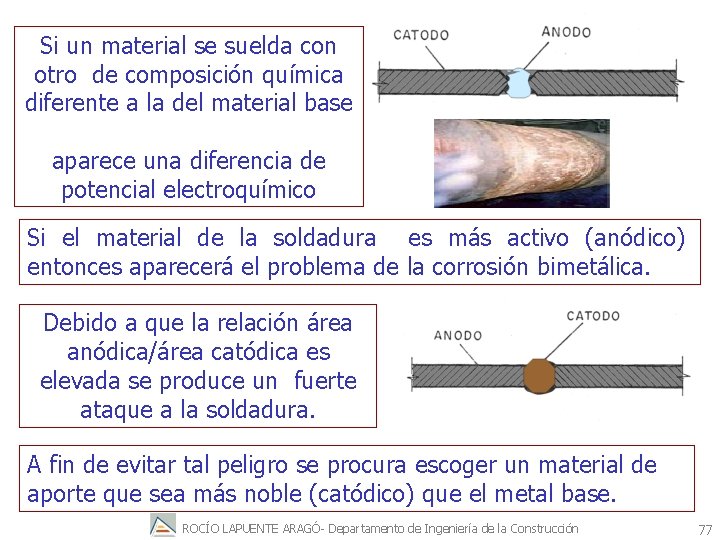
Si un material se suelda con otro de composición química diferente a la del material base aparece una diferencia de potencial electroquímico Si el material de la soldadura es más activo (anódico) entonces aparecerá el problema de la corrosión bimetálica. Debido a que la relación área anódica/área catódica es elevada se produce un fuerte ataque a la soldadura. A fin de evitar tal peligro se procura escoger un material de aporte que sea más noble (catódico) que el metal base. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 77
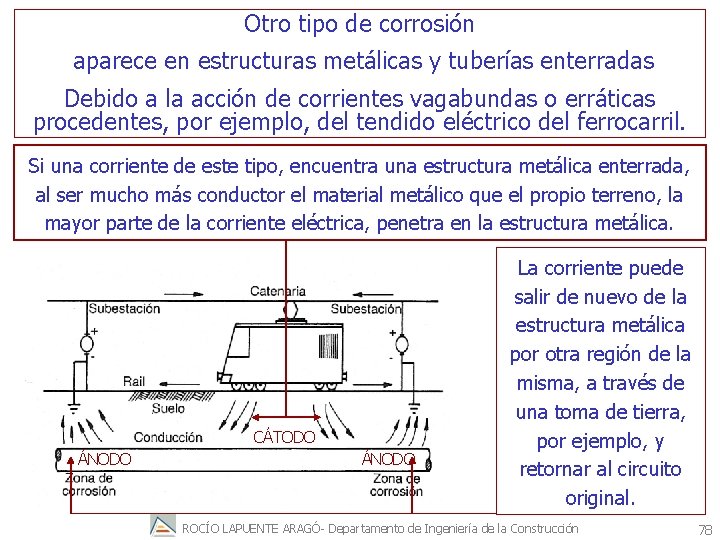
Otro tipo de corrosión aparece en estructuras metálicas y tuberías enterradas Debido a la acción de corrientes vagabundas o erráticas procedentes, por ejemplo, del tendido eléctrico del ferrocarril. Si una corriente de este tipo, encuentra una estructura metálica enterrada, al ser mucho más conductor el material metálico que el propio terreno, la mayor parte de la corriente eléctrica, penetra en la estructura metálica. CÁTODO ÁNODO La corriente puede salir de nuevo de la estructura metálica por otra región de la misma, a través de una toma de tierra, por ejemplo, y retornar al circuito original. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 78

11. Métodos de protección frente a la corrosión ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 79

11. 1. Inhibición de la corrosión por adición de sustancias al ambiente electroquímico en que se encuentra el metal que se corroe. En primer lugar se puede intentar reducir las densidades de corriente de canje de las reacciones de disolución del metal (oxidación) y de reducción. Por ejemplo, si la reacción de desprendimiento de hidrógeno coincide con la de reducción, la adición de compuestos de fósforo, de arsénico, o de antimonio (por ejemplo As 2 O 3) producirá una reducción de la densidad de la corriente de canje para el desprendimiento de hidrógeno O si la reacción que se produce en las zonas fuente de electrones es la reducción del oxígeno, es posible entonces, mediante la adición de sustancias que reaccionen con el oxígeno disuelto, reducir la concentración de O 2 y, con ello, también la densidad de la corriente de canje para la reducción del oxígeno. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 80

Dos sustancias que actúan de esta forma son la hidrazina, N 2 H 4 + 5 O 2 4 NO 2 - + 4 H+ + 2 H 2 O y los iones sulfito, SO 322 SO 32 - + O 2 2 SO 42 Es posible reducir la densidad de corriente para la reacción de disolución del metal mediante la adición de compuestos que sean absorbidos sobre las zonas anódicas del metal sometido a corrosión (creando recubrimientos) con lo que se frenará la reacción de disolución del metal De forma alternativa o junto con las otras opciones ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 81

El número de recubrimientos es casi ilimitado Los de pequeño espesor que pueden ser: de tipo inorgánico y capas de conversión (esmaltado, capas de cemento por proyección, Anodizado, Fosfatado, cromatados, etc); de tipo orgánico (pinturas, lacas, barnices, brea, alquitrán betún, etc). ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 82

Otro tipo de recubrimientos de fuerte espesor pueden ser por ejemplo: sistemas de pintura en capa gruesa, recubrimientos plásticos, recubrimientos bituminosos, cintas adhesivas y recubrimientos de hormigón. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 83

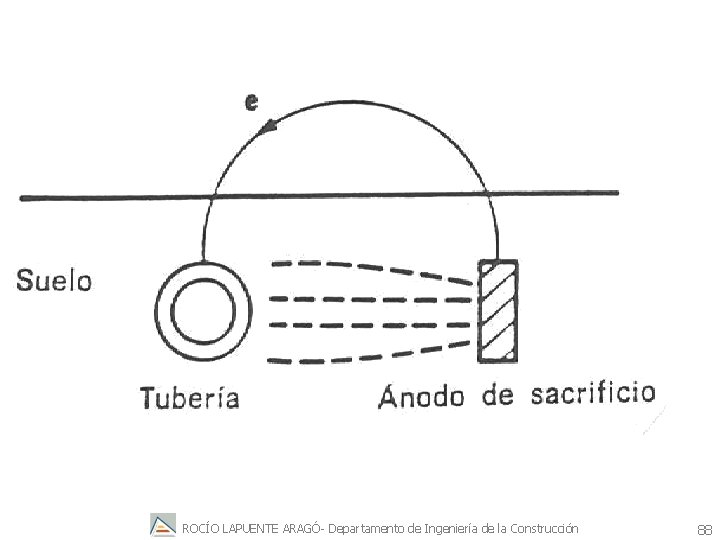
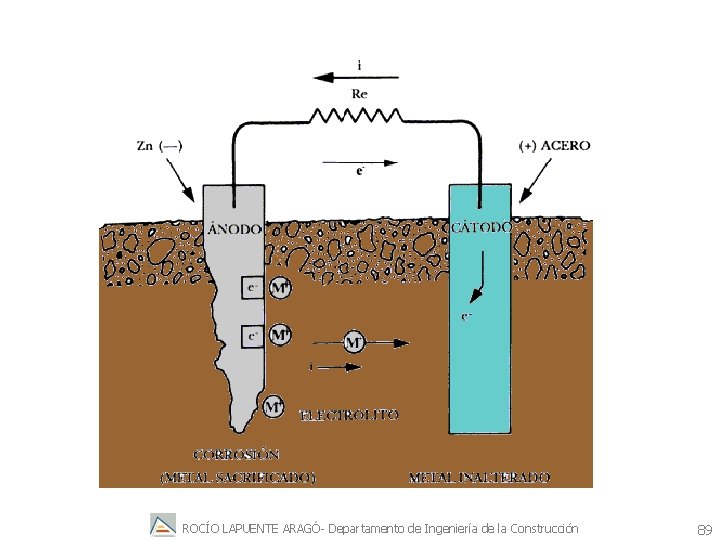
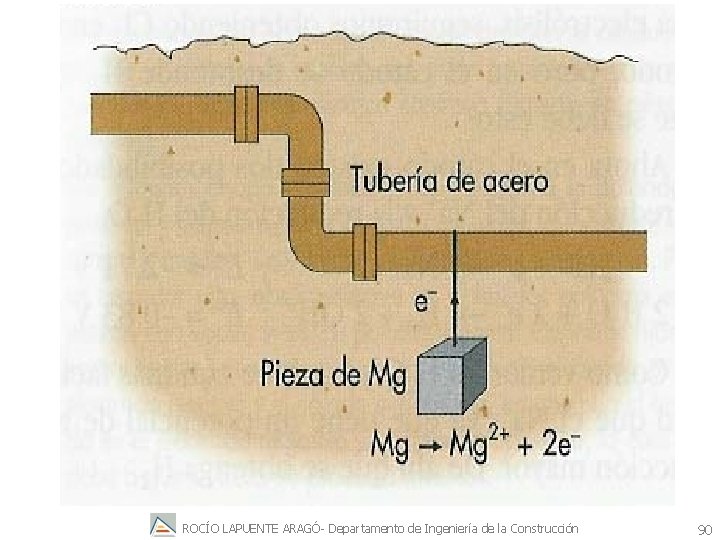
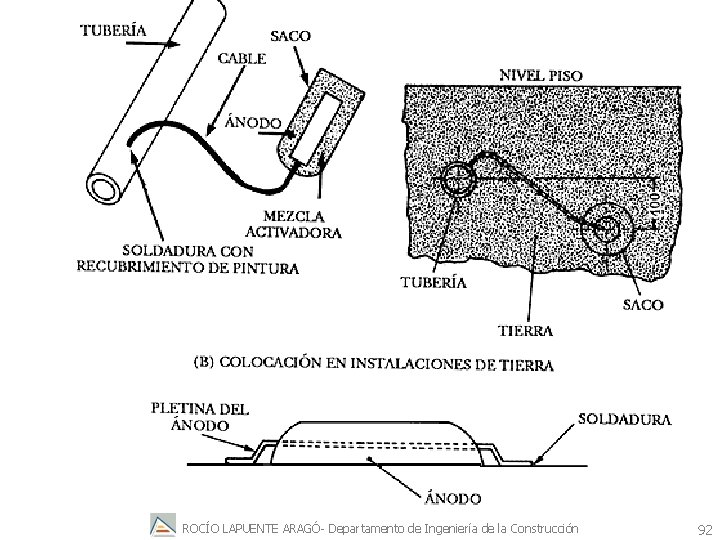
11. 2. Protección catódica mediante ánodo de sacrificio se sumerge en el ambiente corrosivo un metal auxiliar que posea un potencial de equilibrio negativo respecto al metal que se corroe y que se conecta en cortocircuito con el metal que se ha de proteger. En este caso, el metal auxiliar funcionará como sumidero de electrones (ánodo) y se sacrificará disolviéndose (de aquí el nombre ánodo de sacrificio). Además, el metal que se puede corroer actuará como electrodo fuente de electrones para la reacción de reducción, que en otro caso habría producido su corrosión. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 84
e- e- eee- M+ M+ M+ ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 85
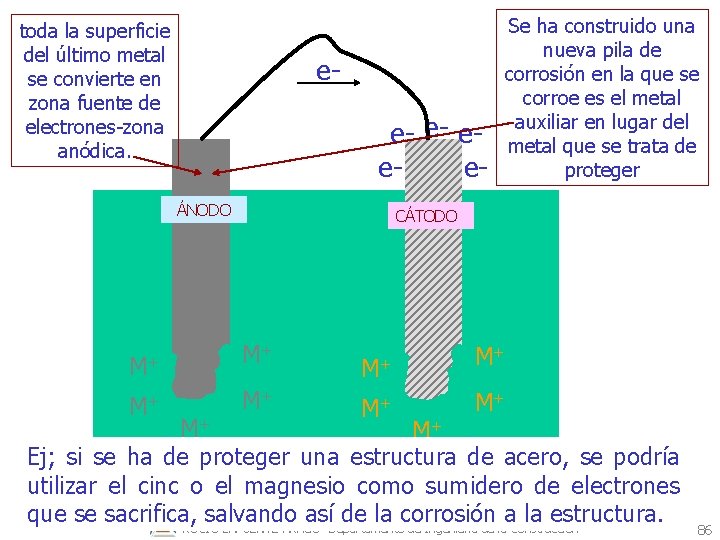
toda la superficie del último metal se convierte en zona fuente de electrones-zona anódica. ee- e- eeeÁNODO Se ha construido una nueva pila de corrosión en la que se corroe es el metal auxiliar en lugar del metal que se trata de proteger CÁTODO M+ M+ M+ Ej; si se ha de proteger una estructura de acero, se podría utilizar el cinc o el magnesio como sumidero de electrones que se sacrifica, salvando así de la corrosión a la estructura. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 86
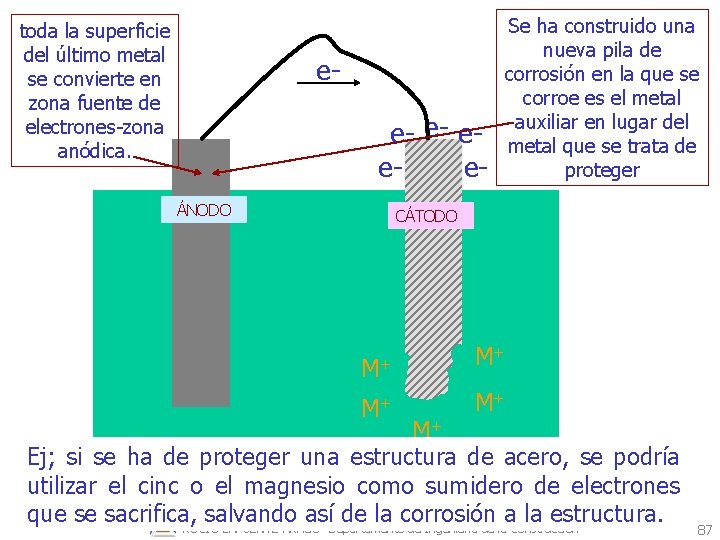
toda la superficie del último metal se convierte en zona fuente de electrones-zona anódica. ee- e- eeeÁNODO Se ha construido una nueva pila de corrosión en la que se corroe es el metal auxiliar en lugar del metal que se trata de proteger CÁTODO M+ M+ M+ Ej; si se ha de proteger una estructura de acero, se podría utilizar el cinc o el magnesio como sumidero de electrones que se sacrifica, salvando así de la corrosión a la estructura. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 87
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 88
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 89
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 90

ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 91
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 92

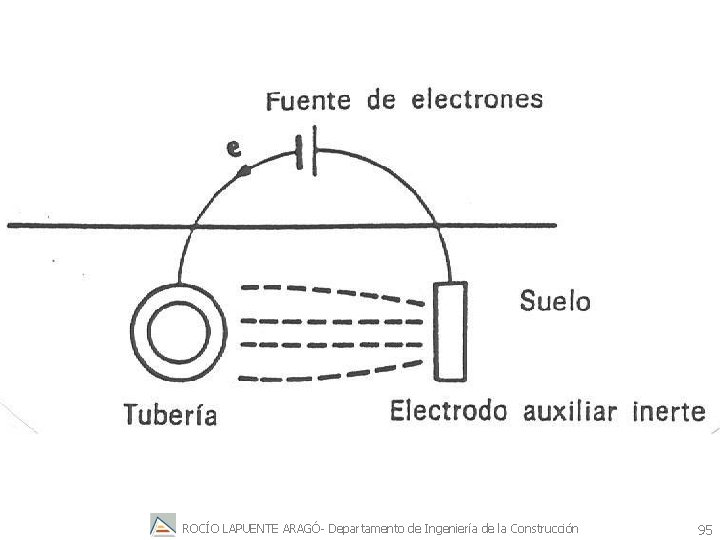
Protección catódica por corriente impresa Los electrones también pueden provenir de una fuente de corriente externa (es decir, de una fuente de corriente eléctrica). Sin embargo, se ha de completar el circuito eléctrico y a este fin es posible insertar un electrodo auxiliar inerte para proporcionar una vía de retorno para la corriente de electrones La fuente externa se ajusta de forma que la diferencia de potencial entre el metal y su ambiente se haga negativa respecto a su potencial de equilibrio. Así, el metal que se ha de proteger contra la corrosión actúa como sumidero de electrones para la reacción de reducción y el segundo electrodo actuará como fuente electrones para alguna reacción de oxidación. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 93
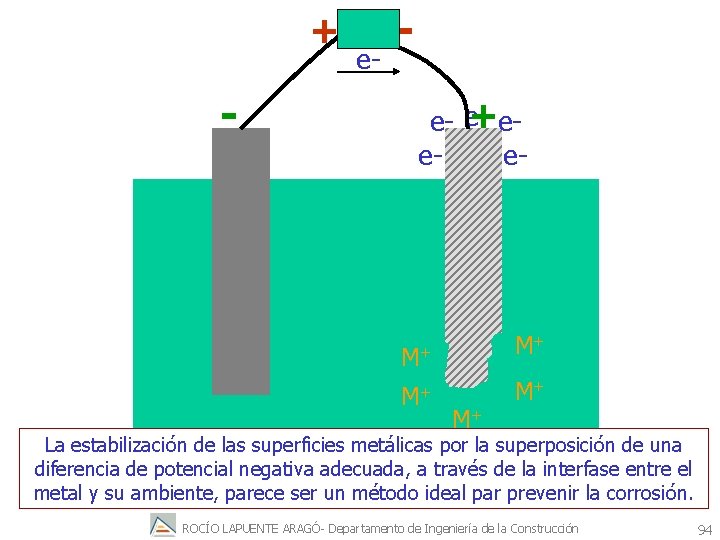
+ - e- +ee- eee- M+ M+ M+ La estabilización de las superficies metálicas por la superposición de una diferencia de potencial negativa adecuada, a través de la interfase entre el metal y su ambiente, parece ser un método ideal par prevenir la corrosión. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 94
ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 95
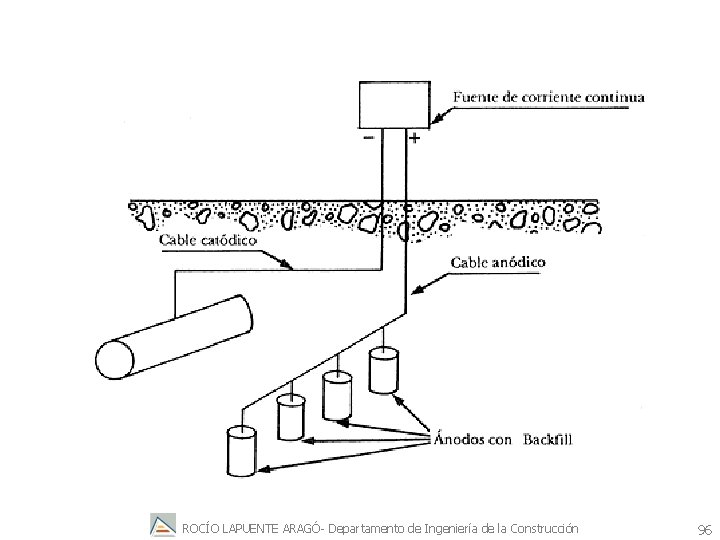
CATÓDICA POR CORRIENTE IMPRESA ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 96

ASPECTOS MENOS FAVORABLES 1. -Es posible que el consumo de energía resulte tan grande que no sea práctico. 2. -Es importante que la diferencia de potencial a través de toda la interfase entre el metal que se ha de proteger y su ambiente se desplace por debajo del potencial de equilibrio. Supongamos que la corriente que circula a través del circuito no se distribuye uniformemente en el metal que se corroe. con frecuencia es mejor sufrir un proceso de disolución muy lento, uniforme, que un ataque localizado con perforación, por ejemplo, en un oleoducto. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 97
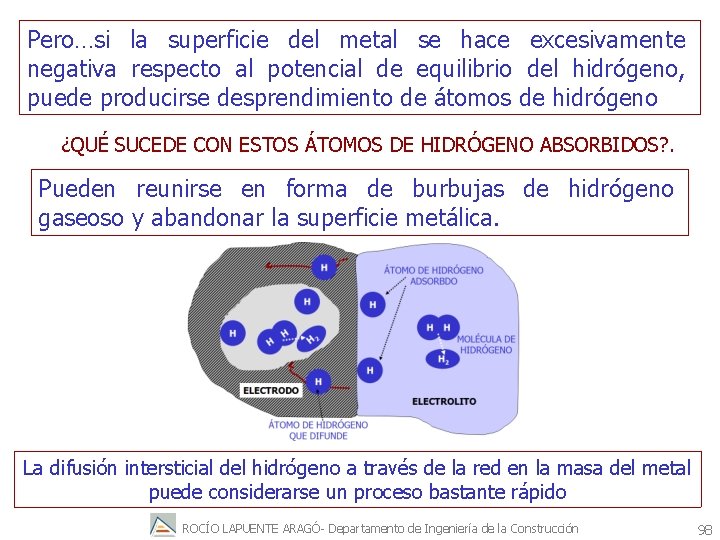
Pero…si la superficie del metal se hace excesivamente negativa respecto al potencial de equilibrio del hidrógeno, puede producirse desprendimiento de átomos de hidrógeno ¿QUÉ SUCEDE CON ESTOS ÁTOMOS DE HIDRÓGENO ABSORBIDOS? . Pueden reunirse en forma de burbujas de hidrógeno gaseoso y abandonar la superficie metálica. La difusión intersticial del hidrógeno a través de la red en la masa del metal puede considerarse un proceso bastante rápido ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 98

la tensión por tracción → aumenta la solubilidad del hidrógeno el campo de tensión por comprensión → decrezca la solubilidad ya pequeña. Por tanto A mayor deformación de la red o distorsión, mayor será la concentración del hidrógeno. Todas las imperfecciones que existen en los cristales son regiones de distorsión o tensión. El hidrógeno absorbido encuentra su camino y se concentra en dichas imperfecciones. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 99
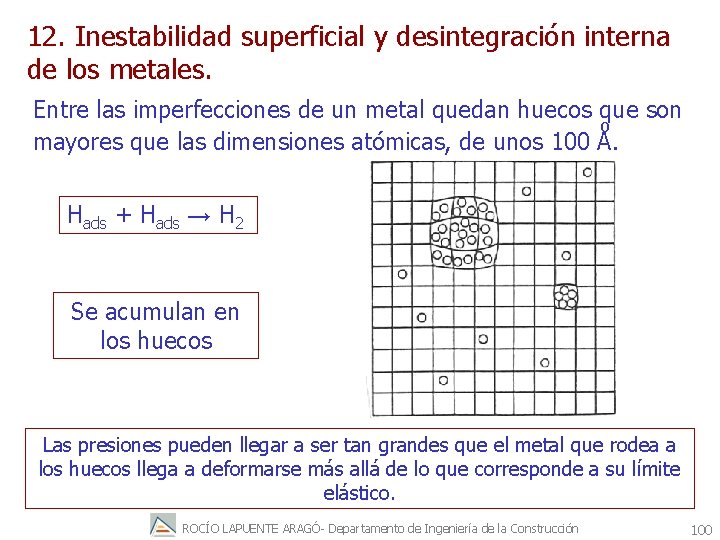
12. Inestabilidad superficial y desintegración interna de los metales. Entre las imperfecciones de un metal quedan huecos que son º mayores que las dimensiones atómicas, de unos 100 A. Hads + Hads → H 2 Se acumulan en los huecos Las presiones pueden llegar a ser tan grandes que el metal que rodea a los huecos llega a deformarse más allá de lo que corresponde a su límite elástico. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 100
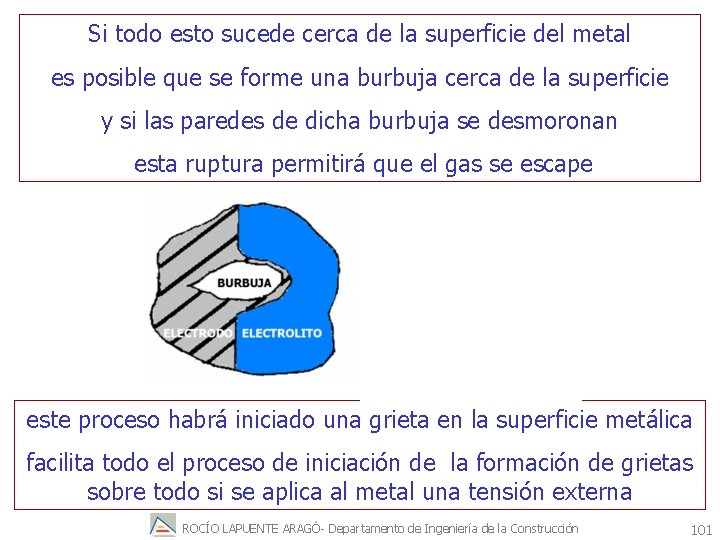
Si todo esto sucede cerca de la superficie del metal es posible que se forme una burbuja cerca de la superficie y si las paredes de dicha burbuja se desmoronan esta ruptura permitirá que el gas se escape este proceso habrá iniciado una grieta en la superficie metálica facilita todo el proceso de iniciación de la formación de grietas sobre todo si se aplica al metal una tensión externa ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 101
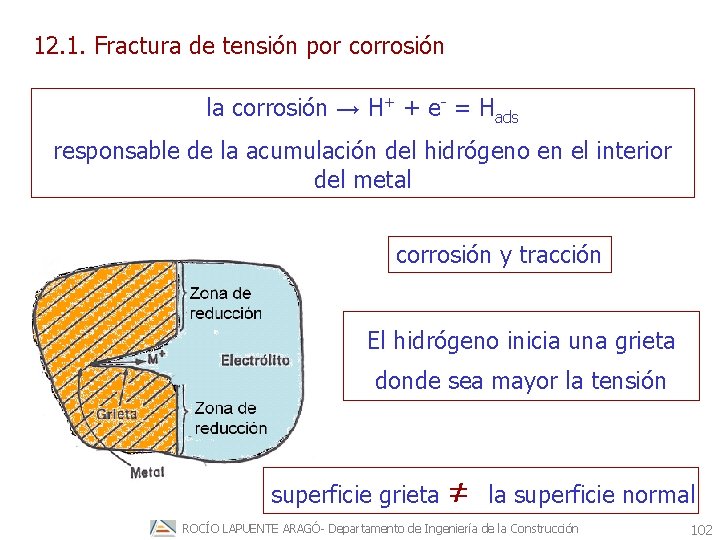
12. 1. Fractura de tensión por corrosión la corrosión → H+ + e- = Hads responsable de la acumulación del hidrógeno en el interior del metal corrosión y tracción El hidrógeno inicia una grieta donde sea mayor la tensión superficie grieta ≠ la superficie normal ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 102
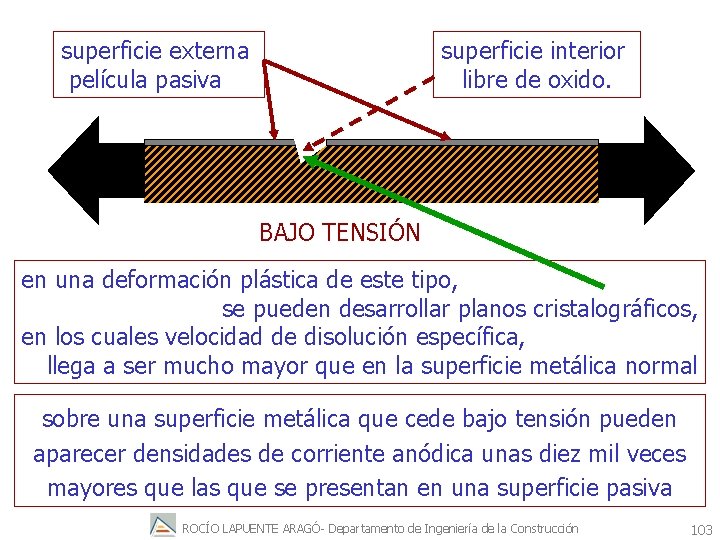
superficie externa película pasiva superficie interior libre de oxido. BAJO TENSIÓN en una deformación plástica de este tipo, se pueden desarrollar planos cristalográficos, en los cuales velocidad de disolución específica, llega a ser mucho mayor que en la superficie metálica normal sobre una superficie metálica que cede bajo tensión pueden aparecer densidades de corriente anódica unas diez mil veces mayores que las que se presentan en una superficie pasiva ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 103
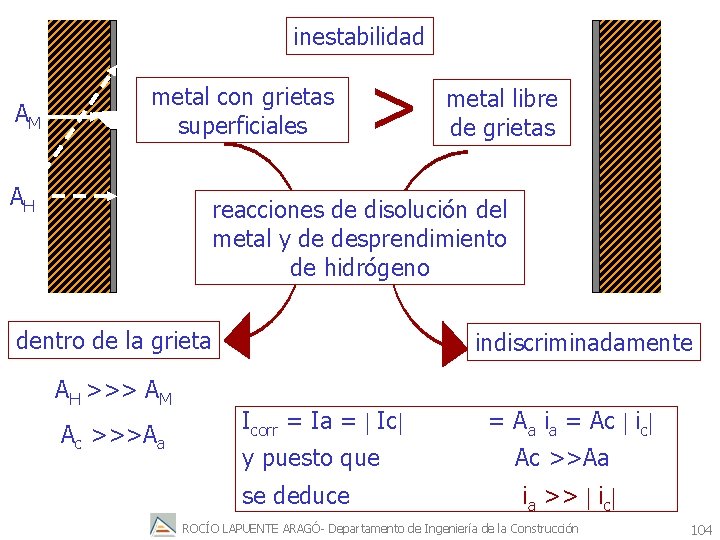
inestabilidad AM metal con grietas superficiales AH > metal libre de grietas reacciones de disolución del metal y de desprendimiento de hidrógeno dentro de la grieta AH >>> AM Ac >>>Aa indiscriminadamente Icorr = Ia = Ic y puesto que se deduce = Aa ia = Ac ic Ac >>Aa ia >> ic ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 104

¡¡La relacion ia/ic puede ser del orden de 103!! Ej: si la corriente de desprendimiento de hidrógeno es pequeña, del orden de 10 -4 A cm-2 La corriente de disolución del metal debe ser del orden de 10 -1 A cm-2 Estas elevadas densidades de corriente sólo es posible que se mantengan por la reacción de disolución del metal dentro de la grieta a consecuencia de las anormalmente elevadas densidades de corriente de canje susceptibles de darse en ella. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 105

Si todo el metal que se corroe esta siendo deformado por una tensión de tracción No basta con la tensión media aplicada para lograr que el metal ceda; la deformación permanecerá dentro del límite elástico. Si se deja de aplicar esa tensión, el metal recuperará sus dimensiones iniciales Pero esto no significa que las tensiones locales sean iguales a la tensión media es perfectamente factible que se produzca una concentración de tensión, anormalmente elevada, en el vértice de una grieta del metal, que lo lleve a la región de deformación plástica de la curva tensióndeformación. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 106

¿Cuál será el resultado del fallo del metal cerca del vértice de la grieta? EL RESULTADO cuando el proceso de disolución anódica elimina la superficie angulosa, la ulterior deformación con fractura plástica origina una nueva superficie llena de escalones en el interior de la grieta y con ello la fractura contribuye a que la velocidad de disolución del metal aumente (por ejemplo, hasta del orden de mm hora) lo que es mucho mayor que lo que sería de esperar para la sobrevoltaje aplicada, de acuerdo con las medidas realizadas sobre una superficie normal. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 107

Pero esto no es todo: la grieta se está propagando hacia el interior del metal sirviendo el borde de la superficie que avanza como zona sumidero de electrones para la reacción de disolución del metal Parece que todo es normal si se mide la diferencia de potencial entre la disolución y la superficie aparente del metal, se obtiene casi el potencial usual de corrosión del metal. Después, las microgrietas empiezan a unirse con otras microgrietas, se producen macrogrietas y la pieza del metal deja de ser un material estructural estable; se quiebra un eje o se desintegra una parte de un avión aun cuando esté sometida únicamente a una tensión normal. Lo que se ha descrito es la llamada fractura de tensión por corrosión. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 108
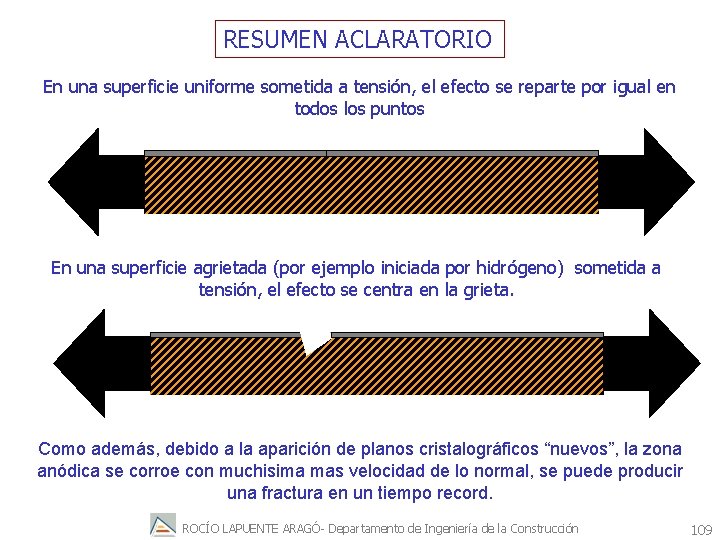
RESUMEN ACLARATORIO En una superficie uniforme sometida a tensión, el efecto se reparte por igual en todos los puntos En una superficie agrietada (por ejemplo iniciada por hidrógeno) sometida a tensión, el efecto se centra en la grieta. Como además, debido a la aparición de planos cristalográficos “nuevos”, la zona anódica se corroe con muchisima mas velocidad de lo normal, se puede producir una fractura en un tiempo record. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 109
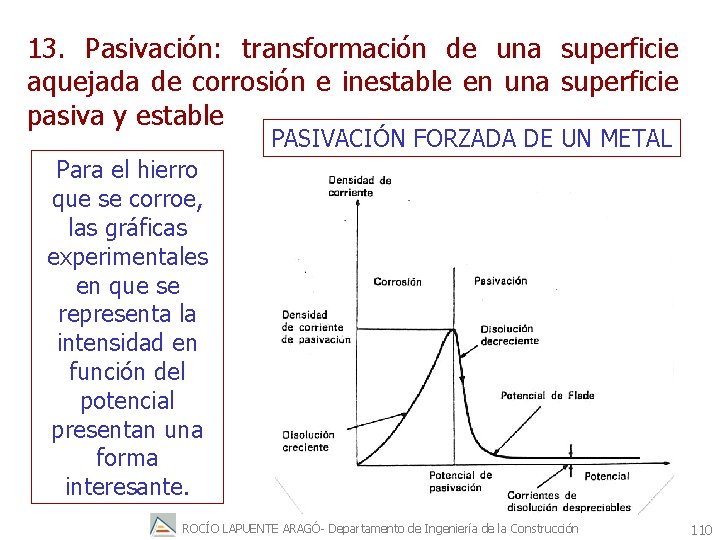
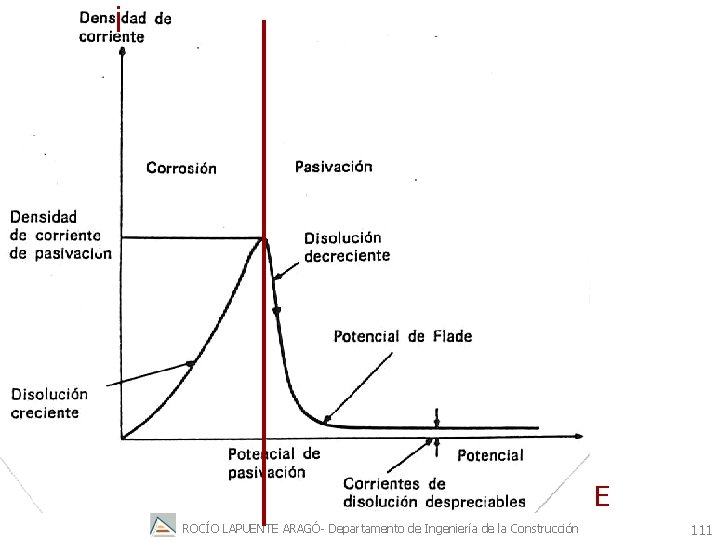
13. Pasivación: transformación de una superficie aquejada de corrosión e inestable en una superficie pasiva y estable PASIVACIÓN FORZADA DE UN METAL Para el hierro que se corroe, las gráficas experimentales en que se representa la intensidad en función del potencial presentan una forma interesante. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 110
i E ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 111

Pasivado el metal, las intensidades que fluyen son de cien a mil veces menores que la corriente de disolución en el máximo de la región corriente-potencial en que crece la corriente de corrosión con el aumento del potencial. Ha cesado totalmente la corrosión y el metal ha quedado protegido anódicamente extrayendo electrones del metal en lugar de inyectarlos como en el proceso catódico. Pero lo más importante es que la protección anódica de metal susceptible de corroerse, puede lograrse mediante el paso de un número muy bajo de coulombs en comparación con el que se necesita para la protección catódica no conduce, en modo alguno, al desprendimiento de hidrógeno que penetre en el metal y lo perjudique, lo cual es posible que ocurra durante el proceso de protección catódica ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 112

En condiciones controladas puede sacarse provecho a este comportamiento, provocando la formación de óxidos protectores, como en el proceso de anodización del aluminio. Con la aparición la película pasivante se reduce drásticamente y, a veces, casi se suprime la corrosión. Para que la protección sea eficaz se requiere que la película sea insoluble en el reactivo, continua, impermeable, adherente y tenaz. Este método de estabilizar un metal se puede utilizar en gran manera; por ejemplo, los grandes tanques para almacenar petróleo, que puede contener agua y ser ácido, algunas veces se protegen de la corrosión con este procedimiento. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 113
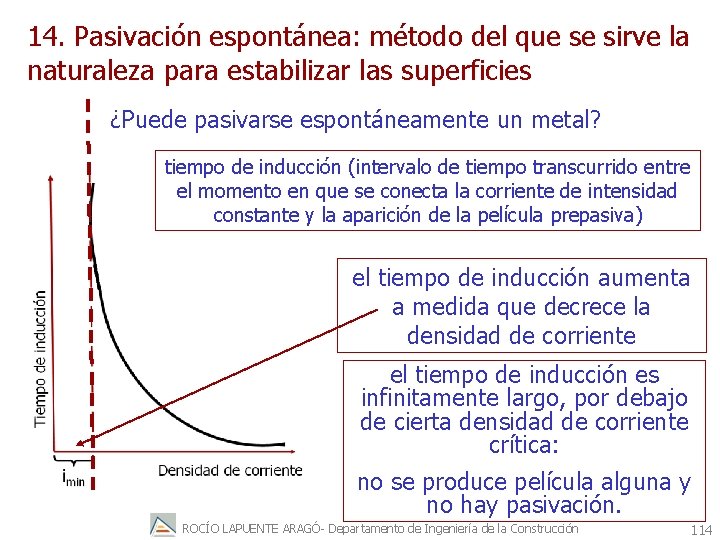
14. Pasivación espontánea: método del que se sirve la naturaleza para estabilizar las superficies ¿Puede pasivarse espontáneamente un metal? tiempo de inducción (intervalo de tiempo transcurrido entre el momento en que se conecta la corriente de intensidad constante y la aparición de la película prepasiva) el tiempo de inducción aumenta a medida que decrece la densidad de corriente el tiempo de inducción es infinitamente largo, por debajo de cierta densidad de corriente crítica: no se produce película alguna y no hay pasivación. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 114

Realmente la velocidad de disolución es tan lenta, que la difusión aleja los iones a medida que se van formando y no permite que se alcance una concentración que sea suficiente para que precipite. si un metal está corroyendo espontáneamente a una velocidad menor que la que corresponde a una densidad de corriente mínima seguirá corroyéndose Pero si la densidad de corriente de la disolución durante la corrosión sea mayor que la densidad de corriente límite; en este caso se formará una película a través del mecanismo de disolución-precipitación y el metal se pasivará espontáneamente. Esto explica el hecho de que el hierro sumergido en ácido nítrico diluido se corroe hasta destruirse, pero quede protegido por una película pasiva si lo está en ácido nítrico concentrado. La naturaleza también recurre al mecanismo o recurso de la pasivación. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 115

15. Costes de la corrosión en nuestra civilización Las pérdidas anuales causadas por la corrosión en los países industrializados y en vías de desarrollo, están en tormo al 3, 5 por 100 del producto nacional bruto. Cualquiera puede imaginarse, a partir de este dato, la elevadísimo cuantía de los costes originados por la corrosión, responsable de que, 1/4 a 1/3 de la producción mundial de acero se dedique a la reposición de las estructuras deterioradas. Pero los daños por corrosión pueden reducirse y, a veces, evitarse incluso, por métodos de protección sancionados por la práctica y rentables económicamente, lo que, por desgracia, es mucho menos conocido de lo que debiera. ROCÍO LAPUENTE ARAGÓ- Departamento de Ingeniería de la Construcción 116
- Slides: 116