Preliminarna Ispitivanja Osobina Organskih Spojeva Ispitivanje fizikalnih osobina

Preliminarna Ispitivanja Osobina Organskih Spojeva

Ispitivanje fizikalnih osobina organskih spojeva • Fizikalne konstante - T. t - t. k. - indeks loma (refrakcija), - opticka rotacija • Elementarna analiza • Odredjivanje topivosti organskih spojeva • Ispitivanje relativne kiselosti i bazičnosti organskog spoja • Ispitivanje sagorljivosti organskog spoja

Ispitivanje Osobina Organskih Spojeva: • Izdvajanje iz smjese i čišćenje • Kada je neki spoj sintetiziran ili izoliran iz prirodnog materijala, on se uvjek nalazi u smjesi sa drugim organskim spojevima. • Treba provesti odvajanje ispitivane komponente od drugih. • Ako je ispitivana supstanca čvrsta, čišćenje se vrši prekristalizacijom • Ako je tečna, odvajanje se vrši destilacijom

• Ekstrakcija-primjenjuje se za razdvajanje svih vrsta smjesa • Hromatografija-univerzalna metoda za razdvajanje

Ispitivanje fizikalnih osobina organskih spojeva • • Agregatno stanje Boja supstance Miris supstance Fizikalne konstante

Agregatno stanje • Daje nam informacije o jačini intermolekularnih sila koje povezuju molekule • Čvrsto agregatno stanje-sile su jače i molekule koje izgrađuju kristalnu rešetku čvršće vezane. • Tečno agregatno stanje-sile su slabije, molekule su u stanju manjeg reda

Boja • Upućuje na prisustvo u molekuli određenih strukturnih elemenata koji apsorbiraju vidljivu svjetlost • Hromoforne grupe (sistemi konjugiranih dvostrukih veza, zavisno od prirode hromoforne grupe, dobije se različito obojenje) • Auksohromne grupe (pojačavaju efekat hromofora, heteroatomi sa slobodnim elektronskim parovima)

Miris • • - Ukazuje na neke odredjene spojeve Karakteristične mirise imaju Esteri Spojevi iz grupe terpena (kamfen, pinen. . . ) Niže kiseline (oštre mirise) Fenoli Merkaptani-neprijatan miris Heterociklični spojevi sa N i S

Fizikalne konstante • To su numeričke vrijednosti koje upućuju na određene osobine organske molekule • Ako se pravilno odrede mogu mnogo pomoći kod identifikacije organske supstance

Tačka topljenja (talište) • Obično se prva odredjuje nakon čišćenja organskog spoja • Podaci dobiveni uporedjuju se sa literaturnim vrijednostima za ispitivanu supstancu Interval topljenja –služi kao indikacija čistoće nekog spoja -kada se topljenje odvija u intervalu od 0. 5°C, takva supstanca je čisti spoj -ako je interval topljenja širi supstanca nije čista i treba je prečistiti (prekristalizirati)

Uticaj nečistoće na talište • Eutektička temperatura –granična temperatura do koje se može sniziti talište neke supstance usljed dodatka druge • Eutektička smjesa-smjesa odredjenog sastava dvaju komponenata koja se tali kod eutektičke temperature

• Depresija tališta omogućava utvrdjivanje identiteta dvije supstance jednakog tališta - Jednake količine obje supstance pomiješaju se i smjesi se odredi talište. - Ako je talište ove smjese nepromijenjeno, obje supstance su identične, a ako je taliste niže, radi se o dvije različite supstance.

• Mnoge organske supstance pri zagrijavanju se raspadaju : - Promjena boje - Razvijanje gasova - Temper. na kojoj se supstance raspadaju nije oštra i zavisi od načina zagrijavanja - Ako se zagrijavanje odvija brzo, dobije se viša tačka raspada (ne mogu se tačno reproducirati)

Kalibracija termometra • Vrši se mjerenjem tališta niza standardnih stabilnih, potpuno čistih supstanci, npr: Spoj talište, °C 3 -fenilpropionska kiselina 48, 6 Acetamid 82, 3 Salicilna kiselna 159 3, 5 -dinitrobenzojeva kiselina 205

Tačka ključanja (vrelište) • Vrelište isto kao i talište, odredjuju sile koje drže molekule na okupu • Ukoliko su ove sile jače, potrebna je veća energija da molekule napuste tekućinu (prelaz u parnu fazu) • Veličina molekule, razgranatost njihove strukture, prisustvo grupa koje se mogu asocirati, povećavaju vrelište.

Tačka ključanja (vrelište) • Vrelište je konstantno samo kod konstantnog pritiska! Nema isto značenje za identifikaciju kao talište • Ako se supstanca ne raspada vrelište se odredjuje na uobicajeni način • Ako se supstanca raspada, vrši se pod sniženim pritiskom
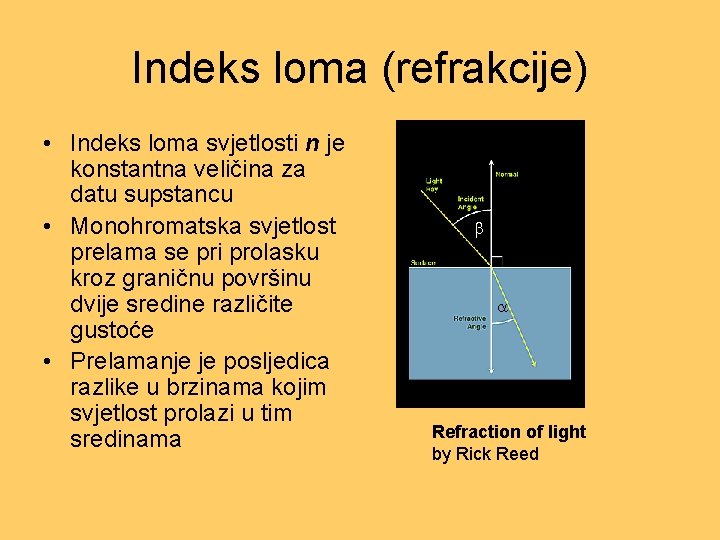
Indeks loma (refrakcije) • Indeks loma svjetlosti n je konstantna veličina za datu supstancu • Monohromatska svjetlost prelama se pri prolasku kroz graničnu površinu dvije sredine različite gustoće • Prelamanje je posljedica razlike u brzinama kojim svjetlost prolazi u tim sredinama Refraction of light by Rick Reed
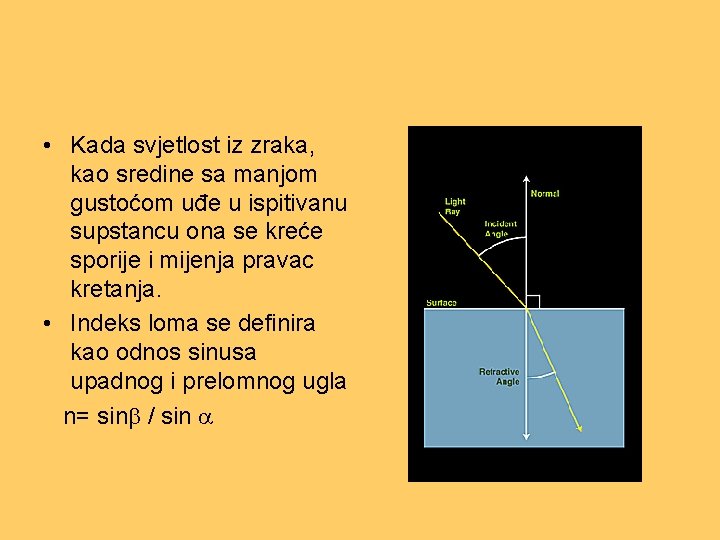
• Kada svjetlost iz zraka, kao sredine sa manjom gustoćom uđe u ispitivanu supstancu ona se kreće sporije i mijenja pravac kretanja. • Indeks loma se definira kao odnos sinusa upadnog i prelomnog ugla n= sin / sin

Veličina ove promjene (n), zavisi od: • Prirode dvije sredine • Talasne dužine propuštene svjetlosti • Temperature -zato se njeno odredjivanje vrši upotrebom monohromatske svjetlosti i kod konstantne temperature • Odredjivanje n, daje brzu informaciju o organskom spoju i o njegovoj čistoći • Određivanje se vrši pomoću refraktometra (obično Abeov refrakrometar)

Optička Rotacija • Određene organske molekule su optički aktivnezakreću planarno polarizovanu svjetlost • Optička aktivnost se javlja kod supstanci čije molekule sadrže hiralni centar • Zakretanje planarno polarizovane svjetlosti na desno, u pravcu kazaljke na satu, označava se sa (+), a znak za zakretanje u suprotnom pravcu (-) • Smijer rotacije zavisi od prirode supstance

Veličina ugla rotacije zavisi od: • Prirode supstance • Talasne dužine upotrijebljene svjetlosti • Debljine sloja kroz koji svjetlost prolazi • Prirode otapala • Temperature i dr.

Specifična Rotacija • Da bi se mogla uporedjivati moć rotacije optički aktivnih supstanci mjerenja se vrše kod odredjenih standardnih uslova, pošto tada moć rotacije zavisi samo od prirode supstance”specifična rotacija” i označava se •

= • 100/d • c -izmjereni ugao rotacije polarizovane svjetlosti izražen u stepenima c- koncentracija optički aktivnie supstance u gramima na 100 m. L otopine L=d, duzina kivete u decimetrima u kojoj se određuje optička aktivnost t- temperatura n akojoj se vrši mjerenje -tasna dužina polarizovane svjetlosti (obično žuta svjetlost natrijumove lampe D 598 nm)

• Koncentracija se izražava u g/100 ml a ne u molovima zato da bi se mogla mjeriti optička aktivnost supstanci cija je molekularna težina nepoznata. • Kada se mjeri u otopinama, obavezno se naznači i otapalo.

ELEMENTARNA ANALIZA • • • Dokazivanje C i H Dokazivanje S Dokazivanje halogenih elemenata Dokazivanje P Dokazivanje O

• Organski spojevi sadrže relativno mali broj elemenata: • C, • H, • O, • N, • S, • Halogeni elementi, • Pi • Neki metali

Mineralizacija • Detekcija pojedinih elemenata započinje razlaganjem kovalentno gradjenog organskog spoja-prevodjenjem prisutnih elemenata u ione. Taj proces se naziva mineralizacija

Dokazivanje C i H • Svi organski spojevi sadrže C • C se obično preliminarno dokazuje spaljivanjem • Svi organski spojevi sadrže i H osim kad su svi H zamijenjeni sa halogenima

MINERALIZACIJA ORGANSKIH JEDINJENJA 1. OKSIDACIONE METODE a. Proba sagorijevanja u vazduhu b. Libigova metoda mineralizacije 2. REDUKCIONE METODE c. Lasenjova metoda mineralizacije d. Kastelanina metoda mineralizacije

OKSIDACIONE METODE Proba sagorijevanja u vazduhu • Obično se preporučuje kao prva-zbog jednostavnosti • Ovako se utvrdi da li je supstanca organska • Pruža i druge osobine o ispitivanoj supstanci • Nesagorljivi ostatak može biti iskoristen za dokazivanje nekih heteroatoma

• Radi se u porcelanskoj zdjelici ili na Pt-žici savijenoj u gustu spiralu. • Mala količina supstance se grije na malom plamenu Bunzenovog plamenika • Da bi se supstanca mogla zapaliti, prije nego što ispari, treba je povremeno izložiti direktnom plamenu.

Treba posmatrati: • Pare i gasove (da li su pare koje se razvijaju kisele ili bazne). Provjeriti sa indikatorskim papirom, navlažen sa destilovanom vodom. • Sagorijevanje (izgled plamena, eventualno prisustvo dima i mirisa (oprez ! Mogu biti štetni!) Ako se supstanca ne zapali, i dalje treba zagrijavati na jakom plamenu do usijanja, da se C ponovo oksiduje bez ostatka. - Ostatak: Ako se i poslije ovog ipak zadrži nesagorjeli ostatak (obično oksid ili karbnat metala), možemo ga ispitati kvalitativnim analitičkim probama radi utvrđivanaj o kom se

Tumačenje rezultata Organska supstanca: • topi se ili raspada a zatim gori više ili manje dimljivim plamenom (C se taloži na hladnim površinama) Neorganska supstanca: • ne ugljeniše se, • obično ostavlja nesagorljiv i neisparljiv ostatak (bijele, žućkaste ili tamne boje)

Topljenje: • pojedine organske supstance se tope i sagorijevaju bez ugljenisanja (npr. urea, oksalna kiselina) Rasprskavanje: • Izvjesne klase organskih jedinjenja se raspadaju uz rasprskavanje (eksplodiraju). Npr. Peroksidi, ozonidi, neka nitrojedinjenja.

Miris: • Šećeri i proteini prilikom sagorijevanja razvijaju karakteristične mirise. Ugljenisanje: • Organske supstance se najčeće ugljenišu (najjednostavniji način da se razlikuju od mineralnih) • Metalne soli organksih kiselina se ne tope nego se raspadaju i ostavljaju nesagorljiv ostatak

• • • Izgled plamena Žutim plamenom gore zasićeni ugljikovodici Čađavim plamenom gore aromatična jedinjenja jer su bogata C Svijetlim plamenom gore nearomatična jedinjenja male molekulske težine Plamen postaje više bezbojan i plavičast što je u molekuli više atoma O (npr. Alifatskih alifatski alkoholi) Jedinjenja koja sadrže halogene teško se zapale, a kada se zapale daju čađav plamen. Halogeni daju zeleno-plavu boju plamenu zagrijavanjem na Bunzenovom plameniku (Bajlštajnova proba)

Izgled ostatka • Metalne soli organskih kiselina se na povišenoj temperaturi ne tope i ostavljaju bijeli ili svijetlo obojeni nesagorljiv ostatak (obično oksidi ili karbonati metala, a neki elementi se izdvajaju u metalnom obliku (Ag, Au, Pt) • Živa pri žarenju ispari • Ako se dobije dovoljno ostatka-treba napraviti neke jednostavne kvalitativne probe na elemente

OKSIDACIONE METODE Libigova (Liebig) metoda mineralizacije • Dokazuje se prisustvo C i H (pod uslovom da je iz reakcionog sistema potpuno isključena voda) • Organska supstanca se zagrijava sa bakar oksidom. • C i H se oksidiraju u CO 2 i H 2 O • Ba(OH)2 se zamuti od CO 2 • Kapljice vode na epruveti od H 2 O

REDUKCIONE METODE Lasenjova (Lassaigne) metoda • Ovo je najbolji postupak • Na visikoj temperaturi se pomoću metalnog Na organska supstanca razori a njeni sastavni dijelovi pretvore u neorganske ione. • Org. supst. (C, H, N, S, X) + Na Na. CN + Na 2 S + Na. X

• Metalni Na svojim redukcionim dejstvom pretvara: • N u cijanid (Na. CN) • X u halogenide (Na. F, Na. Cl, Na. Br, Na. I) • S u sulfid ili tiocijanat (Na 2 S ili Na. SCN) Sa druge strane • C se oksiduje i odlazi u CO 2 • H u obliku H 2 O

• Važno je da metalnog Na bude u višku, da se nebi umjesto Na. CN i Na 2 S nagradio natrijum tiocijanat (Na. SCN), koji ometa prisustvo CNiona, pomoću Fe. Cl 3 (pri čemu od cijanidnih iona nastaje “berlinsko plavilo”), zato što sam tiocijanat (Na. SCN) reguje sa Fe. Cl 3 i daje crvenu boju. • Ako metalnog Na ima u višku, čak i već obrazovani Na. SCN će se razgraditi i dati Na 2 S i Na. CN: Na. SCN + 2 Na Na. CN + Na 2 S

REDUKCIONE METODE Kastelanina (Castellana) metoda • Ovo je samo tehnička varijanta prethodne metode. Za razliku od Lasenjovog postupka za mineralizaciju organske supstance umjesto metalnog Na služi smjesa Mg i K 2 CO 3. • Prisutni elementi prelaze u neorganske anione i dalje se dokazuju.

KVALITATIVNO DOKAZIVANJE

Kvalitativno dokazivanje C i H • Samo u slučajevim akada se želi provjeriti da li se radi o organskoj ili neorganskoj molekuli • Proba sagorijevanja u vazduhu • Za pouzdanije dokazivanje prisustva C i H – Libigova metoda • Kvalitativno dokazivanje H se rijetko preduzima samostalno, jer obično prisustvo C podrazumijeva i prisustvo H (izuzeci: oksalati, neki derivati kao heksahlorbenzen itd. )

Kvalitativno dokazivanje azota u organskim supstancama 1. Dokazivanje prisustva CN iona u mineralizatu organske supstance reakcijom “berlinskog plavila”. 2. Dokazivanje azota kao amina

Dokazivanje prisustva CN iona u mineralizatu organske supstance reakcijom “berlinskog plavila” • Najvažnija metoda dokazivanja N • CN- reaguje sa Fe. SO 4, Fe. Cl 3 i HCl. • Ako je proba pozitivna, pojavi se plava ili zelenkasto plava boja feri-fero cijanida (“berlinskog plavila”)
![”berlinsko plavo” Fe. SO 4 + 6 Na. CN Na 4[Fe(CN)6] + Na 2 ”berlinsko plavo” Fe. SO 4 + 6 Na. CN Na 4[Fe(CN)6] + Na 2](http://slidetodoc.com/presentation_image_h/0dc450420c9542fcf041da02dab53324/image-47.jpg)
”berlinsko plavo” Fe. SO 4 + 6 Na. CN Na 4[Fe(CN)6] + Na 2 SO 4 3 Na 4[Fe(CN)6] + 4 Fe. Cl 3 Fe 4[Fe(CN)6]3+12 Na. Cl Ovom metodom se N teško dokazuje ili se ne može uopšte dokazati u slijedećim jedinjenjima: • Koja se razlažu već poslije malog povišenja temperature (npr. diazonijum soli) • Koja su veoma stabilna (neka nitro jedinjenja i izvjesni heterociklusi) • Koja sadrže malo N, te je boja nastalog “berlinskog plavila” blijeda i slabo primjetna (pomaže dodatak Ba. Cl 2) • Koja sadrže i S, jer tad obrazuje crveni feritiocijanat umjest “berlinskog plavila”, što je dokaz istovremenog prisustva i S i N

• N je vjerovatno najnezgodniji elemenat za zadovoljavajuće dokazivanje • Zato se neophodno izvršiti mineralizaciju i po nekoliko puta i to na oba spomenuta načina (pogotovo ako se dobije sumnjiv rezultat).

Dokazivanje N kao amina • Ako je N u molekuli prisutan kao amino (-NH 2 grupa), postoji mogućnost da se on direktno dokaže (bez prethodne mineralizacije) i to: zagrijavanjem organske supstance sa Ca. O, koji iz molekule istisne amino grupu u vidu amonijaka.

Kvalitativnno dokazivanje halogena a. Provjeriti da li uopšte jedinjenje sadrži halogenide (jednom od opštih reakcija na halogenide) b. Koji od halogena se nalazi u satavu organskog spoja

a. Zajedničke reakcije organskih halogenida b. Specifične reakcije organskih halogenida

a. Zajedničke reakcije organskih halogenida • Bajlštajnovom probom-nepouzdana proba (provjeriti dalje) • pomoću srebro nitrata i rastvorljivost nastalih Ag. X u HNO 3 (nerastvorljivi) • Ako je grupna proba na X u org. Supstancama pozitivna, važno je utvrditi i to da li se halogeni nalaze u samoj organskoj molekuli ili u anionu spojenom ionskom vezom za baznu organsku molekulu koja sama ne sadrži X, npr: hlorhidrata nekog amina. Na isti način se ispituju X za grupno dokazivanje samo što se umjesto mineralizata ispituje vodeni rastvor nepoznate organske supstance.

b. Specifične reakcije organskih halogenida • Kvalitativno dokazivanje Cl pomoću Vilijerovog (Villiers) reagensa: - zasićeni bezbojni rastvor anilina - Zasićeni rastvor o-toluidina - Glacijalna acetatna kiselina Alkalni mineralizat se zakiseli, doda KMn. O 4 Cjevčica se zagrijava i dobiveni gas oboji ljubičasto u epruveti sa Vilijerovim reagensom

Kvalitativno dokazivanje joda i broma pomoću hlorne vode • Prvo se jodidni a zatim bromidni jon oksiduje pomoću hlora (ili hlorne vode) u jod, odnosno brom, koji zatim prelaze u hloroformski sloj dajući rastvoru boju: jod ljubičatu, brom, smedju.

• Kvalitativno dokazivanje broma eozinskom probom Ako se u alkalnom mineralizatu org. supstance, nalazi se bromidni anion, on se može dokazati jednom selektivnom probom: Pomoću Pb. O 2 (koji sa acetatnom kiselinom daje olovo tetra acetat) se bromidni ion oksiduje do Br 2, koji dalje, sa fluoresceinom gradi eozin:
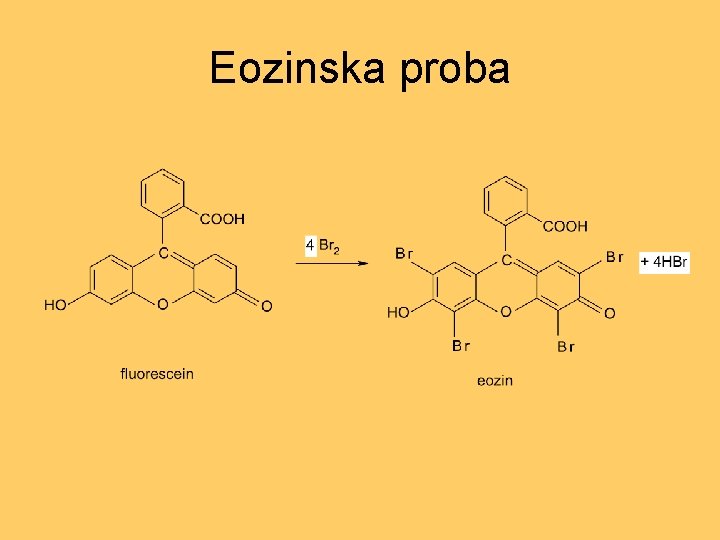
Eozinska proba

Kvalitativno dokazivanje S • Ako je organska supstanca mineralizovana redukcijom, tj. postupkom Lasenja ili Kastelane, onda će ioni sulfida koji tada nastanu moći da se dokažu: a. Stvaranjem crnog sulfida olova ili b. Stvaranjem crnog sulfida srebra c. Pomoću natrijum nitroprusida Ako s tokom mineralizacije stvori SCN- njihovo prisustvo se dokazuje stvarajem feri-tiocijanata.

Kvalitativno dokazivanje S u organskim sulfatima • Kao i halogeni, i S u organskom spoju može poticati od aniona (SO 42 -), vezanog za baznu organsku supstancu, u kojoj nema sumpora, npr. sulfat amina. • Takvo ispitivano org. jedinjenje rastvoreno u vodi daje sa ionom Ba 2+ bijeli talog Ba. SO 4 koje se neće rastvoriti dodavanjem HCl.

Kvalitativno dokazivanje P • Prisustvo fosfora u ispitivanom organskom jedinjenju može se naslutiti iz mirisa fosfina (PH 3), koje nastaje pri stapanju jedinjenja sa Na (tokom Lasenjove mineralizacije) • U mineralizatu P se dokazuje pomoću amonijum molibdatnog reagensa-stvara se žuti amonijfosfor-molibdat.

Diazidinska proba za dokazivanje P Reagesi: I diazidin u acetonu II natrijum perborat u vodi • U tiofosfornim spojevima fosfor se može dokazati bez prethodne mineralizacije diazidinskom probom. • Tiofosforni spojevi daju žuto-crvenu boju. žuto • Osjetljivost reakcije je velika

Dokazivanje O • Ne postoji jednostavna i specifična proba na kisik. Zato se O ne dokazuje u kvalitativnoj organskoj analizi • O prisutnosti O moguće je donijeti zaključak na osnovu feroks probe. Feroks ili feriheksatiocijanoferat je intenzivno obojena so koja nije topiva u ugljikovodicima i u halogenim derivatima a topiva je spojevima koji sadrže O , S ili N.

- Slides: 62