Preanaltica en el procesamiento de muestras para hibridacin

Pre-analítica en el procesamiento de muestras para hibridación in situ (ISH): ¡Esto no va a hibridar nunca! Dra Marta Salido Laboratori de Citogenètica Molecular Servei de Patologia Hospital del Mar 24 de Febrero 2017

1990 BCR/ABL 1993 -95 PML/RARA, AML 1/ETO, MLL… 1993 +12 LLC 1993 -96 MYC, BCL 2, BCL 6 SARCOMAS TUMORES DE MAMA NEOPLASIAS HEMATOLÓGICAS 1992 1998 HER 2 FDA Trastuzumab Pathvysion 1995 -97 TUMORES DE VEJIGA MELANOMAS 2003 2009 Genes candidatos distinguir melanomas vs nevus Kit RREB 1, MYB, CCND 1, CEP 6 FISH EN NEOPLASIAS ALK-EML 4 MET FDA Crizotinib ROS 1, RET FDA ALK kit 2000 2001 2005 TUMORES PULMONARES 2007 2009 2011 2012 2013 EWSR 1 FUS CHOP DDIT 3 MDM 2 TUMORES GÁSTRICOS Y UEG TUMORES CEREBRALES 1998 2006 1 p-/19 q- ODG Uso en rutina +3, +7, +17, 9 p 21 FDA Uro. Vysion recaidas FDA Uro. Vysion diag hematuria 1997 2010 HER 2 FDA Trastuzumab Pathvysion

FISH EN MUETRAS PARAFINADAS • Herramienta útil para el diagnóstico patológico • Permite localizar la alteración genética en una célula específica o en regiones de un tejido, lo que permite estudiar alteraciones en 1 única célula a diferencia de los estudios en DNA que mezclan DNA de cientos de células distintas. • En comparación con la técnica de FISH en muestras en suspensión, la técnica de FISH en parafina: – Técnicamente más laboriosa – Variabilidad en el resultado elevada causada por el procesamiento pre -analítico de las muestras – Interpretación limitada por el solapamiento y rotura de núcleos

FACTORES QUE AFECTAN EL ÉXITO DE UN FISH • Artefactos morfológicos por manejo de la muestra en fresco • Condiciones de fijación de la muestra en fresco • Tipo de Tejido • Grado de fibrosis Fase Pre-analítica • Antigüedad de la muestra parafinada • Corte del bloque: portaobjetos pretratados, grosor • Tiempo que tenemos almacenado el corte para FISH • Desparafinización • Pretratamiento de la muestra • Digestión con pepsina/proteasa • Condiciones de desnaturalización/hibridación • Lavados de post-hibridación Fase Analítica
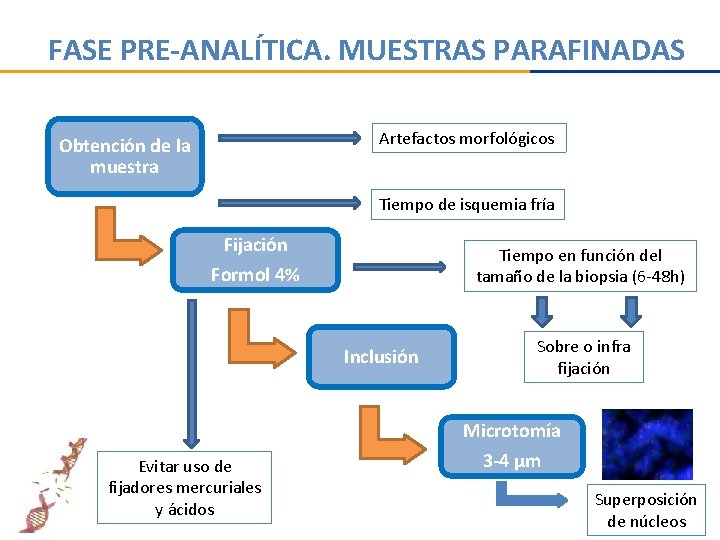
FASE PRE-ANALÍTICA. MUESTRAS PARAFINADAS Artefactos morfológicos Obtención de la muestra Tiempo de isquemia fría Fijación Tiempo en función del tamaño de la biopsia (6 -48 h) Formol 4% Inclusión Sobre o infra fijación Microtomía Evitar uso de fijadores mercuriales y ácidos 3 -4 µm Superposición de núcleos
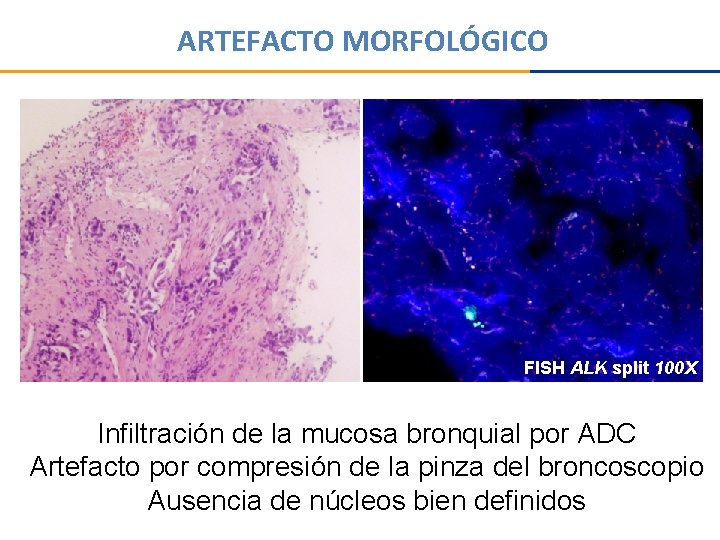
ARTEFACTO MORFOLÓGICO FISH ALK split 100 X Infiltración de la mucosa bronquial por ADC Artefacto por compresión de la pinza del broncoscopio Ausencia de núcleos bien definidos

ISQUEMIA FRÍA Y FIJACIÓN • Isquemia fría: Un retraso en la fijación provoca acidosis tisular y degradación: • Afecta a la correcta preservación de DNA y RNA • Realizar la fijación lo antes posible: 1 -3 horas • Fijación: Reacciones químicas que dan lugar a enlaces entre proteínas y ácidos nucleicos • Fijador recomendado: Formol al 10% tamponado • Evitar el uso de fijadores mercuriales, pícricos y alcohólicos • Tiempo de fijación 6 -48 horas • Una fijación prolongada afecta la calidad del DNA: Degradación DNA UNIÓN ENTRE GRUPOS AMINOS (NH 2) DE LAS PROTEÍNAS Y LOS FIJADORES ALDEHIDOS
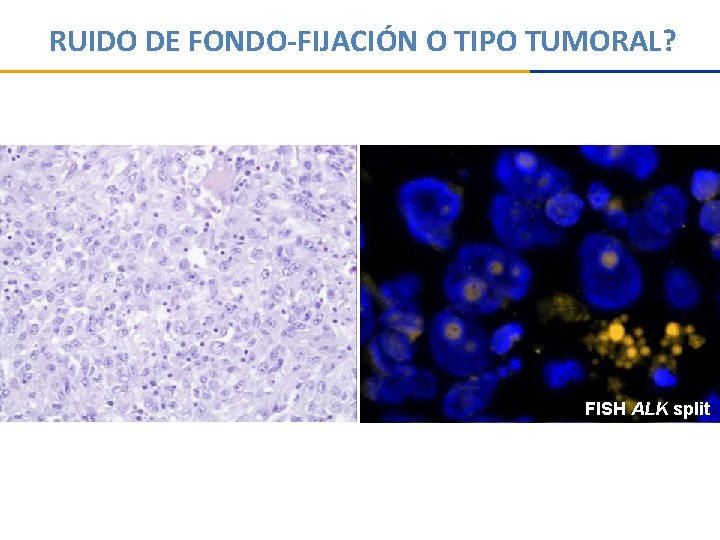
RUIDO DE FONDO-FIJACIÓN O TIPO TUMORAL? FISH ALK split
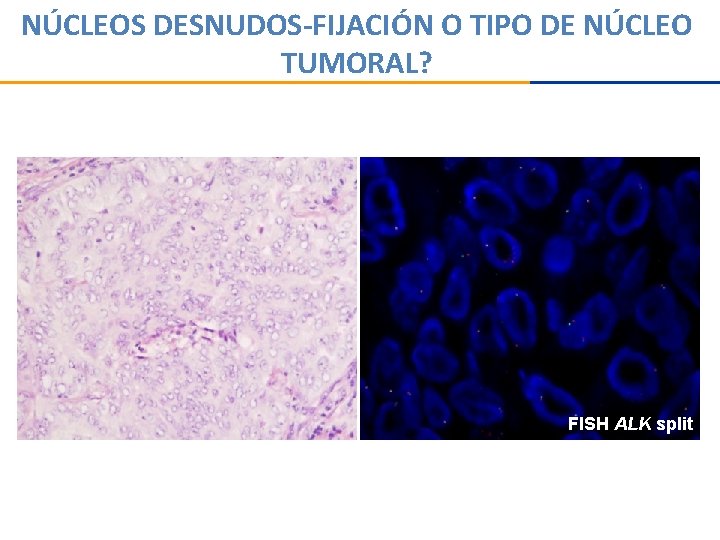
NÚCLEOS DESNUDOS-FIJACIÓN O TIPO DE NÚCLEO TUMORAL? FISH ALK split
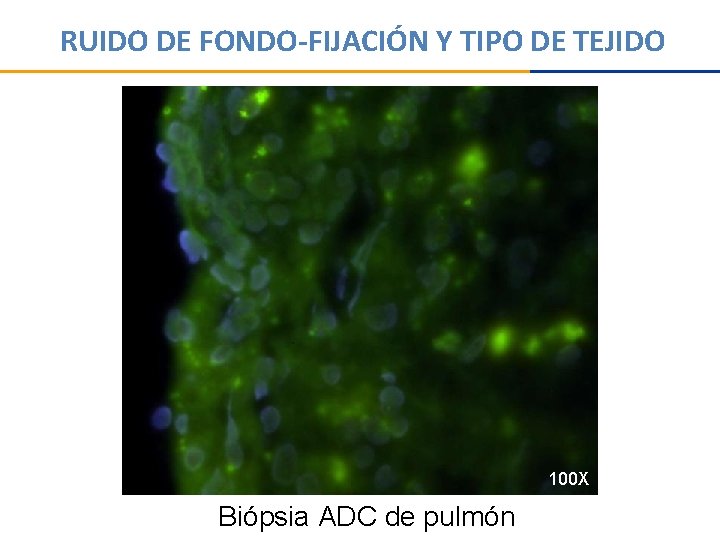
RUIDO DE FONDO-FIJACIÓN Y TIPO DE TEJIDO 100 X Biópsia ADC de pulmón
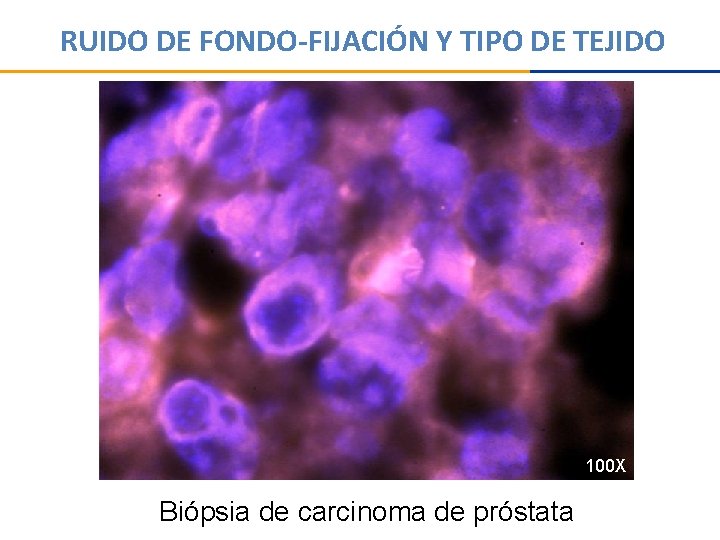
RUIDO DE FONDO-FIJACIÓN Y TIPO DE TEJIDO 100 X Biópsia de carcinoma de próstata
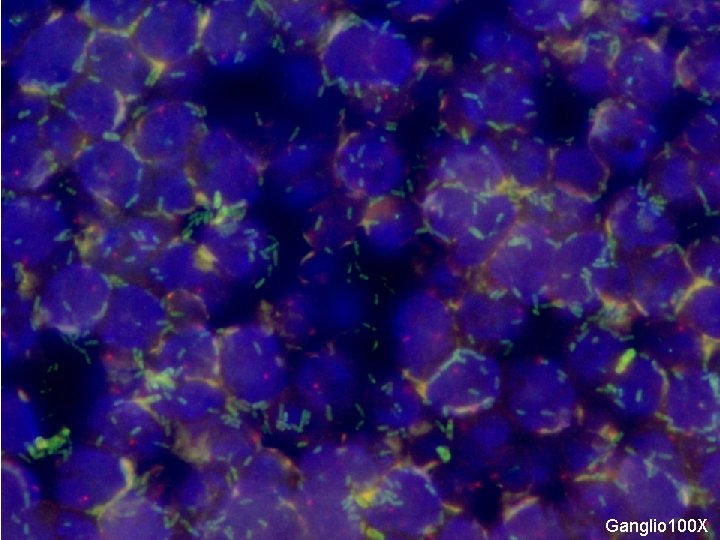
Ganglio 100 X

Monet Col Lombarda
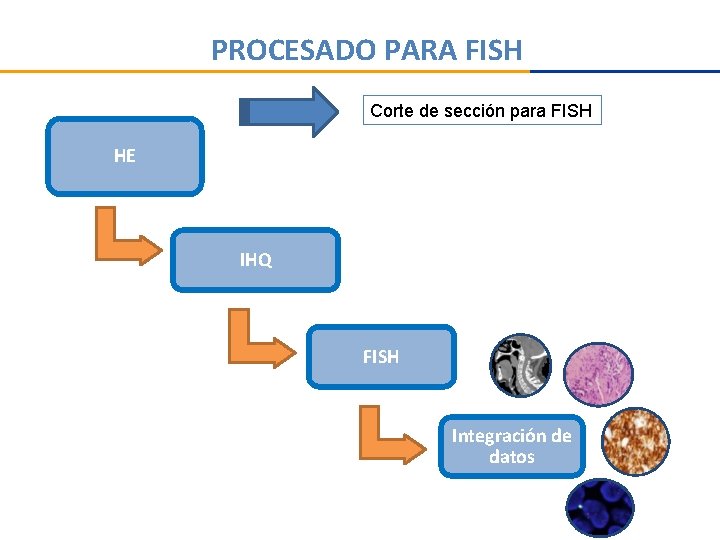
PROCESADO PARA FISH Corte de sección para FISH HE IHQ FISH Integración de datos

CORTE DE SECCIONES PARA FISH Cortes de tejido de 3 -4µm en portaobjetos silanizados o con carga positiva Evitar que se desprenda el tejido Incubación a temperatura elevada Estufa 65°C (1 h’ – overnight) Adecuar las condiciones de preservación del corte para FISH en función del estudio
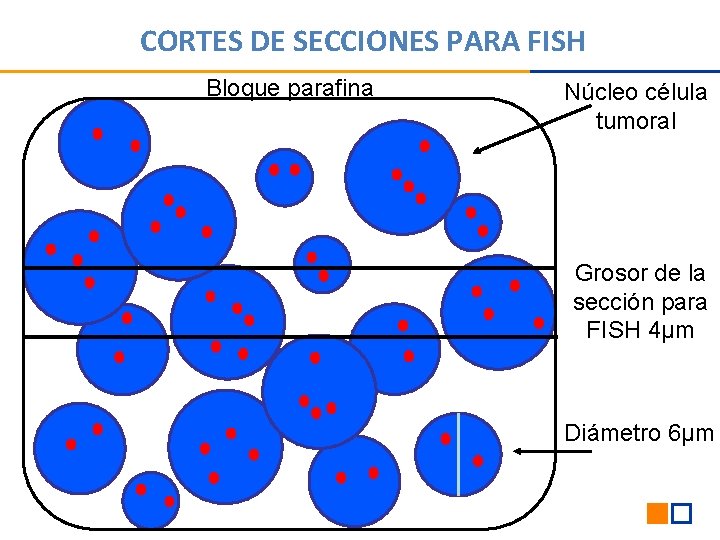
CORTES DE SECCIONES PARA FISH Bloque parafina Núcleo célula tumoral Grosor de la sección para FISH 4µm Diámetro 6µm
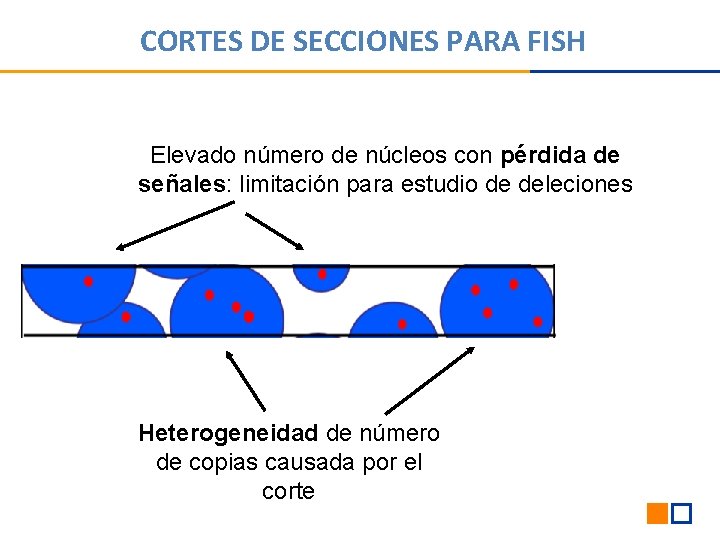
CORTES DE SECCIONES PARA FISH Elevado número de núcleos con pérdida de señales: limitación para estudio de deleciones Heterogeneidad de número de copias causada por el corte
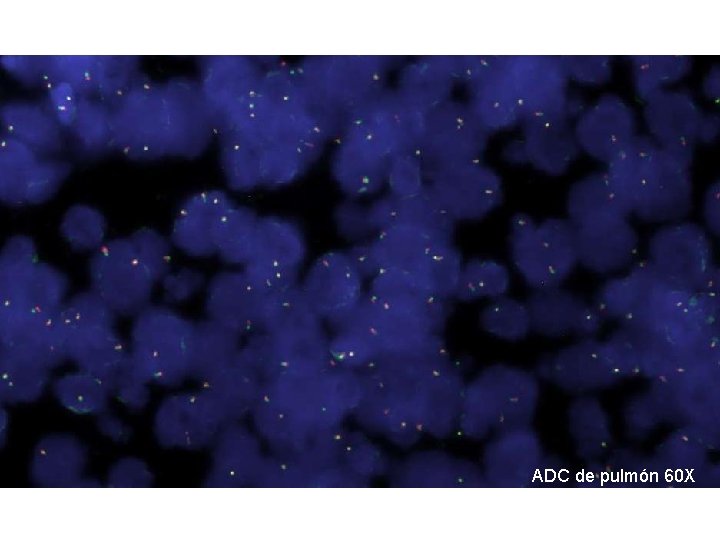
Solapamiento de núcleos ADC de pulmón 60 X
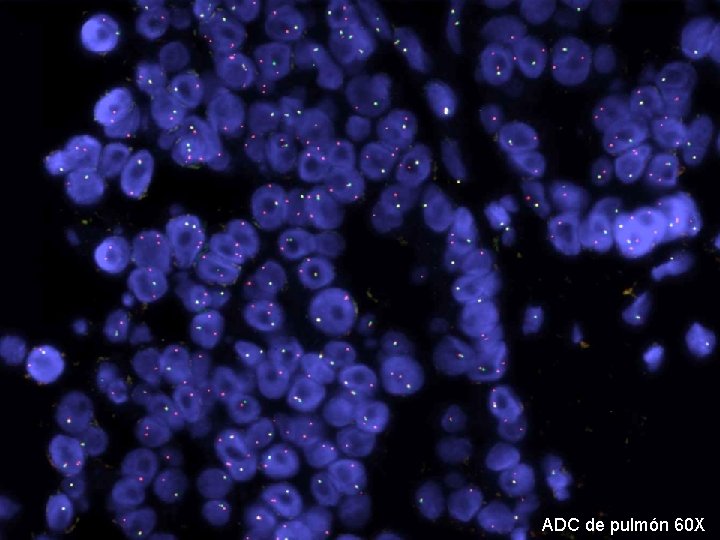
ADC de pulmón 60 X
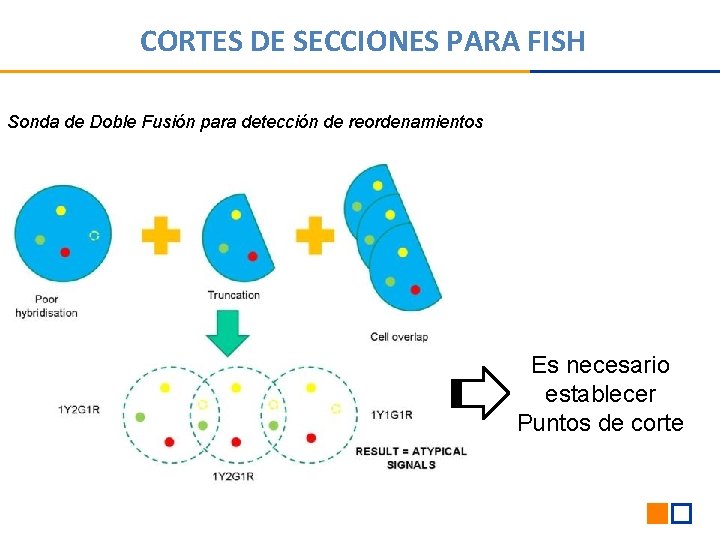
CORTES DE SECCIONES PARA FISH Sonda de Doble Fusión para detección de reordenamientos Es necesario establecer Puntos de corte
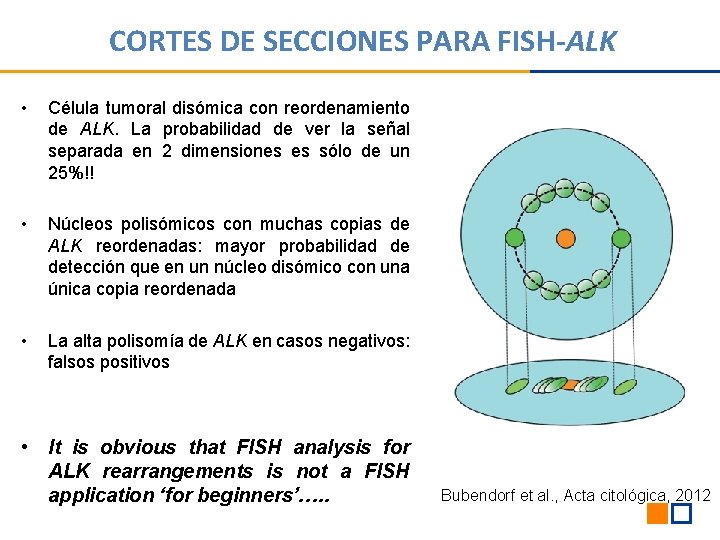
CORTES DE SECCIONES PARA FISH-ALK • Célula tumoral disómica con reordenamiento de ALK. La probabilidad de ver la señal separada en 2 dimensiones es sólo de un 25%!! • Núcleos polisómicos con muchas copias de ALK reordenadas: mayor probabilidad de detección que en un núcleo disómico con una única copia reordenada • La alta polisomía de ALK en casos negativos: falsos positivos • It is obvious that FISH analysis for ALK rearrangements is not a FISH application ‘for beginners’…. . Bubendorf et al. , Acta citológica, 2012
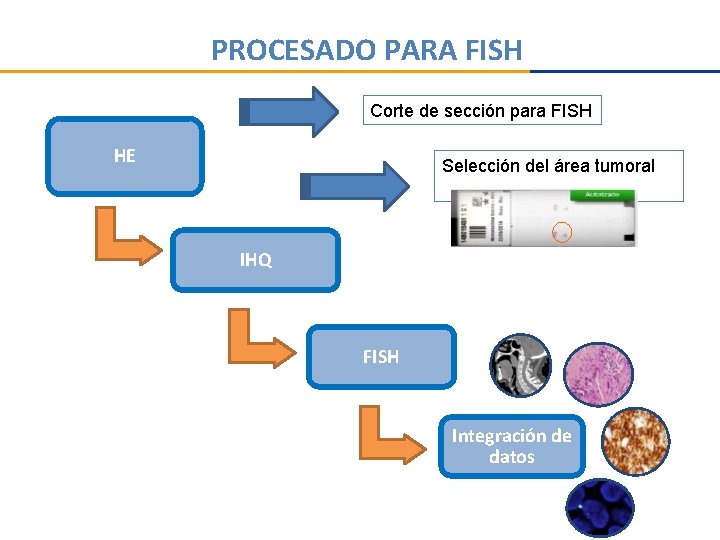
PROCESADO PARA FISH Corte de sección para FISH HE Selección del área tumoral IHQ FISH Integración de datos
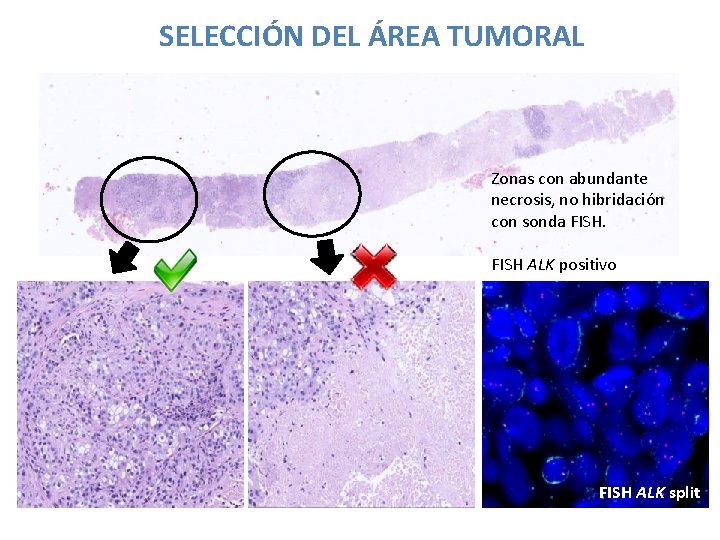
SELECCIÓN DEL ÁREA TUMORAL Zonas con abundante necrosis, no hibridación con sonda FISH ALK positivo FISH ALK split
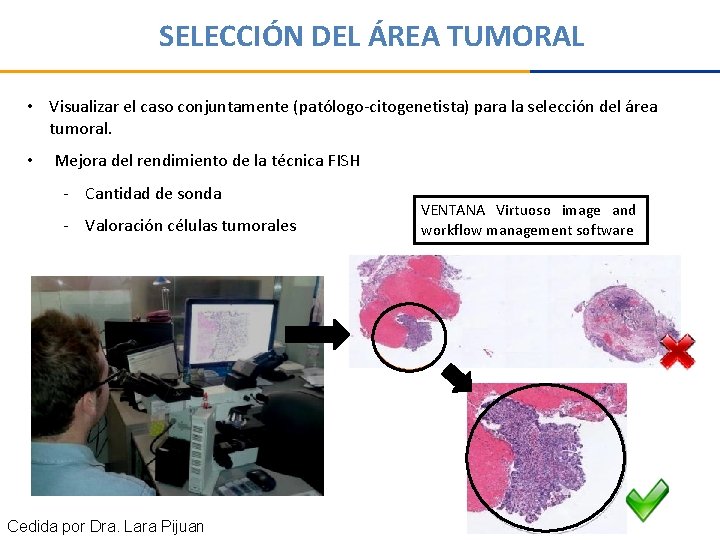
SELECCIÓN DEL ÁREA TUMORAL • Visualizar el caso conjuntamente (patólogo-citogenetista) para la selección del área tumoral. • Mejora del rendimiento de la técnica FISH - Cantidad de sonda - Valoración células tumorales Cedida por Dra. Lara Pijuan VENTANA Virtuoso image and workflow management software
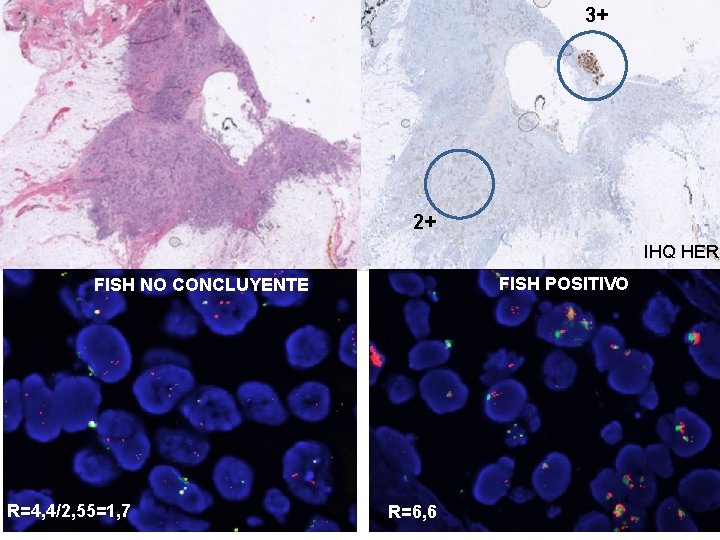
3+ 2+ IHQ HER 2 FISH POSITIVO FISH NO CONCLUYENTE R=4, 4/2, 55=1, 7 R=6, 6
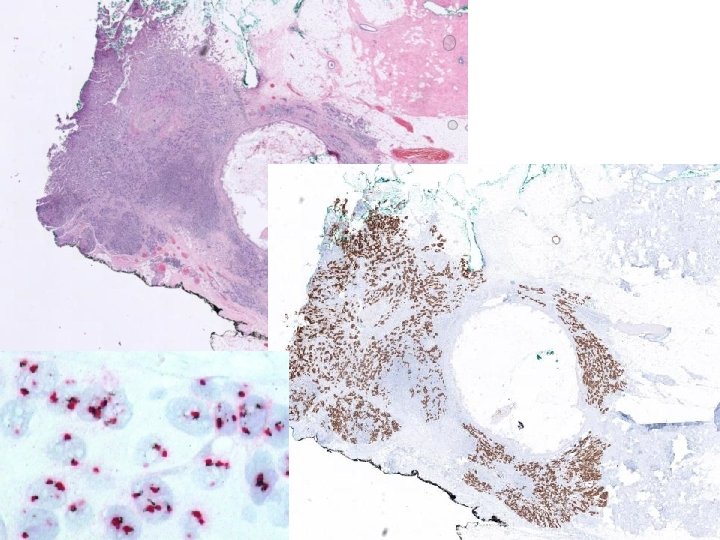

CONCLUSIONES Conocer y controlar la importancia del procesamiento pre-analítico aumenta el rendimiento de la técnica FISH • Conocerlo nos permite ahorrar esfuerzos y sonda (repeticiones) en la fase analítica • Controlarlo nos permite mejorar el análisis de los resultados de FISH

Gracias!!
- Slides: 28