Prcticas de correcta distribucin de principios activos para

Prácticas de correcta distribución de principios activos para medicamentos y la distribución farmacéutica mayorista Luz Lewin Orozco. Directora Técnica y de Calidad , GRUPO COFARES
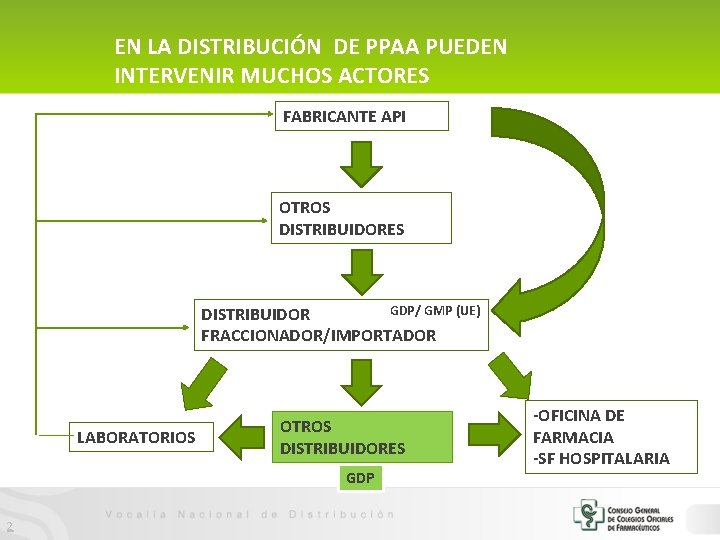
EN LA DISTRIBUCIÓN DE PPAA PUEDEN INTERVENIR MUCHOS ACTORES FABRICANTE API OTROS DISTRIBUIDORES GDP/ GMP (UE) DISTRIBUIDOR FRACCIONADOR/IMPORTADOR LABORATORIOS OTROS DISTRIBUIDORES GDP 2 -OFICINA DE FARMACIA -SF HOSPITALARIA

REGISTRO UNIFICADO DE EMPRESAS DE SUSTANCIAS ACTIVAS (RUESA) • Las empresas fabricantes, importadoras o distribuidoras de principios activos deberán estar inscritas en este registro público de la AEMPS. • Están obligadas a efectuar una declaración 60 días antes del inicio de su actividad, así como una declaración anual en el mes de enero siguiente. • Estas entidades no requieren autorización de laboratorio farmacéutico, siendo excepción las actividades de fabricación de principios activos estériles o de origen biológico. • Serán vigiladas , supervisadas e inspeccionadas por la AEMPS y CCAA. 3

REGISTRO UNIFICADO DE EMPRESAS DE SUSTANCIAS ACTIVAS (RUESA) https: //labofar. aemps. es/labofar/registro/ruesa/ • Las empresas inscritas deberán notificar a la AEMPS cualquier cambio que pueda repercutir en la calidad o la seguridad de los principios activos. • En el registro se pueden buscar : • Las empresas • Para un principio activo : el listado de todos los que fabrican, importan o distribuyen. Registro Unificado de Empresas de Sustancias Activas (RUESA) 4

REGISTRO DE DISTRIBUIDORES DE PPAA EN RUESA 5

BÚSQUEDA POR PPAA EN RUESA 6

ENTIDADES DE DISTRIBUCIÓN FARMACÉUTICA MAYORISTAS Los distribuidores farmacéuticos mayoristas contamos desde el 5 Noviembre de 2013 con las Prácticas de Correcta Distribución de Medicamentos de uso humano (2013/C 343/01). La adecuación a las mencionadas practicas facilita la aplicación de estas Directrices de 19 de marzo de 2015 sobre prácticas correctas de distribución de principios activos para medicamentos de uso humano ( 2015/C 95/01). Efectivas desde el 21 de septiembre de 2015. Simplemente revisando sus capítulos podemos ver el paralelismo entre ambas y la facilidad para su incorporación en nuestros sistemas de calidad, presentando sólo algunas peculiaridades. 7

Directrices de 19 de marzo de 2015 sobre prácticas correctas de distribución de principios activos para medicamentos de uso humano. CAPÍTULO 1: AMBITO DE APLICACIÓN CAPÍTULO 2: SISTEMA DE CALIDAD CAPÍTULO 3: PERSONAL CAPÍTULO 4: DOCUMENTACIÓN CAPÍTULO 5: LOCALES Y EQUIPOS CAPÍTULO 6: OPERACIONES CAPÍTULO 7: DEVOLUCIONES, RECLAMACIONES Y RETIRADAS CAPÍTULO 8: AUTOINSPECCIONES 8

CAPÍTULO 1: AMBITO DE APLICACIÓN Estas directrices se aplican a la distribución de Principios Activos (PPAA). Un principio activo es toda sustancia o mezcla de sustancias destinadas a la fabricación de un medicamento y que al ser utilizados en su producción, se convierten en un componente activo de dicho medicamento. La distribución de principios activos engloba las actividades realizadas con PPAA: Adquirir Importar Conservar Suministrar Exportar No se aplica a sustancias intermedias 9
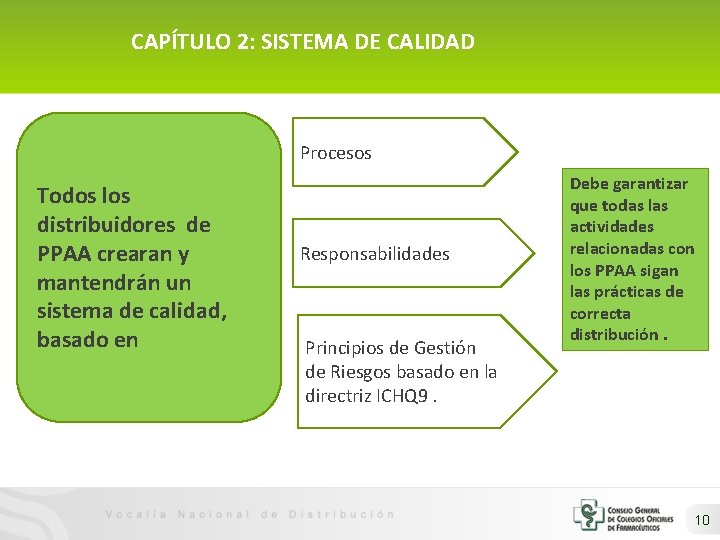
CAPÍTULO 2: SISTEMA DE CALIDAD Procesos Todos los distribuidores de PPAA crearan y mantendrán un sistema de calidad, basado en Responsabilidades Principios de Gestión de Riesgos basado en la directriz ICHQ 9. Debe garantizar que todas las actividades relacionadas con los PPAA sigan las prácticas de correcta distribución. 10

CAPÍTULO 3: PERSONAL PERSONA RESPONSABLE. El distribuidor debe asignar a una “persona responsable”. El Director Técnico Farmacéutico es el que ejerce está función en los almacenes de distribución mayorista. Formación: Inicial , continuada y evaluación de su eficacia. 11

FORMACION SOBRE LOS PRODUCTOS y PICTOGRAMAS. Reglamento (CE) nº 1272/2008. Pictogramas de Peligros Físicos GHS 01 Bomba explotando GHS 02 Llama GHS 03 Llama sobre un circulo GHS 04 Bombona de gas GHS 05 Corrosión Pictogramas de Peligros para la Salud GHS 06 Calavera y tibias cruzadas GHS 07 Signo de exclamación GHS 08 Peligro para la salud GHS 05 Corrosión Pictograma de Peligros para el Medio Ambiente GHS 09 Medio ambiente
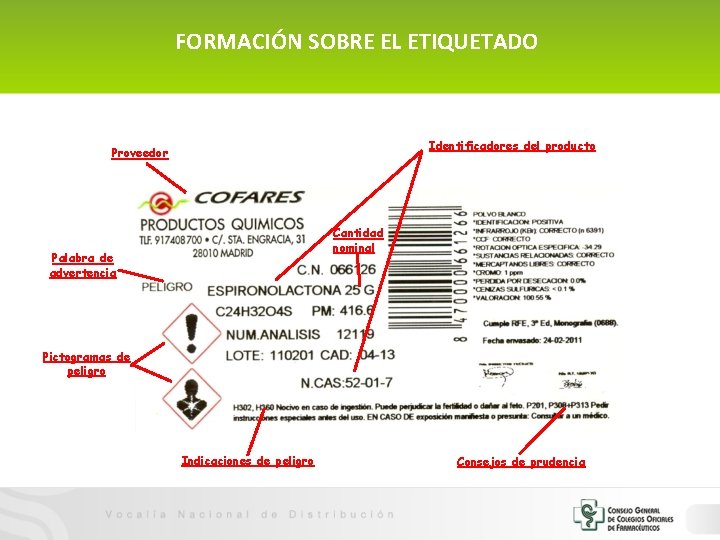
FORMACIÓN SOBRE EL ETIQUETADO Identificadores del producto Proveedor Cantidad nominal Palabra de advertencia Pictogramas de peligro Indicaciones de peligro Consejos de prudencia

FORMACION PARA CASOS DE ROTURAS O DERRAMES • Formación para actuar según el etiquetado del producto derramado con el apoyo de la ficha de datos de seguridad, que contiene el perfil de peligrosidad , toxicidad y seguridad del producto. • Primeros auxilios • Materiales absorbentes , batas , cepillos, guantes , gafas. . • Contenedor de residuos de un solo uso, que herméticamente cerrado se depositara en punto limpio del almacén para su recogida por el gestor de residuos peligrosos. • Exclusión de trabajadores sensibles. 14
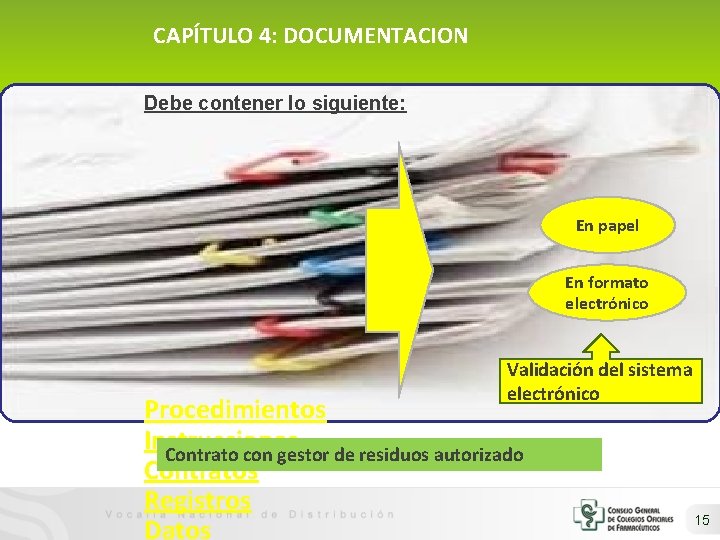
CAPÍTULO 4: DOCUMENTACION Debe contener lo siguiente: En papel En formato electrónico Validación del sistema electrónico Procedimientos Instrucciones Contrato con gestor de residuos autorizado Contratos Registros Datos 15

CAPÍTULO 4: DOCUMENTACIÓN Registros : Traza de todas las actividades Registros de compra y venta con: -Fechas -Nombre del principio activo -Cantidades -Nº de lote y caducidad. -Nombre y dirección de proveedor y /o del fabricante original y destinatario. -Certificados de análisis , incluidos los del fabricante original. Se conservaran hasta después de un año de la fecha de caducidad o tres años tras la distribución total en caso de retest. 16

DATOS DEL FABRICANTE ORIGINAL 17

PROVEEDORES DE PPAA • El Proveedor puede ser fabricante , importador o distribuidor, y debe estar registrado en RUESA. • Para la Oficina de Farmacia es importante que además del distribuidor , el fabricante total o parcial de PPAA este registrado en la AEMPS, y que tenga la Certificación en las Normas de Correcta Fabricación y Distribución. Sí no fuera así la farmacia tendría que realizar el análisis completo de los PPAA según farmacopea. • Los distribuidores fabricantes parciales en España contamos con las Asociación de Distribuidores de Sustancias (ADS ) dónde se exige la NCF a sus asociados. 18
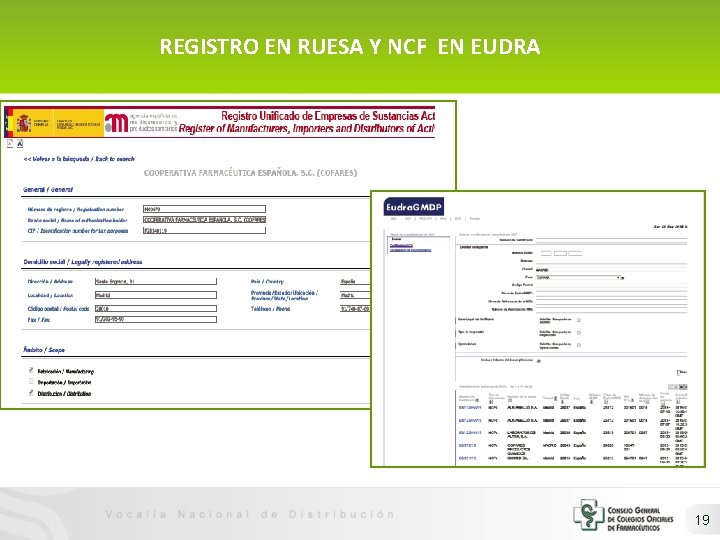
REGISTRO EN RUESA Y NCF EN EUDRA 19

CLIENTES de PPAA Los Distribuidores mayoristas podrán suministrar los PPAA a : -Distribuidores -Fabricantes -Farmacias o servicios de farmacia. 20

CAPÍTULO 5: LOCALES Y EQUIPO. Los distribuidores de PPAA deben disponer de locales, instalaciones y equipos adecuados para poder garantizar que se conservan y distribuyen de forma apropiada. Control de acceso y equipos calibrados vs estándar trazable. Pueden requerir cuartos, armarios con medidas especiales de seguridad , separados del resto de productos. Deben garantizar la protección contra contaminaciones cruzadas. Especial precaución con PPAA sensibilizantes, farmacológicamente muy activos y toxicidad elevada.

CAPÍTULO 7: DEVOLUCIONES, RECLAMACIONES Y RETIRADAS DE MEDICAMENTOS 22

Gracias por su Atención
- Slides: 23