Prast rakkude detergentidega ttlemist jb jrele valguline tstoskelett
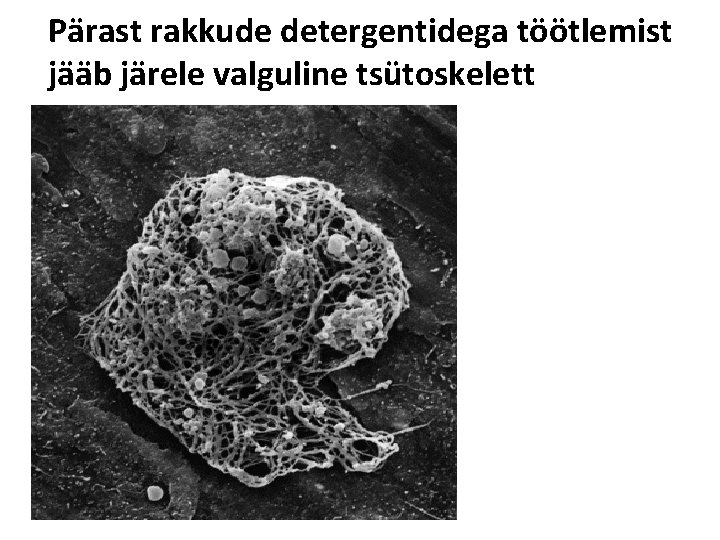
Pärast rakkude detergentidega töötlemist jääb järele valguline tsütoskelett
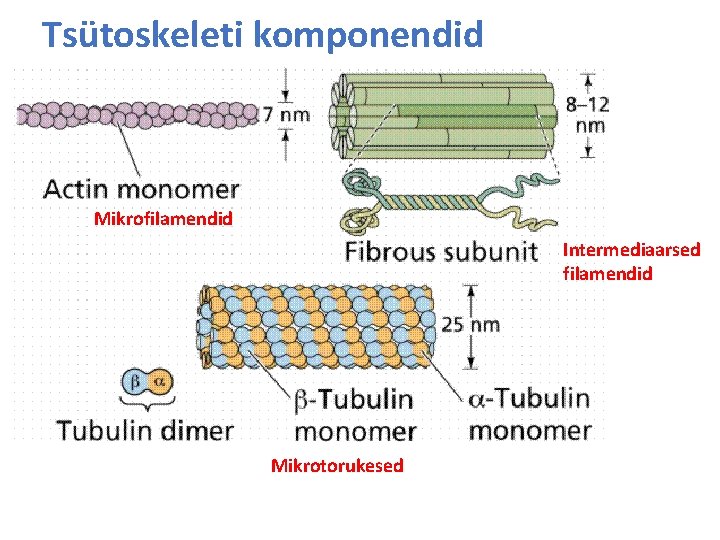
Tsütoskeleti komponendid Mikrofilamendid Intermediaarsed filamendid Mikrotorukesed
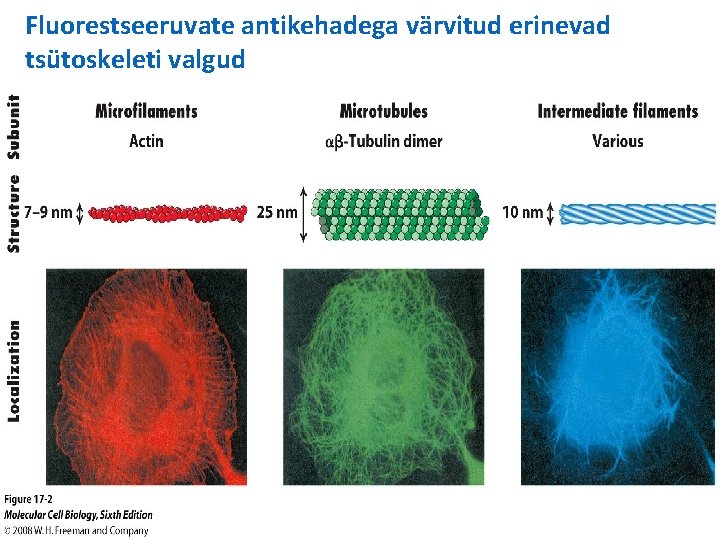
Fluorestseeruvate antikehadega värvitud erinevad tsütoskeleti valgud
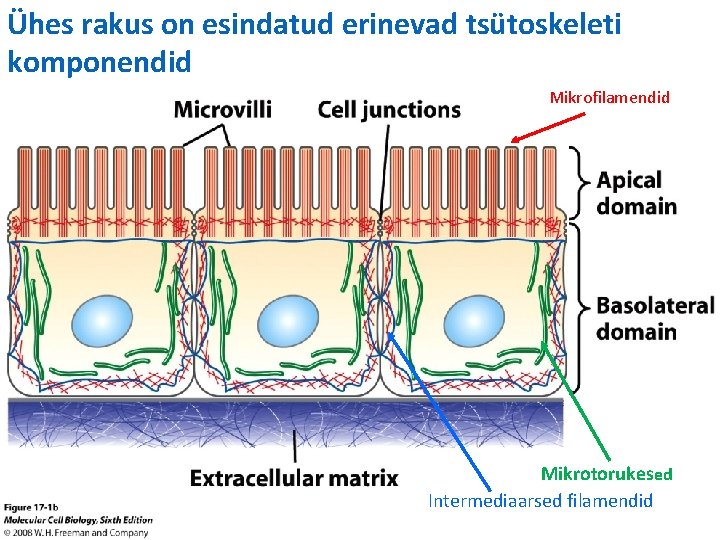
Ühes rakus on esindatud erinevad tsütoskeleti komponendid Mikrofilamendid Mikrotorukesed Intermediaarsed filamendid

Tsütoskeleti roll rakus Liikumised lihasrakud viburid kromosoomid organellid Ainete transport (vesiikulites) Kuju Polaarsus Signaali ülekanne

Tsütoskeleti struktuur võimaldab organellide/ rakkude liikumisel kasutada kahte erinevat mehhanismi: 1) Liikumine eriliste ensüümide, mida nim mootorvalkudeks, abil. Mootorvalgud kasutavad ATP hüdrolüüsi energiat libisemiseks piki mikrofilamenti või mikrotorukest, võimaldades nendega seotud organellidel ja vesiikulitel liikuda, võimaldades mikrofilamentidel või mikrotorukestel libiseda üksteise suhtes. 2) Liikumine mikrofilamentide ja mikrotorukeste monomeerideks lagunemise ja uuesti polümeriseerumise vahendusel

Aktiin ja mikrofilamendid

Aktiini koostis ja omadused *Aktiin on mittefotosünteesiva eukarüootse raku kõige levinumaks valguks, moodustades 1 -5% koguvalgust (~0. 5 m. M), aga lihasrakkudes võib aktiini kontsentratsioon olla kuni 10 korda kõrgem. * kodeeritud geenide perekonna poolt (Inimesel on 6 geeni, taimedel võib olla kuni 60 geeni) Selgroogsetes aktiinide geenide produktid erinevad ainult 45 aminohappe poolest, kuid erinevate geenide kodeeritud aktiinimolekulide funktsioonid on erinevad *geenid on konserveerunud molekulis ~375 aminohappe jääki (42 k. Da) *esineb kahel kujul: globulaarne monomeer (G-aktiin) G-aktiini molekul on polaarne - molekuli jaotab kaheks osaks vagumus, millesse seostuvad ATP ja Mg niitjas polümeer G-aktiinist (F-aktiin)
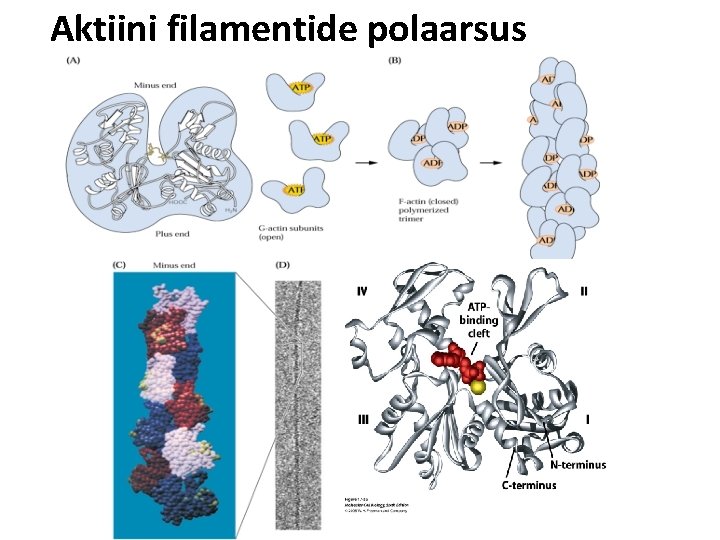
Aktiini filamentide polaarsus
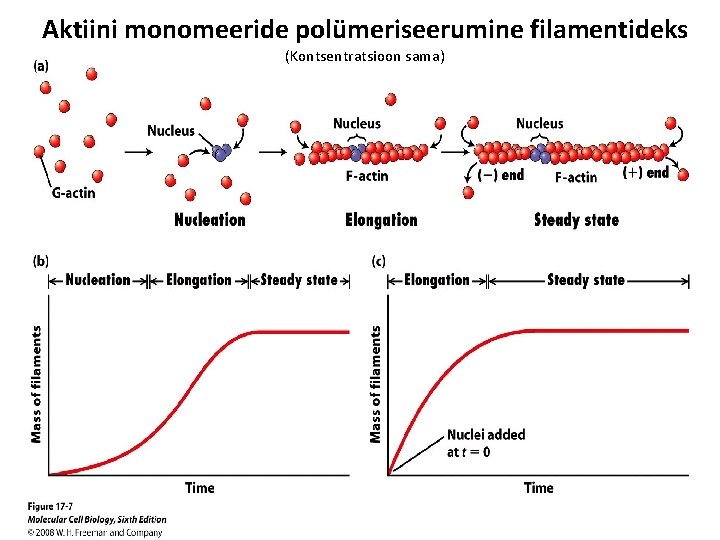
Aktiini monomeeride polümeriseerumine filamentideks (Kontsentratsioon sama)
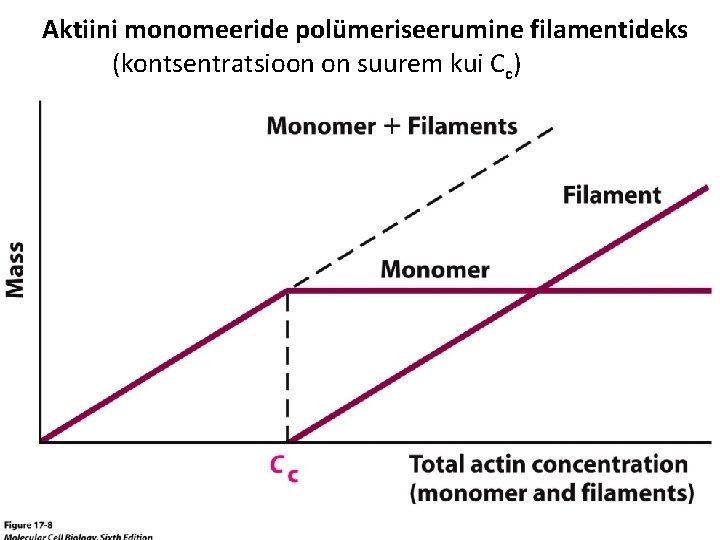
Aktiini monomeeride polümeriseerumine filamentideks (kontsentratsioon on suurem kui Cc) 0, 1 u. M
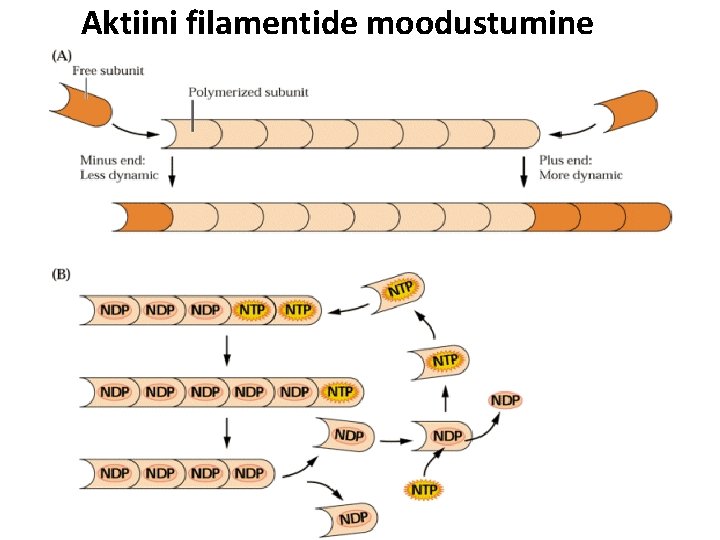
Aktiini filamentide moodustumine

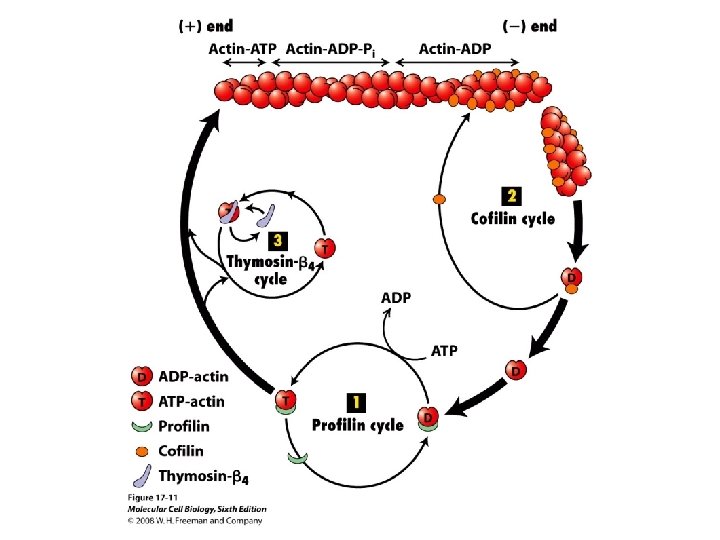
Mitmesugused toksiinid muudavad aktiini monomeer-polümeer tasakaalu • Seentest pärit alkaloid tsütohalasiini toimel aktiini fibrillid depolümeriseeruvad. Selle põhjuseks on toksiini seostumine filamentide (+) otsale ja filamentide pikenemise pärssimine. • Latrunkuliin käsnadest seostub G aktiiniga ja takistab subühikute polümeriseerumist. Mõlemi toksiini toimel elusates rakkudes kaob tsütoskelett ja liikumised (näiteks tsütokinees) lakkavad. • Toksiin falloidiin (seenest Amanita phalloides) seostub F aktiiniga, ühendades naabermonomeerid nii tugevalt, et nende dissotsieerumist ei toimu. Seetõttu kasutatakse fluorestsentsvärvidega värvitud ja falloidiiniga ühendatud aktiini filamentide värvimiseks UV mikroskoopia jaoks.
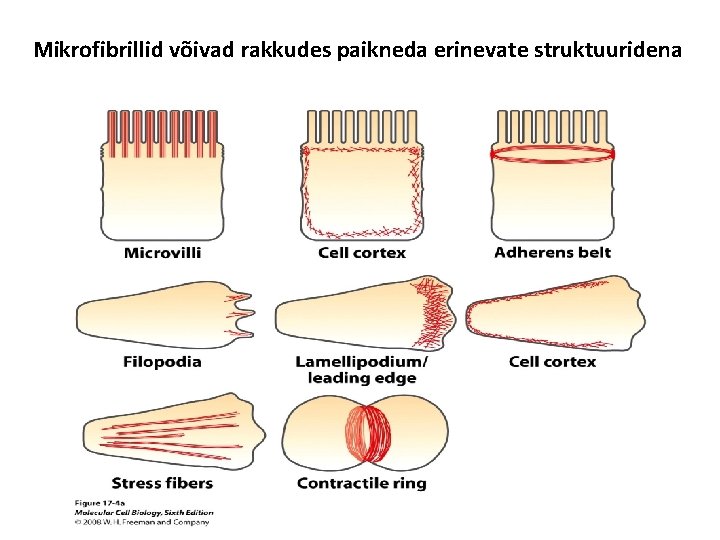
Mikrofibrillid võivad rakkudes paikneda erinevate struktuuridena
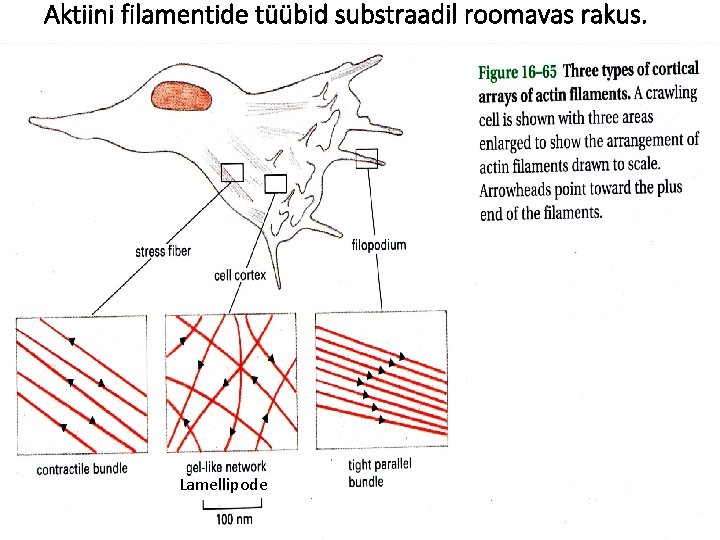
Aktiini filamentide tüübid substraadil roomavas rakus. Lamellipode
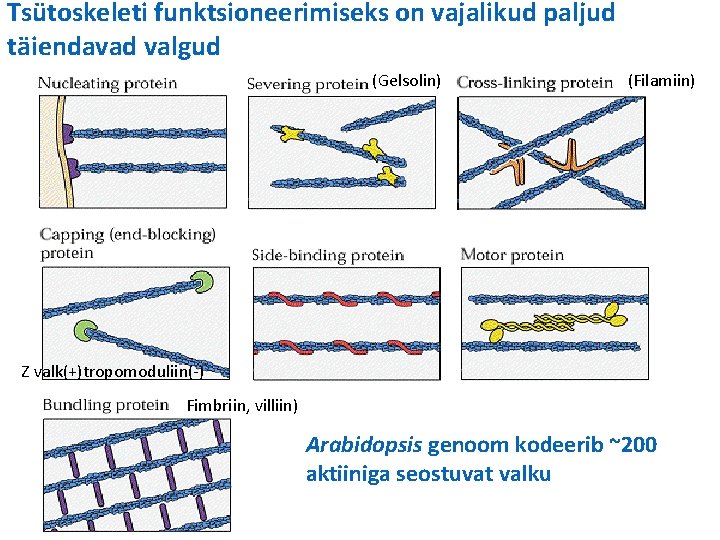
Tsütoskeleti funktsioneerimiseks on vajalikud paljud täiendavad valgud (Gelsolin) ARP valgud Gelsoliin, kofiliin (Filamiin) filamiin Z valk(+)tropomoduliin(-) Troponiin, Fimbriin, villiin) tropomüosiin Arabidopsis genoom kodeerib ~200 seostuvat valku Fimbriin, aktiiniga villiin
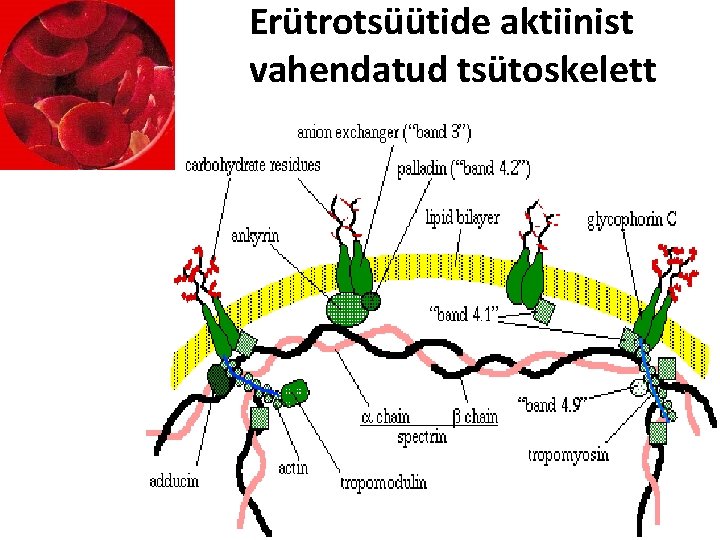
Erütrotsüütide aktiinist vahendatud tsütoskelett

Erütrotsüütide aktiinist vahendatud tsütoskelett
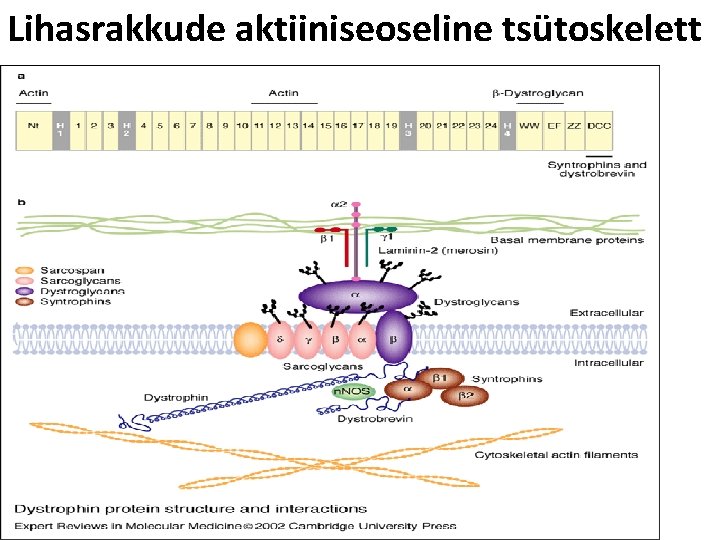
Lihasrakkude aktiiniseoseline tsütoskelett
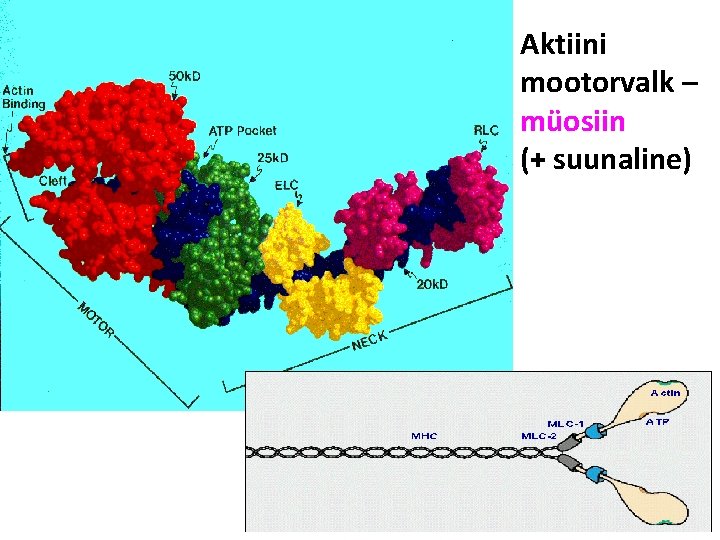
Aktiini mootorvalk – müosiin (+ suunaline)
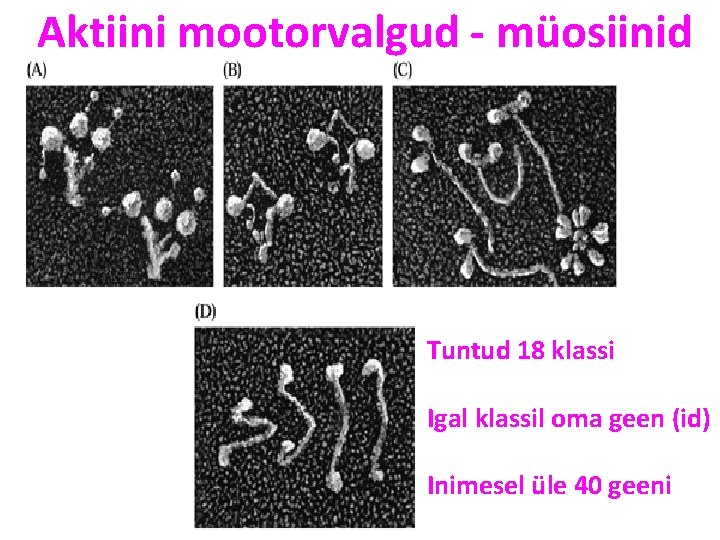
Aktiini mootorvalgud - müosiinid Tuntud 18 klassi Igal klassil oma geen (id) Inimesel üle 40 geeni
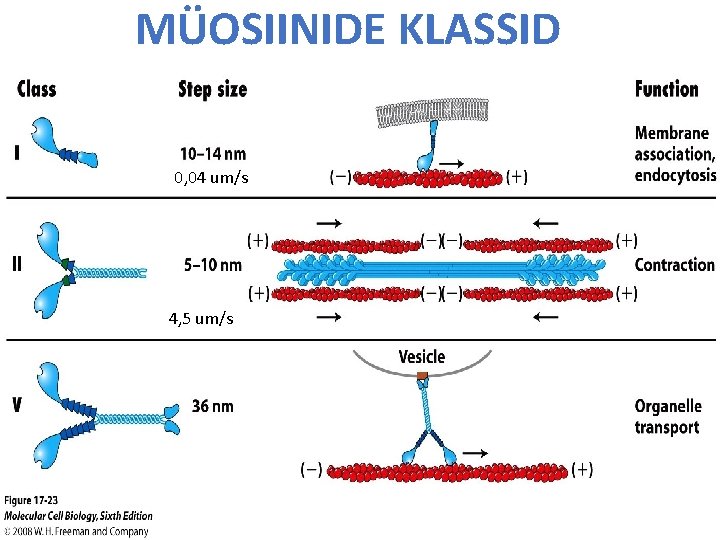
MÜOSIINIDE KLASSID 0, 04 um/s 4, 5 um/s
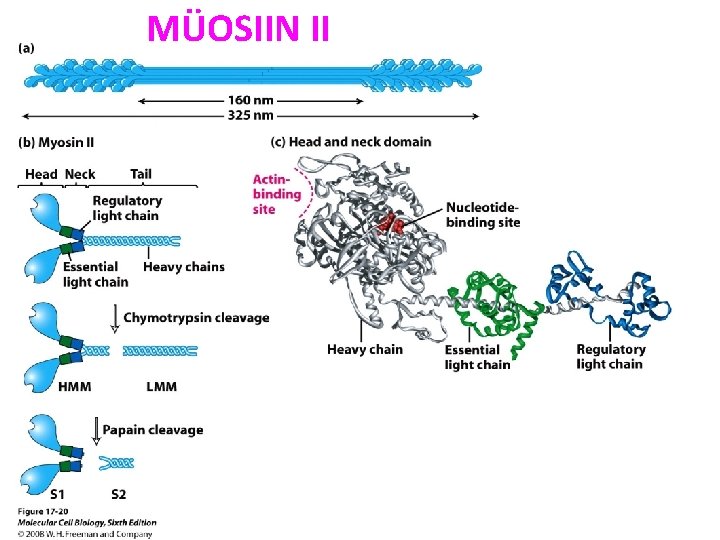
MÜOSIIN II
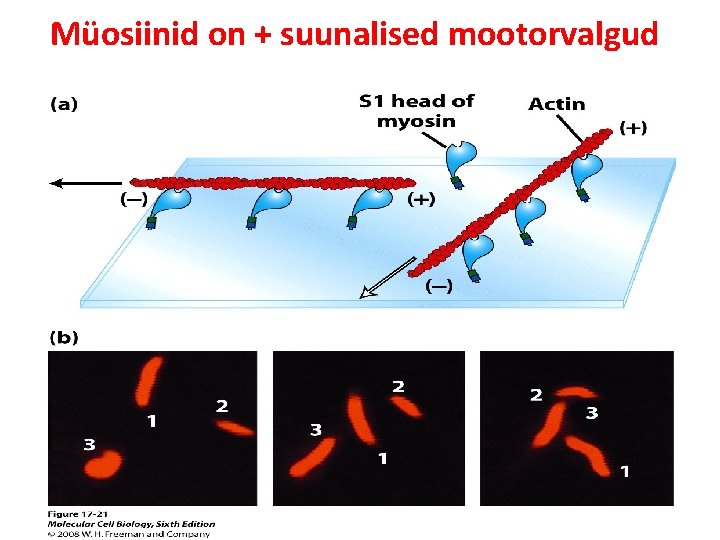
Müosiinid on + suunalised mootorvalgud
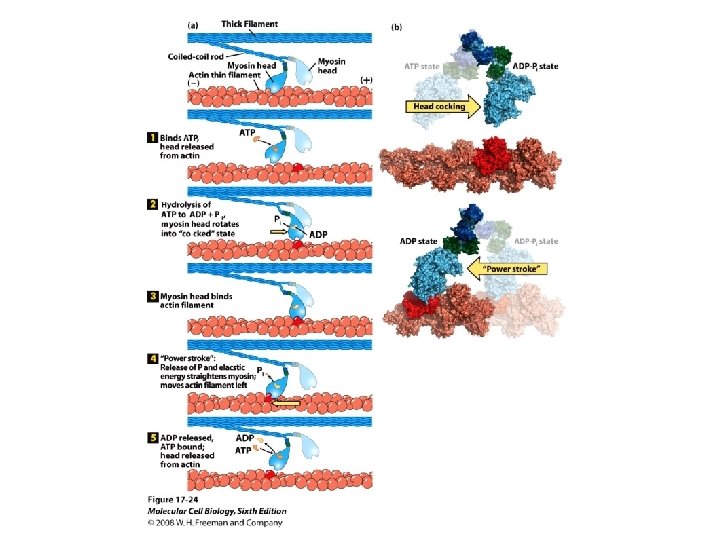
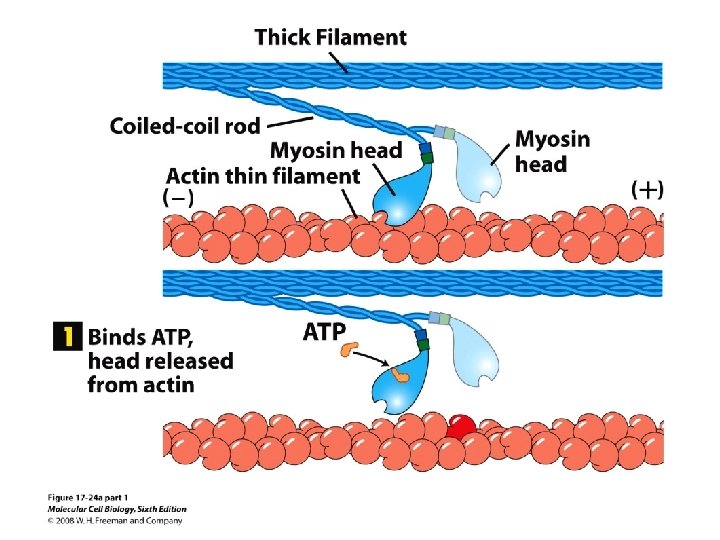
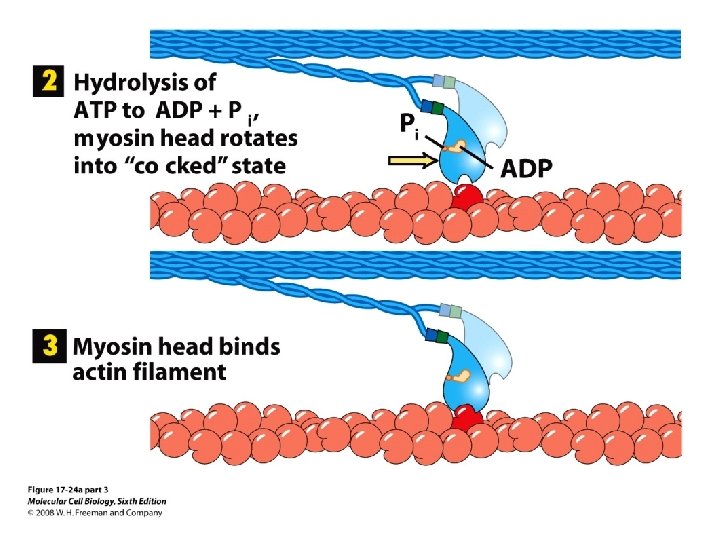
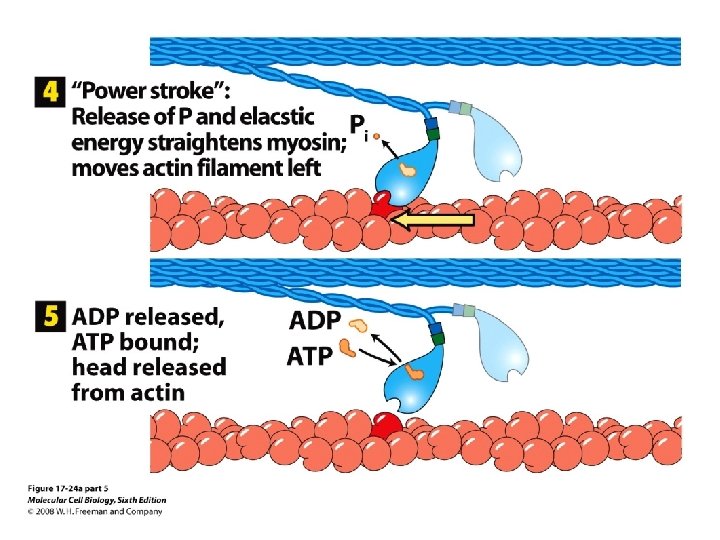
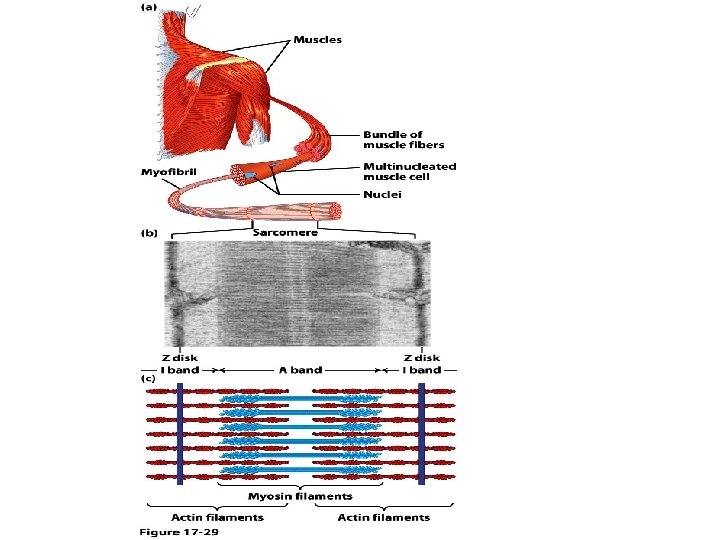
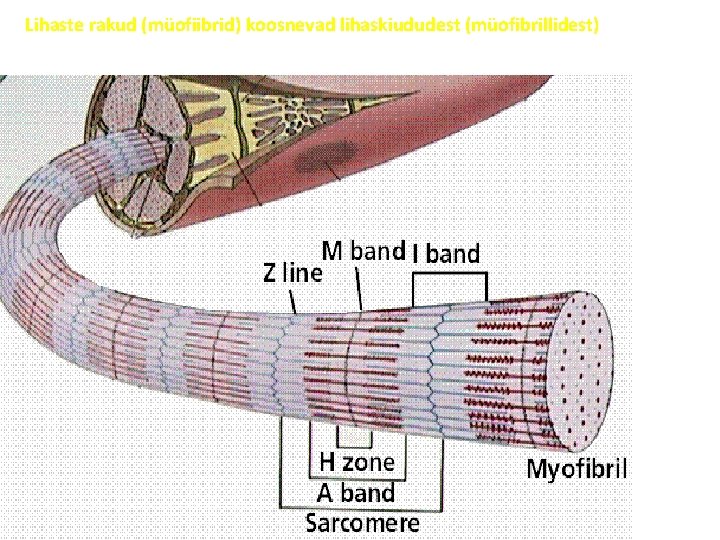
Lihaste rakud (müofiibrid) koosnevad lihaskiududest (müofibrillidest)
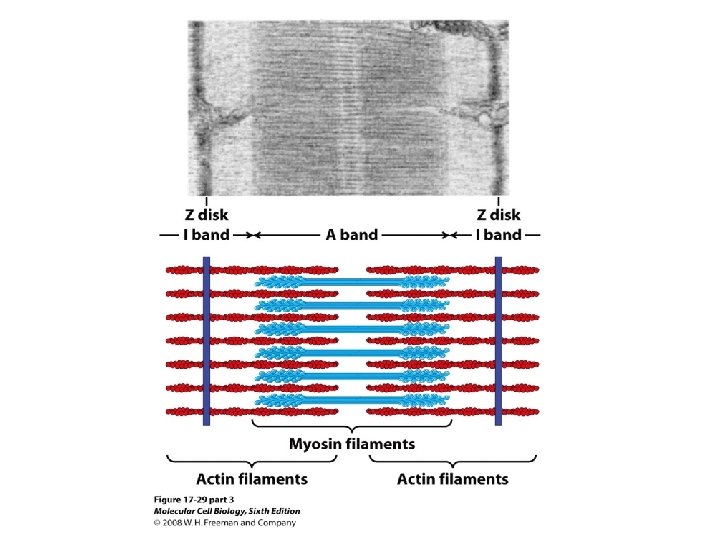
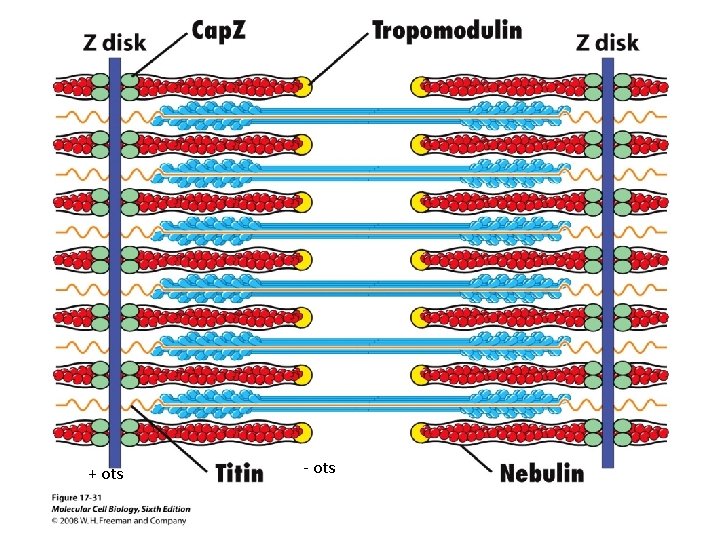
+ ots - ots
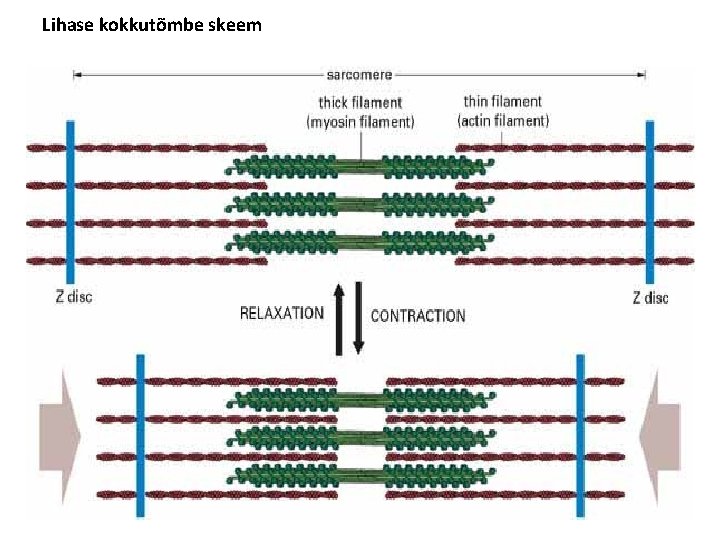
Lihase kokkutõmbe skeem
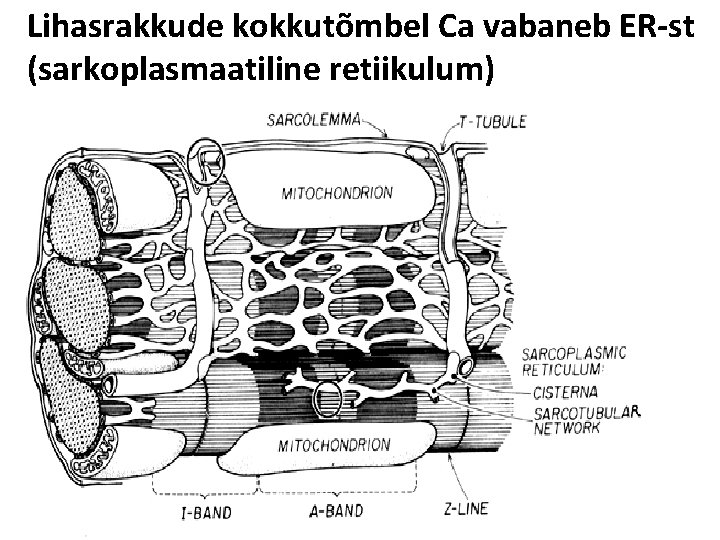
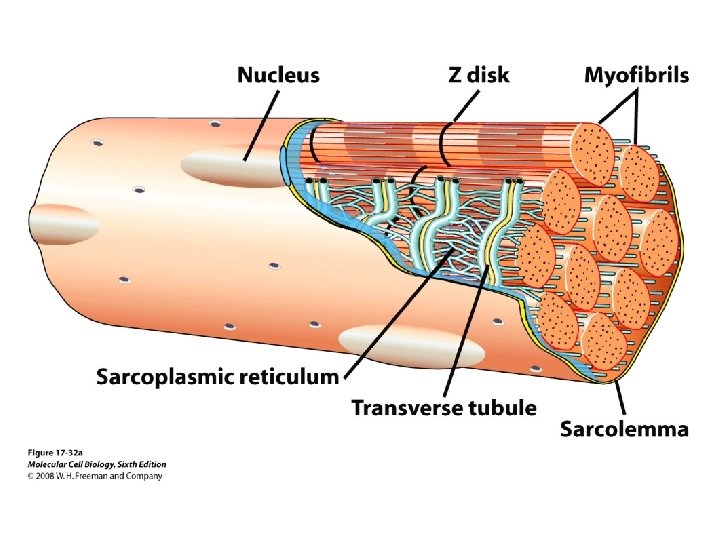
Lihasrakkude kokkutõmbel Ca vabaneb ER-st (sarkoplasmaatiline retiikulum)
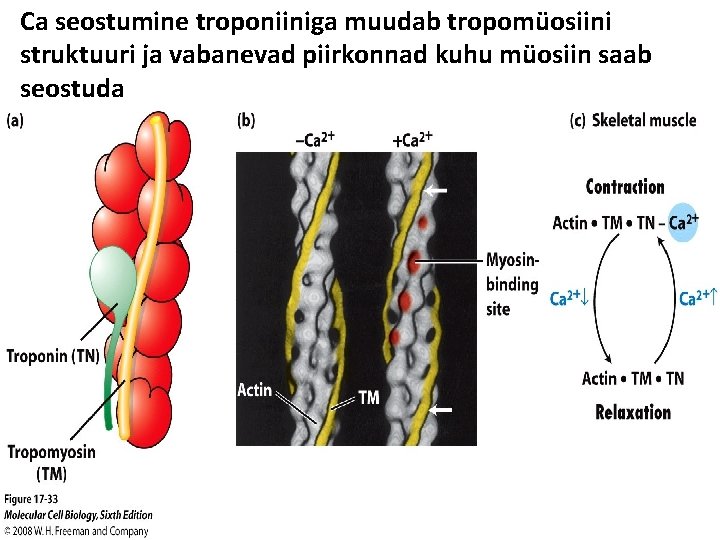
Ca seostumine troponiiniga muudab tropomüosiini struktuuri ja vabanevad piirkonnad kuhu müosiin saab seostuda
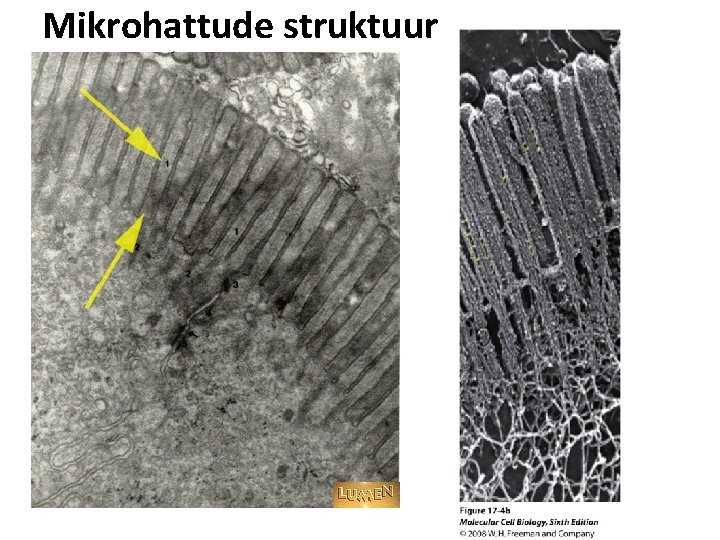
Mikrohattude struktuur
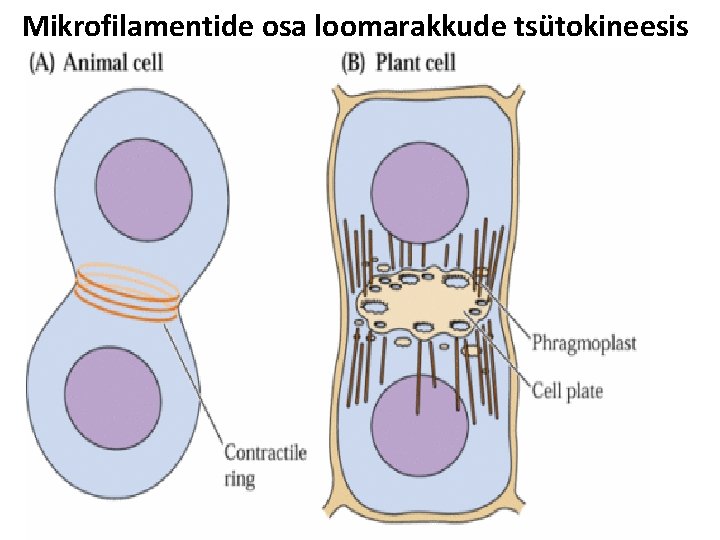
Mikrofilamentide osa loomarakkude tsütokineesis

Kasutamata
- Slides: 40