Prambule anmie Excs de destruction Dfaut de production
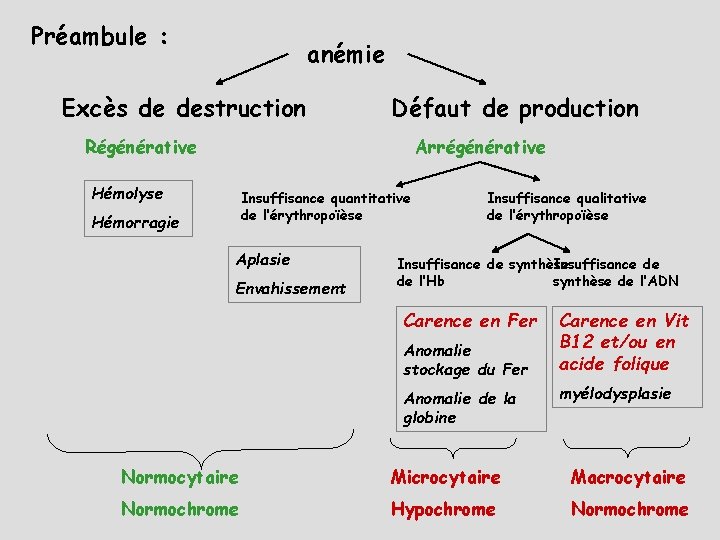
Préambule : anémie Excès de destruction Défaut de production Régénérative Arrégénérative Hémolyse Insuffisance quantitative de l’érythropoïèse Hémorragie Aplasie Envahissement Insuffisance qualitative de l’érythropoïèse Insuffisance de synthèse Insuffisance de de l’Hb synthèse de l’ADN Carence en Fer Anomalie stockage du Fer Anomalie de la globine Carence en Vit B 12 et/ou en acide folique myélodysplasie Normocytaire Microcytaire Macrocytaire Normochrome Hypochrome Normochrome

Cours DCEM 1 2009 -2010 Métabolisme du Fer Pascale CORNILLET-LEFEBVRE Laboratoire d’Hématologie CHU de REIMS

Plan 1 -Fonctions et anomalies 2 -Besoins et apports alimentaires 3 - Cycle journalier : en circuit fermé 4 - Description des étapes du Cycle du Fer : mécanismes et acteurs 4 -1 absorption intestinale/ transferrine 4 -2 captation du Fer par la MO/ récepteur à la transferrine 4 -3 boucle de l’érythropoïèse 4 -4 captation du Fer par le foie/ ferritine/hémosidérine 4 -5 élimination

Plan (suite) 5 -Régulation de l’homéostasie du Fer Senseurs et Cibles Les acteurs Mécanismes d’augmentation de l’absorption intestinale Système IRE/IRP Hepcidine HFE 6 - Conséquences d’une carence en Fer 7 - Tests d’exploration 8 - Diagnostics étiologiques d’une carence en Fer

Fonctions et Anomalies du métabolisme du Fer Fonctions : Anomalies : • Transporteur d’Oxygène • Carence : Anémie microcytaire ferriprive • Transporteur d’électron Fe+++ Catalyseur des réactions d’oxydo-réduction • Surcharge Hémochromatose

Besoin en Fer : Homme : 1 mg/j Femme : 2 mg/j Augmentation physiologique des besoins : femme : menstruation : 8 à 20 mg/mois femme enceinte : 3 -6 mg/j (total = 500 -900 mg) femme allaitante : 3 mg/j Nourisson : ( croissance et régime lacté) Adolescent : + 0, 5 mg/j (croissance)

Distribution du Fer dans l’organisme : 3 à 4 g Tissus/cellules Enzymes ** 65 -70% 5% 0, 5% Erythroblastes GR Muscle Transport Transferrine 0, 1% Plasma Réserve Ferritine Hémosidérrine 15% Macrophages (Foie Rate MO) Hépatocytes Muscles Trois Fer (Fe++) compartiments héminique lié Fonctionnel Hémoglobine Myoglobine Enzymes * Fer (Fe+++) non héminique FNL * Ex: cytochrome, ** Ex : ribonucléotide réductase Plasma Tissus

Cycle journalier du Fer : « en circuit fermé » ferritine 1 mg/j transferrine Boucle de l’érythropoïèse 25 mg/j
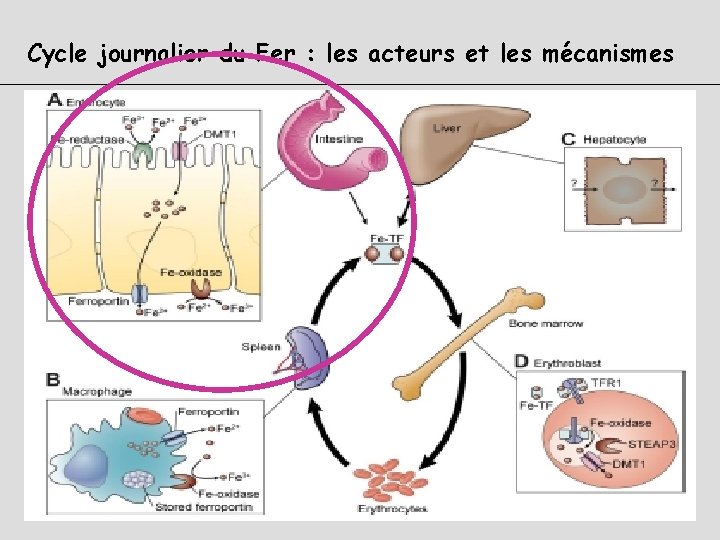
Cycle journalier du Fer : les acteurs et les mécanismes

Absorption intestinale (1) Apport alimentaire : 10 -20 mg /j Taux d’absorption = 10 % de la ration alimentaire Foie de porc : 19 mg/100 mg Levure de bière : 17, 3 Cacao : 12, 5 Lentilles : 8, 6 Soja : 8, 4 Jaune d’œuf : 7, 2 Fruits secs : 4, 5 Epinards : 3, 1 Côtes de bœuf : 3, 1 Vin : 0, 3 -0, 5 Lait de vache : 0, 04 Lait maternel : 0, 05 Mécanismes : Absorption du Fer héminique Absorption du Fer non héminique Facteurs « alimentaires » influençant l’absorption ration alimentaire : X 2 (max) Fer héminique = 20% Fer non héminique = 1 -4% favorisée par : vit C Inhibée par: lait, thé (45 -95%)
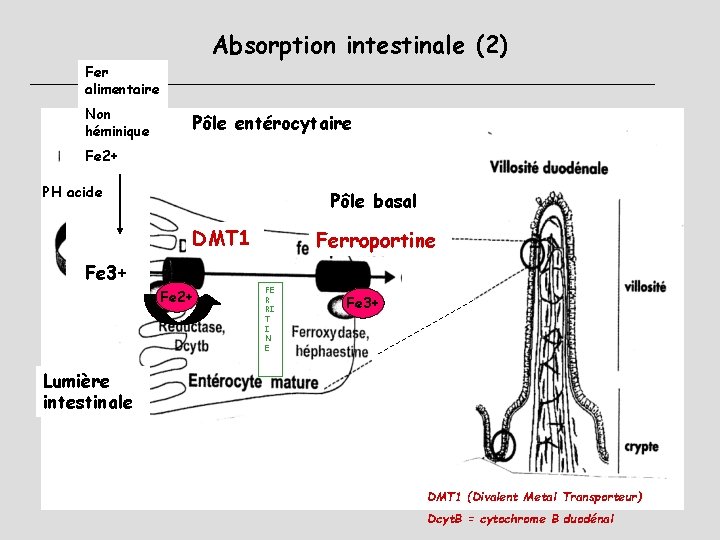
Absorption intestinale (2) Fer alimentaire Non héminique Pôle entérocytaire Fe 2+ PH acide Pôle basal DMT 1 Ferroportine Fe 3+ Fe 2+ FE R RI T I N E Fe 3+ Lumière intestinale DMT 1 (Divalent Metal Transporteur) Dcyt. B = cytochrome B duodénal
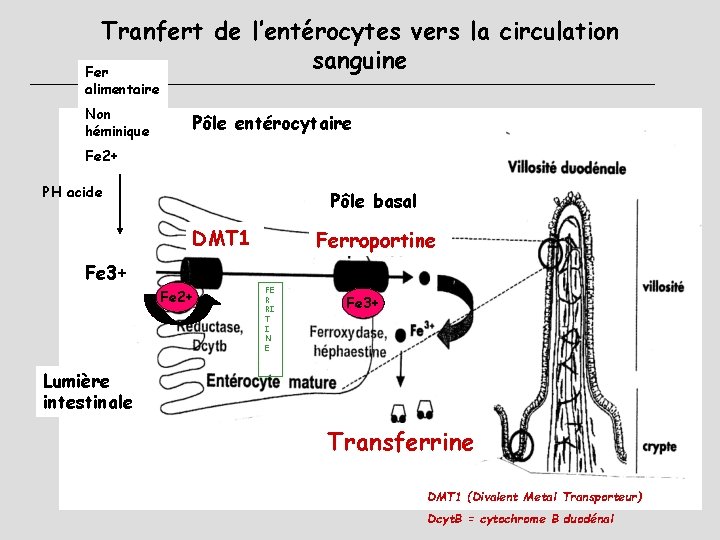
Tranfert de l’entérocytes vers la circulation sanguine Fer alimentaire Non héminique Pôle entérocytaire Fe 2+ PH acide Pôle basal DMT 1 Ferroportine Fe 3+ Fe 2+ FE R RI T I N E Fe 3+ Lumière intestinale Transferrine DMT 1 (Divalent Metal Transporteur) Dcyt. B = cytochrome B duodénal
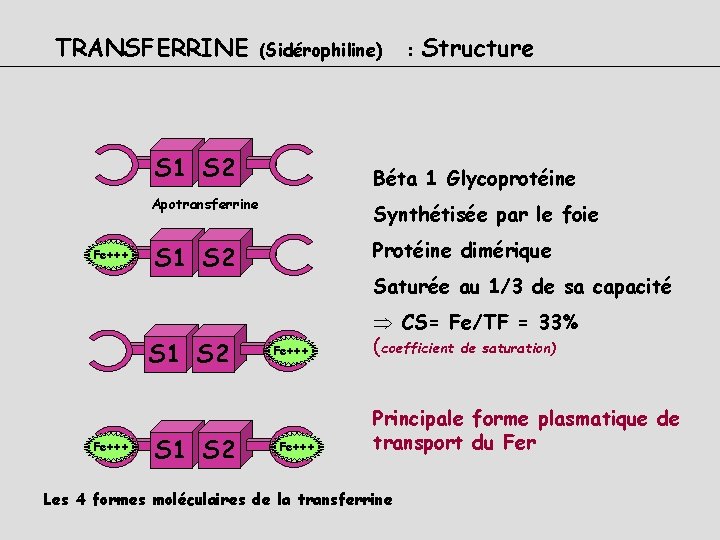
TRANSFERRINE (Sidérophiline) S 1 S 2 Fe+++ Structure Béta 1 Glycoprotéine Apotransferrine Synthétisée par le foie S 1 S 2 Protéine dimérique S 1 S 2 Fe+++ : S 1 S 2 Saturée au 1/3 de sa capacité Fe+++ Þ CS= Fe/TF = 33% (coefficient de saturation) Principale forme plasmatique de transport du Fer Les 4 formes moléculaires de la transferrine

TRANSFERRINE (Sidérophiline) : rôles majeurs üTransport sanguin du Fer üCapte le Fer : • apporté par l’absorption intestinale • du SRH (via macrophages) après hémolyse physiologique des GR üApport du Fer aux cellules : • à la MO pour la synthèse de l’hème • aux réserves dans les cellules du SRH et dans les hépatocytes
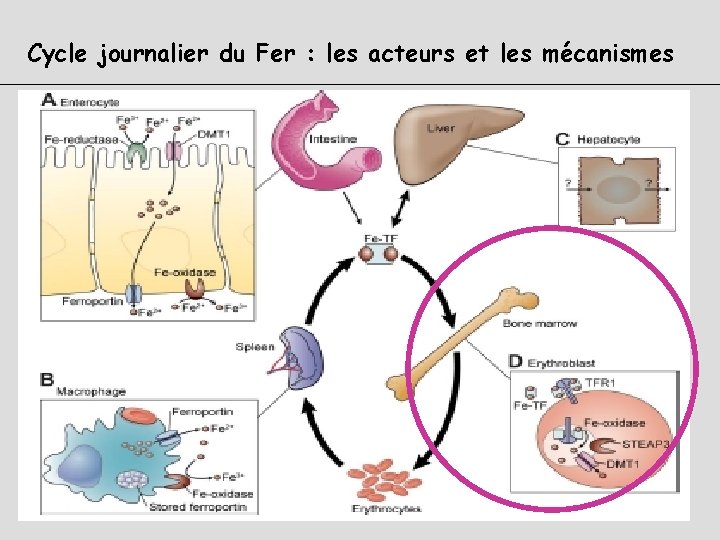
Cycle journalier du Fer : les acteurs et les mécanismes
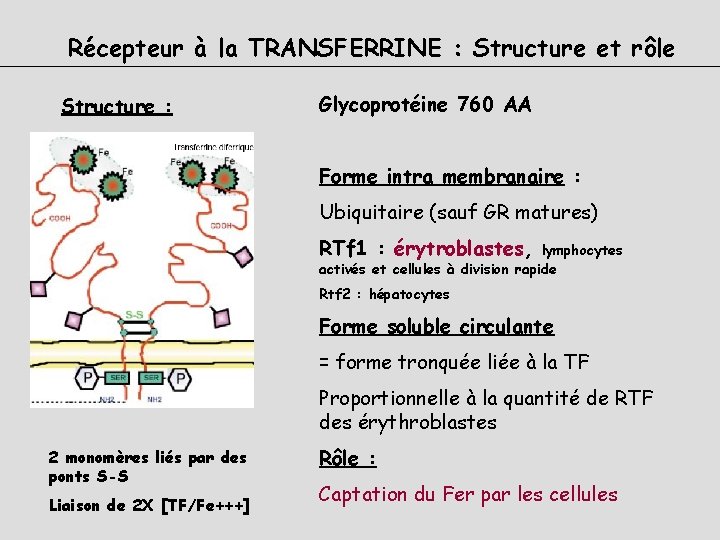
Récepteur à la TRANSFERRINE : Structure et rôle Structure : Glycoprotéine 760 AA Forme intra membranaire : Ubiquitaire (sauf GR matures) RTf 1 : érytroblastes, lymphocytes activés et cellules à division rapide Rtf 2 : hépatocytes Forme soluble circulante = forme tronquée liée à la TF Proportionnelle à la quantité de RTF des érythroblastes 2 monomères liés par des ponts S-S Liaison de 2 X [TF/Fe+++] Rôle : Captation du Fer par les cellules
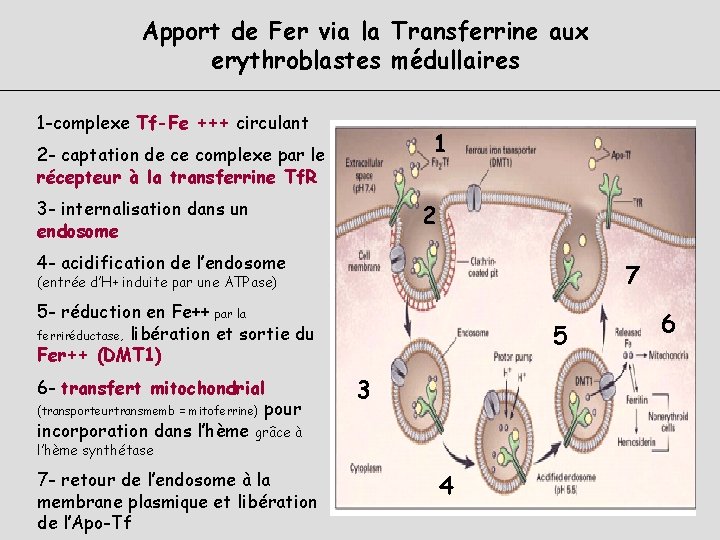
Apport de Fer via la Transferrine aux erythroblastes médullaires 1 -complexe Tf-Fe +++ circulant 1 2 - captation de ce complexe par le récepteur à la transferrine Tf. R 3 - internalisation dans un endosome 2 4 - acidification de l’endosome 7 (entrée d’H+ induite par une ATPase) 5 - réduction en Fe++ par la ferriréductase, libération et sortie du Fer++ (DMT 1) 6 - transfert mitochondrial (transporteurtransmemb = mitoferrine) pour incorporation dans l’hème grâce à 5 3 l’hème synthétase 7 - retour de l’endosome à la membrane plasmique et libération de l’Apo-Tf 4 6
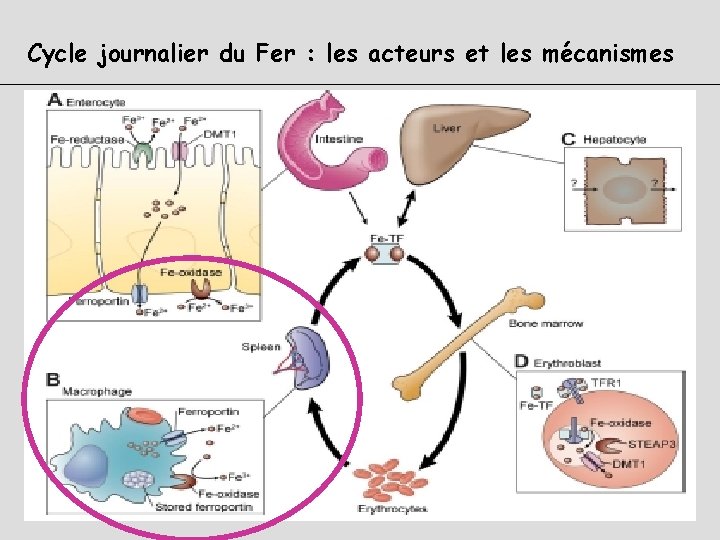
Cycle journalier du Fer : les acteurs et les mécanismes
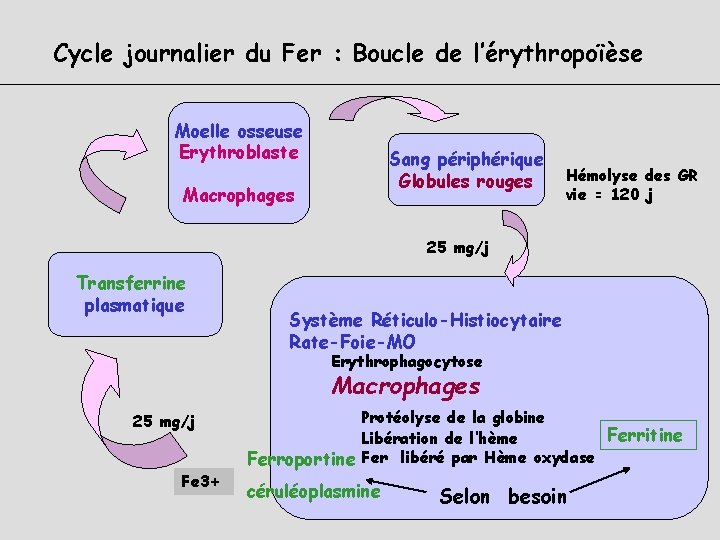
Cycle journalier du Fer : Boucle de l’érythropoïèse Moelle osseuse Erythroblaste Sang périphérique Globules rouges Macrophages Hémolyse des GR vie = 120 j 25 mg/j Transferrine plasmatique Système Réticulo-Histiocytaire Rate-Foie-MO Erythrophagocytose Macrophages 25 mg/j Fe 3+ Protéolyse de la globine Ferritine Libération de l’hème Ferroportine Fer libéré par Hème oxydase céruléoplasmine Selon besoin
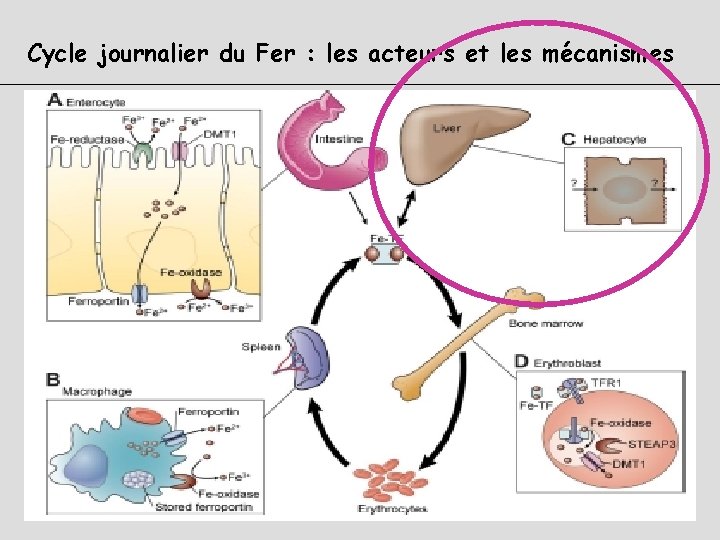
Cycle journalier du Fer : les acteurs et les mécanismes

Apport de Fer via la Transferrine au foie Captation du complexe Tf-Fe +++ circulant par le récepteur à la transferrine RTf 2 Libération du fer et relargage de la transferrine par un mécanisme homologue à celui décrit dans les érythroblastes Mise en réserve dans les hépatocytes et dans les macrophages hépatiques Sous 2 formes : FERRITINE et HEMOSIDERINE

FERRITINE glycoprotéine soluble , principale forme de stockage du Fer FOIE (1/3) , RATE MO (macrophages) (1/3), MUSCLE (1/3) macromolécule « cage » (24 sous-unités) au centre 4500 atomes de Fer ferrique (Fe+++) libération par système rédox Fe 3+-> Fe 2+ 3 formes : 1 -sans Fer, circulante (+/- hydrosoluble) : apoferritine (reflet des réserves) : dosable 2 -ferritine 3 -dénaturées et agrégée en micelle = hémosidérine fonction : réserve intratissulaire rapidement mobilisable = transfert rapide à la transferrine (régulation)
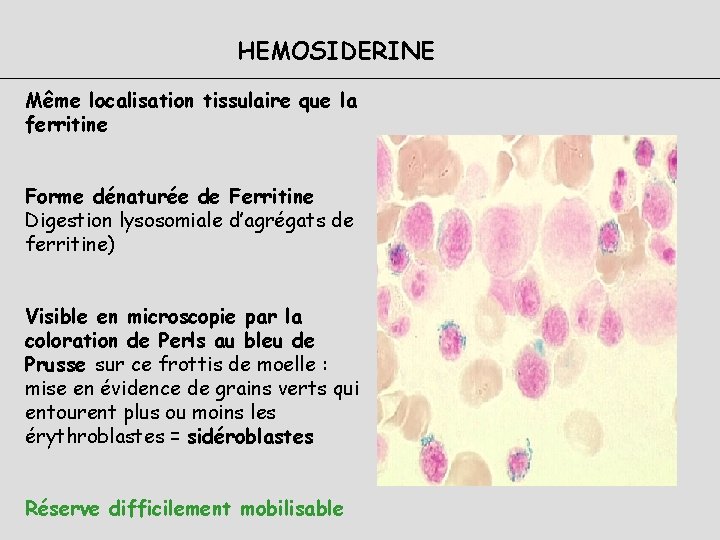
HEMOSIDERINE Même localisation tissulaire que la ferritine Forme dénaturée de Ferritine Digestion lysosomiale d’agrégats de ferritine) Visible en microscopie par la coloration de Perls au bleu de Prusse sur ce frottis de moelle : mise en évidence de grains verts qui entourent plus ou moins les érythroblastes = sidéroblastes Réserve difficilement mobilisable

Cycle journalier du Fer : Elimination Pertes physiologiques journalière faible = 1 mg Þ urinaires : < 0, 1 mg (+ si SN) Þ biliaires Þ desquamation (peau, phanères, muqueuse intestinale)=0, 9 mg Perte supplémentaire pour la femme menstruation = 30 mg/cycle soit 1 mg/j NB : 1 L de sang = 500 mg de Fer

Régulation de l’homéostasie du Fer : senseurs et cibles 2 senseurs : Réserve en Fer 2 cibles : Taux d’absorption = 10 % (1 mg/j) X 2 au maximum « signal régulateur des réserves » Taux d’érythropoïèse Relargage par le Macrophage Équilibre Délivrance <-> Réserve « signal régulateur érythroïde »

Régulation de l’homéostasie du Fer : les acteurs Ce sont des facteurs humoraux ou membranaires : Système IRE/IRP Transferrine DMT 1 Ferroportine Héphaestine/Céruloplasmine Hepcidine Récepteur à la transferrine HFE-B 2 m Mais restent des questions en suspens……. .
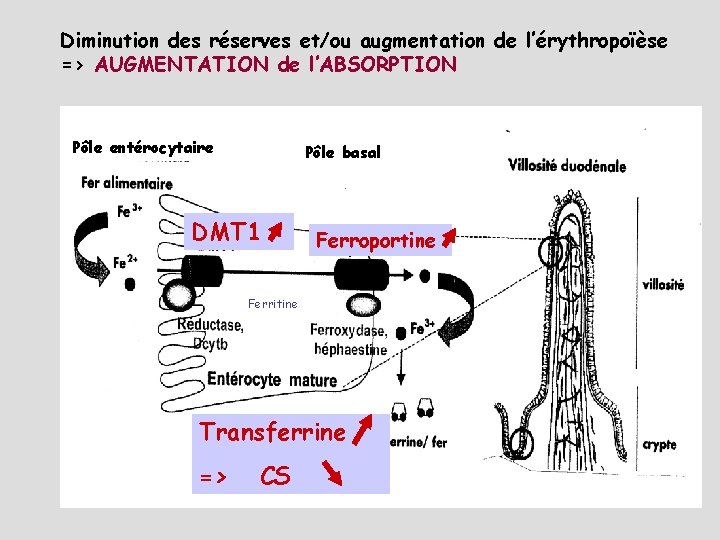
Diminution des réserves et/ou augmentation de l’érythropoïèse => AUGMENTATION de l’ABSORPTION Pôle entérocytaire Pôle basal DMT 1 Ferroportine Ferritine Transferrine => CS
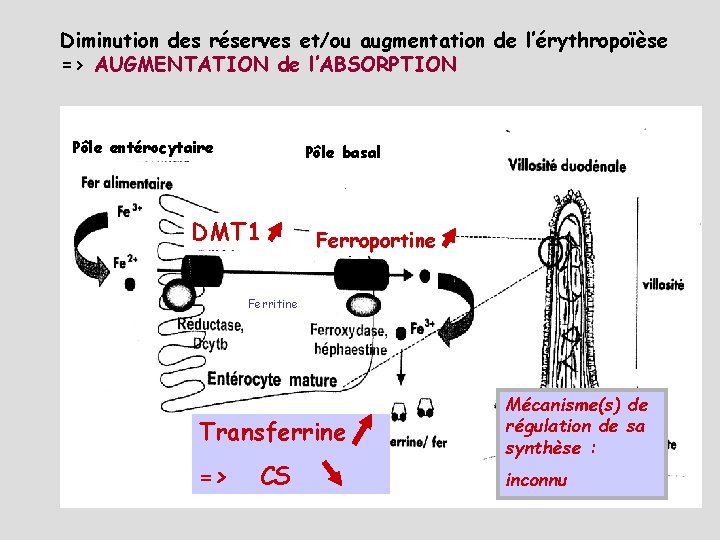
Diminution des réserves et/ou augmentation de l’érythropoïèse => AUGMENTATION de l’ABSORPTION Pôle entérocytaire Pôle basal DMT 1 Ferroportine Ferritine Transferrine => CS Mécanisme(s) de régulation de sa synthèse : inconnu
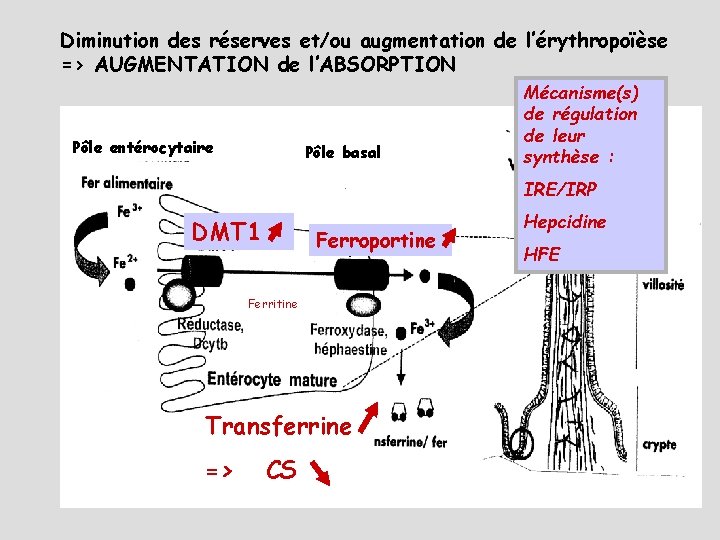
Diminution des réserves et/ou augmentation de l’érythropoïèse => AUGMENTATION de l’ABSORPTION Pôle entérocytaire Pôle basal Mécanisme(s) de régulation de leur synthèse : IRE/IRP DMT 1 Ferroportine Ferritine Transferrine => CS Hepcidine HFE
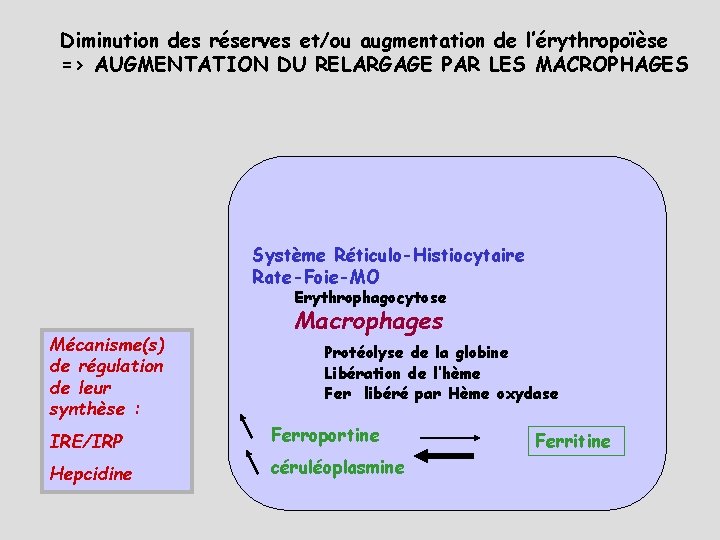
Diminution des réserves et/ou augmentation de l’érythropoïèse => AUGMENTATION DU RELARGAGE PAR LES MACROPHAGES Système Réticulo-Histiocytaire Rate-Foie-MO Erythrophagocytose Mécanisme(s) de régulation de leur synthèse : Macrophages Protéolyse de la globine Libération de l’hème Fer libéré par Hème oxydase IRE/IRP Ferroportine Hepcidine céruléoplasmine Ferritine

Régulation INTRACELLULAIRE de l’homéostasie du Fer : système IRP/IRE = Iron Regulatory Element séquence nucléique présente en 5 exemplaires en 5’ ou en 3’ d’un gène sensible au Fer site de reconnaissance spécifique de IRP. IRE IRP = Iron Regulatory Proteins protéine à centre Soufre-Fer 4 Fe-S Fixe 4 atomes de Fer-S = aconitase niche pour le Fer intracellulaire en présence de Fer la protéine est saturée en Fer et ne peut se fixer à l’IRE en absence de Fer l’IRP peut se fixer à l’IRE
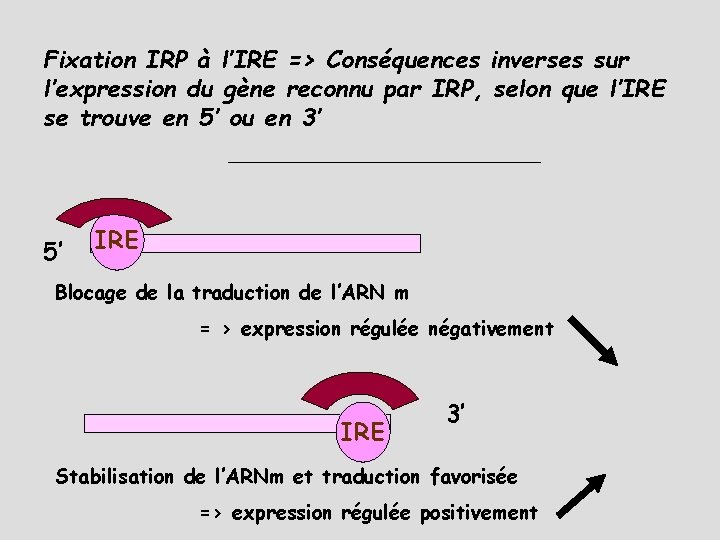
Fixation IRP à l’IRE => Conséquences inverses sur l’expression du gène reconnu par IRP, selon que l’IRE se trouve en 5’ ou en 3’ 5’ IRE Blocage de la traduction de l’ARN m = > expression régulée négativement IRE 3’ Stabilisation de l’ARNm et traduction favorisée => expression régulée positivement

SYSTEME IRE/IRP : Conclusions Le contenu cellulaire en Fer régule la conformation des protéines IRP Si déficit en FER : IRP est désaturée, se fixe sur les séquence IRE Si IRE est en 5’ => bloque la traduction ex FERRITINE (stockage) Si IRE est en 3’ => bloque la dégradation de l’ARN ex RECEPTEUR à la TRANSFERRINE (erythropoïèse) ex DMT 1 (absorption intestinale) ex FERROPORTINE (absorption instestinale) Si excès de Fer : mécanismes inverses

Régulation de l’homéostasie du Fer : Hepcidine : • découverte après screening des gènes hyperexprimés lors d’une surcharge en Fer (2001) • synthétisée dans le foie • structure = polypeptide (25 AA) • Rôle clé dans le métabolisme du Fer : bloque l’absorption du Fer alimentaire bloque le relargage du Fer macrophagique du foie • Comment agit-elle ? • Quels sont les évènements qui favorisent son expression ? • Quel est le mécanisme de régulation de son expression ?
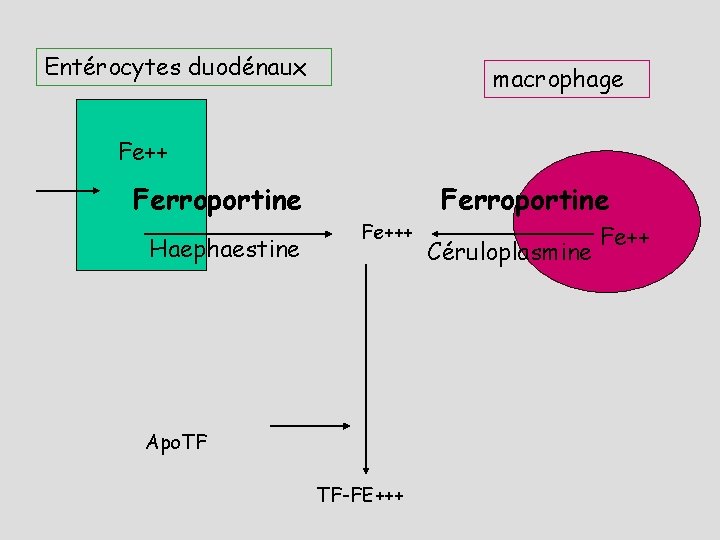
Entérocytes duodénaux macrophage Fe++ Ferroportine Haephaestine Fe+++ Apo. TF TF-FE+++ Ferroportine Céruloplasmine Fe++
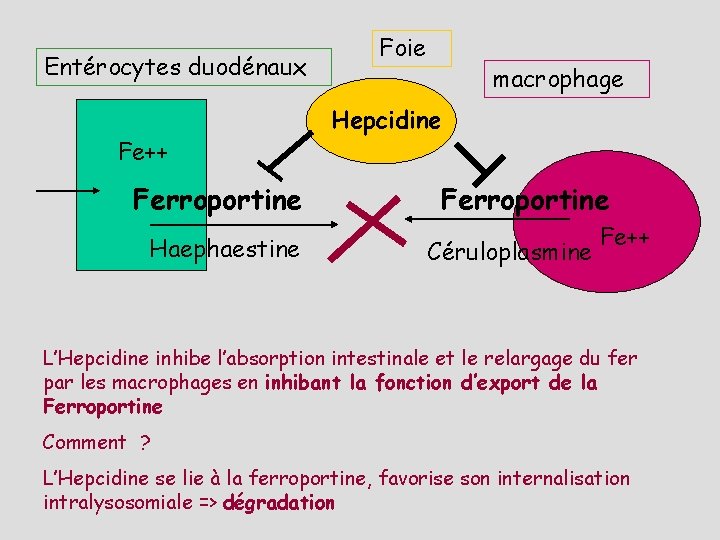
Entérocytes duodénaux Fe++ Ferroportine Haephaestine Foie macrophage Hepcidine Ferroportine Céruloplasmine Fe++ L’Hepcidine inhibe l’absorption intestinale et le relargage du fer par les macrophages en inhibant la fonction d’export de la Ferroportine Comment ? L’Hepcidine se lie à la ferroportine, favorise son internalisation intralysosomiale => dégradation
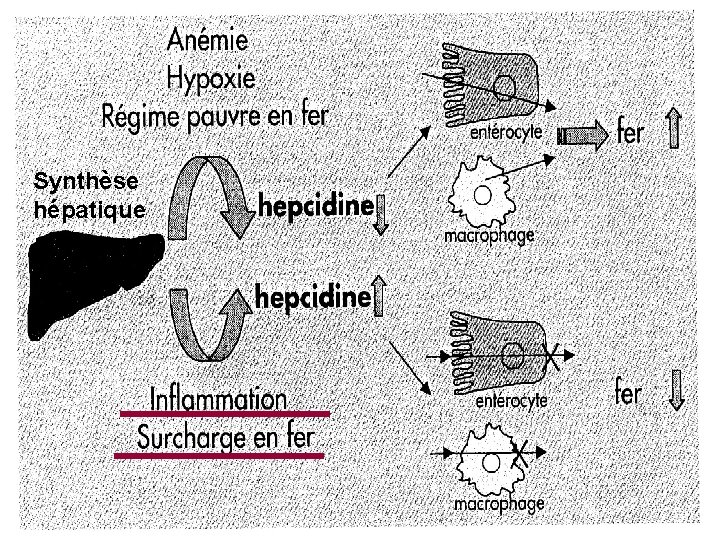
Synthèse hépatique
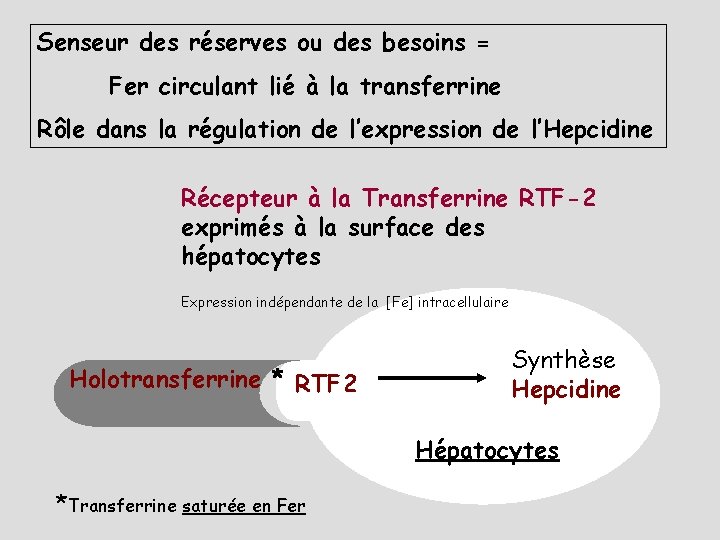
Senseur des réserves ou des besoins = Fer circulant lié à la transferrine Rôle dans la régulation de l’expression de l’Hepcidine Récepteur à la Transferrine RTF-2 exprimés à la surface des hépatocytes Expression indépendante de la [Fe] intracellulaire Holotransferrine * RTF 2 Synthèse Hepcidine Hépatocytes *Transferrine saturée en Fer

Régulation de l’homéostasie du Fer : HFE : Rôle majeur dans la régulation de l’absorption HFE est une molécule HLA de classe I. Elle capture le Fer au niveau de l’entérocyte de la crypte via un complexe (transferine/ RTf 1/b 2 m/HFE) la libération du Fer va agir sur l’expression des gènes sensibles au système IRP/IRE => modulation de l’expression de certains gènes et notamment de la ferroportine et de DMT 1 migration et différenciation des cellules de la crypte vers les villosités => diminution de l’absorption : plus la captation du Fer est grande dans la crypte, moins grande sera l’absorption du Fer dans les villosités. muté dans l’hémochromatose de type 1 (C 282 Y) => pas de liaison avec la B 2 m => pas de capture du Fer au niveau de la crypte => pas de régulation de l’absorption => surcharge en Fer
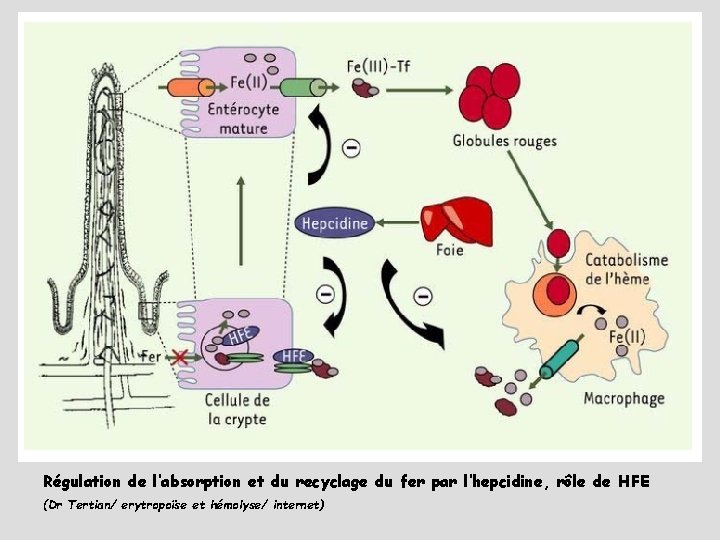
4 j Régulation de l’absorption et du recyclage du fer par l’hepcidine, rôle de HFE (Dr Tertian/ erytropoïse et hémolyse/ internet)

Mutation des transporteurs connus à l’origine d’ une hémochromatose : Mutation DMT 1 Mutation Hephaestine Mutation de la céruloplasmine Mutation HFE Mutation Ferroportine Mutation Récepteur de la Transferrine 2 Mutation Hepcidine etc…. Modèles animaux transgéniques Amélioration de la compréhension du métabolisme du Fer => Thérapeutiques ciblées
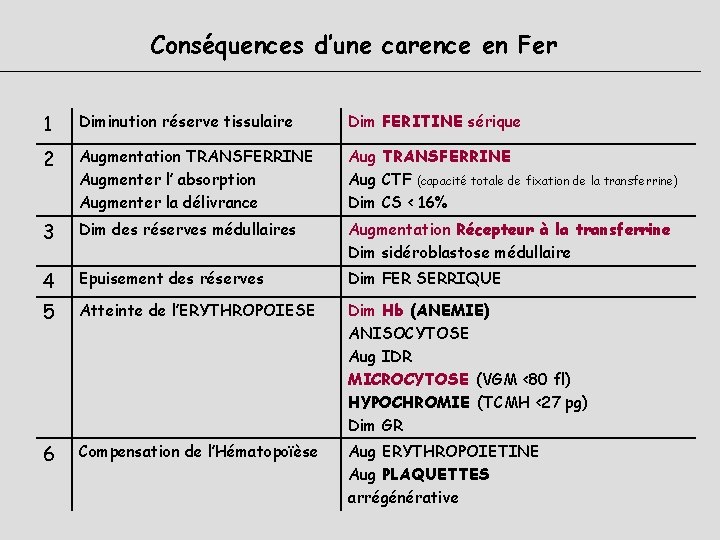
Conséquences d’une carence en Fer 1 Diminution réserve tissulaire Dim FERITINE sérique 2 Augmentation TRANSFERRINE Augmenter l’ absorption Augmenter la délivrance Aug TRANSFERRINE Aug CTF (capacité totale de fixation de la transferrine) Dim CS < 16% 3 Dim des réserves médullaires Augmentation Récepteur à la transferrine Dim sidéroblastose médullaire 4 Epuisement des réserves Dim FER SERRIQUE 5 Atteinte de l’ERYTHROPOIESE Dim Hb (ANEMIE) ANISOCYTOSE Aug IDR MICROCYTOSE (VGM <80 fl) HYPOCHROMIE (TCMH <27 pg) Dim GR 6 Compensation de l’Hématopoïèse Aug ERYTHROPOIETINE Aug PLAQUETTES arrégénérative

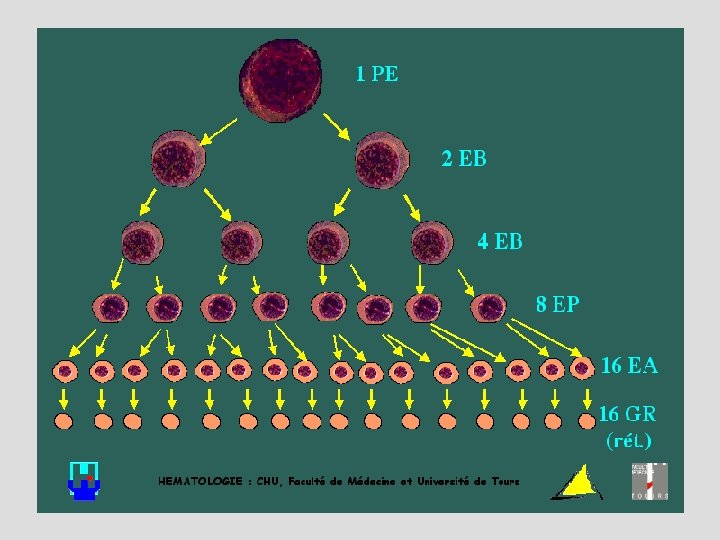
Erythropoïèse : Contrôle du nombre des divisions cellulaires • Entre le Proerythroblaste et l’erythroblaste acidophile > ou = 4 divisions (8 à 32 cellules) • À chaque division => diminution du volume globulaire (VGM) • Deux critères qui contrôlent la division cellulaire : – la maturité du noyau = densité de la chromatine • seuil d’ADN atteint => division cellulaire – la maturité du cytoplasme = CCMH (concentration en Hb) • seuil d’Hb atteint => arrêt des divisions • Anomalie Hémoglobine => • microcytose par augmentation des divisions cellulaires – Carence en Fer (Hb) (carence martiale) – Anomalie répartition du Fer (syndrome inflammatoire) – Anomalie Globine (thalassémie)

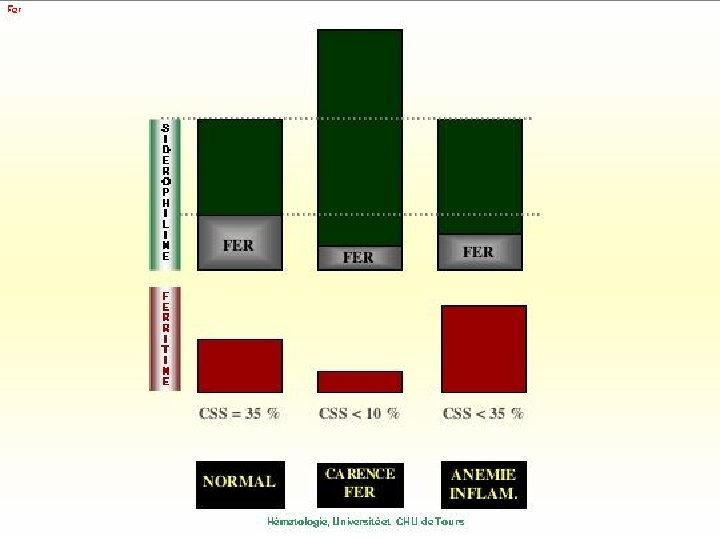
Quels tests prescrire pour déceler une carence martiale ? Tests actuellement utilisés en pratique médicale courante Dosage de la Ferritine sérique : reflet fidèle et précis des réserves (1 mg de Ferritine = à 10 mg de Fer de réserve) ou test le plus sensible et le plus spécifique peu de variabilité nycthémérale, inter-individuelle (par opposition au Fer) dosage CRP utile pour déceler l’existence d’un syndrome inflammatoire Détermination du Coefficient de Saturation de la Transferrine (dosage du Fer sérique et CTF de la transferrine) reflet d’une erythropoïèse sidéroprive CS = Fer sérique X 100/CTF = capacité totale de fixation (dosage indirect ou direct = transferrine)

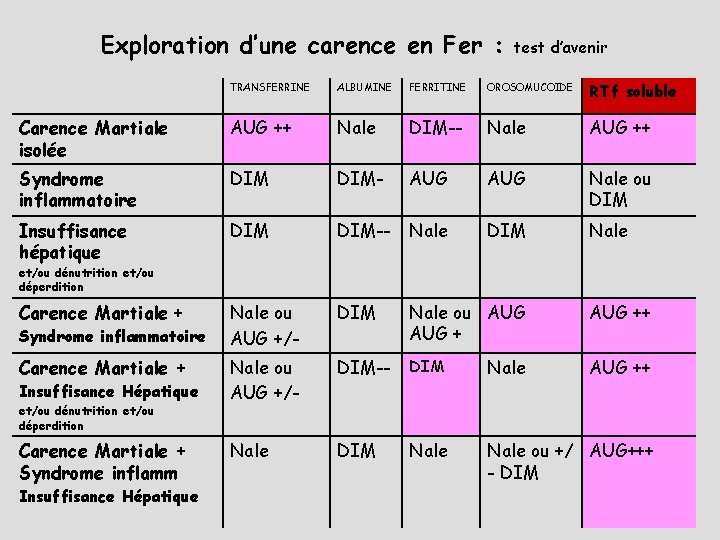
Exploration d’une carence en Fer : test d’avenir TRANSFERRINE ALBUMINE FERRITINE OROSOMUCOIDE RTf soluble Carence Martiale isolée AUG ++ Nale DIM-- Nale AUG ++ Syndrome inflammatoire DIM- AUG Nale ou DIM Insuffisance hépatique DIM-- Nale DIM Nale ou AUG +/- DIM Nale ou AUG ++ Nale ou AUG +/- DIM-- DIM Nale AUG ++ Nale DIM Nale ou +/ AUG+++ - DIM et/ou dénutrition et/ou déperdition Carence Martiale + Syndrome inflammatoire Carence Martiale + Insuffisance Hépatique et/ou dénutrition et/ou déperdition Carence Martiale + Syndrome inflamm Insuffisance Hépatique

Diagnostic étiologique d’une carence martiale 1 - Insuffisance ou défaut d’apport nourisson (allaitement maternel, prématuré, gémellité) anorexie 2 - Augmentation des pertes : saignements génitaux (règles normales = 12 à 15 mg de Fer/mois) saignements digestifs autres saignements (rares) dons de sang chez la femme (400 ml = 200 mg de Fer) hémolyses intravasculaires prolongées 3 - Augmentation des besoins grossesse (700 mg) / lactation (1 mg)/ adolescence 4 - Malabsorption gastrectomie/ antiulcéruex/lait+++/reflux biliaires/thé+++ anomalie du grêle proximal (atrophie villositaire, maladie coeliaque)

Fin
- Slides: 50