Praktikum 1 Cara Pembuatan Media dan Sterilisasi OLEH

Praktikum 1 Cara Pembuatan Media dan Sterilisasi OLEH : DANANG RYAN I (115100307111003) KELOMPOK: 17 ASISTEN HANA AFIFAH

Alat dan Bahan A. Sterilisasi alat dan bahan : -Autoclave -Alkohol 70% -Karet -Kertas payung -Plastik -Kapas -Tabung Reaksi -Cawan Petri

B. Pembuatan Media Agar alat dan bahan : -Agar Bacteriological -Hot Plate -Gelas Baker -Timbangan Digital -Kapas -Aquades -Rak Tabung Reaksi -Cawan Petri -Tabung Reaksi -Kertas Payung -Karet
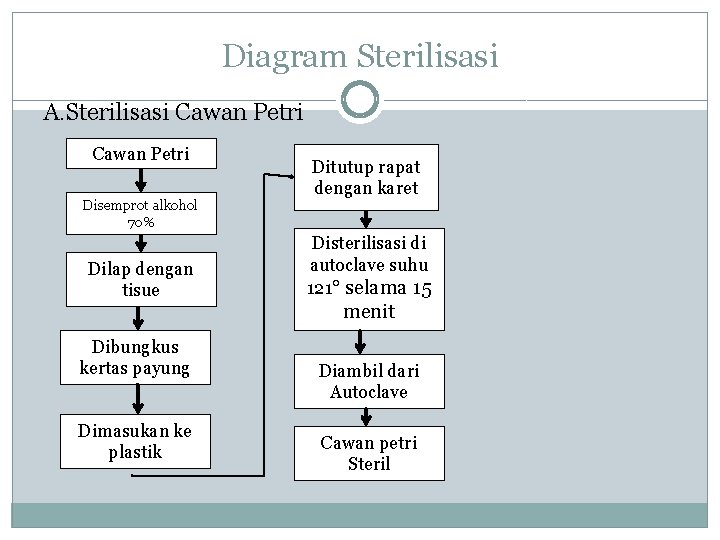
Diagram Sterilisasi A. Sterilisasi Cawan Petri Disemprot alkohol 70% Dilap dengan tisue Dibungkus kertas payung Dimasukan ke plastik Ditutup rapat dengan karet Disterilisasi di autoclave suhu 121° selama 15 menit Diambil dari Autoclave Cawan petri Steril
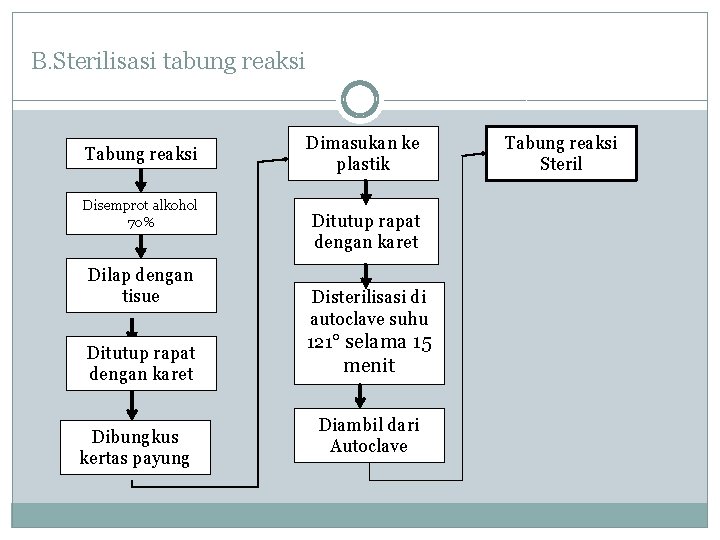
B. Sterilisasi tabung reaksi Tabung reaksi Disemprot alkohol 70% Dilap dengan tisue Ditutup rapat dengan karet Dibungkus kertas payung Dimasukan ke plastik Ditutup rapat dengan karet Disterilisasi di autoclave suhu 121° selama 15 menit Diambil dari Autoclave Tabung reaksi Steril

Keterangan Sterilisasi � Langkah pertama yang dilakukan adalah menyiapkan alat yang akan disterilisasi yaitu erlenmeyer dan cawan petri. Masing-masing dibersihkan dahulu dengan alkohol 70% kemudian ditiriskan, lalu dibungkus dengan kertas payung yang bertujuan supaya air dari autoklaf saat proses sterilisasi tidak masuk pada alat. Pada erlenmeyer perlakuannya sedikit berbeda, yakni sebelum dibungkus dengan kertas payung erlenmeyer terlebih dahulu disumbat dengan kapas, dan harus dipastikan kerapatannya dengan cara memasang penyumbat lalu dilepas sampai berbunyi. Jika sudah dipastikan ukuran penyumbat bisa menutup dengan rapat maka penyumbat tersebut dipasang kembali. Langkah selanjutnya adalah memasukkan peralatan pada plastik bening kemudian ditali dengan karet gelang, langkah ini sebagai upaya pertama pencegahan supaya air dalam autoklaf saat sterilisasi tidak masuk ke dalam alat yang disterilisasi. Langkah berikutnya, bungkusan dimasukkan dalam autoklaf dan diset suhunya 121°C, lalu autoklaf ditutup dan dirapatkan penguncinya secara bersamaan pada kunci yang sejajar untuk memastikan tidak ada kebocoran. Kemudian, kabel autoklaf dicolokkan dinyalakan, periksa kenaikkan suhu pada autoklaf hingga suhu menunjukkan angka 121°C lalu tunggu selama 15 menit pada suhu tersebut. Kemudian, matikan autoklaf, tetapi jangan langsung dibuka penutupnya selama suhu belum kembali seperti awal, hal ini bisa menyebabkan alat pecah karena perubahan suhu yang drastis karena perbedaan suhu di dalam dan di luar autoklaf. Tunggu sampai suhu menunjukkan pada kondisi awal kemudian alat bisa diambil dan sudah dalam keadaan steril.
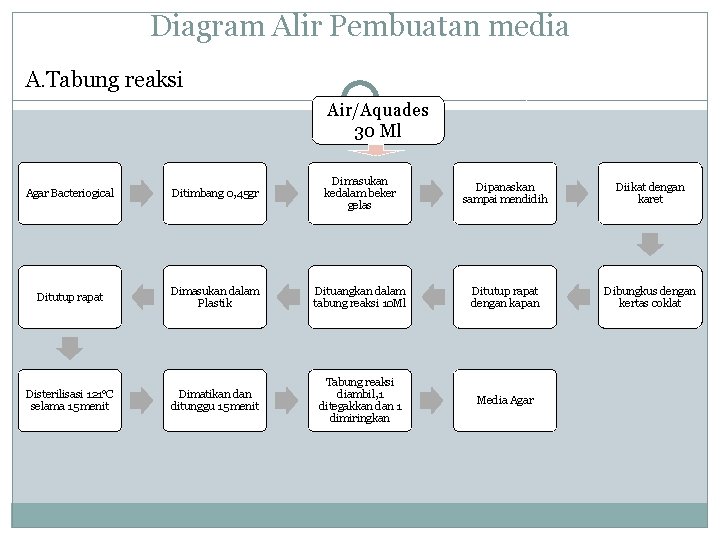
Diagram Alir Pembuatan media A. Tabung reaksi Air/Aquades 30 Ml Agar Bacteriogical Ditimbang 0, 45 gr Dimasukan kedalam beker gelas Dipanaskan sampai mendidih Diikat dengan karet Ditutup rapat Dimasukan dalam Plastik Dituangkan dalam tabung reaksi 10 Ml Ditutup rapat dengan kapan Dibungkus dengan kertas coklat Disterilisasi 121°C selama 15 menit Dimatikan ditunggu 15 menit Tabung reaksi diambil, 1 ditegakkan dan 1 dimiringkan Media Agar
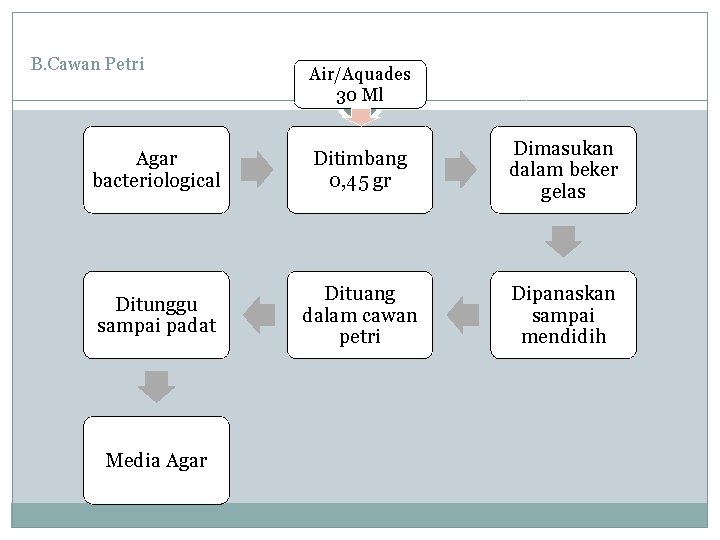
B. Cawan Petri Air/Aquades 30 Ml Agar bacteriological Ditimbang 0, 45 gr Dimasukan dalam beker gelas Ditunggu sampai padat Dituang dalam cawan petri Dipanaskan sampai mendidih Media Agar

Keterangan Diagram Pembuatan media Pertama yang dilakukan adalah persiapan alat dan bahan yang akan digunakan yaitu aquades dan serbuk agar bakteorogical. Aquades diukur sebanyak 30 ml dan serbuk agar sebanyak 0, 45 gram. Aquades 30 ml dimasukkan dalam gelas beker kemudian dipanaskan di hot plate sampai mendidih (menghasilkan gelembung-gelembung) lalu dimasukkan serbuk agar dan dihomogenkan dengan cara diaduk, ditunggu sampai campuran mendidih kembali sembari tetap diaduk supaya homogen sempurna. Setelah larutan agar mendidih matikan hot plate kemudian agar panas dimasukkan dalam 2 tabung reaksi dan 1 cawan petri dibagi secara rata pada ketiga wadah tersebut, pada tabung reaksi satu untuk media agar miring dan lainnya untuk media agar tegak. Pada cawan petri untuk pembuatan media lempengan. Setelah semua perlakuan selesai, alat yang telah dituangi agar (media) kemudian disterilisasi dengan langkah yang sama seperti pada ulasan prosedur kerja “Sterilisasi”.

Praktikum 2 PENGAMATAN DAN PERHITUNGAN MIKROORGANISME �Alat dan Bahan : Alat : -Khamir biakan 24 jam -Mikroskop -Khamir biakan 48 jam -Hemacytometer -Aquades -Pipet tetes -Alkohol -Jarum ose -Cover glass -Bunsen
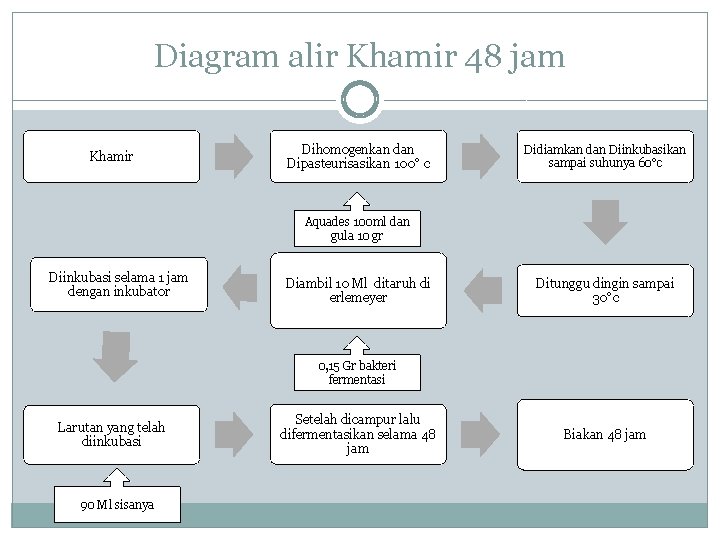
Diagram alir Khamir 48 jam Khamir Dihomogenkan dan Dipasteurisasikan 100° c Didiamkan dan Diinkubasikan sampai suhunya 60°c Aquades 100 ml dan gula 10 gr Diinkubasi selama 1 jam dengan inkubator Diambil 10 Ml ditaruh di erlemeyer Ditunggu dingin sampai 30°c 0, 15 Gr bakteri fermentasi Larutan yang telah diinkubasi 90 Ml sisanya Setelah dicampur lalu difermentasikan selama 48 jam Biakan 48 jam
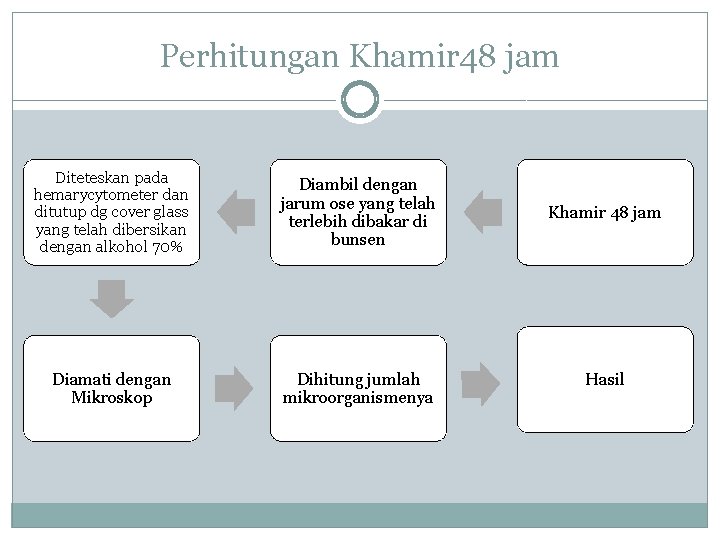
Perhitungan Khamir 48 jam Diteteskan pada hemarycytometer dan ditutup dg cover glass yang telah dibersikan dengan alkohol 70% Diambil dengan jarum ose yang telah terlebih dibakar di bunsen Diamati dengan Mikroskop Dihitung jumlah mikroorganismenya Khamir 48 jam Hasil

Keterangan Diagram Alir � Pertama disiapkan khamir sebanyak 1 ml yang diambil dari gelas Erlenmeyer menggunakan bola hisap. kemudian diletakkan di tabung reaksi. Kemudian, diambil aquades sebanyak 9 ml dan dimasukkan kedalam tabung reaksi untuk proses pengenceran biakan 48 jam. Setelah itu, hemacytometer disterilkan dengan menggunakan alkohol. Alkohol disemprotkan pada hemacytometer kemudian dikeringkan dengan tisu. Begitu pun dengan cover glass terlebih dahulu disterilisasi. Setelah disterilisasi, kedua alat tersebut difiksasi. Disini pengenceran berfungsi mengurai koloni yang menumpuk pada biakan sehingga memudahkan pada saat mengamati dan menghitung jumlah mikroorganismenya. Hasil dari pengenceran kemudian diambil dengan jarum oose dan diletakkan di hemacytometer dan ditutup cover glass. Lalu diamati dengan mikroskop. Setelah diamati, kemudian hasil penghitungan dimasukkan dalam persegi 4× 4, dan dihitung jumlah khamir petak, serta dihitung khamir total.

Praktikum 3 Pembuatan Produk Hasil Fermentasi �Alat Dan Bahan : -Pengukus Nasi -Pengaduk -Panci atau Baskom Tampah -kipas -Beras ketan Putih -Ragi Tape -Pembungkus/ Daun pisang
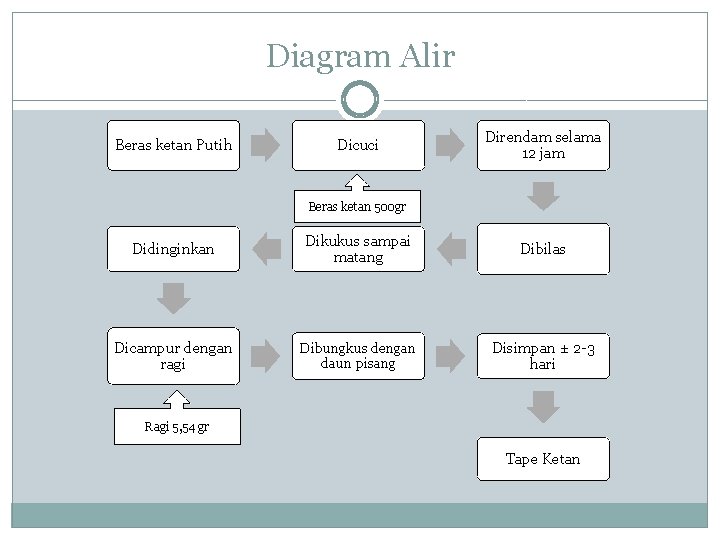
Diagram Alir Beras ketan Putih Dicuci Direndam selama 12 jam Beras ketan 500 gr Didinginkan Dikukus sampai matang Dibilas Dicampur dengan ragi Dibungkus dengan daun pisang Disimpan ± 2 -3 hari Ragi 5, 54 gr Tape Ketan

Keterangan Diagram Alir Cuci beras ketan sampai bersih, lalu rendam dalam 1 liter air selama satu malam agar beras ketan menjadi lembek. Setelah direndam, kukus beras ketan sampai menguap, dan siram dengan menggunakan air panas, lalu kukus kembali sekitar 15 menit. Setelah itu, angkat dan tiriskan. Ambil setengah bagian beras ketan dan letakan dalam wadah lalu ratakan. Taburkan ragi setengahnya, dan jika perlu bisa dimasukan gula. Tutupi ketan yang telah ditaburi ragi dengan ketan yang tersisa tadi, kemudian taburkan ragi kembali sampai habis. Tutup pembungkus/daun pisang yang telah diisi oleh ketan tersebut dengan rapat, dan letakan di tempat yang kering dan hangat. Diamkan selama 2 - 3 hari untuk proses fermentasi, setelah itu tape ketan siap dimakan.
- Slides: 16