PPTCANCBBLA 04004 V 4 Clase Biomolculas orgnicas protenas

PPTCANCBBLA 04004 V 4 Clase Biomoléculas orgánicas: proteínas y ácidos nucleicos
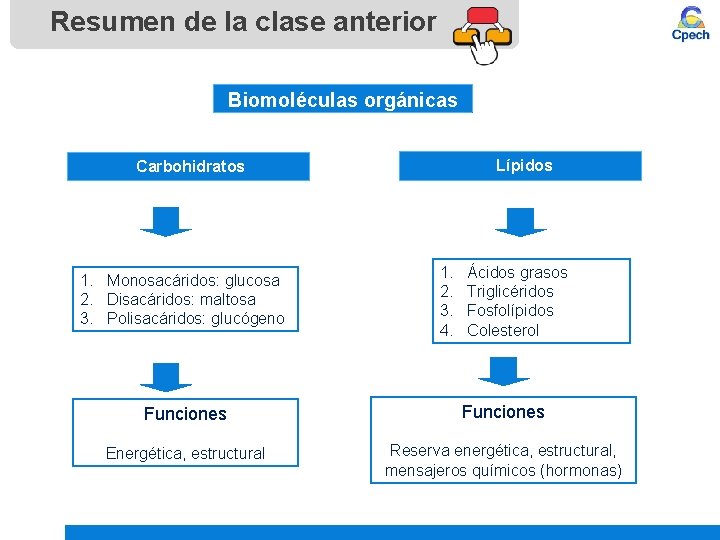
Resumen de la clase anterior Biomoléculas orgánicas Lípidos Carbohidratos 1. Monosacáridos: glucosa 2. Disacáridos: maltosa 3. Polisacáridos: glucógeno 1. 2. 3. 4. Ácidos grasos Triglicéridos Fosfolípidos Colesterol Funciones Energética, estructural Reserva energética, estructural, mensajeros químicos (hormonas)

Aprendizajes esperados • Comprender las formas de clasificación de proteínas y ácidos nucleicos. • Identificar y comprender los niveles de organización y funciones de las proteínas. • Identificar los tipos de ácidos nucleicos y sus características.
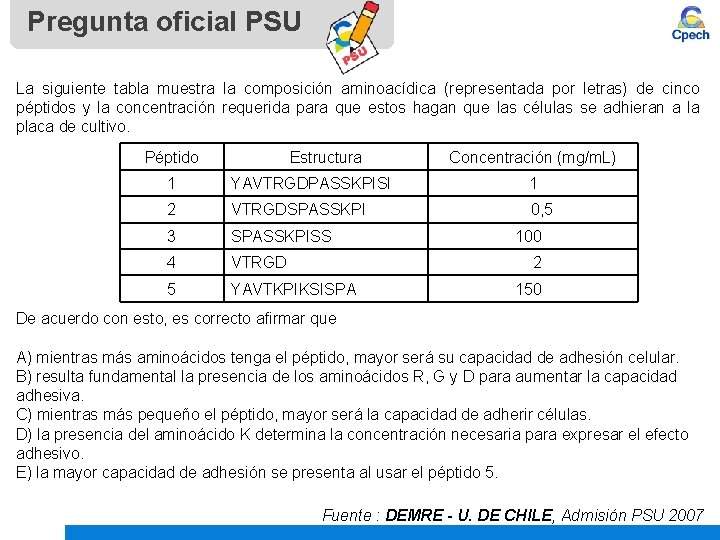
Pregunta oficial PSU La siguiente tabla muestra la composición aminoacídica (representada por letras) de cinco péptidos y la concentración requerida para que estos hagan que las células se adhieran a la placa de cultivo. Péptido Estructura Concentración (mg/m. L) 1 YAVTRGDPASSKPISI 1 2 VTRGDSPASSKPI 0, 5 3 SPASSKPISS 4 VTRGD 5 YAVTKPIKSISPA 100 2 150 De acuerdo con esto, es correcto afirmar que A) mientras más aminoácidos tenga el péptido, mayor será su capacidad de adhesión celular. B) resulta fundamental la presencia de los aminoácidos R, G y D para aumentar la capacidad adhesiva. C) mientras más pequeño el péptido, mayor será la capacidad de adherir células. D) la presencia del aminoácido K determina la concentración necesaria para expresar el efecto adhesivo. E) la mayor capacidad de adhesión se presenta al usar el péptido 5. Fuente : DEMRE - U. DE CHILE, Admisión PSU 2007

1. Proteínas 2. Ácidos nucleicos

Introducción Tal como se vio en la clase anterior, los elementos químicos se organizan de tal forma que aumentan su complejidad y desarrollan funciones que son específicas. En esta sesión revisaremos dos compuestos más, que son las proteínas y los ácidos nucleicos, los cuales permitirán comprender otras funciones que se producen en los seres vivos relacionadas con el material genético y su expresión.
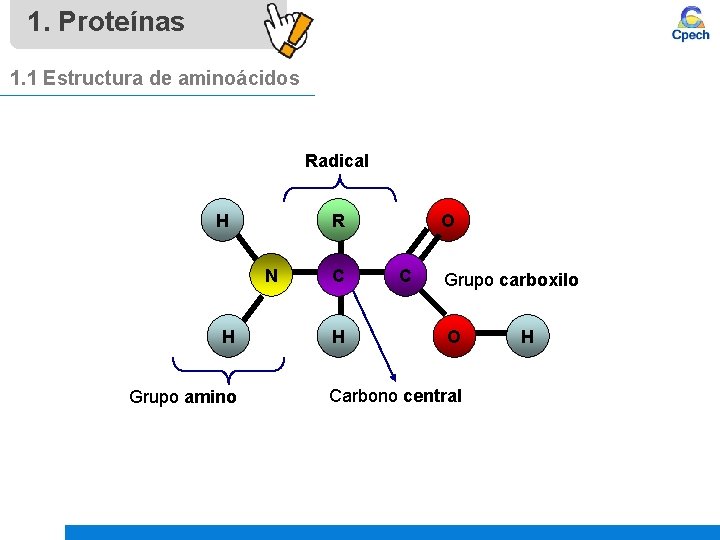
1. Proteínas 1. 1 Estructura de aminoácidos Radical H R N H Grupo amino C H O C Grupo carboxilo O Carbono central H
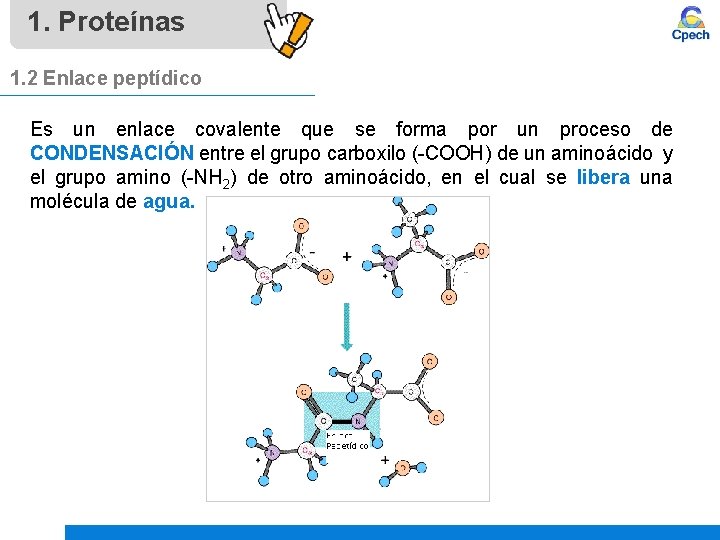
1. Proteínas 1. 2 Enlace peptídico Es un enlace covalente que se forma por un proceso de CONDENSACIÓN entre el grupo carboxilo (-COOH) de un aminoácido y el grupo amino (-NH 2) de otro aminoácido, en el cual se libera una molécula de agua.
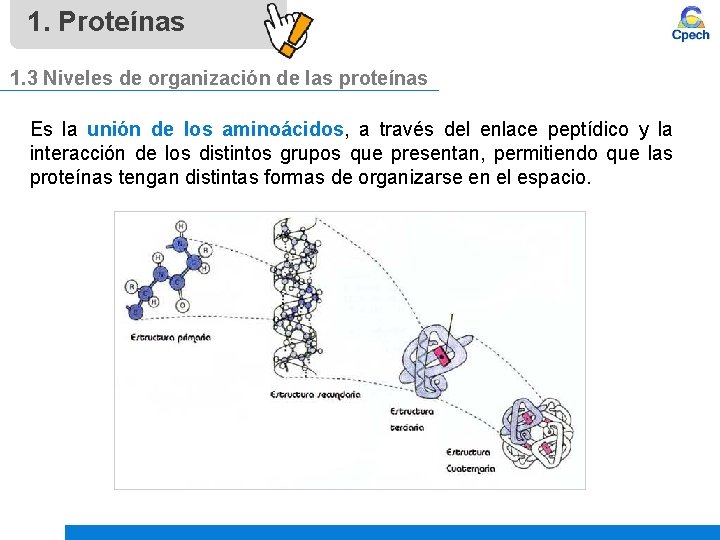
1. Proteínas 1. 3 Niveles de organización de las proteínas Es la unión de los aminoácidos, a través del enlace peptídico y la interacción de los distintos grupos que presentan, permitiendo que las proteínas tengan distintas formas de organizarse en el espacio.
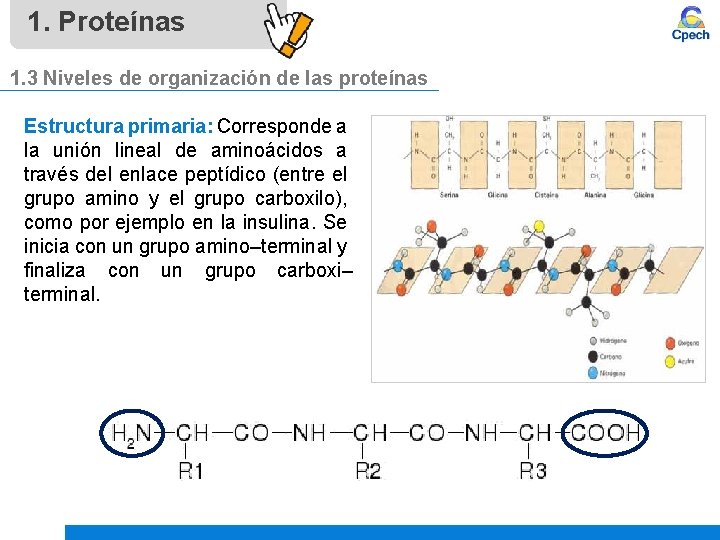
1. Proteínas 1. 3 Niveles de organización de las proteínas Estructura primaria: Corresponde a la unión lineal de aminoácidos a través del enlace peptídico (entre el grupo amino y el grupo carboxilo), como por ejemplo en la insulina. Se inicia con un grupo amino–terminal y finaliza con un grupo carboxi– terminal.
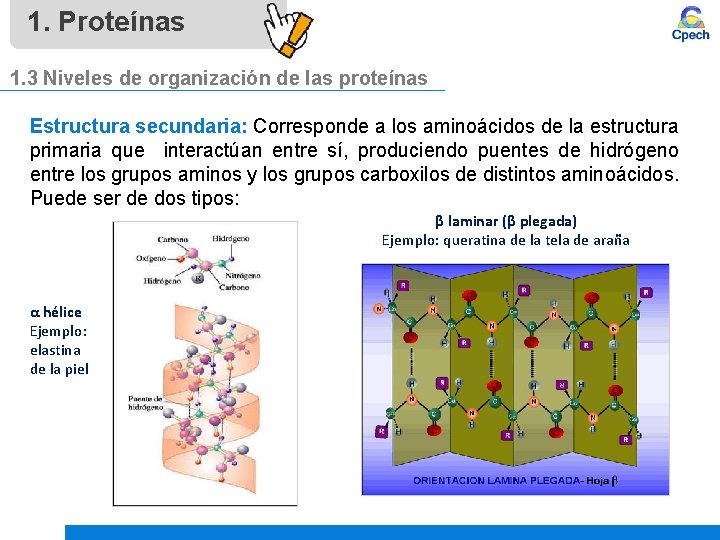
1. Proteínas 1. 3 Niveles de organización de las proteínas Estructura secundaria: Corresponde a los aminoácidos de la estructura primaria que interactúan entre sí, produciendo puentes de hidrógeno entre los grupos aminos y los grupos carboxilos de distintos aminoácidos. Puede ser de dos tipos: β laminar (β plegada) Ejemplo: queratina de la tela de araña α hélice Ejemplo: elastina de la piel
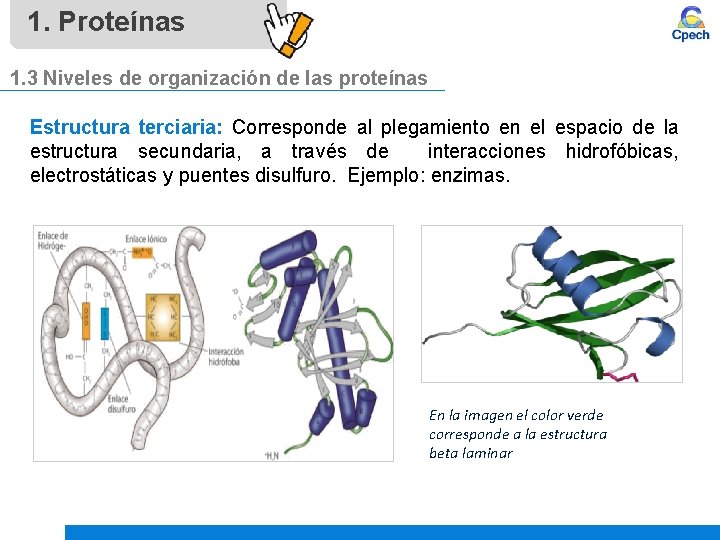
1. Proteínas 1. 3 Niveles de organización de las proteínas Estructura terciaria: Corresponde al plegamiento en el espacio de la estructura secundaria, a través de interacciones hidrofóbicas, electrostáticas y puentes disulfuro. Ejemplo: enzimas. En la imagen el color verde corresponde a la estructura beta laminar
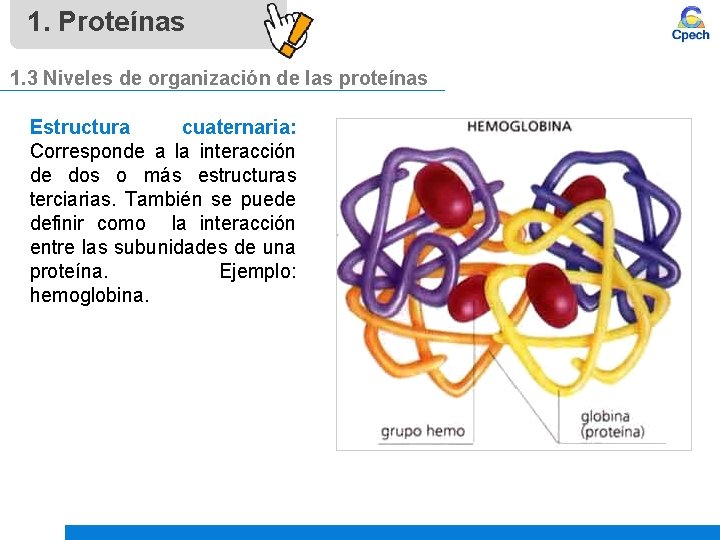
1. Proteínas 1. 3 Niveles de organización de las proteínas Estructura cuaternaria: Corresponde a la interacción de dos o más estructuras terciarias. También se puede definir como la interacción entre las subunidades de una proteína. Ejemplo: hemoglobina.
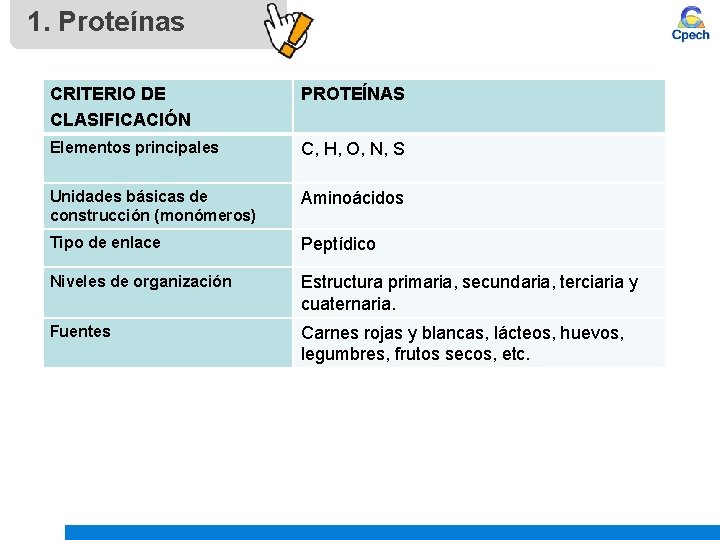
1. Proteínas CRITERIO DE CLASIFICACIÓN PROTEÍNAS Elementos principales C, H, O, N, S Unidades básicas de construcción (monómeros) Aminoácidos Tipo de enlace Peptídico Niveles de organización Estructura primaria, secundaria, terciaria y cuaternaria. Fuentes Carnes rojas y blancas, lácteos, huevos, legumbres, frutos secos, etc.
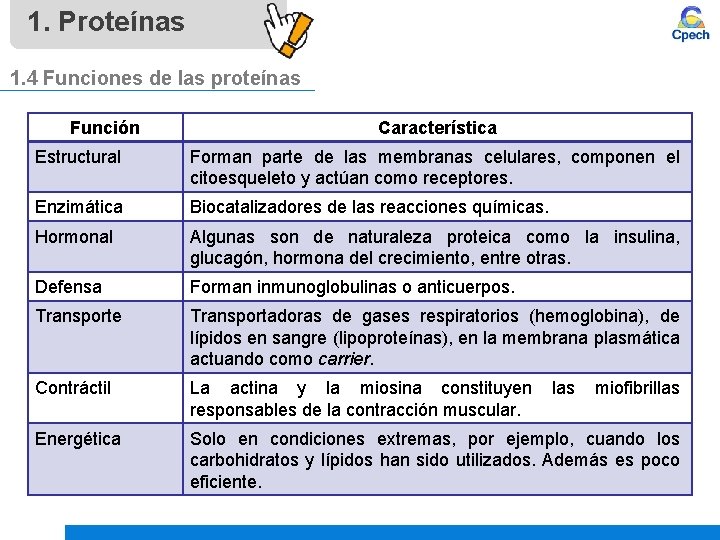
1. Proteínas 1. 4 Funciones de las proteínas Función Característica Estructural Forman parte de las membranas celulares, componen el citoesqueleto y actúan como receptores. Enzimática Biocatalizadores de las reacciones químicas. Hormonal Algunas son de naturaleza proteica como la insulina, glucagón, hormona del crecimiento, entre otras. Defensa Forman inmunoglobulinas o anticuerpos. Transporte Transportadoras de gases respiratorios (hemoglobina), de lípidos en sangre (lipoproteínas), en la membrana plasmática actuando como carrier. Contráctil La actina y la miosina constituyen responsables de la contracción muscular. Energética Solo en condiciones extremas, por ejemplo, cuando los carbohidratos y lípidos han sido utilizados. Además es poco eficiente. las miofibrillas
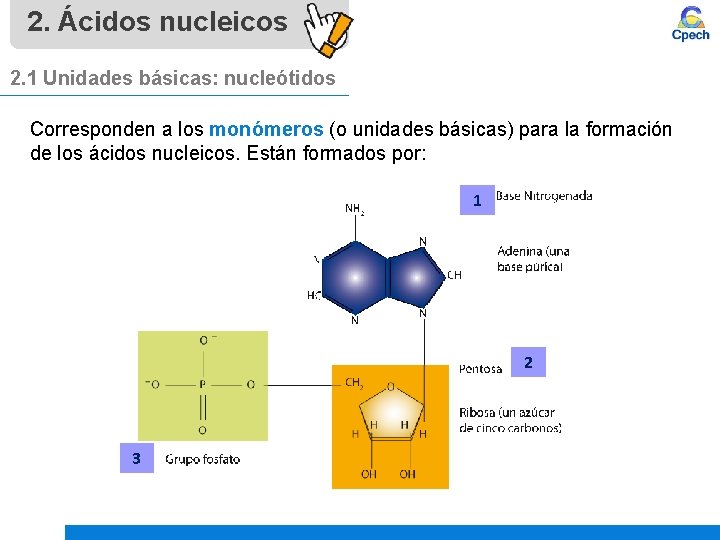
2. Ácidos nucleicos 2. 1 Unidades básicas: nucleótidos Corresponden a los monómeros (o unidades básicas) para la formación de los ácidos nucleicos. Están formados por: 1 2 3
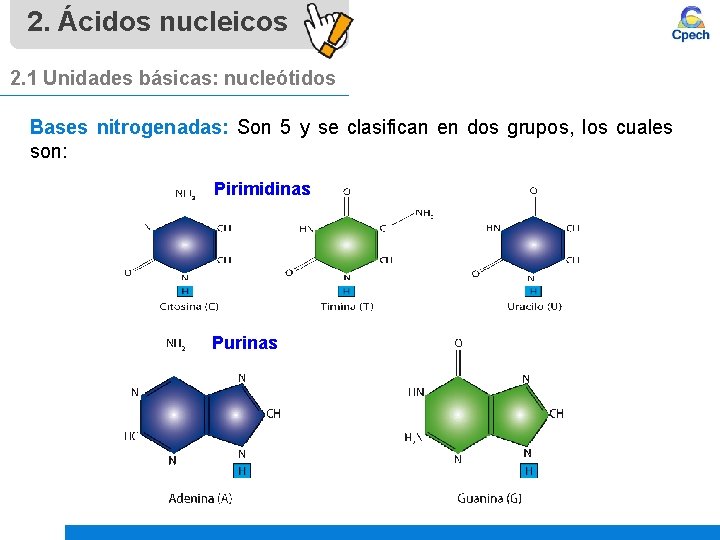
2. Ácidos nucleicos 2. 1 Unidades básicas: nucleótidos Bases nitrogenadas: Son 5 y se clasifican en dos grupos, los cuales son: Pirimidinas Purinas
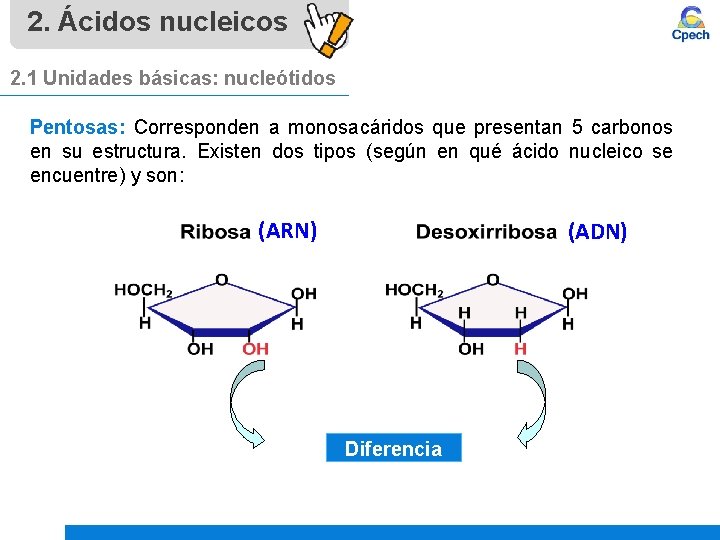
2. Ácidos nucleicos 2. 1 Unidades básicas: nucleótidos Pentosas: Corresponden a monosacáridos que presentan 5 carbonos en su estructura. Existen dos tipos (según en qué ácido nucleico se encuentre) y son: (ARN) (ADN) Diferencia
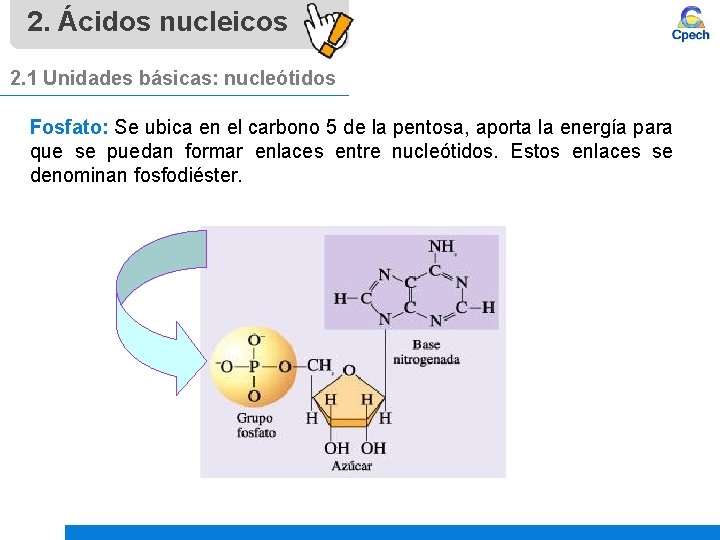
2. Ácidos nucleicos 2. 1 Unidades básicas: nucleótidos Fosfato: Se ubica en el carbono 5 de la pentosa, aporta la energía para que se puedan formar enlaces entre nucleótidos. Estos enlaces se denominan fosfodiéster.
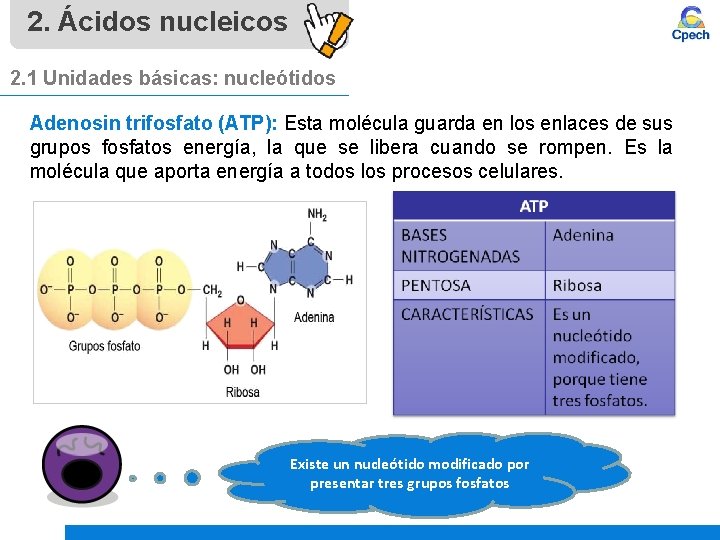
2. Ácidos nucleicos 2. 1 Unidades básicas: nucleótidos Adenosin trifosfato (ATP): Esta molécula guarda en los enlaces de sus grupos fosfatos energía, la que se libera cuando se rompen. Es la molécula que aporta energía a todos los procesos celulares. Existe un nucleótido modificado por presentar tres grupos fosfatos
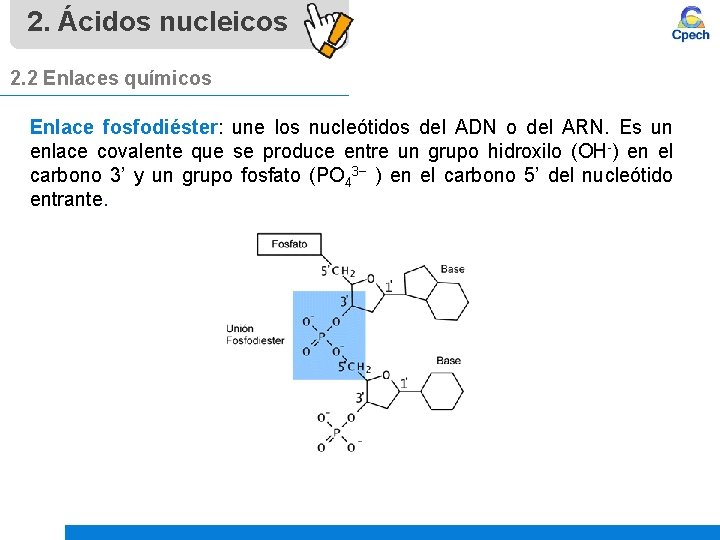
2. Ácidos nucleicos 2. 2 Enlaces químicos Enlace fosfodiéster: une los nucleótidos del ADN o del ARN. Es un enlace covalente que se produce entre un grupo hidroxilo (OH-) en el carbono 3’ y un grupo fosfato (PO 43− ) en el carbono 5’ del nucleótido entrante.
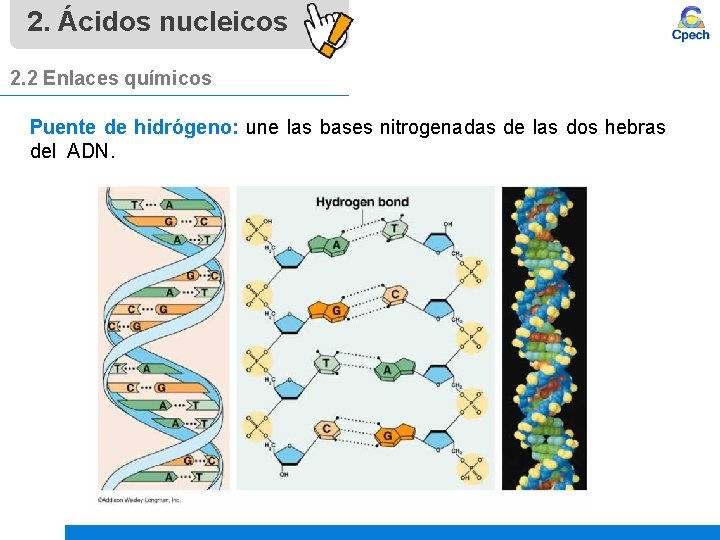
2. Ácidos nucleicos 2. 2 Enlaces químicos Puente de hidrógeno: une las bases nitrogenadas de las dos hebras del ADN.
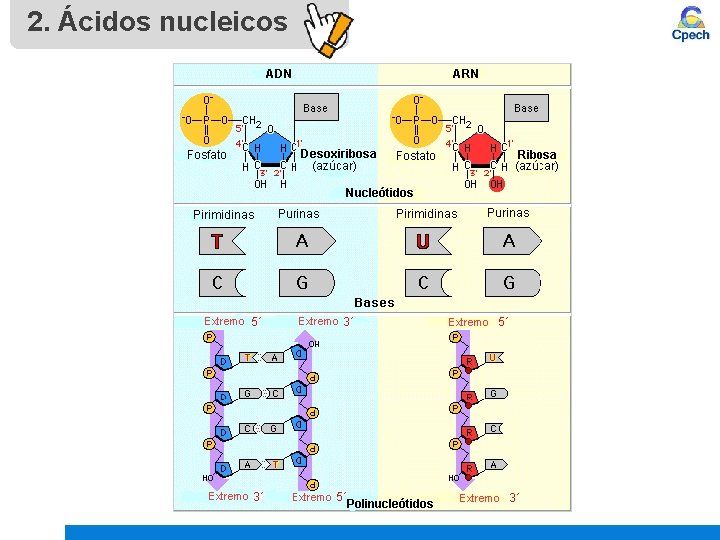
2. Ácidos nucleicos 2. 3 ADN Ácido desoxirribonucleico Bases nitrogenadas Adenina Guanina Timina Citosina Pentosa Desoxirribosa Características • Corresponde a la unión de muchos nucleótidos. • Está formado por dos cadenas conformando una doble hélice. Funciones Codifica la información genética, guardando en forma segura y fiel las características de los organismos.
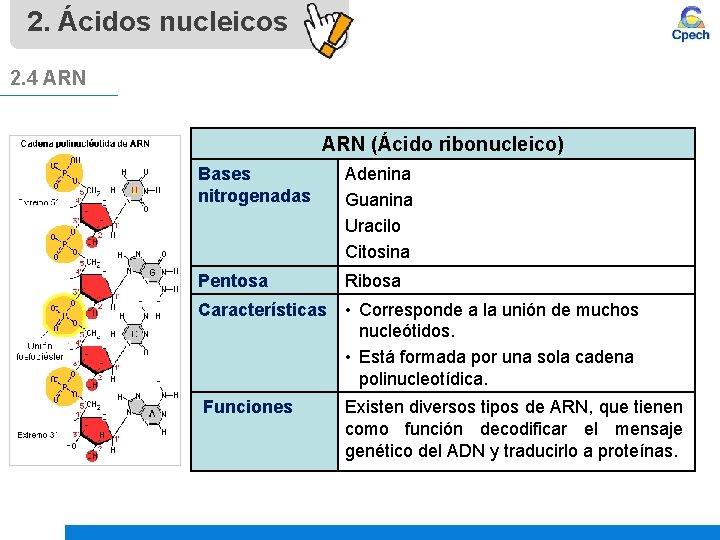
2. Ácidos nucleicos 2. 4 ARN (Ácido ribonucleico) Bases nitrogenadas Adenina Guanina Uracilo Citosina Pentosa Ribosa Características • Corresponde a la unión de muchos nucleótidos. • Está formada por una sola cadena polinucleotídica. Funciones Existen diversos tipos de ARN, que tienen como función decodificar el mensaje genético del ADN y traducirlo a proteínas.
2. Ácidos nucleicos
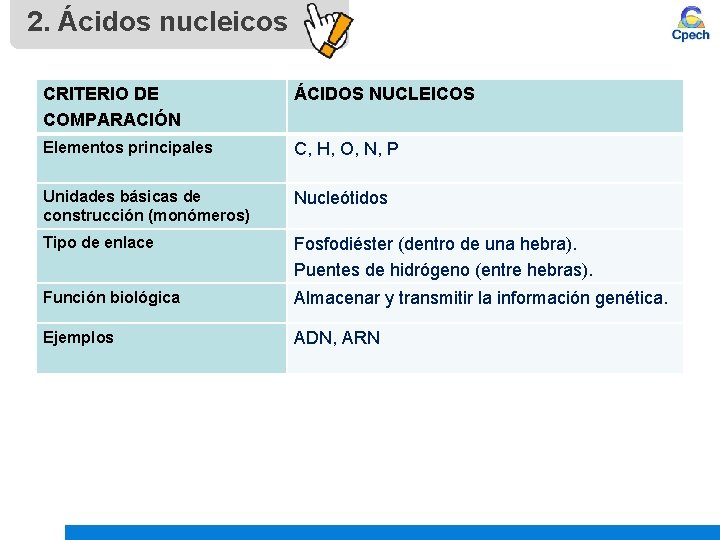
2. Ácidos nucleicos CRITERIO DE COMPARACIÓN ÁCIDOS NUCLEICOS Elementos principales C, H, O, N, P Unidades básicas de construcción (monómeros) Nucleótidos Tipo de enlace Fosfodiéster (dentro de una hebra). Puentes de hidrógeno (entre hebras). Función biológica Almacenar y transmitir la información genética. Ejemplos ADN, ARN
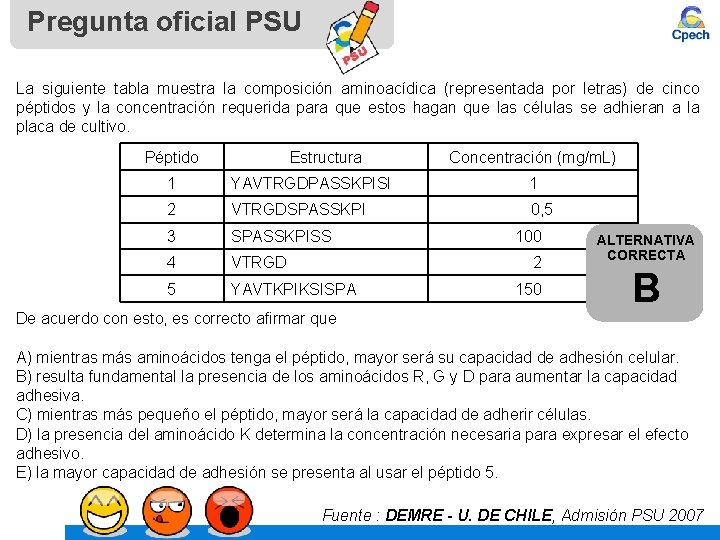
Pregunta oficial PSU La siguiente tabla muestra la composición aminoacídica (representada por letras) de cinco péptidos y la concentración requerida para que estos hagan que las células se adhieran a la placa de cultivo. Péptido Estructura Concentración (mg/m. L) 1 YAVTRGDPASSKPISI 1 2 VTRGDSPASSKPI 0, 5 3 SPASSKPISS 4 VTRGD 5 YAVTKPIKSISPA 100 2 De acuerdo con esto, es correcto afirmar que 150 ALTERNATIVA CORRECTA B A) mientras más aminoácidos tenga el péptido, mayor será su capacidad de adhesión celular. B) resulta fundamental la presencia de los aminoácidos R, G y D para aumentar la capacidad adhesiva. C) mientras más pequeño el péptido, mayor será la capacidad de adherir células. D) la presencia del aminoácido K determina la concentración necesaria para expresar el efecto adhesivo. E) la mayor capacidad de adhesión se presenta al usar el péptido 5. Fuente : DEMRE - U. DE CHILE, Admisión PSU 2007
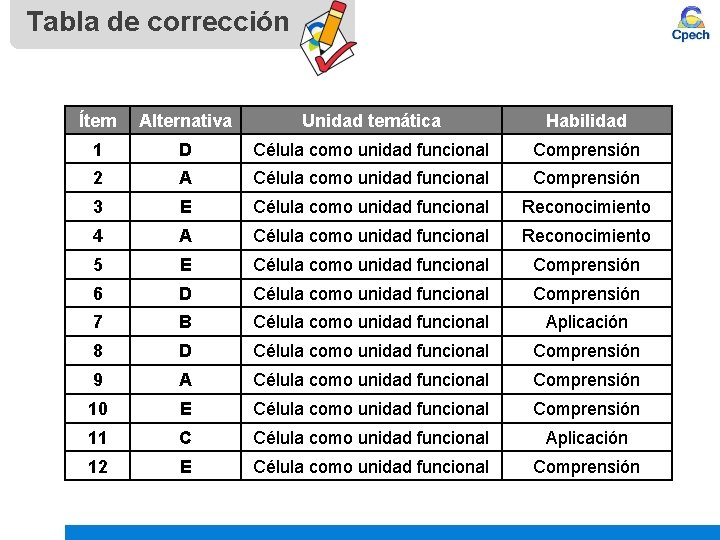
Tabla de corrección Ítem Alternativa Unidad temática Habilidad 1 D Célula como unidad funcional Comprensión 2 A Célula como unidad funcional Comprensión 3 E Célula como unidad funcional Reconocimiento 4 A Célula como unidad funcional Reconocimiento 5 E Célula como unidad funcional Comprensión 6 D Célula como unidad funcional Comprensión 7 B Célula como unidad funcional Aplicación 8 D Célula como unidad funcional Comprensión 9 A Célula como unidad funcional Comprensión 10 E Célula como unidad funcional Comprensión 11 C Célula como unidad funcional Aplicación 12 E Célula como unidad funcional Comprensión
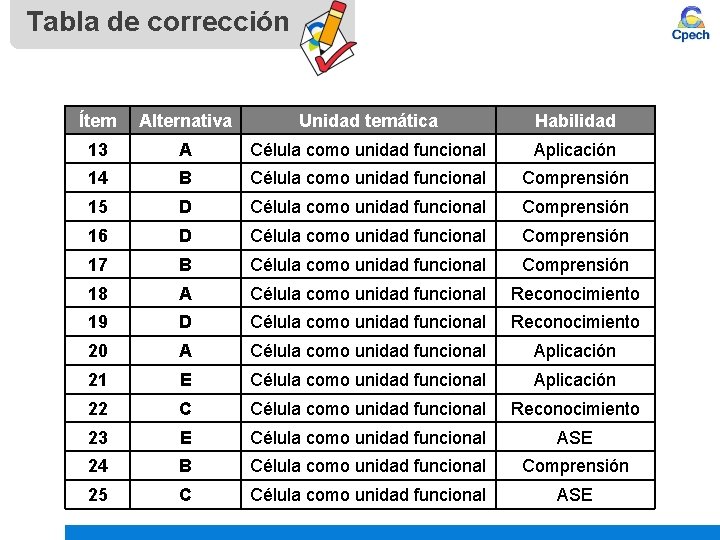
Tabla de corrección Ítem Alternativa Unidad temática Habilidad 13 A Célula como unidad funcional Aplicación 14 B Célula como unidad funcional Comprensión 15 D Célula como unidad funcional Comprensión 16 D Célula como unidad funcional Comprensión 17 B Célula como unidad funcional Comprensión 18 A Célula como unidad funcional Reconocimiento 19 D Célula como unidad funcional Reconocimiento 20 A Célula como unidad funcional Aplicación 21 E Célula como unidad funcional Aplicación 22 C Célula como unidad funcional Reconocimiento 23 E Célula como unidad funcional ASE 24 B Célula como unidad funcional Comprensión 25 C Célula como unidad funcional ASE
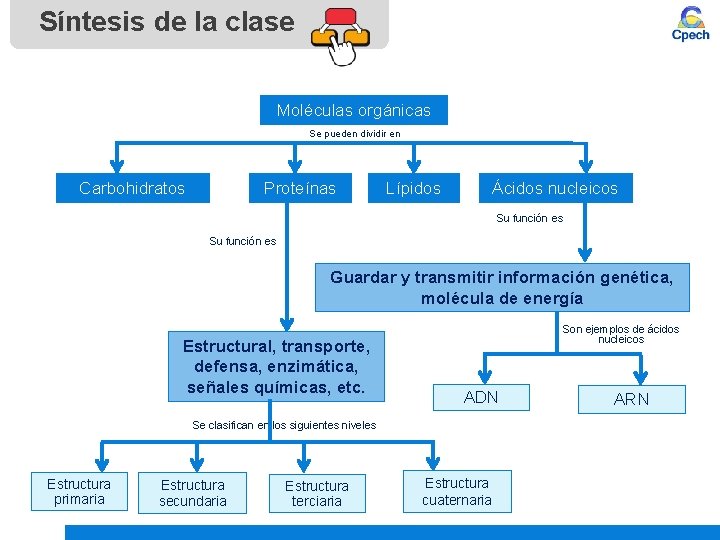
Síntesis de la clase Moléculas orgánicas Se pueden dividir en Carbohidratos Proteínas Lípidos Ácidos nucleicos Su función es Guardar y transmitir información genética, molécula de energía Estructural, transporte, defensa, enzimática, señales químicas, etc. Son ejemplos de ácidos nucleicos ADN Se clasifican en los siguientes niveles Estructura primaria Estructura secundaria Estructura terciaria Estructura cuaternaria ARN

Para visualizar este PPT de la clase 4 en la intranet, utiliza la siguiente clave PPTCANCBBLA 04004

Prepara tu próxima clase En la próxima sesión, estudiaremos Teoría celular. Diversidad celular: células procariontes y eucariontes

Equipo Editorial Área Ciencias: Biología ESTE MATERIAL SE ENCUENTRA PROTEGIDO POR EL REGISTRO DE PROPIEDAD INTELECTUAL. Propiedad Intelectual Cpech RDA: 186414
- Slides: 33