Pozorne si pozrite obrzky a urte pojem ktor

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. HCl Kyselina 1

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. Zásada čpavok Na. OH blen 2

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. Soľ 3

Kyseliny a kyslé roztoky Poznatky o kyselinách z domáceho prostredia: • Ktoré bežné kyseliny nájdete v domácnosti? • Ktorá kyselina rozožiera zubnú sklovinu? • Ktoré kyseliny používame pri zaváraní? • Ktorá kyselina je v tele človeka? • Ktorá kyselina rozpúšťa zlato? • Ktorá kyselina odoberá látkam vodu? • Prečo tmavý čaj po pridaní citrónu zožltne? • Prečo je kyslé mlieko kyslé? 4

Zásady a alkalické roztoky Poznatky o zásadach z domáceho prostredia: • Ktoré bežné zásady nájdete v domácnosti? • Ktorú zásaditú látku používame na umývanie ? • Ktorú zásaditú látku používame v stavebníctve? • Prečo zubná pasta znižuje kyslosť v ústach? • Prečo kvety v Belanských Tatrách sú veľmi často modrej farby (horec) , ale vo Vysokých Tatrách ich nenájdeme? • Akú chuť majú zásadité látky napr. kofeín? 5

Soli a slané roztoky Poznatky o soliach z domáceho prostredia: • Vymenujte aspoň tri soli ktoré sa používajú v domácnosti? • • • Sú všetky soli slanej chuti? Ktoré soli sa používajú na konzervovanie? Je slaná morská voda skutočne slaná? Ktorá soľ sa používa na zmäkčovanie vody? Ako sa volá roztok soli, ktorú lekári používajú pri operáciách? • Prečo nesmieme jesť veľa slaných výrobkov? 6
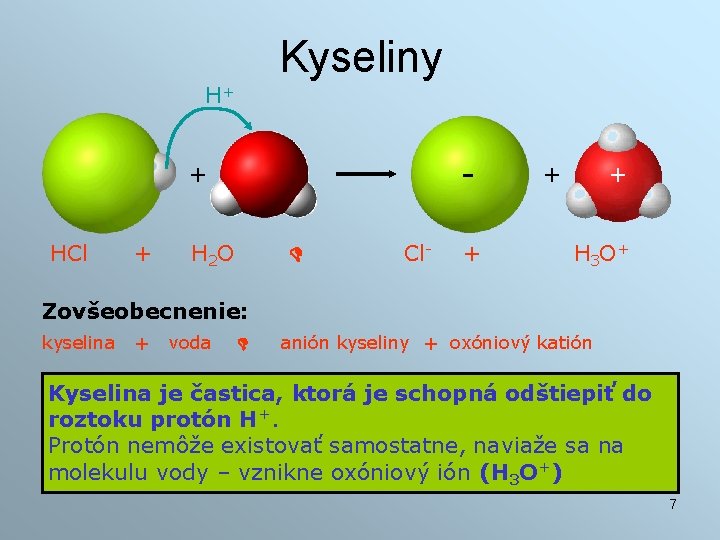
Kyseliny H+ - + HCl + H 2 O Cl- + + + H 3 O+ Zovšeobecnenie: kyselina + voda anión kyseliny + oxóniový katión Kyselina je častica, ktorá je schopná odštiepiť do roztoku protón H+. Protón nemôže existovať samostatne, naviaže sa na molekulu vody – vznikne oxóniový ión (H 3 O+) 7
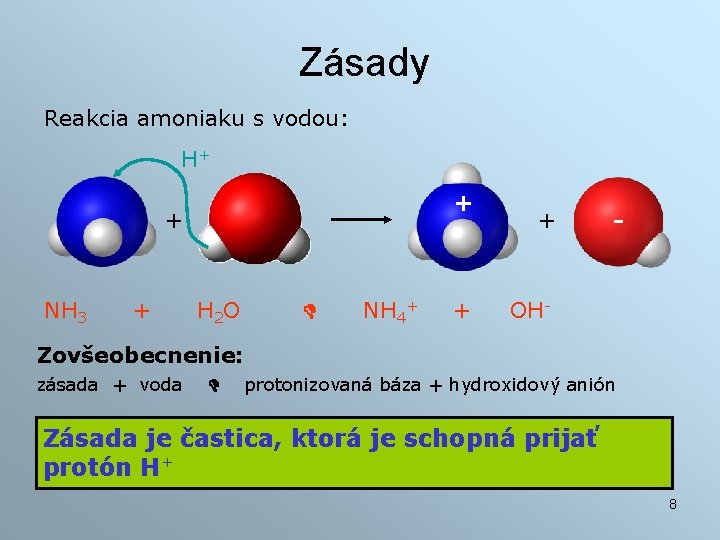
Zásady Reakcia amoniaku s vodou: H+ + + NH 3 + H 2 O NH 4+ + + - OH- Zovšeobecnenie: zásada + voda protonizovaná báza + hydroxidový anión Zásada je častica, ktorá je schopná prijať protón H+ 8
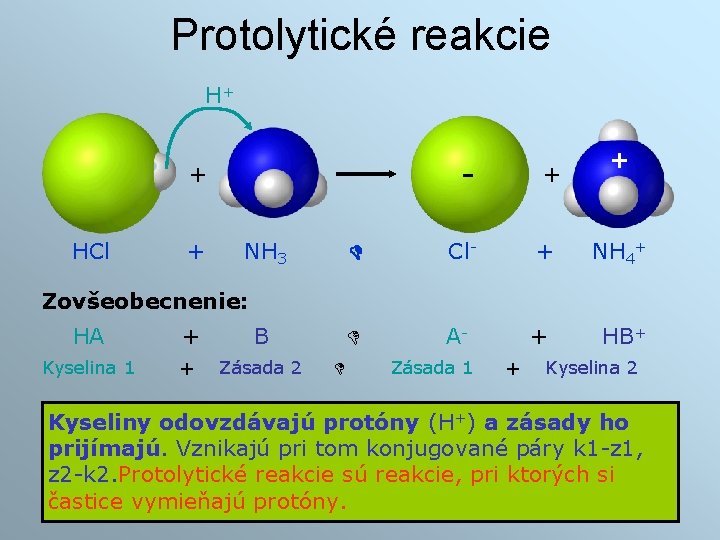
Protolytické reakcie H+ - + HCl + NH 3 + + Cl- + NH 4+ A- + HB+ Zovšeobecnenie: HA + B Kyselina 1 + Zásada 2 Zásada 1 + Kyselina 2 Kyseliny odovzdávajú protóny (H+) a zásady ho prijímajú. Vznikajú pri tom konjugované páry k 1 -z 1, z 2 -k 2. Protolytické reakcie sú reakcie, pri ktorých si častice vymieňajú protóny. 9
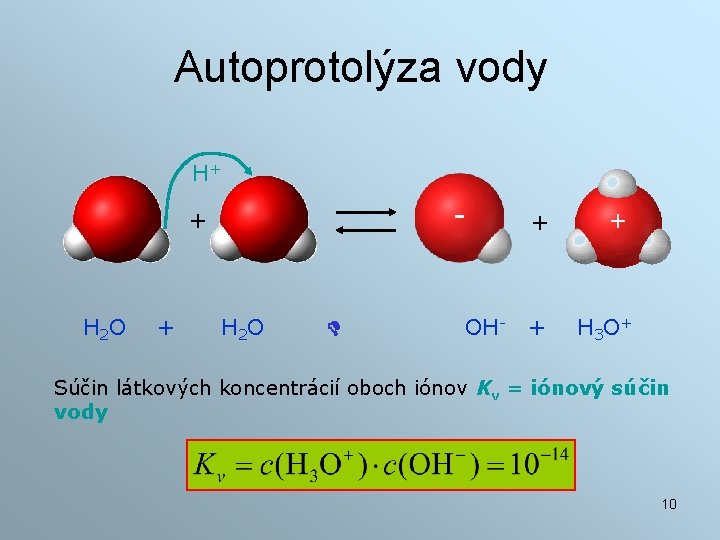
Autoprotolýza vody H+ - + H 2 O OH- + + + H 3 O+ Súčin látkových koncentrácií oboch iónov Kv = iónový súčin vody 10
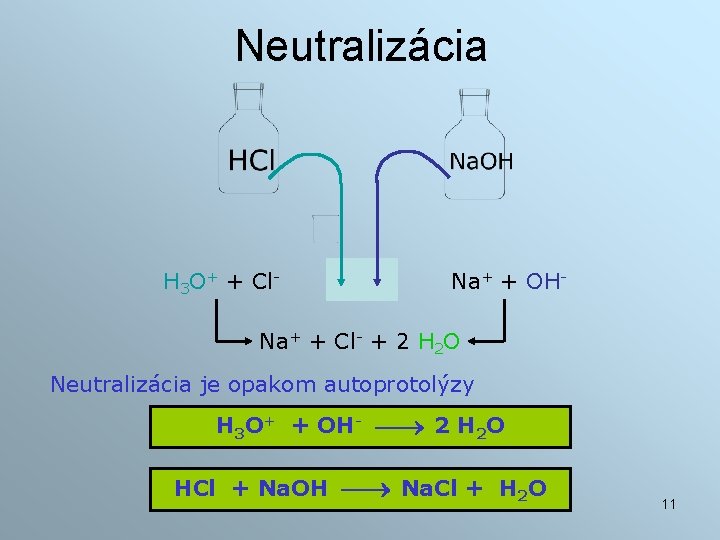
Neutralizácia H 3 O+ + Cl- Na+ + OH- Na+ + Cl- + 2 H 2 O Neutralizácia je opakom autoprotolýzy H 3 O+ + OH- 2 H 2 O HCl + Na. OH Na. Cl + H 2 O 11

p. H je záporný logaritmus koncentrácie H 3 O+ p. H = -log [c(H 3 O+)] Neutrálny roztok: c(H 3 O+) = c(OH-) Kv = 10 -7 mol/l = p. H 7 p. H Rastúca kyslosť Rastúca zásaditosť c(H 3 O+) 100 10 -2 10 -4 10 -6 10 -7 10 -8 10 -10 10 -12 p. H 0 2 4 6 7 8 10 12 10 -14 14 12

Acidobázické indikátory Farbivá, ktoré pri zmene kyslosti zmenia farbu 13

Meranie p. H Indikátory p. H meter 14
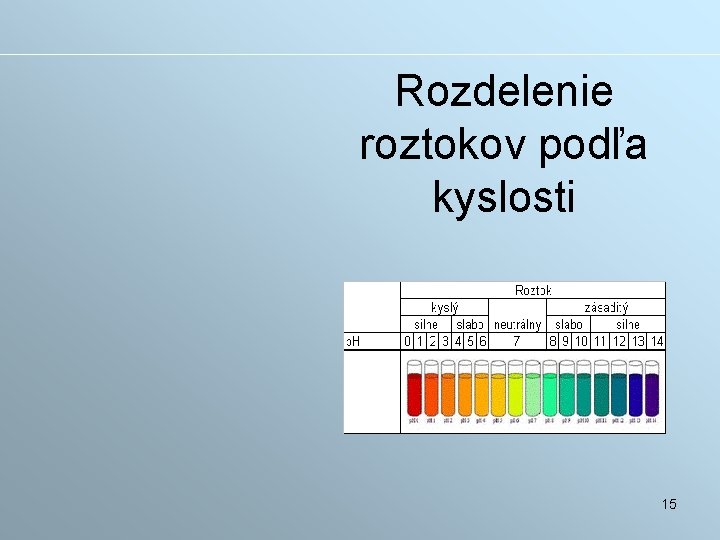
Rozdelenie roztokov podľa kyslosti 15
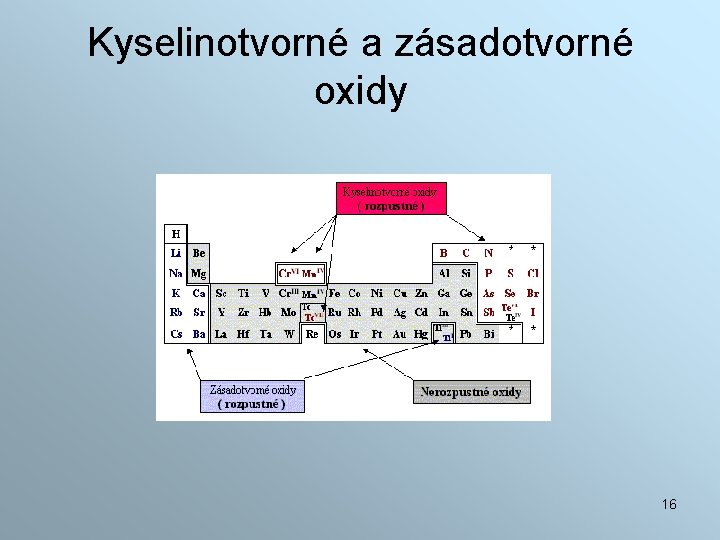
Kyselinotvorné a zásadotvorné oxidy 16
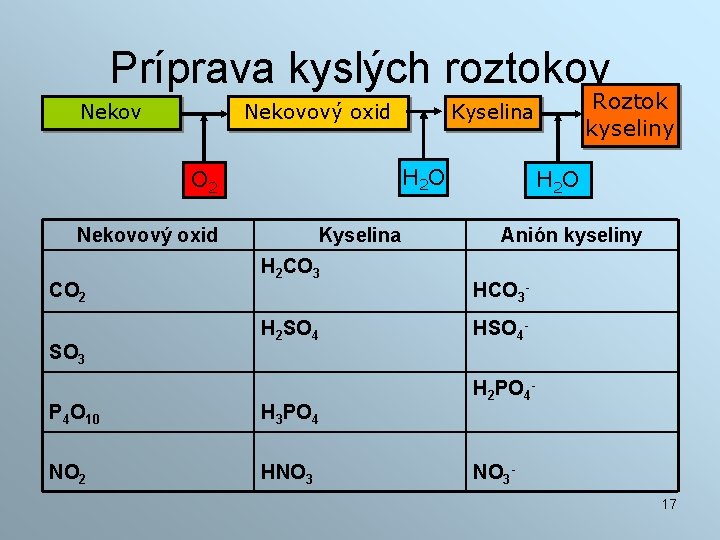
Príprava kyslých roztokov Nekovový oxid H 2 O O 2 Nekovový oxid CO 2 SO 3 Kyselina H 2 CO 3 H 2 SO 4 P 4 O 10 H 3 PO 4 NO 2 HNO 3 Roztok kyseliny Kyselina H 2 O Anión kyseliny HCO 3 HSO 4 H 2 PO 4 - NO 317
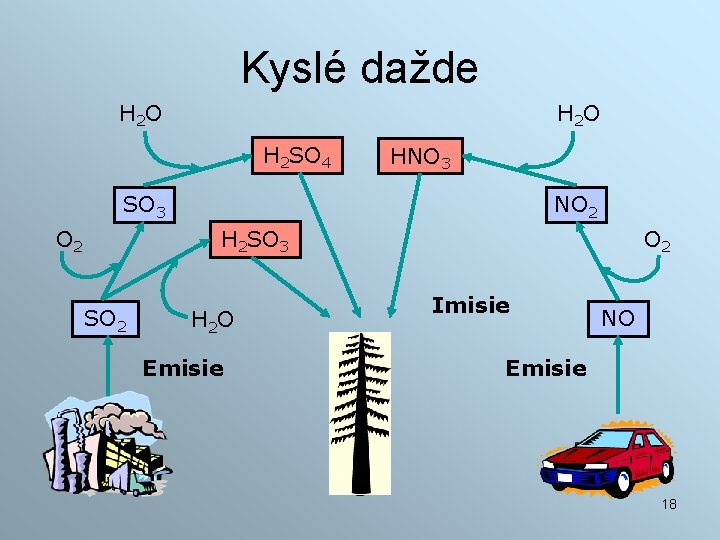
Kyslé dažde H 2 O H 2 SO 4 HNO 3 SO 3 O 2 NO 2 H 2 SO 3 SO 2 H 2 O Emisie O 2 Imisie NO Emisie 18

Kyslé dažde : Škody na budovách Vápenec reaguje s kyselinou sírovou a vzniká sadrovec: Ca. CO 3 (s) + H 2 O + H 2 SO 4 (aq) [Ca. SO 4 2 H 2 O] + CO 2 (g) Rozpad malty 19
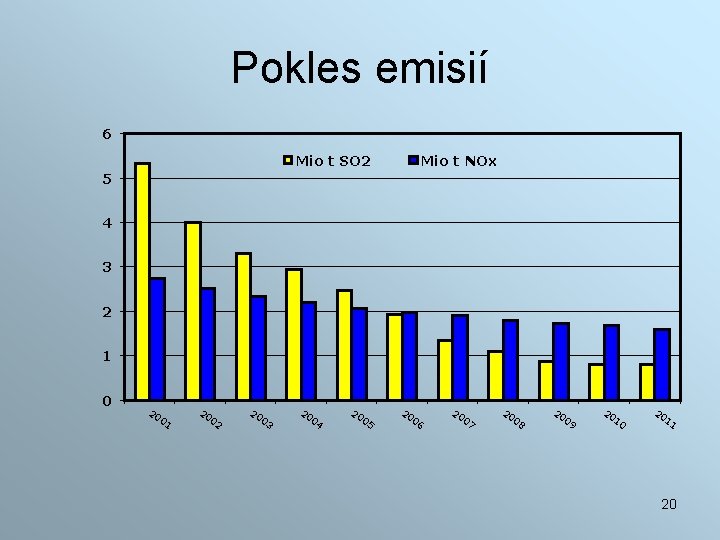
Pokles emisií 6 Mio t SO 2 Mio t NOx 5 4 3 2 1 0 20 0 1 20 0 2 20 0 3 20 04 20 05 20 06 20 07 20 08 20 09 20 10 20 11 20
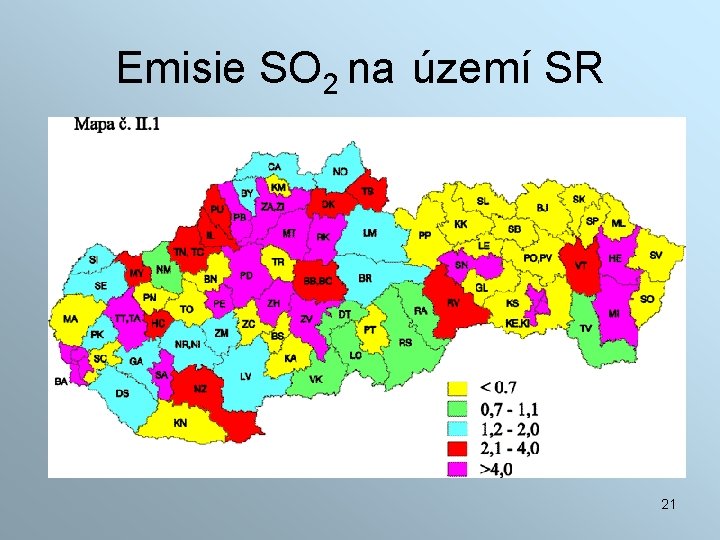
Emisie SO 2 na území SR 21

Emisie NOx na území SR 22

Domáca úloha a voľný čas Motivačné pokusy: Motivačné pokusy a problémové otázky a úlohy k téme "Kyseliny a zásady bežného života" 23
- Slides: 23