Pozorne si pozrite obrzky a urte pojem ktor

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. HCl Kyselina 1

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. Zásada čpavok Na. OH blen 2

Pozorne si pozrite obrázky a určte pojem, ktorý ich spája. Na papier napíšte niekoľko typických vlastností týchto látok. Soľ 3

Kyseliny a kyslé roztoky Skupenstvo: • Kyseliny môžu byť pevné, kvapalné alebo plynné látky rozpustené vo vode. Vlastnosti kyslých roztokov: • • Kyslá chuť Charakteristický sfarbujú indikátory Elektrická vodivosť prítomnosť iónov Pri elektrolýze vedenie elektrického prúdu vo vodných roztokoch • Rozkladajú rôzne látky, napr. vápenec, kovy 4

Zásady a alkalické roztoky Skupenstvo: • Zásady môžu byť pevné, kvapalné alebo plynné látky rozpustené vo vode. Vlastnosti zásaditých roztokov: • • Mydlová alebo horká chuť Charakteristicky sfarbujú indikátory Elektrická vodivosť prítomnosť iónov Pri elektrolýze vedenie elektrického prúdu vo vodných roztokoch • Drogy, alkaloidy 5

Soli a slané roztoky Skupenstvo: • Soli môžu byť pevné alebo kvapalné • Vlastnosti slaných roztokov: • • Slaná chuť alebo sú bez chuti Nesfarbujú indikátory Elektrická vodivosť prítomnosť iónov Pri elektrolýze vedenie elektrického prúdu vo vodných roztokoch • Konzervačné látky 6
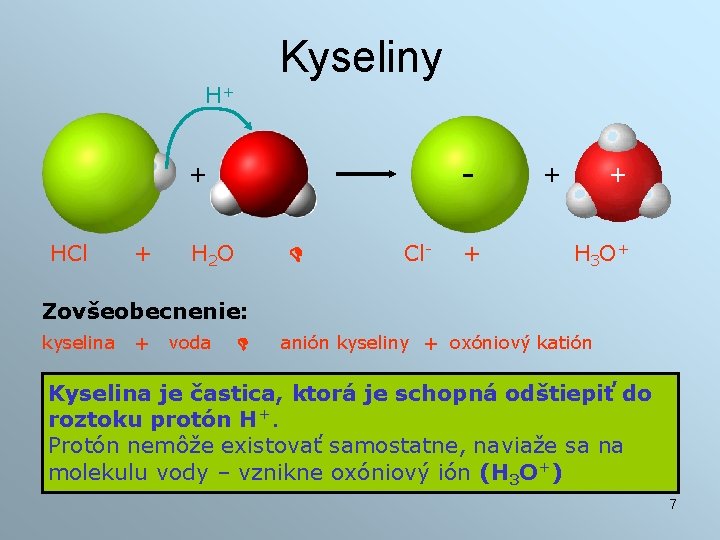
Kyseliny H+ - + HCl + H 2 O Cl- + + + H 3 O+ Zovšeobecnenie: kyselina + voda anión kyseliny + oxóniový katión Kyselina je častica, ktorá je schopná odštiepiť do roztoku protón H+. Protón nemôže existovať samostatne, naviaže sa na molekulu vody – vznikne oxóniový ión (H 3 O+) 7
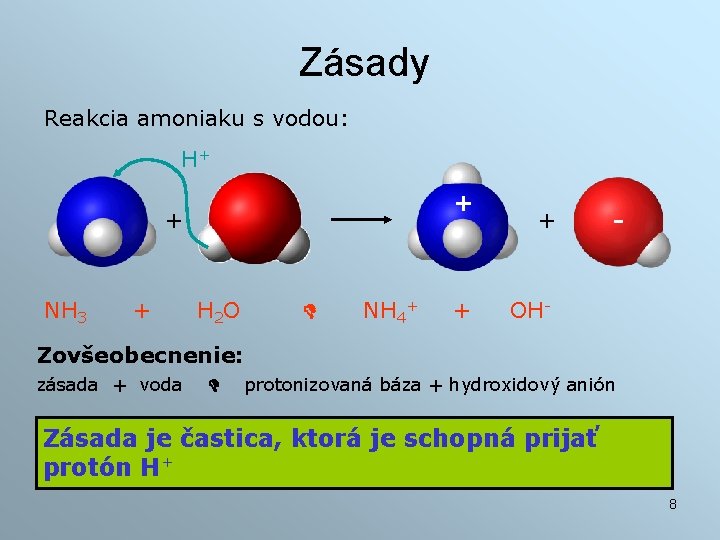
Zásady Reakcia amoniaku s vodou: H+ + + NH 3 + H 2 O NH 4+ + + - OH- Zovšeobecnenie: zásada + voda protonizovaná báza + hydroxidový anión Zásada je častica, ktorá je schopná prijať protón H+ 8
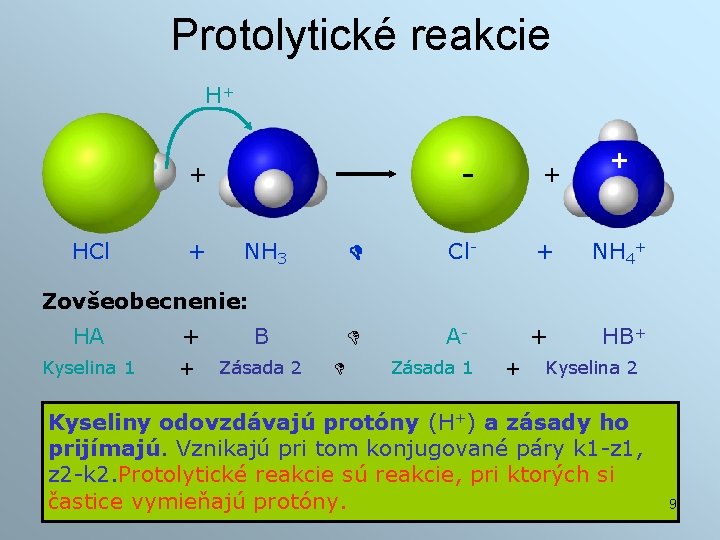
Protolytické reakcie H+ - + HCl + NH 3 + + Cl- + NH 4+ A- + HB+ Zovšeobecnenie: HA + B Kyselina 1 + Zásada 2 Zásada 1 + Kyselina 2 Kyseliny odovzdávajú protóny (H+) a zásady ho prijímajú. Vznikajú pri tom konjugované páry k 1 -z 1, z 2 -k 2. Protolytické reakcie sú reakcie, pri ktorých si častice vymieňajú protóny. 9
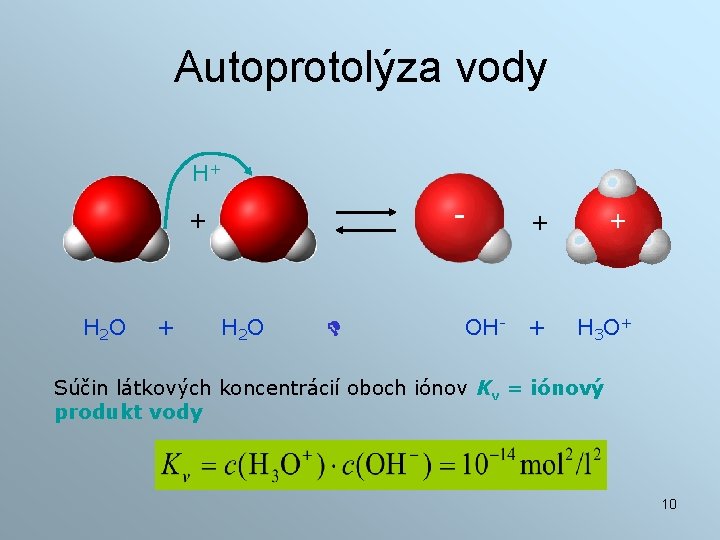
Autoprotolýza vody H+ - + H 2 O OH- + + + H 3 O+ Súčin látkových koncentrácií oboch iónov Kv = iónový produkt vody 10
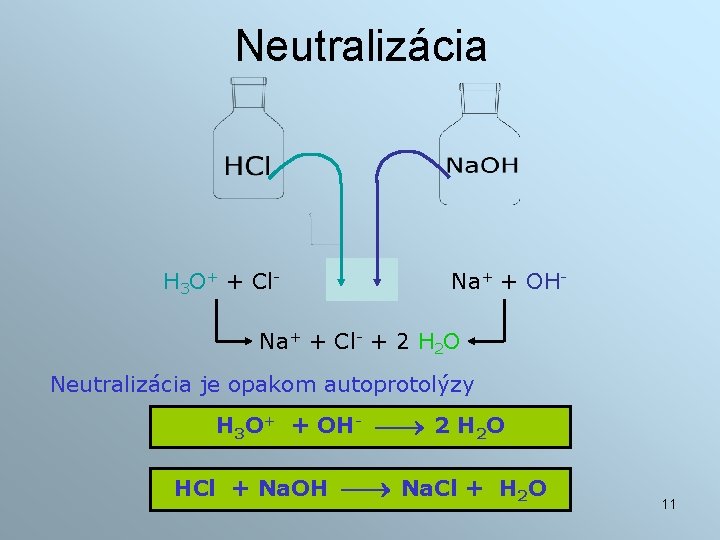
Neutralizácia H 3 O+ + Cl- Na+ + OH- Na+ + Cl- + 2 H 2 O Neutralizácia je opakom autoprotolýzy H 3 O+ + OH- 2 H 2 O HCl + Na. OH Na. Cl + H 2 O 11

p. H je záporný logaritmus koncentrácie H 3 O+ p. H = -log {c(H 3 O+)} Neutrálny roztok: c(H 3 O+) = c(OH-) Kv = 10 -7 mol/l = p. H 7 p. H Rastúca kyslosť Rastúca zásaditosť c(H 3 O+) 100 10 -2 10 -4 10 -6 10 -7 10 -8 10 -10 10 -12 p. H 0 2 4 6 7 8 10 12 10 -14 14 12

Acidobázické indikátory Farbivá, ktoré pri zmene kyslosti zmenia farbu 13

Meranie p. H Indikátory p. H meter 14
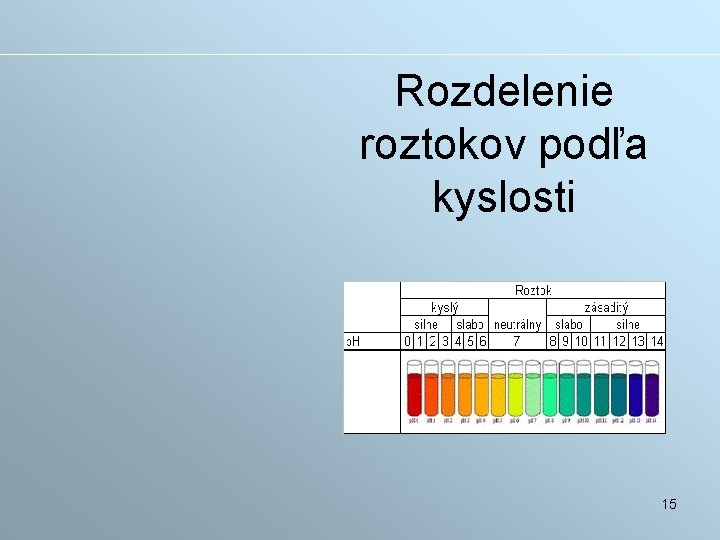
Rozdelenie roztokov podľa kyslosti 15
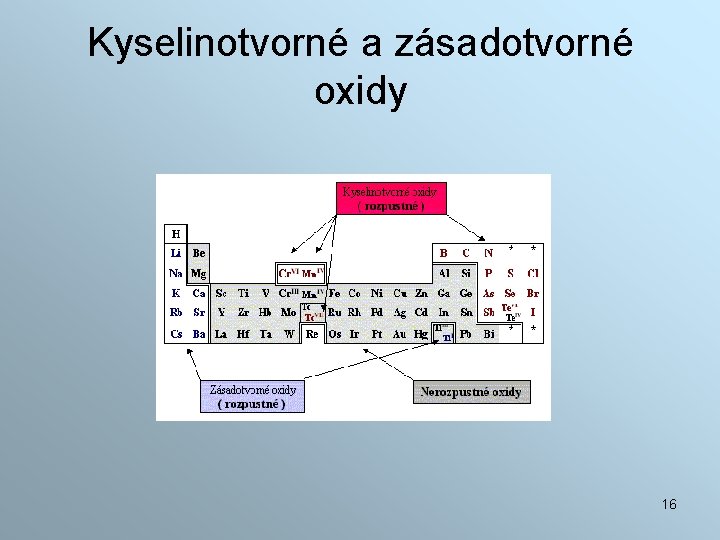
Kyselinotvorné a zásadotvorné oxidy 16
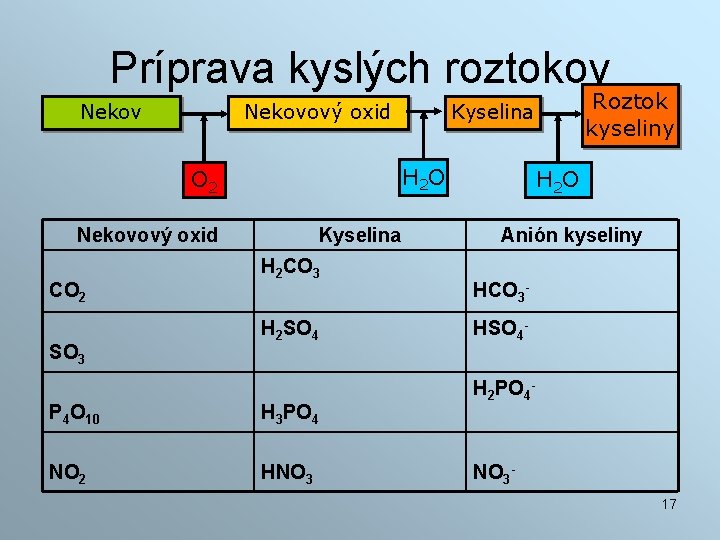
Príprava kyslých roztokov Nekovový oxid H 2 O O 2 Nekovový oxid CO 2 SO 3 Kyselina H 2 CO 3 H 2 SO 4 P 4 O 10 H 3 PO 4 NO 2 HNO 3 Roztok kyseliny Kyselina H 2 O Anión kyseliny HCO 3 HSO 4 H 2 PO 4 - NO 317
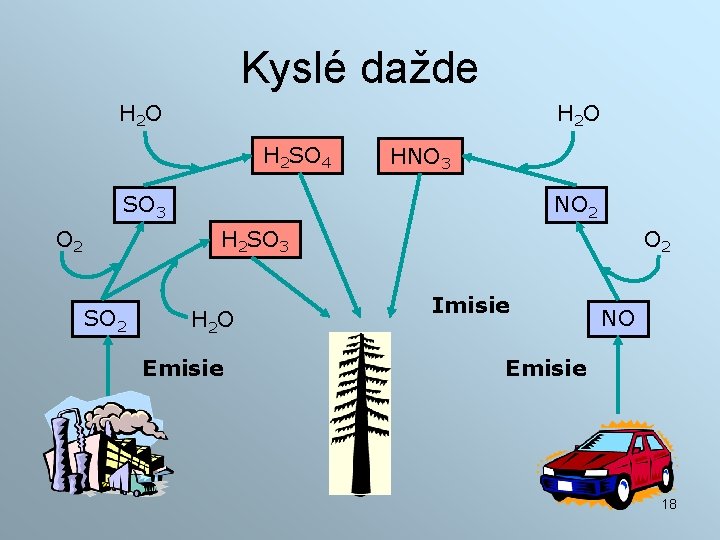
Kyslé dažde H 2 O H 2 SO 4 HNO 3 SO 3 O 2 NO 2 H 2 SO 3 SO 2 H 2 O Emisie O 2 Imisie NO Emisie 18

Kyslé dažde : Škody na budovách Vápenec reaguje s kyselinou sírovou a vzniká sadrovec: Ca. CO 3 (s) + H 2 O + H 2 SO 4 (aq) [Ca. SO 4 2 H 2 O] + CO 2 (g) Rozpad malty 19
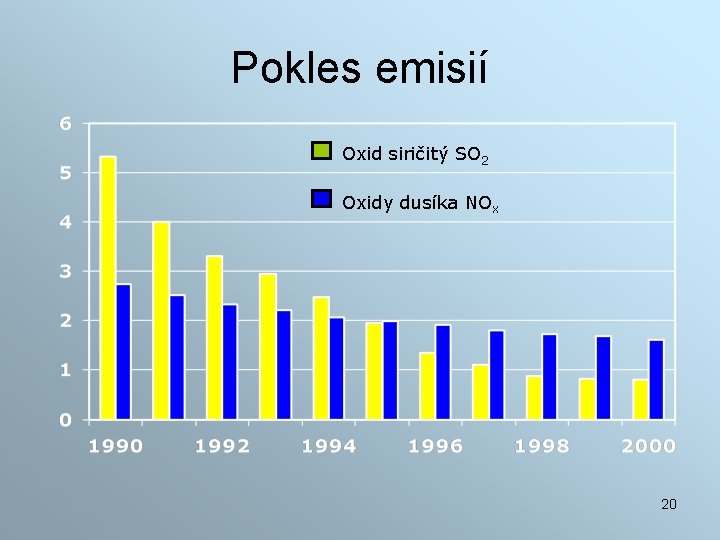
Pokles emisií Oxid siričitý SO 2 Oxidy dusíka NOx 20
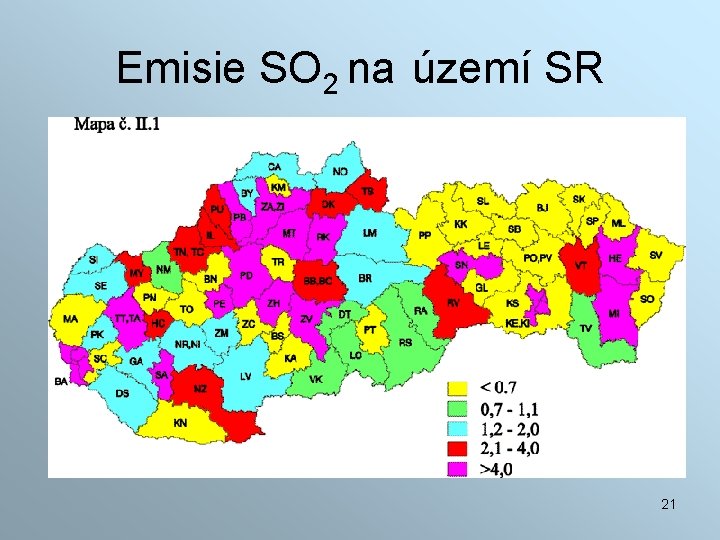
Emisie SO 2 na území SR 21

Emisie NOx na území SR 22

Domáca úloha a voľný čas Motivačné pokusy: http: //kekule. science. upjs. sk/chemia/kuch/kaz/6. htm#kapitola 24 23
- Slides: 23