Potaov chemie 5 pednka vod 1 pednka Molekula















- Slides: 23

Počítačová chemie (5. přednáška) • Úvod (1. přednáška) • Molekula – Struktura molekuly (2. , 3. a 4. přednáška) – Geometrie molekuly (5. přednáška) – Vhled do praxe (6. přednáška) • Molekulové modelování – Molekulová mechanika (7. a 8. přednáška) – Kvantová mechanika (9. a 10. přednáška) – Molekulová dynamika (11. přednáška) – Vhled do praxe (12. přednáška)

Geometrie molekuly • Základní chemické pojmy • Souřadnice atomů: – Kartézské – Interní • Porovnávání geometrií

Základní chemické pojmy Rozměry objektů v chemii: • Elektron: – hmotnost: 9, 12. 10 -31 kg – poloměr: 10 -15 m • Proton: – hmotnost: 1, 67. 10 -27 kg – poloměr: 10 -13 m

Základní chemické pojmy • Atomy a molekuly: – Rozměr se udává v nm (nm = 10 -9 m) nebo angströmech (Å = 10 -10 m). – Hmotnost se uvádí ve formě relativní atomové hmotnosti (AR). AR je rovna podílu hmotnosti atomu a hmotnosti atomové hmotnostní jednotky u: u = 1, 66057. 10 -27 kg (1/12 hmotnosti 1 atomu nuklidu uhlíku C 612)

Základní chemické pojmy • Atomy - příklad: Uhlík: Poloměr: 0, 77 Å; relativní atomová hmotnost: 12, 011 • Molekula: – Rozměry: jednotky - stovky Å (u makromolekul i podstatně více) – Hmotnost: Součet hmotností atomů : -)

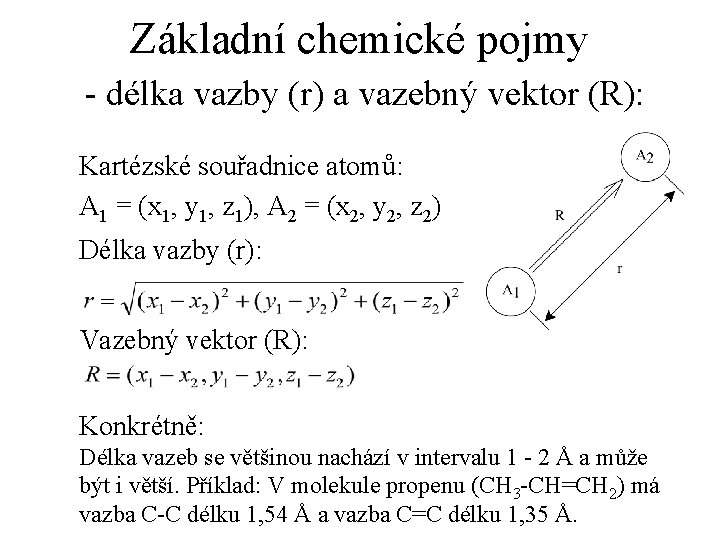
Základní chemické pojmy - délka vazby (r) a vazebný vektor (R): Kartézské souřadnice atomů: A 1 = (x 1, y 1, z 1), A 2 = (x 2, y 2, z 2) Délka vazby (r): Vazebný vektor (R): Konkrétně: Délka vazeb se většinou nachází v intervalu 1 - 2 Å a může být i větší. Příklad: V molekule propenu (CH 3 -CH=CH 2) má vazba C-C délku 1, 54 Å a vazba C=C délku 1, 35 Å.

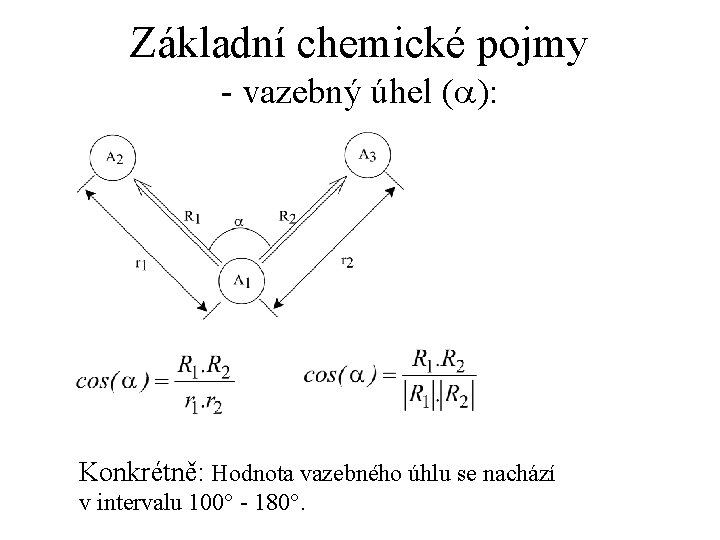
Základní chemické pojmy - vazebný úhel (a): Konkrétně: Hodnota vazebného úhlu se nachází v intervalu 100° - 180°.

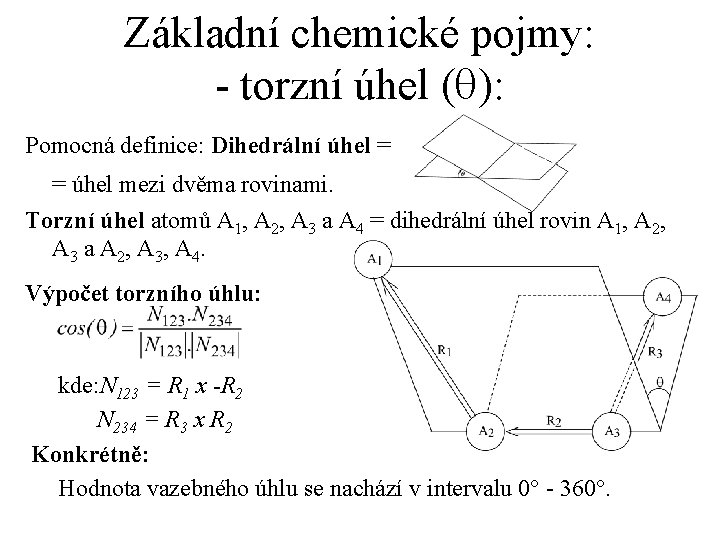
Základní chemické pojmy: - torzní úhel (q): Pomocná definice: Dihedrální úhel = = úhel mezi dvěma rovinami. Torzní úhel atomů A 1, A 2, A 3 a A 4 = dihedrální úhel rovin A 1, A 2, A 3 a A 2, A 3, A 4. Výpočet torzního úhlu: kde: N 123 = R 1 x -R 2 N 234 = R 3 x R 2 Konkrétně: Hodnota vazebného úhlu se nachází v intervalu 0° - 360°.

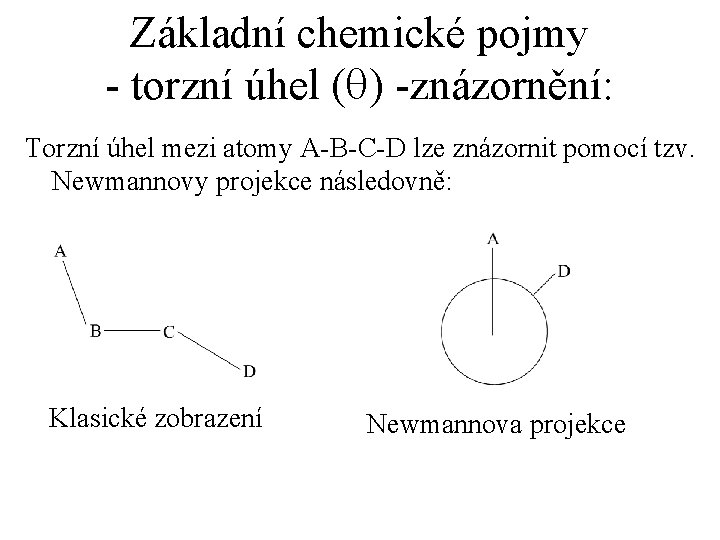
Základní chemické pojmy - torzní úhel (q) -znázornění: Torzní úhel mezi atomy A-B-C-D lze znázornit pomocí tzv. Newmannovy projekce následovně: Klasické zobrazení Newmannova projekce

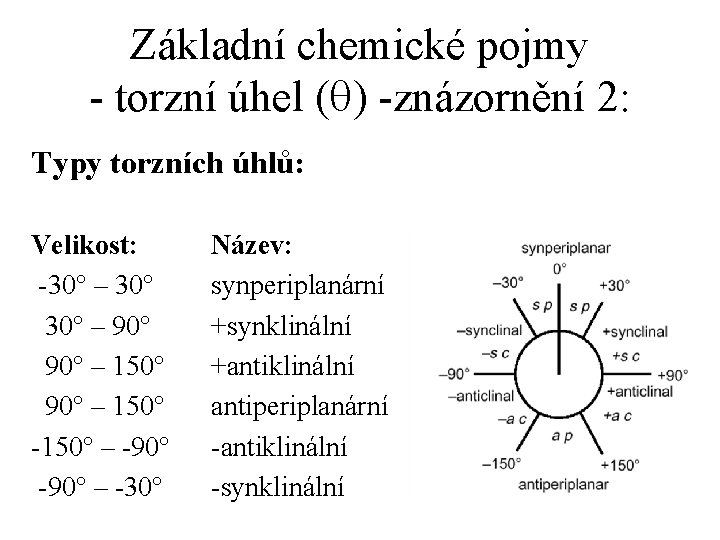
Základní chemické pojmy - torzní úhel (q) -znázornění 2: Typy torzních úhlů: Velikost: -30° – 90° – 150° -150° – -90° – -30° Název: synperiplanární +synklinální +antiklinální antiperiplanární -antiklinální -synklinální

Kartézské souřadnice atomů • Poloha každého atomu popsána x-ovu, y-ovou a z-ovu souřadnicí v kartézské soustavě souřadnic. • Pro molekulu s N atomy je nutno znát 3 N - 6 souřadnic. Poloha a orientace molekuly vzhledem ke vztažné soustavě totiž může být libovolná.

Kartézské souřadnice atomů příklad: Molekula methanu: Souřadnice: C H H H 0. 000* 1. 100 0. 000* -0. 367 -1. 037 -0. 367 0. 519 H -0. 367 0. 519 0. 000* 0. 898 -0. 898 * Tyto souřadnice mohou být zvoleny libovolně, ale stále se bude jednat o tutéž molekulu (pouze bude posunuta v prostoru).

Interní souřadnice atomů • Je vyjádřena Z-maticí. • Poloha atomu D je popsána: – vzdáleností mezi atomy C a D – vazebným úhlem mezi atomy B, C a D – dihedrálním úhlem mezi atomy A, B, C a D • Vyjímka: – Pro 1. atom v z-matici nejsou uvedeny žádné informace. – Pro 2. atom v z-matici jsou uvedeny jen informace o vazbě. – Pro 3. atom v z-matici jsou uvedeny jen informace o vazbě a vazebném úhlu.

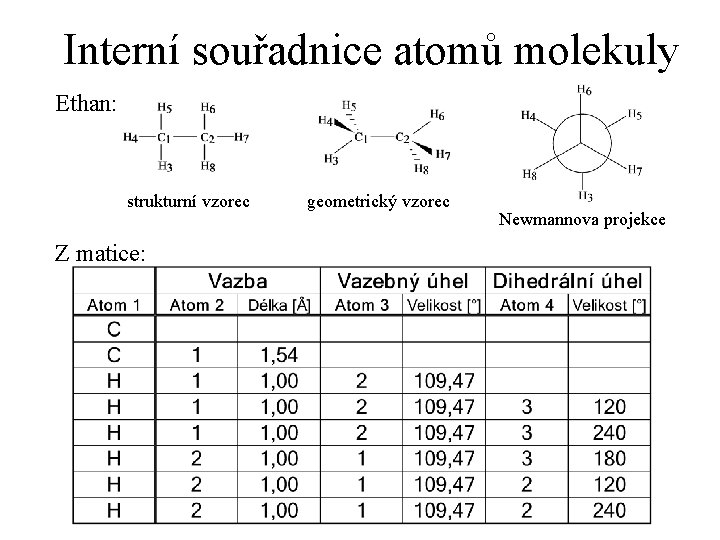
Interní souřadnice atomů molekuly Ethan: strukturní vzorec Z matice: geometrický vzorec Newmannova projekce

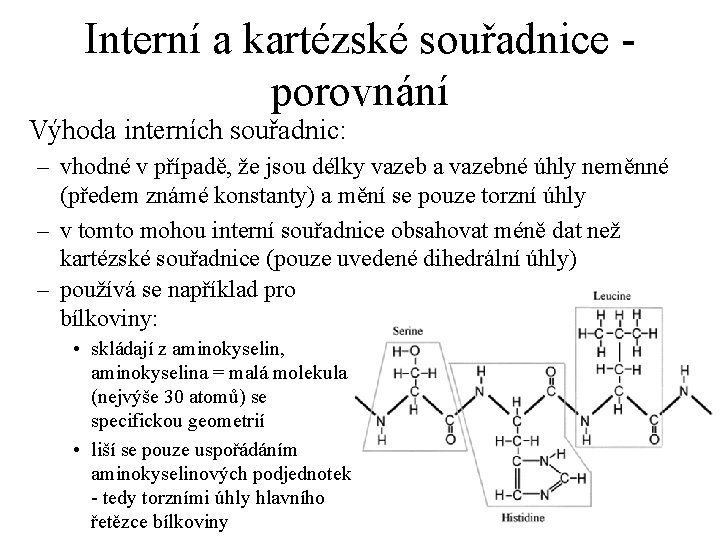
Interní a kartézské souřadnice porovnání Výhoda interních souřadnic: – vhodné v případě, že jsou délky vazeb a vazebné úhly neměnné (předem známé konstanty) a mění se pouze torzní úhly – v tomto mohou interní souřadnice obsahovat méně dat než kartézské souřadnice (pouze uvedené dihedrální úhly) – používá se například pro bílkoviny: • skládají z aminokyselin, aminokyselina = malá molekula (nejvýše 30 atomů) se specifickou geometrií • liší se pouze uspořádáním aminokyselinových podjednotek - tedy torzními úhly hlavního řetězce bílkoviny

Interní a kartézské souřadnice porovnání II Nevýhoda interních souřadnic: – Některé základní výpočty jsou mnohem obtížnejší • Vzdálenost mezi dvěma body • Určení nejbližších atomů (bodů) vzhledem k určitému atomu – Porovnávání nezávislých objektů – Mnohem více nelineárních vztahů mezi souřadnicemi => obtížná případně nemožná optimalizace výpočtů

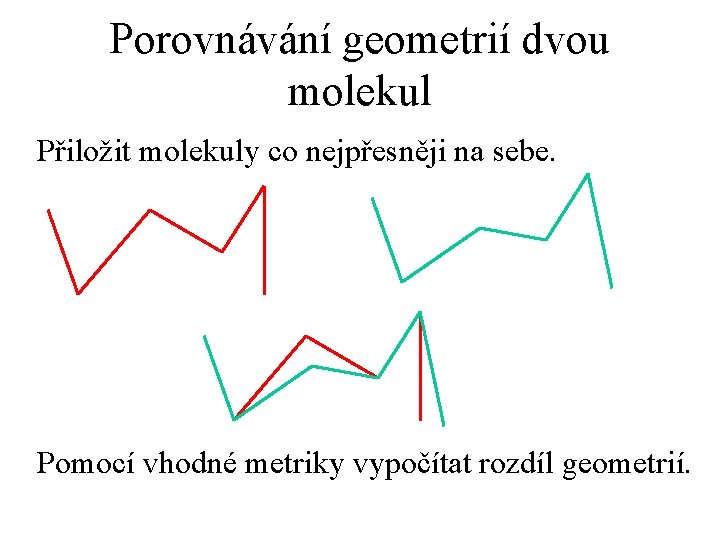
Porovnávání geometrií dvou molekul Přiložit molekuly co nejpřesněji na sebe. Pomocí vhodné metriky vypočítat rozdíl geometrií.

Porovnání geometrií dvou molekul II • Podmínka: Atomy daných molekul jsou indexovány (seřazeny) tak, že odpovídající atomy* mají stejné indexy. * Atom x z molekuly X odpovídá atomu y z molekuly Y, pokud lze atom x zobrazit na atom y pomocí zobrazení izomorfismu. Je zřejmé, že pro všechny atomy musí být použit stejný izomorfismus.

Porovnání geometrií dvou molekul III Porovnávací kritérium: RMSD (root mean square deviation). Jednotky: Å Kde: d(xi, yi) N w vzdálenost odpovídajících atomů xi a yi počet atomů ohodnocení jednotlivých atomů Nejčastěji používaná ohodnocení: 1 - stejné pro všechny atomy AR - atomová relativní hmotnost atomu

Porovnání geometrií dvou molekul IV Problém porovnávání geometrií: Máme 2 uspořádané množiny bodů v R 3: X: (x 1, …, x. N) a Y: (y 1, …, y. N), kde xi odpovídá yi. Hledáme transformaci T = r + t v R 3, kde r je rotace a t je translace tak, že: RMSD(X, T(Y)) ® min

Porovnání geometrií dvou molekul V Vyhledání translace Výpočet těžišť obou molekul podle vztahu: Analogicky TY. Translace molekuly Y: Posunutí TY do TX.

Porovnání geometrií dvou molekul VI Vyhledání rotace Vytvořeno mnoho metod, nejpoužívanější: • Mc. Lachlan (1972): Iterativní metoda, která rotuje molekulu Y o malý úhel (b) v každém kroku a hledá minimální RMSD. Složitost: O(p 3), kde p je počet pootočení (p = 360°/b) • Kabsch a Diamond (1976): Převádí problém nalezení rotace na problém nalezení vlastních vektorů matice 3 x 3 (matice tenzorů definované metriky). Složitost: lineární.

Literatura 1) Leach A. R. : Molecular modelling. Longman (1996) 2) Jensen F. : Computational chemistry. Wiley (1999) 3) Wampler J. E. : Different Concepts of Molecular Structure. The University of Georgia (1999): http: //bmbiris. bmb. uga. edu/wampler/ 8200/structure