PORUCHY VIVY PATOFYZIOLGIA OBEZITY VYBRAN METABOLICK OCHORENIA Prof

PORUCHY VÝŽIVY PATOFYZIOLÓGIA OBEZITY VYBRANÉ METABOLICKÉ OCHORENIA Prof. MUDr. Jana Plevková Ph. D Ústav patologickej fyziológie JLF UK 2017

regulácia metabolizmu znížený príjem potravy (kwashiorkor, malnutrícia) zvýšený príjem potravy (obezita) patofyziológia vybraných metabolických ochorení

• anabolizmus vs katabolizmus • Odolnosť voči ochoreniam • Schopnosť zvládať záťaž • Možnosti hojenia/sanácie • Psychika

Metabolizmus Dostatok energie v organizme ovplyvňuje jeho celkovú výkonnosť, jeho odolnosť vzhľadom k záťaži /chorobám/, metabolizmus je aj zdrojom látok potrebných pre štruktúru a funkciu organizmu a jeho súčastí Hodnotenie z hľadiska kvalitatívneho a kvantitatívneho – dostatok energie vs primerané zastúpenie jednotlivých živín a esenciálnych prvkov Poruchy metabolizmu vedú k deficitu /energie, substrátov/, deplécii esenciálnych mikronutrientov, nadbytku tuku prítomnosti látok potenciálne toxických pre organizmus /ketolátky/, atd.

Regulácia metabolických dejov • Inzulín – pôsobí anabolicky, vstup glukózy do bb. svalov a tukového tkaniva (GLUT 4) stimuluje proteosyntézu, tlmí lipolýzu, vstup K do buniek, zvyšuje chuť do jedla • Glukagón – glykémiu (glykogenolýza a glukoneogenéza), lipolýzu, jeho hladina stúpa pri hladovaní • STH – proteoanabolický účinok, (niektoré efekty cez IGF – 1) zvyšuje glykémiu, pri vysokých koncentráciách navodzuje inzulinorezistenciu • Pohlavné hormóny – pôsobia anabolicky, androgény – /svaly, pozitívna dusíková bilancia/ estrogény – distribúcia tukového tkaniva, retencia Na a vody, zasahujú do metabolizmu cholesterolu, progesteron termogenézu

Regulácia metabolických dejov • Glukokortikoidy – glykémiu cez glukoneogenézu, proteokatabolický účinok (periféria) proteoanabolický účinok v pečeni stimulujú syntézu glykogénu permisívny efekt na účinky KA & glukagónu stresové hormóny (inzulinorezistencia) mineralokortikoidný efekt • T 3 a T 4 – bazálneho metabolizmu spotreba kyslíka a produkcia tepla senzibilizujú tkanivá k účinku KA zvyšujú vstrebávanie cukrov z čreva fyziologické konc. majú proteoanabolický účinok vysoké konc. majú účinok katabolický zvýšené hladiny nepriaznivo ovplyvňujú svaly – myokard

Postavenie orgánov v metabolizme • Pečeň – zaradenie do portálneho obehu – kontakt so vstrebanými látkami, regulácia glykémie, syntéza proteínov, vznik močoviny, skladovanie lipidov, tvorba lipoproteínov, žlčové kyseliny, zásobné miesto vitamínov • Svalová hmota – cca 40% telesnej hmotnosti, významné miesto spotreby energie, ale i rezervoár bielkovín, vstup glukózy do svalov • Tukové tkanivo – je zásobárňou energie – lipolýza a následný transport MK do svalov, pečene, atd. , premena steroidných hormónov

Postavenie orgánov v metabolizme • Tráviaci systém – miesto trávenia, vstrebávania a vylučovania niektorých látok, tvorba chilomikrónov, veľká proliferačná aktivita črevnej sliznice • Kosti – zásoby vápnika, nárazníková kapacita • Koža – premena vit. D, termoregulácia, ukladanie podkožného tuku • Obličky – aktivácia vit D, spätná reabsorbcia glukózy, AMK, tubulárne transportné systémy sú metabolicky veľmi náročné • Respiračný systém a KVS – dostatočný prísun kyslíka a živín pre tkanivá tak, úmerné ich metabolickým požiadavkám, oba systémy sú závislé na dodávke energie

Zdroje energie v organizme • Hierarchia vo využívaní energetických zdrojov • Glukóza – najpohotovejší zdroj, presne regulovaná, doplňovaná príjmom z potravy, z glykogénu a glukoneogenézou, neklesá pod kritické hodnoty ani pri dlhodobom hladovaní • Nedostatok glukózy v organizme, alebo „nemožnosť“ využívať glukózu pre deficit inzulínu alebo IR energia sa získava z tukov a bielkovín. tukov pri nedostatku cukrov tvorba ketolátok, ktoré môžu byť energetickým zdrojom, dokonca aj pre mozog pri dlhodobom hladovaní, ketogenéza tak šetrí bielkoviny, pokles efektivity ketogenézy – v starobe, v dôsledku čoho prevládne katabolizmus • Štiepenie

Poruchy výživy a ich dôsledky • Vody, proteíny, glycidy, tuky, mikronutrienty – uvedené zložky potravy musia zodpovedať normám tak po stránke kvalitatívnej ako i kvantitatívnej • Závažný a dlhodobý nedostatok potravy ako celku – malnutrícia, hladovanie, hypo, či avitaminózy • Dlhodobý nadmerný prívod – obezita • Nadmerný príjem niektorých zložiek – hypervitaminóza A, D • Dlhodobo nesprávne zloženie potravy – civilizačné ochorenia, zhubné nádory

Poruchy výživy Hyponutrícia – nedostatočná výživa Malnutrícia – neadekvátne zloženie potravy vzhľadom k jej kvalite energetické krytie dostatočné, avšak chýbajú urč. látky, ktorých deficit spôsobuje závažné zdravotné problémy napríklad kwashiorkor Kwashiorkor – je typ podvýživy s nedostatkom bielkovín hypoalbuminémia pokles onkotického tlaku a opuchy steatóze pečene, poruche trofiky kože, poruchy činnosti NS, anémia, hypotermia, hypotenzia, bradykardia, poruchy vnútorného prostredia Okrem primárne nutrične sp. kwashiorkoru v rozvojových krajinách, môže podobný stav nastať pri závažných katabolických stavoch /u starých pacientov so závažnou chorobou, počas hospitalizácie/ - stresom sp. katabolizmus

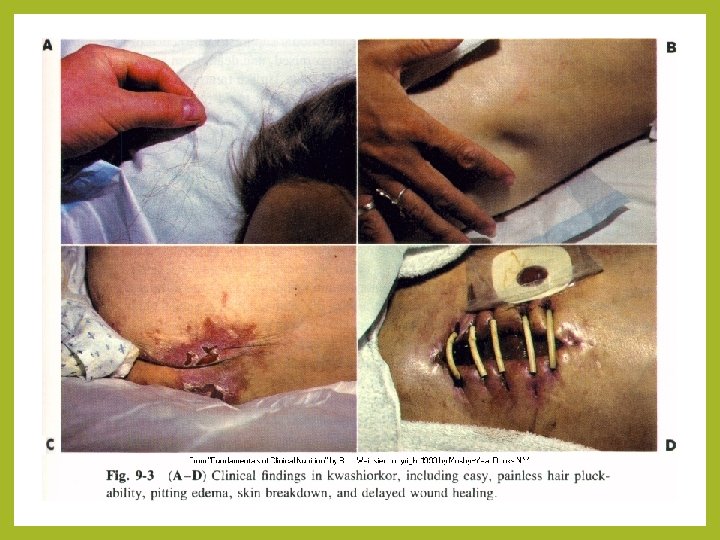

Poruchy výživy • Karencia zdravia – nedostatok určitej látky v potrave spôsobujúci poruchu • Marazmus – je to typ podvýživy charakterizovaný nedostatkom všetkých základných živín, proporcionálny nedostatok živín. Dochádza k úbytku podkožného tuku a svalov, (kosť a koža), celkové zníženie úrovne metabolizmu, vzniká pri hladovaní, mentálnej anorexii. • Na rozdiel od kwashiorkoru je tento stav prognosticky priaznivý po obnovení dodávky potravy sa stav upraví

Jednoduché hladovanie obmedzený, nie celkom potlačený prívod potravy - zmena metabolizmu je fyziologickou odpoveďou na hladovanie princípom je čo najúspornejšie využívanie energie dlhotrvajúce hladovanie okrem nedostatku energie a substrátov aj deplécia vitamínov a stopových prvkov (železo) najprv sa spotrebujú zásoby glykogénu (12 – 24 hod) potom nastupuje glukoneogenéza v pečeni, hladina inzulínu a hladina kontraregulačných hormónov vzostup lipolýzy a B oxidácie MK so vznikom acetyl Co. A tvorba ketolátok potlačenie sa glukoneogenézy a proteokatabolizmu – adaptačné procesy manifestácia - telesnej hmotnosti – chudnutie, ktoré môže mať až charakter marazmu

Sekundárna malnutrícia Na rozdiel od jednoduchého hladovania je podmienená určitým primárnym ochorením, ktoré vedie k nedostatočnej výžive organizmu viacerými mechanizmami 1. Znížený príjem potravy – anorexia, nausea, rôzne ochorenia GIT 2. Zvýšené straty – exsudatívna gastro a enteropatia, krvácanie, hnačky 3. Zvýšené nutričné požiadavky – horúčka, infekcia, nádory, chirurgické výkony Pri tomto type malnutrície sú narušené regulačné mechanizmy využitia energie a dochádza ku proteokatabolizmu

Katabolické stavy • Vznikajú na základe narušenia regulácie metabolických procesov • Odlišujú sa od jednoduchého hladovania, horšia prognóza • Negatívna bielkovinová a energetická bilancia sa vyvinie veľmi rýchlo • V patogenéze sa uplatňujú dôsledky zápalovej reakcie /vplyv zápalových mediátorov, cytokínov, eikozanoidov/ ako aj stresovej reakcie /akt. os hypotalamus, hypofýza, nadoblička – metabolické dôsledky/ • Nádorové ochorenia – trvale zvýšená lipolýza, proteolýza a glukoneogenéza v pečeni, nádor produkuje látky ovplyvňujúce metabolizmus – TNF kachektín • Rozsiahle traumy, popáleniny, ťažké celkové infekcie, FUO,
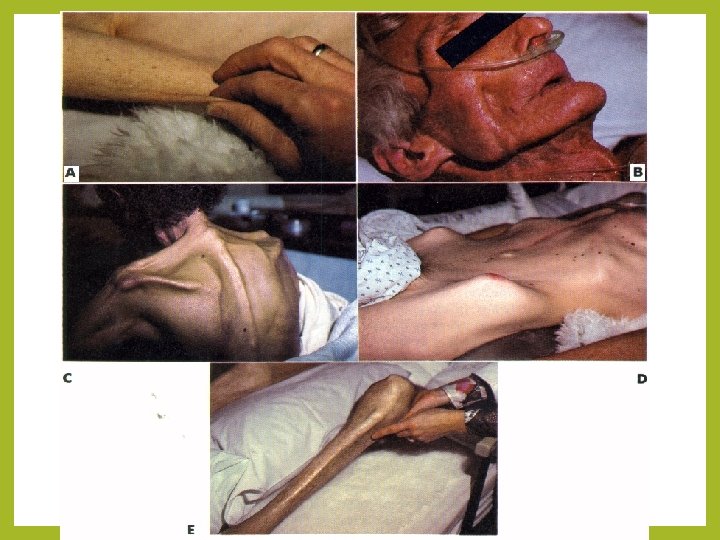

Orgánové zmeny pri proteínovom a energetickom deficite • váhový úbytok – zmenšenie adipocytov, atrofia tkanív • objem ECT sa relatívne nemení, čím dochádza k poklesu onkotického tlaku • myokard – zníženie SVO, kontraktility, obsahu glykogénu a objavuje sa atrofia myofibríl, zmeny sú reverzibilné • RS – minimálne ovplyvnenie, zmeny kontraktility dýchacích svalov, zníženie VT, VC, a min. ventilácie • GIT – zníženie motility žalúdka, i sekrécie, atrofia sliznice čreva a strata črevných klkov, postihnutá je obnova enterocytov • Pankreas – exokrinná f. je znížená pri zachovaní endokrinnej

Orgánové zmeny pri proteínovom a energetickom deficite • obličky – capsaula adiposa renis, atrofia obličky, zhoršenie konc. schopnosti z dôvodu zníženia osmotického gradientu v dreni • hepar – atrofia, zmenšenie objemu bb, zníženie obsahu glykogénu, proteosyntéza je znížená, u kwashiorkoru – je hapatomegália pre steatózu • endokrinný systém – zníženie produkcie hormónov, pokles testosterónu u mužov, pokles FSH a LH u žien, porušená konverzia T 4 na T 3 • imunitný systém – všetky zložky, bunková i humorálna imunita, granulocyty majú zníženú schopnosť migrácie a usmrcovania baktérií, pri zachovalej schopnosti fagocytózy • porušenie bariér – atrofia kože, sliznice GIT • zhoršené hojenie rán

Obezita Obézny človek jeho telesná hmotnosť výrazne presahuje hornú hranicu fyziologických hodnôt a je spôsobená nahromadením tuku u mužov nad 25%, u žien nad 30% celkovej telesnej hmotnosti Obezita je chronická choroba, ktorá vyúsťuje do multiorgánového poškodenia a z toho vyplývajúcich komplikácií Obezita je výsledkom pôsobenia viacerých mechanizmov

WHO október 2017 • Výskyt obezity celosvetovo sa trojnásobne zvýšil od r. 1975. • V r. 2016, viac ako 1. 9 billion dospelých malo nadváhu, viac ako 650 mil, z nich bolo obéznych • Je to v % 39% dospelých, ktorí majú nadváhu a 13% má už obezitu. • Väčšina svetovej populácie žije v krajinách kde nadváha a obezita zabíja viac ľudí ako podvýživa. • 41 mil. detí pod 5 rokov má nadváhu alebo obezitu, viac ako 340 million detí a adolescentov od 5 -19 rokov má nadváhu, alebo obezitu. • Obezita je preventabilné ochorenie.

Riziká obezity • KVS – ateroskleróza, ICHS, srdcové zlyhanie, varixy, tromboembolické komplikácie • endokrinné – PCO, poruchy menštruácie a fertility • GIT – GERD, steatóza pečene, cholelitiáza, hernie a kolorektálny Ca • genitourinárne – erektilná dysfunkcia, inkontinencia, CHRI, hypogonadizmus u mužov, Ca prsníka a uteru, predčasný pôrod • koža a adnexá – lymfedém, celulitída, kožné infekcie • muskuloskeletálne – dna, imobilita, osteoartritída, lumbalgie • neurologické – CMP, syndróm karpálneho tunela • respiračné – Pickwickov sy, OSA • psychologické – depresia, nízke sebavedomie, sociálna stigmatizácia

Postupy zisťovania obezity 1) Stanovenie indexu telovej hmoty – BMI telesná hmotnosť ( v kg) BMI = výška ( v m)2 Norma: BMI = 19 – 25 Nadváha: BMI = 26 – 30 Obezita: BMI > 30 „Malígna“ obezita: BMI > 40 2) Obvod pása : obvod bokov Norma: 0, 7 – 0, 95 3) Meranie hrúbky kožných rias 4) Obvod pása: muži < 95 cm; ženy < 81 cm

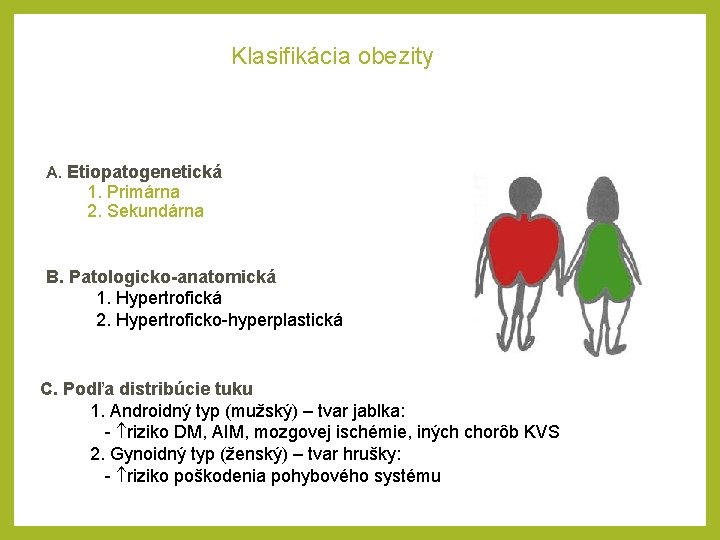
Klasifikácia obezity A. Etiopatogenetická 1. Primárna 2. Sekundárna B. Patologicko-anatomická 1. Hypertrofická 2. Hypertroficko hyperplastická C. Podľa distribúcie tuku 1. Androidný typ (mužský) – tvar jablka: riziko DM, AIM, mozgovej ischémie, iných chorôb KVS 2. Gynoidný typ (ženský) – tvar hrušky: riziko poškodenia pohybového systému

Hlavné príčiny a mechanizmy vzniku obezity Genetické determinanty vzniku obezity – asi u 33% obéznych pacientov monogénové poruchy – mutácia génu kódujúceho syntézu leptínu, alebo mutácie leptínového receptora polygénové poruchy – mutácie viacerých génov, ktorých kombinácia a súčasný podiel vonkajších faktorov vedú k vzniku obezity tieto poruchy sa môžu týkať receptorov s metabolickými účinkami, génov pre uncoupling proteíny, LDL – R receptor

Hlavné príčiny a mechanizmy vzniku obezity Najčastejšie faktory podmieňujúce vznik nadváhy a obezity: genetická predispozícia energeticky bohatá strava obmedzený pohyb a sedavý spôsob života dôsledok iného ochorenia /hypotyreóza/ poruchy regulácie príjmu potravy psychický stres nežiaduce účinky liečiv

Hlavné príčiny a mechanizmy vzniku obezity Najzávažnejšia príčina je že príjem energie prevyšuje počas dlhšej doby energetickú spotrebu organizmu I. primárne zvýšenie príjmu energie na úroveň, ktorú organizmus nedokáže spotrebovať ani pri normálnom fungovaní metabolizmu II. primárne zníženie spotreby energie na úroveň, ktorá spôsobí zvýšenie ukladania energie aj pri normálnom nezvýšenom príjme energie III. kombinácia oboch predchádzajúcich mechanizmov

Gény versus behaviorálne vplyvy Fyzikálne zákony : málo kalórií – obezita nevzniká • avšak - veľa kalórií nemusí vždy viesť k obezite (substrátové cykly – uncoupling proteiny – „dobrý metabolizmus“ Behaviorálne zmeny v príjme potravy raz denne, veľa bez raňajok • Fast food • Alkohol (pivo) • Nibbling (zobkanie) (TV) • Stres • Nočné eating • „Pažravé“ prejedanie sa • Poruchy príjmu potravy mentálna anorexia a bulímia
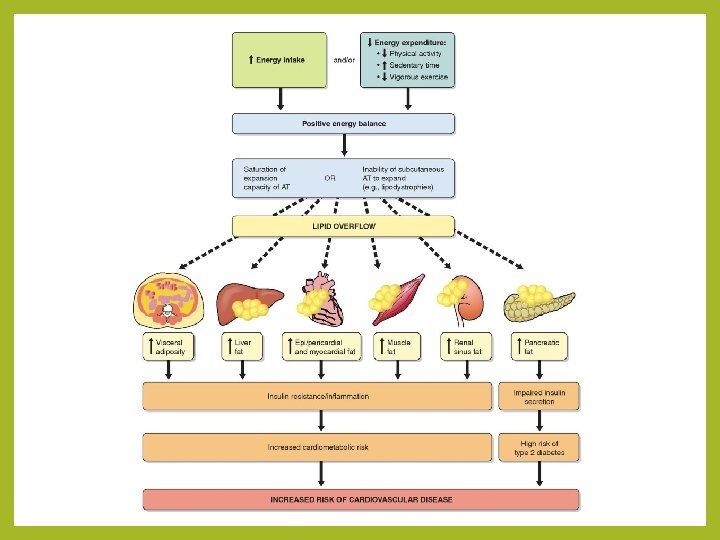

Regulácia príjmu potravy a výdaja energie Príjem potravy je kontrolovaný hypotalamom • Centrum hladu – jeho aktivácia dáva vznik pocitu hladu a podporuje príjem • Centrum sýtosti – jeho aktivácia dáva vznik pocitu sýtosti, a potláča príjem potravy Arcuate nucleus v hypotalame • Obsahuje dve populácie neurónov s recipročnou aktivitou, ktoré regulujú príjem potravy • Neuróny produkujúce NPY – zvyšuje pocit hladu a príjem potravy • Neuróny produkujúce melanokortín – potláčajú apetít a príjem potravy


Regulácia príjmu potravy a výdaja energie • Adipocyty • Produkujú hormón leptin – jeden z najdôležitejších adipokínov, redukuje apetít, pocit hladu a potláča príjem potravy • Inzulín – hormón produkovaný pankreasom, ako odpoveď na vzostup plazmatickej koncentrácie glukózy, ihnibičný účinok na príjem potravy • Ghrelin – hormón hladu, stimuluje chuť do jedla (apetít), je produkovaný bunkami žalúdka pri jeho vyprázdnení, a regulovaný príjmom potravy – po distenzii žalúdka sa jeho produkcia zníži , stimuluje hypotalamické NPY produkujúce neuróny

Regulácia príjmu potravy a výdaja energie • PYY – produkovaný tenkým a hrubým črevom, na najnižšie hodnoty klesá pred jedlom, jeho hladina stúpa po jedle a signalizuje nasýtenie, predpokladá sa, že je dôležitým faktorom v regulácii pravidelnosti príjmu potravy • Laterálny hypotalamus – produkuje orexín – silný stimulant príjmu potravy • Paraventrikulárne potravy jadrá – produkcia neuropeptidov, ktoré znižujú príjem

Regulácia príjmu potravy a výdaja energie • NTS – nucleus tractus solitarii v mozgovom kmeni • Slúži ako centrum sýtosti • Hrá dôležitú úlohu v krátkodobej regulácii príjmu potravy od jedla po jedlo • Psychologické a environmentálne faktory tiež ovplyvňujú príjem potravy a niekedy sú nadradené autonómnym centrám
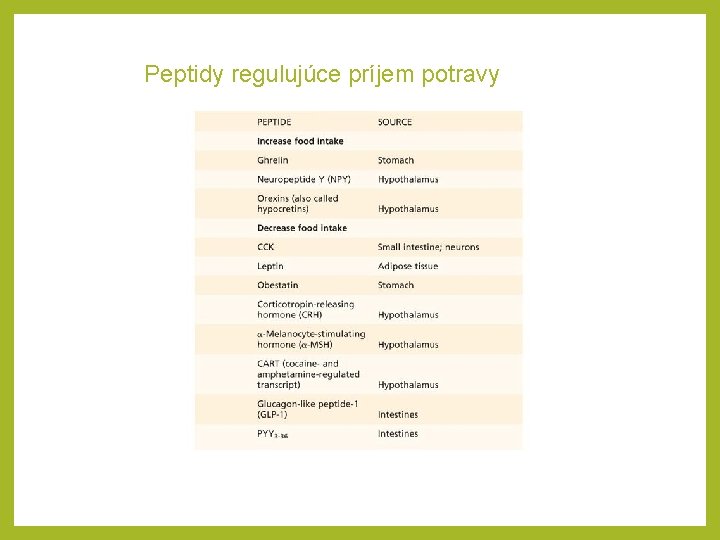
Peptidy regulujúce príjem potravy

Faktory regulujúce príjem potravy vplyvom na CNS


Dve teórie regulácie príjmu potravy • Glukostatická teória – teória predpokladá, že hladina glukózy v krvi kotroluje príjem potravy, pocit hladu a sýtosti • Lipostatická teória – teória predpokladá, že množstvo telesného tuku reguluje pocit hladu, sýtosti a príjem potravy, novšie objavy, hlavne leptín a NPY, podporuje túto hypotézu • Krátkodobá regulácia – zameriava sa primárne na prevenciu prejedania sa pri každom jedle • Dlhodobá regulácia – zameriava sa primárne na udržanie rovnakého množstva zásob energie (tuku) v tele


leptín • peptid (167 AMK) • kódovaný ob génom (7. chromozóm) charakter hormónu – tvorí sa v tukovom tkanive, vylučuje sa v pulzoch, krvou transportovaný do hypotalamu Pri dostatočných zásobch tuku – leptín ihibuje príjem potravy wviaže sa na receptory A a B v hypotalame wriadi tvorbu CCK a NPY, navodzuje pocit sýtosti, reguluje metabolizmus znižuje príjem potravy a zvyšuje energetický výdaj • Leptínová rezistenica !
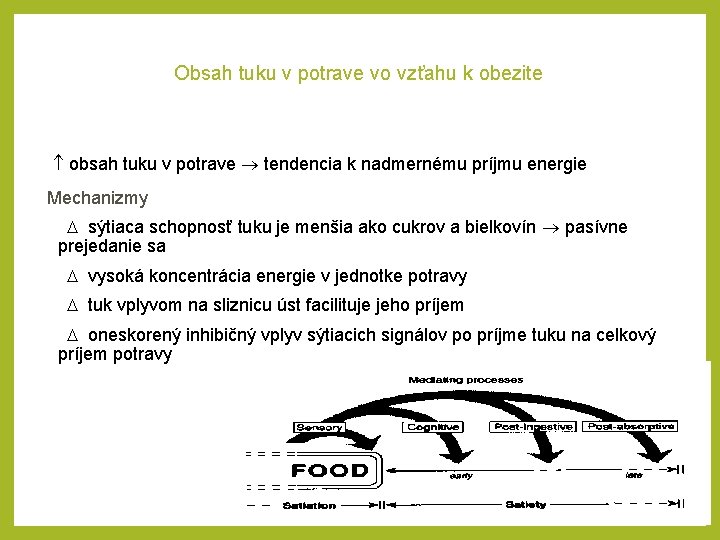
Obsah tuku v potrave vo vzťahu k obezite obsah tuku v potrave tendencia k nadmernému príjmu energie Mechanizmy sýtiaca schopnosť tuku je menšia ako cukrov a bielkovín pasívne prejedanie sa vysoká koncentrácia energie v jednotke potravy tuk vplyvom na sliznicu úst facilituje jeho príjem oneskorený inhibičný vplyv sýtiacich signálov po príjme tuku na celkový príjem potravy

Tukový paradox Tukom indukované signály sýtosti vs nadmerný príjem tuku Tuk v tenkom čreve silný pre absorbčný signál sýtosti mediovaný: najmä CCK, ale aj glukagónom, bombezínom, SST enterostatínom (pentapeptid z pro kolipázy) produktmi trávenia tuku Tuk vstup do TČ s časovým posunom je zriedený inými nutrientami Výsledok: menej intenzívne a oneskorené signály sýtenia Tuk v ústach stimulácia chuťových pohárikov facilitácia jeho príjmu, prirodzený sýtiaci mechanizmus tuku je prekonaný energie v tuku príjem množstva energie, kým sa uplatnia sýtiace signály z tráveného tuku denzita

Krátkodobá vs dlhodobá redukcia hmotnosti Množstvo tuku v tele je homeostaticky regulované Dôsledok: redukcia masy tuku aktivácia kompenzačných mechanizmov obnovenie pôvodného stavu Je teda možné znížiť obsah tuku v organizme aj keď je regulovaný?

Krátkodobá vs dlhodobá redukcia hmotnosti Masa tuku, ktorá je „chránená“ sa môže meniť, teda nemožno hovoriť o nemennom „set pointe“ pre zásoby tuku v organizme Jej veľkosť sa môže zvýšiť vplyvom napr. Vnútorných faktorov: zmien emočného stavu úrovne BMR Vonkajších faktorov: chuti a dostupnosti potravy vysokého obsahu tuku Jej veľkosť sa môže znížiť vplyvom napr. Príjmom nízko tukovej diéty ad libitum Zvýšením fyzickej aktivity a jej dlhodobým udržaním

Viscerálna obezita Silná väzba medzi viscerálnou obezitou a vznikom metabolických komplikácií Príklad: 2 skupiny obéznych s rovnakým BMI 1. sk – tuk v podkoží na bruchu a hrudníku 2. sk – tuk v brušnej dutine Rozdielne metabolické parametre ! 2. Sk mala vyššie hodnoty PGTT, a vyššie hodnoty TAG v plazme Zväčšenie množstva viscerálneho tuku vedie, nezávisle na veľkosti BMI, k zníženiu citlivosti na inzulín !! hladina VMK v krvi inzulínová rezistencia dyslipidémia TAG, koncentrácie nízkodenzitných LDL, koncentrácie HDL cholesterolu, predispozícia k ateroskleróze, riziko NCMP, AIM, iných KV chorôb

Mechanizmy vzniku viscerálnej obezity Starnutie Hormóny Nepriame dôkazy: menej častý výskyt VO u premenopauzálnych žien ako u mužov predpokladá sa, že estrogény stimulujú ukladanie tuku v gluteo femorálnej oblasti progestagény „súťažia“ s glukokortikoidmi o väzbu na glukokortikoidové receptory spomalenie akumulácie tuku vo viscerálnej oblasti Viscerálny tuk – vysoká lipolytická aktivita VMK a glycerolu v krvi (vplyvom adrenergnej aktivity)
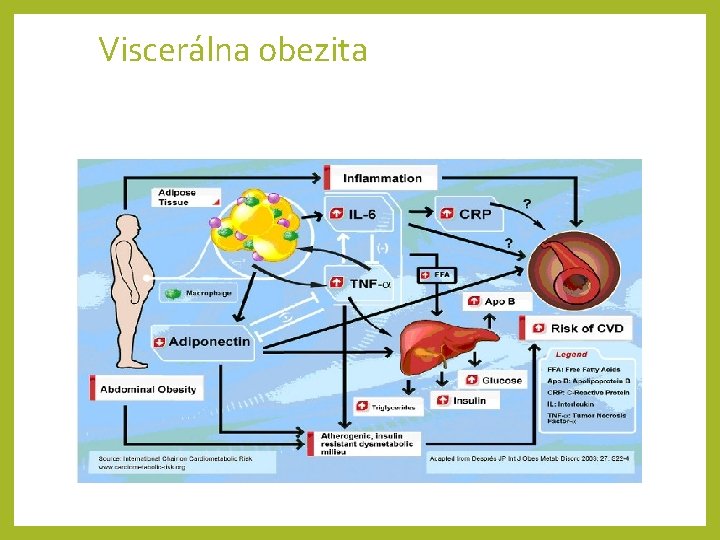
Viscerálna obezita

Poruchy metabolizmu lipidov A. Význam lipidov v organizme 1. zdroj a zásoba energie 2. stavba buniek, tkanív a orgánov 3. súčasť funkčných molekúl B. Základné typy porúch 1. Hyperlipoproteinémia 2. Hypolipoproteinémia

Liporoteíny (LP) guľovité útvary transportujúce nepolárne lipidy krvou Zloženie a vlastnosti: vo vnútri guľovej častice sú nepolárne lipidy povrch tvoria polárne molekuly umožňujúce transport v plazme fosfolipidy, neesterifikovaný cholesterol, apolipoproteíny (apo) – sú dôležité pre metabolizovanie LP jednotlivé typy LP sa líšia hustotou, veľkosťou, objemom prenášaných lipidov, množstvom a typom apo, miestom vzniku, metabolizmom a ďalšími parametrami

• Chylomikróny (CM) – sú najväčšie LP a majú najnižšiu hustotu • VLDL – sú menšie ako CM a sú hustejšie – prenášajú najmä endogénne triacylglyceroly (TAG) syntetizované v pečeni • IDL – (intermediate – density LP) • LDL – obsahujú hlavne estery cholesterolu a jediný apo (B 100) • HDL – majú najmenšiu veľkosť a najvyššiu hustotu zo všetkých LP ( reverzný transport cholesterolu) • Lipoproteín (a) – lipoproteínová častica, je súčasťou LDL molekuly, má na seba naviazanú molekulu podobnú plazminogénu Je významným rizikovým faktorom aterosklerózy

Enzýmy dôležité v metabolizme LP • Lipoproteínová lipáza (LPL) uvoľňuje MK z TAG v CM a VLDL nachádza sa v endotelových bb. aktivuje ju Apo C II (ten sa nachádza v CM aj VLDL) • Pečeňová lipáza hydrolyzuje TAG v pečeni k jej aktivácií prispieva interakcia s apo E • LCAT = lecitín : cholesterol acyl transferáza • CETP = cholesterol ester transfer proteín

• LDL receptor – vychytáva LDL (IDL), je lokalizovaný na bunkách v mnohých tkanivách, najmä hepatocytoch ! U predisponovaných jedincov: príjem cholesterolu down regulácia LDLr v pečeni a tým zníženie vychytávanie LDL • HDL receptor – odstraňovanie HDL z plazmy lokalizácia najmä v tkanivách so steroidogenézou (kôra nadobličiek, ovária tropné hormóny stimulujú jeho tvorbu) • Scavenger receptory (SR) - vychytávanie LDL, ktoré neboli zachytené LDL receptormi významne sa podieľajú na vychytávaní oxidovaných LDL častíc sú prítomné najmä v makrofágoch, v bunkách hladkých svalov ciev aterogenéza

Hyperlipoproteinémie patologický proces charakterizovaný zvýšením koncentrácie jedného alebo viacerých typov lipoproteínov v plazme • Hyperlipidémia koncentrácia lipidov ( obyčajne TAG + CH) v plazme • Dyslipoproteinémia (dyslipidémia) porucha zastúpenia jednotlivých typov LP, obyčajne so zníženou hodnotou HDL cholesterolu

a) Hypercholesterolémie zvýšenie koncentrácie cholesterolu v krvi • 75 % cholesterolu krvi tvorí LDL cholesterol • LDL cholesterol je aterogénny • aterogenita LDL cholesterolu so stupňom jeho oxidácie a glykácie • oxidovaný a glykovaný LDL cholesterol je vychytávaný SC receptormi na makrofágoch a bunkách hladkých svalov tvorba penových buniek b) Hypertriacylglycerolémia c) Kombinácia a a b

KLASIFIKÁCIA HYPERLIPOPROTEINÉMIÍ (Nečas a spol. , 2000) Typ lipoproteínu - druh lipid - druh 1 CM TAG 2 a LDL cholesterol 2 b LDL, VLDL cholesterol, TAG 3 IDL, CM zostatky TAG, cholesterol 4 VLDL TAG 5 VLDL, CM TAG, cholesterol CM = chylomikróny

Hlavné druhy hyperlipoproteinémií (HLP) A. Primárne 1. Familiárna kombinovaná HLP • je najčastejšou geneticky podmienenou HLP (autozomálne dominantne dedičná – ADD) • prejavuje sa fenotypmi 2 a, 2 b alebo 4, zriedkavo 5 • býva sprievodným znakom metabolického sy X • riziko vzniku aterosklerózy a ICHS 2. Familiárna hypercholesterolémia (ADD) Podstata : mutácia LDL receptora • prejavuje sa najčastejšie fenotypom 2 a • výrazná akcelerácia vývoja aterosklerózy • výskyt IM už vo 4. dekáde života! • nápadná je šlachová xantomatóza a arcus lipoides corneae

3. Polygénová hypercholesterolémia najčastejšia hypercholesterolémia ( typ 2 a ) Mechanizmus vzniku: • genetická predispozícia zmena resorbcie a endogénnej syntézy cholesterolu, zmena metabolizmu LDL a iné mechanizmy • vonkajšie faktory – alkohol, diabetes, príjem glycidov, tukov • Na rozdiel od familiárnej hypercholesterolémie (heterozygótov) nie sú prítomné xantómy a v rodine je nižší výskyt hypercholesterolémie u príbuzných v 1. línii. 4. Familiárna dyslipoproteinémia polygénová porucha • prejavuje sa fenotypom 3 HLP • výrazná xantomatóza a akcelerácia aterosklerózy

5. Familiárna hypertriacyglycerolémia autozomálna dedičná porucha • častá porucha podobná kombinovanej HLP • prejavuje sa obyčajne fenotypom 4 HLP • nebýva zvýšená koncentrácia sérového cholesterolu • na jej manifestácií sa podieľajú aj vonkajšie faktory 6. Familiárny defekt lipoproteínovej lipázy (LPL) a apo C II • vzácna AR dedičná poruchu • homozygótna forma ukladanie TAG v tkanivách: xantómy, hepatosplenomegália a vysoké riziko ak. pankreatitídy • prejavuje sa fenotypom 1 (defekt LPL) alebo 5 (defekt apo CII ) 7. Familiárna hyperalfaliporoteinémia • HDL mierne riziko vzniku aterosklerózy • malé dávky alkoholu HDL • estrogény HDL

B. Sekundárne Sú podmienené prítomnosťou iného základného ochorenia Najčastejšie choroby sprevádzané HLP: • diabetes mellitus • nefrotický sy, chronické zlyhávanie obličiek • hypotyreóza • primárna biliárna cirhóza • alkoholizmus (! nezamieňať s požívaním malých dávok alkoholu ! ) Na vzniku sekundárnej HLP sa môžu podieľať aj lieky, napr. perorálne kontraceptíva


Hypolipoproteinémie Sú to zriedkavé dedične podmienené poruchy (ARP) Príklady: Familiárna abetalipoproteinémia – defekt v syntéze apoproteínu chýbanie lipoproteínov: CM, VLDL, znížená koncentrácia cholesterolu v sére, TAG v sére Prejavy: • porucha resorbcie tukov v GIT e • porucha funkcie a štruktúry nervového systému Tangierska choroba – chýba HDL v plazme neuropatia, nie je akcelerácia aterosklerózy ! • ukladanie esterov cholesterolu vo fagocytoch ( veľké oranžové mandle )

Ďalšie poruchy metabolizmu lipidov • patria sem dôsledky genetických enzymopatií • poruchy metabolizmu lipidov lipidózy • ukladanie lipidov v orgánoch ( tezaurizmózy ) Typy lipidóz a) Niemanova – Pickova choroba – sfingomyelinóza: akumulácia sfingomyelínu v makrofágoch pečene, sleziny, lymfatických uzlín. Dôsledok: závažné poškodenie nervového systému b) Gaucherova choroba – cerebrozidóza, cerebrozidolipidóza • hromadenie glukocerebrozidu Dôsledok: závažná retardácia vývoja v skorom dojčenskom veku s poškodením NS

Poruchy metabolizmu bielkovín a aminokyselín 1. Poruchy dusíkovej bilancie a) Pozitívna dusíková bilancia – rast, rekonvalescencia, tehotenstvo, športovci, manuálne pracujúci b) Negatívna dusíková bilancia – katabolické procesy ( rakovina, horúčka, poruchy výživy. . ) 2. Poruchy proteínového zloženia krvi a) tvorba monoklonálnych imunoglobulínov • Waldenströmova makroglobulinémia hyperviskozita krvi Mechanizmus vzniku: tvorba Ig. M

• Mnohopočetný myelóm hyperviskozita krvi Mechanizmus vzniku: tvorba Ig. A b) tvorba kryoglobulínov poruchy mikrocirkulácie Mechanizmus vzniku porúch mikrocirkulácie: precipitácia kryoglobulínov pri znížení teploty. c) hyperfibrinogenémia, kryofibirinogenémia fibrinogén je pri reaktívnych stavoch organizmu d) hypoalbuminémia nedostatočná tvorba alb. v pečeni, alebo zvýšené straty obličkami pri nefrotickom syndróme – dôsledkom je zníženie onkotického tlaku krvi – porušenie Starlingových mechanizmov –vznik edému

Poruchy metabolizmu aminokyselín (AMK) a) Fenylketonúria – ARP Phe = esenciálna AMK, mení sa na Tyr enzýmom Phe hydroxylázou Mechanizmus vzniku: mutácia fenylalanínhydroxylázy Dôsledok: • akmulácia fenylalanínu vznik jeho abnormálnych metabolitov: fenylpyruvát, fenylacetát • závažné poškodenie nervového systému • hypopigmentácia: v dôsledku inhibičného vplyvu fenylalanínu na tvorbu melanínu • ekzém m. ú. zvýšených hladím Phe, alebo jeho metabolitov nie je presne známy

b) Albinizmus – alebo absenccia melanínu v koži, v kožných adnexách, v oku Mechanizmus vzniku: defekt enzýmu tyrozinázy, ktorý normálne premieňa Tyr na DOPA Normálne: tyrozín v melanocytoch Prejavy: • okulokutánny albinizmus (najčastejšie) • senzitivita kože na UV žiarenie bazoceluárne karcinómy • hypopigmentácia kože • svetloplachosť a porucha zraku

c) Alkaptonúria (ochronóza) ARP Mechanizmus vzniku: defekt oxidázy kyseliny homogentisovej (vzniká pri metabolizme fenylalanínu, resp. tyrozínu) Dôsledky: • hromadenie hnedočerveného (niekedy až modročierneho) pigmentu v spojivovom tkanive (ochronóza) • poškodenie kĺbových chrupaviek artróza • poškodenie srdcových chlopní chlopňové chyby • vylučovanie pigmentu močom, potom • zafarbenie ušníc a sklér H Č; M Č

d) Homocystinúria Mechanizmus vzniku: porušený metabolizmus AMK obsahujúcich síru ( cystein, metionin ) typ I homocysteinúrie je spôsobený defektným enzýmom cystationsyntáza ( jeho kofaktorom je vitamín B 6 – pyridoxín) • koncentrácia homocysteínu v krvi • poškodenie zraku • cievne komplikácie (akcelerovaná ateroskleróza, trombóza) typ II homocystinúrie • je spôsobený defektnou resyntézou metionínu z homocysteínu. Na resyntéze sa normálne podieľa kyselina listová a vitamín B 12 Homocysteín – poškodzuje cievny endotel !!!!

Poruchy metabolizmu purínov a pyrimidínov Heterocyklické zlúčeniny, súčasť NK a nukleotidov Poruchy ich metabolizmu sa manifestujú ako hyperurikémia a dna Hyperurikémia – zvýšená hladina k. močovej koncový produkt premeny purínov v organizme, na jej hladine v plazme participuje príjem potravou a endogénna tvorba Normálna hladina k. močovej je do 340 mol/l u žien, do 420 mol/l u mužov 1. primárna: príčina nie je jednoznačne známa 2. sekundárna: jej príčinou sú známe chorobné procesy (katabolizmus NK, napr. pri cytostatickej terapii nádorov; vylučovanie kyseliny močovej pri zlyhaní obličiek).
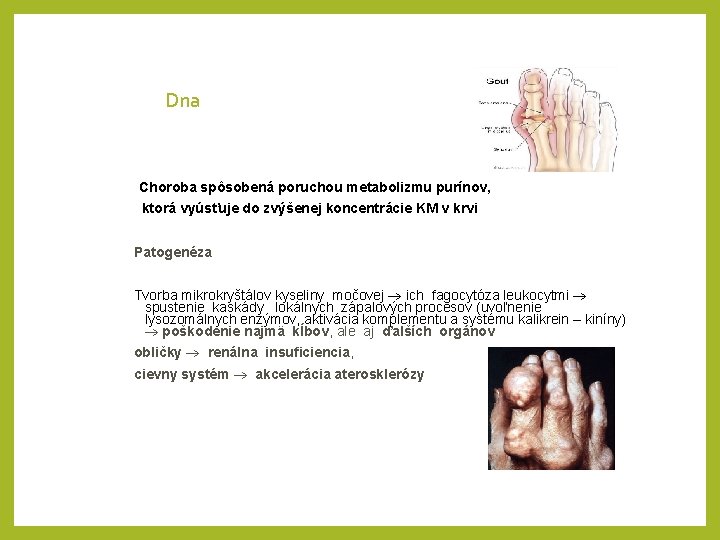
Dna Choroba spôsobená poruchou metabolizmu purínov, ktorá vyúsťuje do zvýšenej koncentrácie KM v krvi Patogenéza Tvorba mikrokryštálov kyseliny močovej ich fagocytóza leukocytmi spustenie kaskády lokálnych zápalových procesov (uvoľnenie lysozomálnych enzýmov, aktivácia komplementu a systému kalikrein – kiníny) poškodenie najmä kĺbov, ale aj ďalších orgánov obličky renálna insuficiencia, cievny systém akcelerácia aterosklerózy

Poruchy metabolizmu porfyrínov Porfyríny – prekurzory biosyntézy hemu • hemoglobín, myoglobín – väzba a prenos 02 • cytochrómy – vznik energie v bunkách pri prenose elektrónu v dýchacom reťazci v mitochondriách • cytochróm P- 450 – hydroxylácia, detoxikácia • kataláza, peroxidáza – metabolizmus kyslíkových zlúčenín • syntéza NO

Poruchy metabolizmu porfyrínov Normálny metabolizmu porfyrínov a) prekurzorom je k. delta aminolevulová a jej syntáza je prvým kľúčovým enzýmom v tejto metabolickej ceste b) táto sa ďalej mení cez porfirinogény (URO, KOPRO a PROTO) na finálny produkt c) posledným enzýmom je ferochelatáza, ktorá zabuduje do molekuly atóm kovu Typy porfyrínov: - uroporfyríny - koproporfyrín III - protoporfyrín hem


Porfýrie – choroby spôsobené porušenou syntézou hemu a z toho vyplývajúcim hromadením porfyrínov v organizme Klasifikácia a) hepatálne b) erytropoetické Základné príčiny vzniku a) zdedené (genetické) b) získané Mechanizmy vzniku: mutácia a následná dysfunkcia niektorého z 8 enzýmov potrebných pre syntézu hemu

Akútne porfýrie Akútna intermitentná porfýria Charakteristika AIP: je najčastješie, nie je fotosenzitivita! Prejavy: vyvolané hromadením prekurzorov porfyrínov, k. delta – amínolevulovej, porfobilinogénu a hemoproteinov v nervových bunkách, syntézou falošných neurotransmiterov, porucha syntézy NO akútna brušná príhoda parézy psychické poruchy zmeny vnútorného prostredia ( hyponatrémia, hypochlorémia) systémová hypertenzia Faktory provokujúce vznik AIP: pohlavné hormóny ( výskyt u žien vo fertilnom veku, ATK), stres, hladovanie, horúčka

Chronické porfýrie Porphyria cutanea tarda (PCT)- najčastejšia CHP u nás Charakteristika PCT: fotosenzitivita ! vznik pľuzgierov na koži vystavenej slnku Mechanizmy vzniku fotosenzitivity: • porfyríny (na rozdiel od porfyrínogénov) obsahujú systém konjugovaných dvojitých väzieb vznik kyslíkových radikálov poškodenie štruktúry buniek vznik pľuzgierov Získané porfýrie: pri expozícii polychlorovaným uhľovodíkom, griseofulvínu, olovu
- Slides: 78