PON C 1 Lequilibrio chimico Acidi e basi

PON C 1 L’equilibrio chimico Acidi e basi Esperto prof. C. Formica Immagini e testi tratti dai website di: genome. wellcome. ac. uk, dnaftb. org, unipv. it, unimi. it, wikipedia. it, unibs. it, unisi. it, unina. it, uniroma 2. it, nih. gov, zanichelli. it, sciencemag. org, ncbi. gov

Acidi e basi secondo Brønsted–Lowry acido = donatore di protoni base = accettore di protoni acidi: HCl, HNO 3, H 2 O, NH 4+, HS-, HSO 4 -, HCN, Al(H 2 O)63+, etc. basi: H 2 O, OH-, HS-, NH 3, Cl-, O 2 -, SO 42 -, CN- etc. Le sostanze che possono comportarsi come acidi e come basi, a seconda dell'ambiente in cui si trovano (H 2 O, HS-, HSO 4 -, etc. ) sono dette anfiprotiche. La classificazione è valida anche per sistemi non acquosi. Acidi e basi secondo Lewis acido = accettore di una coppia di elettroni (H 3 O+ Fe 3+, Ag+, Al. Cl 3) base = donatore di una coppia di elettroni non impegnati in legami chimici (OH-, CN-, Cl- NH 3, H 2 O. . . ) 2
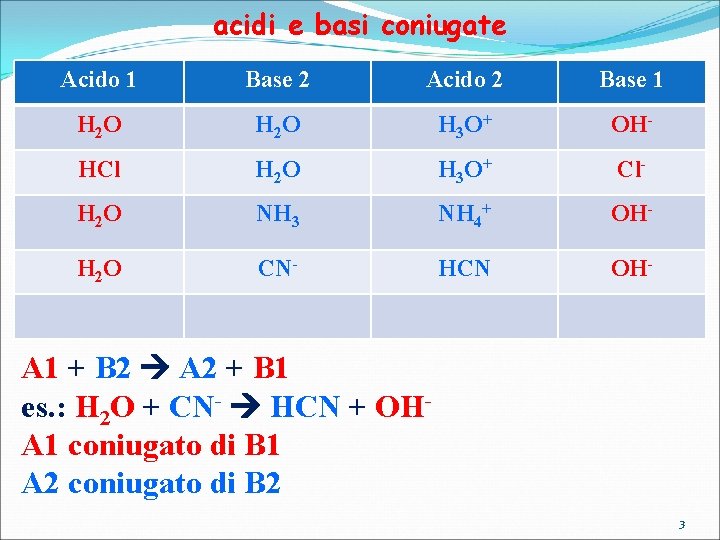
acidi e basi coniugate Acido 1 Base 2 Acido 2 Base 1 H 2 O H 3 O+ OH- HCl H 2 O H 3 O+ Cl- H 2 O NH 3 NH 4+ OH- H 2 O CN- HCN OH- A 1 + B 2 A 2 + B 1 es. : H 2 O + CN- HCN + OHA 1 coniugato di B 1 A 2 coniugato di B 2 3
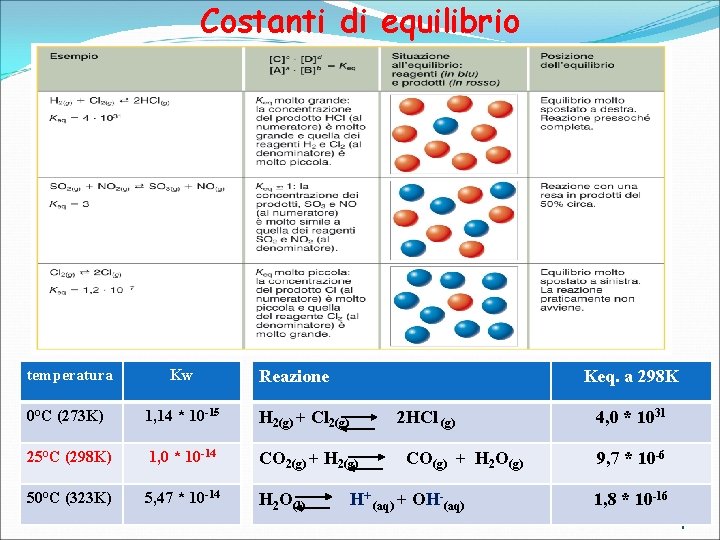
Costanti di equilibrio temperatura Kw 0°C (273 K) 1, 14 * 10 -15 H 2(g) + Cl 2(g) 25°C (298 K) 1, 0 * 10 -14 CO 2(g) + H 2(g) 50°C (323 K) 5, 47 * 10 -14 H 2 O(l) Reazione Keq. a 298 K 2 HCl (g) CO(g) + H 2 O(g) H+ (aq) + OH-(aq) 4, 0 * 1031 9, 7 * 10 -6 1, 8 * 10 -16 4
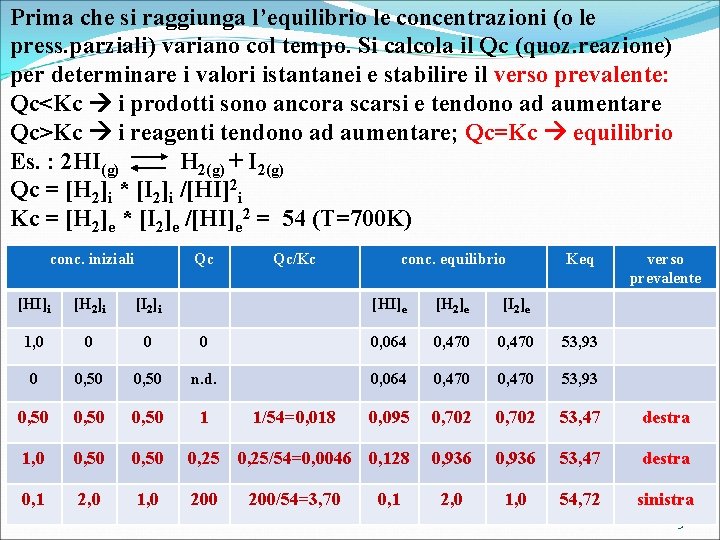
Prima che si raggiunga l’equilibrio le concentrazioni (o le press. parziali) variano col tempo. Si calcola il Qc (quoz. reazione) per determinare i valori istantanei e stabilire il verso prevalente: Qc<Kc i prodotti sono ancora scarsi e tendono ad aumentare Qc>Kc i reagenti tendono ad aumentare; Qc=Kc equilibrio Es. : 2 HI(g) H 2(g) + I 2(g) Qc = [H 2]i * [I 2]i /[HI]2 i Kc = [H 2]e * [I 2]e /[HI]e 2 = 54 (T=700 K) conc. iniziali Qc [HI]i [H 2]i [I 2]i 1, 0 0 0, 50 Qc/Kc conc. equilibrio Keq verso prevalente [HI]e [H 2]e [I 2]e 0 0, 064 0, 470 53, 93 0, 50 n. d. 0, 064 0, 470 53, 93 0, 50 1 0, 095 0, 702 53, 47 destra 1, 0 0, 50 0, 25/54=0, 0046 0, 128 0, 936 53, 47 destra 0, 1 2, 0 1, 0 200 2, 0 1, 0 54, 72 sinistra 1/54=0, 018 200/54=3, 70 0, 1 5
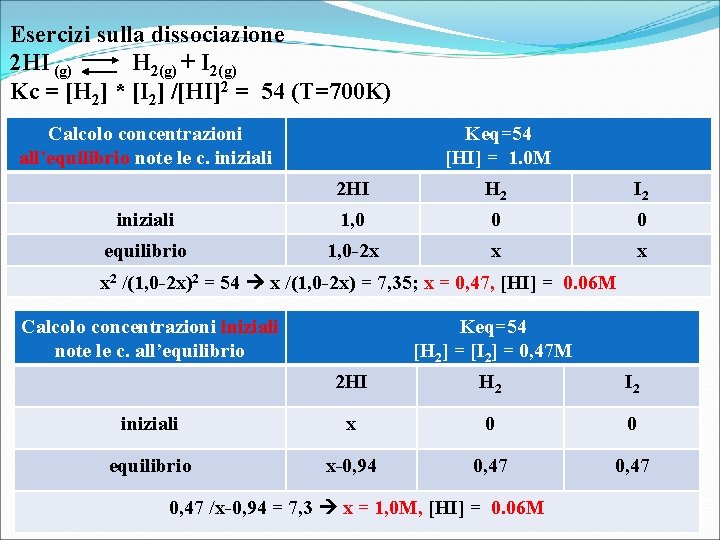
Esercizi sulla dissociazione 2 HI (g) H 2(g) + I 2(g) Kc = [H 2] * [I 2] /[HI]2 = 54 (T=700 K) Calcolo concentrazioni all’equilibrio note le c. iniziali Keq=54 [HI] = 1. 0 M 2 HI H 2 I 2 iniziali 1, 0 0 0 equilibrio 1, 0 -2 x x 2 /(1, 0 -2 x)2 = 54 x /(1, 0 -2 x) = 7, 35; x = 0, 47, [HI] = 0. 06 M Calcolo concentrazioni iniziali note le c. all’equilibrio Keq=54 [H 2] = [I 2] = 0, 47 M 2 HI H 2 I 2 iniziali x 0 0 equilibrio x-0, 94 0, 47 /x-0, 94 = 7, 3 x = 1, 0 M, [HI] = 0. 06 M 6

Keq e temperatura Nelle reazioni esotermiche la Keq diminuisce all’aumentare della temperatura In quelle endotermiche Keq aumenta all’aumento di T. Es. : N 2 O 4 (g) 2 NO 2 (g) Keq=[NO 2]2 e/[N 2 O 4]e reaz. endotermica spostata a ds ad alta T aumento Keq T Keq 273 0, 59*10 -3 298 4, 5*10 -3 373 260*10 -3 All’aumento di T: Keq aumenta con ∆H>0 -endotermiche Keq diminuisce con ∆H<0 -esotermiche ∆H reazione = +57, 2 J endotermica ∆ H (entalpia): calore scambiato a pressione costante 7

Principio di Le Châtelier (equilibrio mobile) Il sistema reagisce in modo da compensare i cambiamenti. Es. in un sistema in fase gassosa all’equilibrio, l’aumento di pressione comporta lo spostamento dell’equilibrio nella direzione in cui è presente il minor numero di moli. Es. : N 2 O 4 (g) 2 NO 2 (g) si sposta a destra se diminuisce la P, a sn se P aumenta. 8
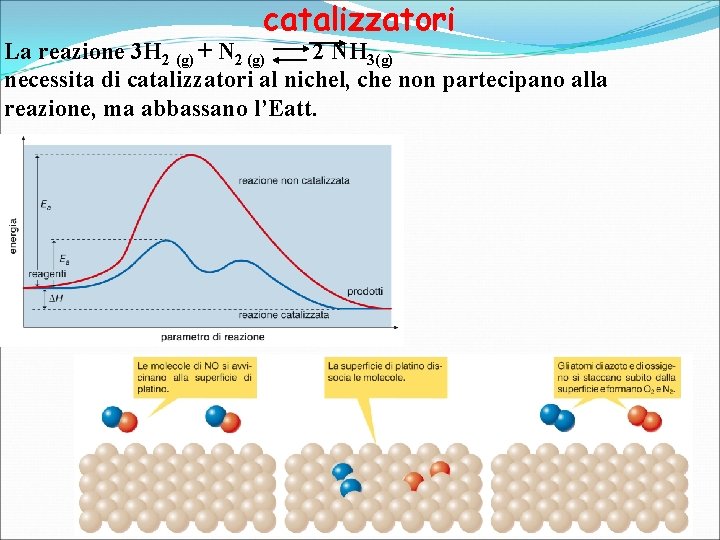
catalizzatori La reazione 3 H 2 (g) + N 2 (g) 2 NH 3(g) necessita di catalizzatori al nichel, che non partecipano alla reazione, ma abbassano l’Eatt. 9

Soluzioni acquose ed elettroliti Nell’interazione acqua-soluti si distinguono: composti molecolari es. saccarosio l’acqua rompe i legami deboli tra le molecole neutre, che si disperdono composti polari HCl l’acqua (dipolo δ+, δ-) rompe i legami covalenti polari tra H e Cl e determina la rottura delle molecole: HCl (aq) ⇆ H+ (aq) e Cl- (aq), ionizzazione HCl (g) + H 2 O(l) ⇆ H 3 O+ (aq) + Cl- (aq) composti ionici Na. Cl l’acqua rompe il reticolo cristallino, interferisce col legame ionico tra Na e Cl e determina la separazione in cationi e anioni: Na. Cl (s) ⇆ Na+ (aq) e Cl- (aq), dissociazione ionica 10

Calcolo p. H acidi forti (HCl, HCl. O 4 , HNO 3) HCl (aq) ⇆ H+ (aq) + Cl- (aq) HCl. O 4 ⇆ H+ (aq) + Cl. O 4 - (aq), p. H = -log [H+] , p. OH = -log [OH-], p. H + p. OH = 14 es. sol. 0, 1 M HCl p. H = -log [H+] = -log 0, 1 = 1 concentrazioni calcolo p. H [HCl] [H+] [Cl-] iniziali 0, 1 0 0 equilibrio 0 0, 1 iniziali 0, 01 0 0 equilibrio 0 0, 01 p. H = -log [H+] = -log 0, 1 = 1 p. H = -log [H+] = -log 0, 01 = 2 HCl. O 4 ⇆ H+ (aq) + Cl. O 4 - (aq) sol. 0, 862 M p. H = 0, 062 11
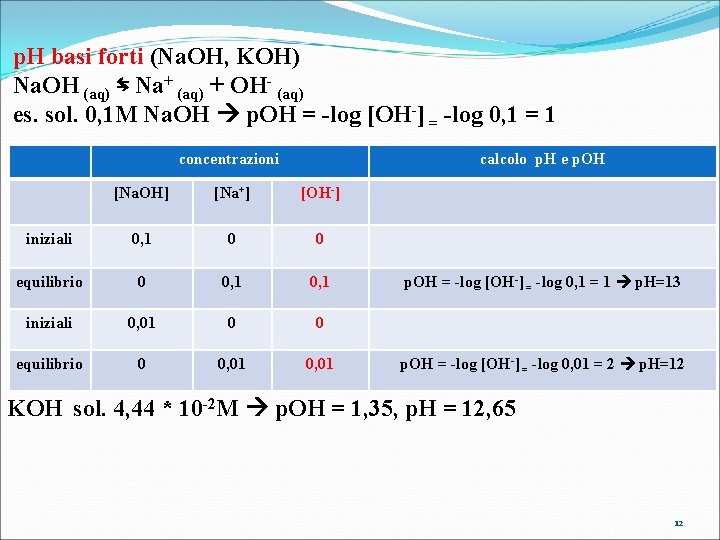
p. H basi forti (Na. OH, KOH) Na. OH (aq) ⇆ Na+ (aq) + OH- (aq) es. sol. 0, 1 M Na. OH p. OH = -log [OH-] = -log 0, 1 = 1 concentrazioni calcolo p. H e p. OH [Na. OH] [Na+] [OH-] iniziali 0, 1 0 0 equilibrio 0 0, 1 iniziali 0, 01 0 0 equilibrio 0 0, 01 p. OH = -log [OH-] = -log 0, 1 = 1 p. H=13 p. OH = -log [OH-] = -log 0, 01 = 2 p. H=12 KOH sol. 4, 44 * 10 -2 M p. OH = 1, 35, p. H = 12, 65 12

p. H acidi deboli (CH 3 COOH, H 2 CO 3) a- CH 3 COOH (aq) + H 2 O(l) ⇆ CH 3 COO- (aq) + H 3 O+ (aq) es. sol. Ca=0, 1 M CH 3 COOH , Ka=1, 8* 10 -5 , 1, 8* 10 -5 = x 2 /0, 1 -x Si può trascurare il –x se: Ka/Kb ≤ 10 -5 Ca≥ 10 -2 x≈ √ 1, 8* 10 -5 *0, 1 = 1, 34 * 10 -3 p. H = -log [H+] = -log 1, 34 * 10 -3 ≈ 2, 87 b- H 2 CO 3 (aq) + H 2 O(l) ⇆ HCO 3 - (aq) + H 3 O+ (aq) es. sol. satura di CO 2 con [H 3 O+]=1, 3* 10 -4 p. H = -log 1, 3 * 10 -4 ≈ 3, 89 concentrazioni [CH 3 COOH] [CH 3 COO+] p. H [H+] iniziali 0, 1 0 0 equilibrio 0, 1 -x x x 2. 87 13
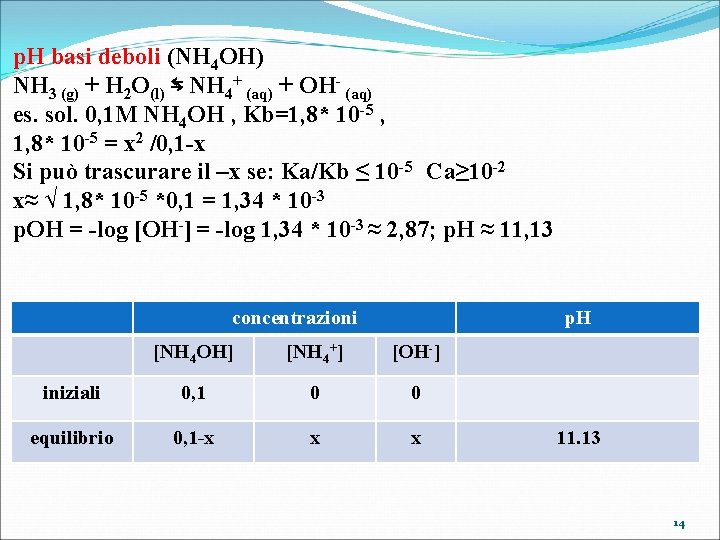
p. H basi deboli (NH 4 OH) NH 3 (g) + H 2 O(l) ⇆ NH 4+ (aq) + OH- (aq) es. sol. 0, 1 M NH 4 OH , Kb=1, 8* 10 -5 , 1, 8* 10 -5 = x 2 /0, 1 -x Si può trascurare il –x se: Ka/Kb ≤ 10 -5 Ca≥ 10 -2 x≈ √ 1, 8* 10 -5 *0, 1 = 1, 34 * 10 -3 p. OH = -log [OH-] = -log 1, 34 * 10 -3 ≈ 2, 87; p. H ≈ 11, 13 concentrazioni p. H [NH 4 OH] [NH 4+] [OH-] iniziali 0, 1 0 0 equilibrio 0, 1 -x x x 11. 13 14
![dal p. H alla [H+] o [OH-] es. soluzione a p. H 4, 4 dal p. H alla [H+] o [OH-] es. soluzione a p. H 4, 4](http://slidetodoc.com/presentation_image_h2/d89e01ff7208392435fd4b07459ce063/image-15.jpg)
dal p. H alla [H+] o [OH-] es. soluzione a p. H 4, 4 [H+] = 10 -4, 4= 0, 0000398 ≈ 3. 98*10 -5 p. H [H+] [OH-] 1, 0 1. 0*10 -13 3, 0 1. 0*10 -3 1. 0*10 -11 4, 4 10 -4, 4= 0, 0000398 ≈ 3. 98*10 -5 0. 25*10 -9 7, 4 3. 9*10 -8 0. 25*10 -6 9, 2 6, 31 *10 -10 10 -14 /6, 31 *10 -10 = 0, 16 *10 -4 12, 5 3. 16*10 -13 0. 32*10 -1 15

Soluzioni tampone Sono formate da acidi e basi coniugate 1 -un acido debole e un suo sale di base forte es. acido acetico e acetato di sodio CH 3 COOH/CH 3 COONa CH 3 - COOH ⇆ CH 3 COO- + H+ CH 3 - COONa ⇆ CH 3 COO- + Na+ acido coniugato CH 3 COOH, base coniugata CH 3 COO[CH 3 COOH] = Ca (concentrazione acido) [CH 3 COO - ] = Cs (concentrazione sale) p. H = p. Ka + log Cs/Ca (valida se si libera 1 mol anione. Per 2 mol anioni la [CH 3 COO -] = 2 Cs) 2 -una base debole e un suo sale di acido forte es. idrossido di ammonio e cloruro di ammonio NH 3 /NH 4 Cl NH 3 (g) + H 2 O(l) ⇆ NH 4+ (aq) + OH- (aq) NH 4 OH ⇆ NH 4+ + OHNH 4 Cl ⇆ NH 4+ + Cl[NH 4 OH] = Cb (concentrazione base) [NH 4 Cl] = Cs (concentrazione sale) 16 p. H = p. Kb + log Cs/Cb

acido carbonico e carbonato/bicarbonato di sodio H 2 CO 3 ⇆ H+ + HCO 3 - ⇆ H+ + CO 32 Reazione complessiva: H 2 CO 3 ⇆ 2 H+ + CO 32 Na 2 CO 3 ⇆ 2 Na+ + CO 32[H 2 CO 3] = Ca (concentrazione acido) [Na 2 CO 3] = Cs (concentrazione sale) p. H = p. Ka+log Ca/Cs 17

Idrolisi salina Un sale solubile libera in soluzione cationi e anioni, poiché possiede un reticolo ionico. I sali sono elettroliti forti (si completa dissociaz. Kps molto alta) e i loro ioni in acqua, vengono solvatati. acidi coniugati di basi molto forti: Li+, Na+, K+ , basi coniugate di acidi molto forti: Cl-, NO 3 -, Cl. O 4 -, IO 4 restano invariati, perciò non provocano nessuna variazione di p. H. 1 -sale di acido forte e base forte: non avviene idrolisi es. Na. Cl ⇆ Na+ (aq) + Cl- (aq) Molti altri invece, sono una coppia coniugata acido-base: più un acido è forte, più la sua base coniugata è debole (e viceversa). Dopo la solvatazione, possono reagire con molecole di acqua secondo reazioni acido-base idrolisi varia il p. H soluzione. 18

2 -sale di acido debole e base forte: Na 2 CO 3, KCN, KF, CH 3 COONa, Na. HS, es. per il KNO 2: NO 2 - + H 2 O HNO 2 + OHNO 2 - (aq) : base coniugata 1, OH- (aq) base coniugata 2 ( reaz. basica) H 2 O acido coniugato 2, HNO 2 acido coniugato 1 Reagiscono con acqua e rendono la soluzione basica le basi coniugate di acidi deboli: NO 2 - CO 32 - CH 3 COO- SO 323 -sale di acido forte e base debole: NH 4 Cl, NH 4 NO 3, Zn. Cl 2, Al 2(SO 4)3 es. per NH 4 Cl: NH 4+ + H 2 O NH 3 + H 3 O+ NH 4+ (aq): acido coniugato 1, H 3 O+(aq) acido coniugato 2( reaz. acida) H 2 O base coniugata 2, NH 3 base coniugata 1 Reagiscono con acqua e rendono la soluzione acida le basi coniugate di basi deboli: es. NH 3 Ki = Kw/Ka 4 -sale di acido debole e base debole: (NH 4)2 CO 3 reaz. acida o basica 19

Equilibri eterogenei: solubilità (s) e Kps Ca. F 2⇆ 1 Ca 2+ + 2 FKps = [Ca 2+]. [F-]2 = 1, 7*10 -10 [Ca. F 2] = [F-]/2 = [Ca 2+]/1 [F-] = 2[Ca 2+] Ca 2+ = s F- = 2 Ca 2+ = 2 s Kps = s * (2 s)2 = 4 s 3 = 1, 7*10 -10 s = 3√ 1, 7*10 -10 = 1, 7*10 -10 /4 = 3, 5*10 -4 M 20

solubilità e ione in comune tra 2 sali Ag. Cl ⇆ Ag+ + Cl. Kps = [Ag+]. [Cl-] = 1, 6*10 -10 s = [Ag+] = [Cl-] = 1, 265*10 -5 se si aggiunge Na. Cl =10 -2 M [Ag+] = 1, 6*10 -10 /10 -2 = 1, 6*10 -8 se si aggiunge Ag. NO 3 = 0, 1 M [Ag+] = 1, 6*10 -10 /10 -1 = 1, 6*10 -9 (si tratta di valori approssimati, da calcoli semplificati) Calcolare la solubilità del Pb. F 2 in una soluzione 0, 3 M in Na. F. Kps=7 · 10– 9 Pb. F 2 ⇆ Pb 2+ + 2 FKps = [Pb 2+]. [F-]2 = 7*10 -9 [Pb 2+] = Kps/[F-]2 = 7*10 -9 /(0, 3)2 = 7, 8*10 -8 21

Titolazione acido-base Si esegue con una buretta graduata e consiste nel determinare la concentrazione di [H+] o di [OH-] mediante l’aggiunta di una base forte titolante a concentrazione nota (buretta) -goccia a goccia- ad una soluzione di acido forte nel quale sia stato immesso un opportuno indicatore. La base fa aumentare il p. H repentinamente fino alla neutralità ed oltre. Il viraggio dell’indicatore segnalerà l’avvenuta neutralizzazione. Il volume e la molarità di titolante utilizzato, insieme al volume di soluzione da titolare, consentirà di ricavare la concentrazione x. 22
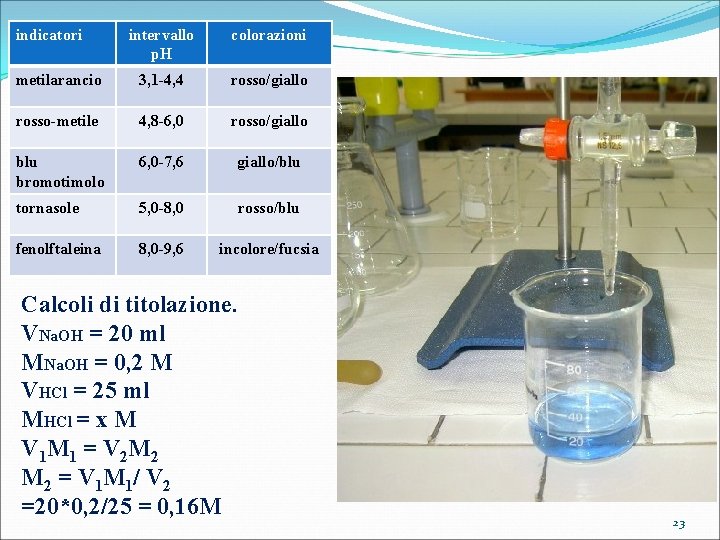
indicatori intervallo p. H colorazioni metilarancio 3, 1 -4, 4 rosso/giallo rosso-metile 4, 8 -6, 0 rosso/giallo blu bromotimolo 6, 0 -7, 6 giallo/blu tornasole 5, 0 -8, 0 rosso/blu fenolftaleina 8, 0 -9, 6 incolore/fucsia Calcoli di titolazione. VNa. OH = 20 ml MNa. OH = 0, 2 M VHCl = 25 ml MHCl = x M V 1 M 1 = V 2 M 2 = V 1 M 1/ V 2 =20*0, 2/25 = 0, 16 M 23

Proprietà colligative: Δte, Δtf Determinare massa molare M (g/mol) di sostanze non note. 1 - mediante la ΔTf. La canfora è un solido che fonde a 179, 5°C ed ha Kf=40°C/m. Se 1, 07 mg di un composto sono sciolti in 78, 1 mg di canfora fusa la soluzione congela a 176, 0 °C. Determinare la massa molare M del composto. ΔTf= 179, 5 – 176, 0 = 3, 5 °C molalità soluzione: m = ΔTf/kf = 3, 5/40 C = 0, 0875 m m = mol soluto/kg solvente mol soluto = m*kg = 0, 0875*78, 1 = 6, 84 *10 -6 mol canfora M canfora = massa/mol = 1, 07/6, 84 = 156 g/mol verifica: formula bruta C 10 H 16 O (chetone ciclico) MM = 120+16+16 = 152 24

Proprietà colligative: pressione osmotica 2 - M mediante la π. Una soluzione acquosa di volume 50 ml contiene 1, 08 g di una proteina, con una π di 5, 85 mm. Hg. T=298 K. Determinare M (g/mol) della proteina. P= 5, 85/760 = 7, 7 *10 -3 atm π = n/V * RT n/V = π/RT = 7, 7 *10 -3 /0, 082*298 = 3, 15 m/L mol = 3, 15 *10 -3 *0, 050 = 1, 58 *10 -5 M proteina = massa/mol = 1, 08/1, 58 *10 -5 = 6, 85 *104 g/mol Verifica approssimativa: La proteina pesa circa 68. 500 C 2100 H 3200 O 1200 N 800 S 300 MM = 25200+3200+19200+11200+9600 = 68. 400 25
![Parametri dell’equilibrio acido-base nell’organismo - valori medi e range fisiologico [H+] 40 n. Eq/L Parametri dell’equilibrio acido-base nell’organismo - valori medi e range fisiologico [H+] 40 n. Eq/L](http://slidetodoc.com/presentation_image_h2/d89e01ff7208392435fd4b07459ce063/image-26.jpg)
Parametri dell’equilibrio acido-base nell’organismo - valori medi e range fisiologico [H+] 40 n. Eq/L (36 -44) p. H 7. 40 (7. 36– 7. 44) Pa. CO 2 40 mm. Hg (36 -44) HCO 3 24 m. Eq/L (22– 26) Dove si misurano: L’equilibrio acido-base nel suo complesso si può valutare solamente sul sangue arterioso, che consente di analizzare il ruolo dei tre componenti fondamentali della regolazione: trasporto ematico sotto forma di tamponi, polmone, rene l’emogasanalisi arteriosa rappresenta l’esame più importante [H+] parametro fondamentale acidi fissi e volatili 26
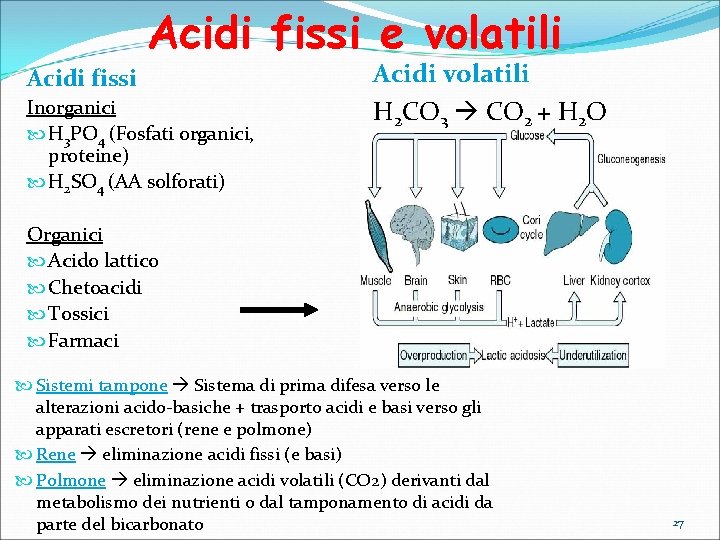
Acidi fissi e volatili Acidi fissi Inorganici H 3 PO 4 (Fosfati organici, proteine) H 2 SO 4 (AA solforati) Acidi volatili H 2 CO 3 CO 2 + H 2 O Organici Acido lattico Chetoacidi Tossici Farmaci Sistemi tampone Sistema di prima difesa verso le alterazioni acido-basiche + trasporto acidi e basi verso gli apparati escretori (rene e polmone) Rene eliminazione acidi fissi (e basi) Polmone eliminazione acidi volatili (CO 2) derivanti dal metabolismo dei nutrienti o dal tamponamento di acidi da parte del bicarbonato 27

Un sistema tampone è costituito da un acido e dalla sua base coniugata ed è in grado di rilasciare o legare H+ a seconda delle necessità. In caso di legame l’H+ cessa temporaneamente di esistere come specie dissociata autonoma (e quindi altamente reattiva) nel fluido contenente il tampone 28
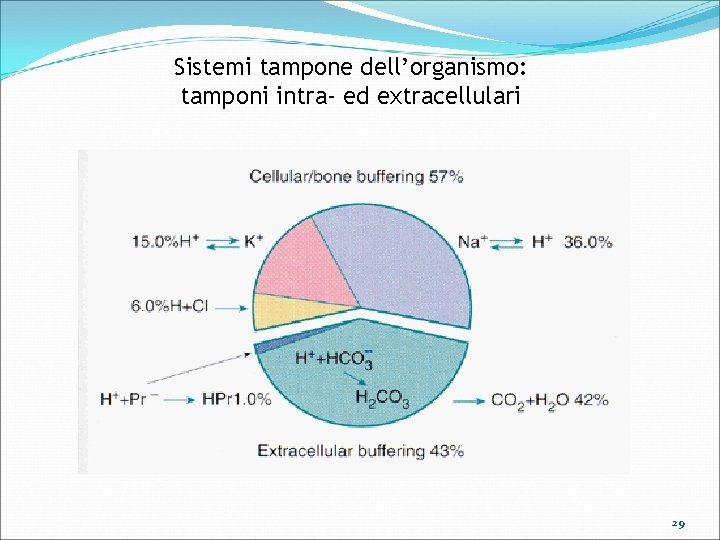
Sistemi tampone dell’organismo: tamponi intra- ed extracellulari 29

Ruolo centrale del sistema tampone bicarbonato/ acido carbonico CO 2 + H 2 O H 2 CO 3 HCO 3 - + H+ • tampone extracellulare più abbondante • è in equilibrio con i sistemi tampone intracellulari • la componente metabolica è controllata dal rene • la componente respiratoria è controllata dal polmone • componenti facilmente misurabili per valutare l’equilibrio acido-base dell’organismo, attraverso l’equazione di Henderson-Hasselbalch 30
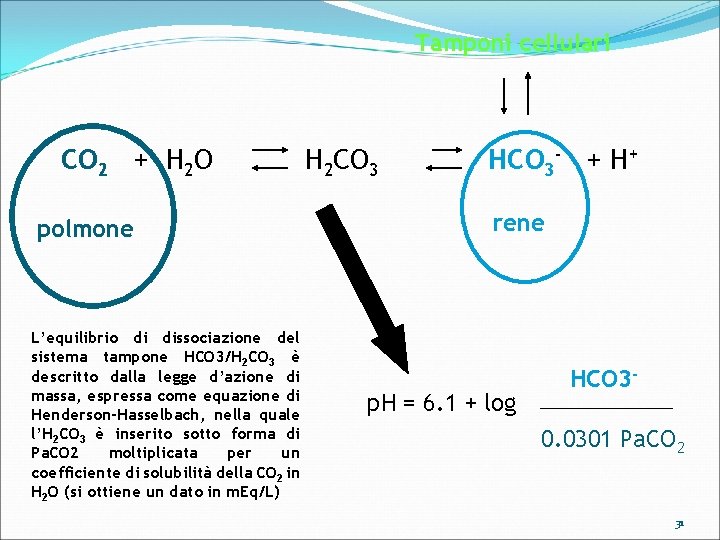
Tamponi cellulari CO 2 + H 2 O polmone L’equilibrio di dissociazione del sistema tampone HCO 3/H 2 CO 3 è descritto dalla legge d’azione di massa, espressa come equazione di Henderson-Hasselbach, nella quale l’H 2 CO 3 è inserito sotto forma di Pa. CO 2 moltiplicata per un coefficiente di solubilità della CO 2 in H 2 O (si ottiene un dato in m. Eq/L) H 2 CO 3 HCO 3 - + H+ rene p. H = 6. 1 + log HCO 30. 0301 Pa. CO 2 31

HCO 3 - p. H = 6. 1 + log 0. 0301 x. Pa. CO 2 24 m. Eq/L p. H = 6. 1 + log 0. 0301 x 40 mm. Hg p. H = 6. 1 + log 24 m. Eq/L 1. 2 m. Eq/L p. H = 6. 1 + log (24/1. 2) p. H = 6. 1 + log 20 p. H = 6. 1 + 1. 3 = 7. 40 32

Le alterazioni dell’equilibrio acido-base: Acidosi respiratoria Acidosi metabolica Alcalosi respiratoria Alcalosi metabolica 33
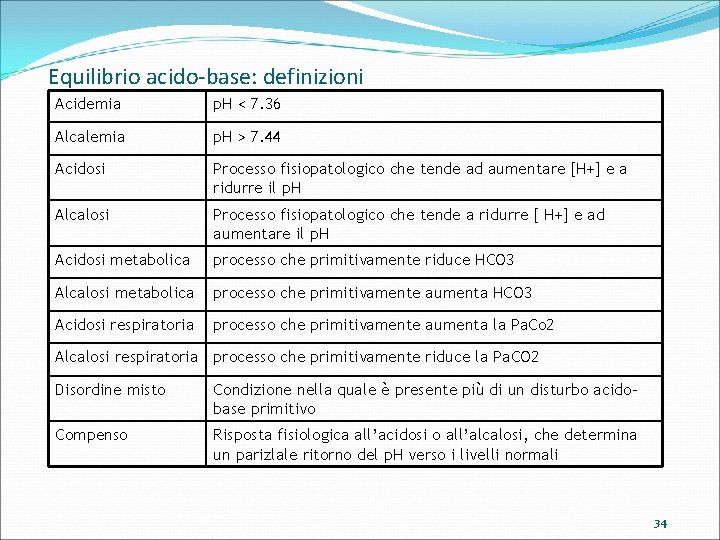
Equilibrio acido-base: definizioni Acidemia p. H < 7. 36 Alcalemia p. H > 7. 44 Acidosi Processo fisiopatologico che tende ad aumentare [H+] e a ridurre il p. H Alcalosi Processo fisiopatologico che tende a ridurre [ H+] e ad aumentare il p. H Acidosi metabolica processo che primitivamente riduce HCO 3 Alcalosi metabolica processo che primitivamente aumenta HCO 3 Acidosi respiratoria processo che primitivamente aumenta la Pa. Co 2 Alcalosi respiratoria processo che primitivamente riduce la Pa. CO 2 Disordine misto Condizione nella quale è presente più di un disturbo acidobase primitivo Compenso Risposta fisiologica all’acidosi o all’alcalosi, che determina un parizlale ritorno del p. H verso i livelli normali 34
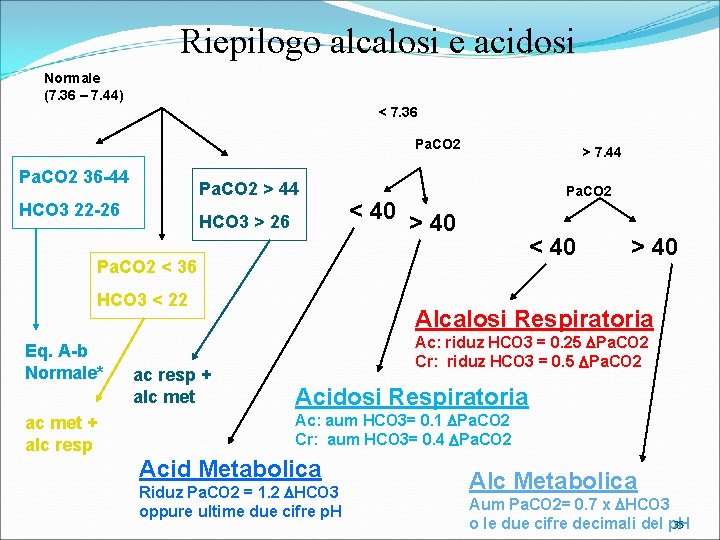
Riepilogo alcalosi e acidosi Normale (7. 36 – 7. 44) < 7. 36 Pa. CO 2 36 -44 Pa. CO 2 > 44 HCO 3 22 -26 HCO 3 > 26 > 7. 44 Pa. CO 2 < 40 > 40 < 40 Pa. CO 2 < 36 HCO 3 < 22 Eq. A-b Normale* ac met + alc resp ac resp + alc met > 40 Alcalosi Respiratoria Ac: riduz HCO 3 = 0. 25 Pa. CO 2 Cr: riduz HCO 3 = 0. 5 Pa. CO 2 Acidosi Respiratoria Ac: aum HCO 3= 0. 1 Pa. CO 2 Cr: aum HCO 3= 0. 4 Pa. CO 2 Acid Metabolica Riduz Pa. CO 2 = 1. 2 HCO 3 oppure ultime due cifre p. H Alc Metabolica Aum Pa. CO 2= 0. 7 x HCO 3 35 o le due cifre decimali del p. H
- Slides: 35