Polymerization by monofunctional radical initiator 1 General radical


Ⅰ. Polymerization by monofunctional radical initiator 1. General radical initiator

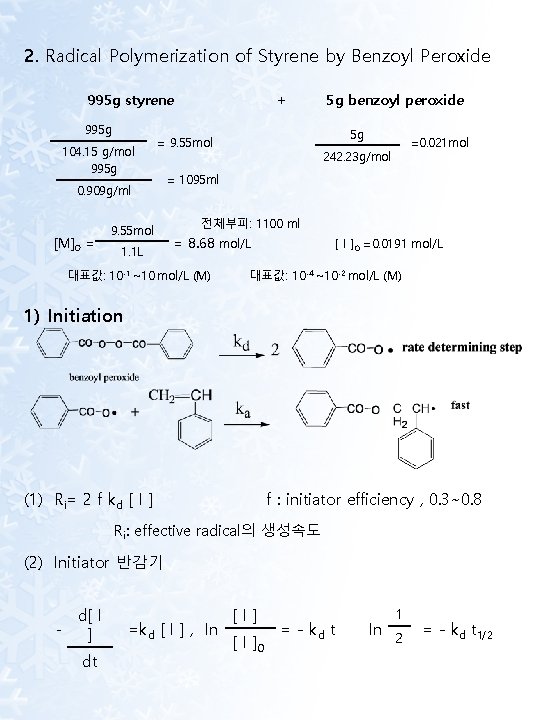
2. Radical Polymerization of Styrene by Benzoyl Peroxide 995 g styrene 995 g 104. 15 g/mol 995 g 9. 55 mol 1. 1 L 5 g benzoyl peroxide 5 g = 9. 55 mol 0. 909 g/ml [M]0 = + =0. 021 mol 242. 23 g/mol = 1095 ml 전체부피: 1100 ml = 8. 68 mol/L 대표값: 10 -1 ~10 mol/L (M) [ I ] 0 =0. 0191 mol/L 대표값: 10 -4 ~10 -2 mol/L (M) 1) Initiation (1) Ri= 2 f kd [ I ] f : initiator efficiency , 0. 3~0. 8 Ri: effective radical의 생성속도 (2) Initiator 반감기 - d[ I ] dt =kd [ I ] , In [I] [ I ]0 = - kd t In 1 2 = - kd t 1/2
![2) Propagation (1) General Rp = - d[M] dt = kp [M∙] [M] Rp 2) Propagation (1) General Rp = - d[M] dt = kp [M∙] [M] Rp](http://slidetodoc.com/presentation_image/10b9cb0771588e8fd2ccc82c6463c706/image-6.jpg)
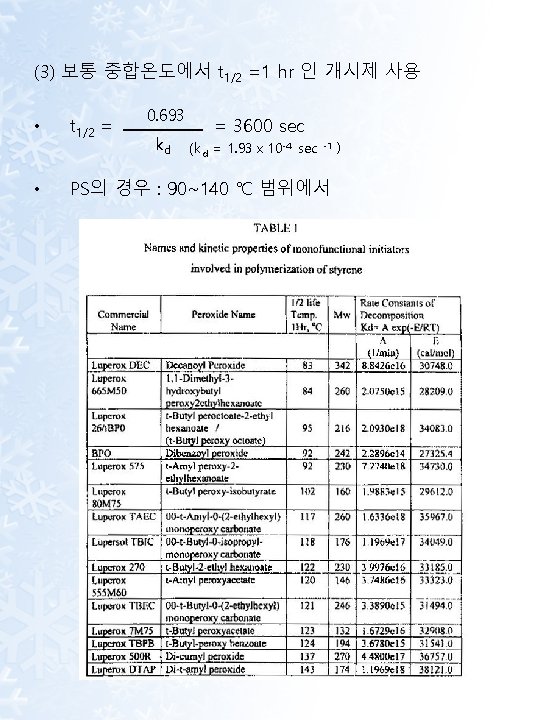
2) Propagation (1) General Rp = - d[M] dt = kp [M∙] [M] Rp : Monomer 소모속도, Polymer 생성속도 [M·] : 다양한 radical의 총 농도 kp 의 대표값: 102 ~104 L/mol·sec
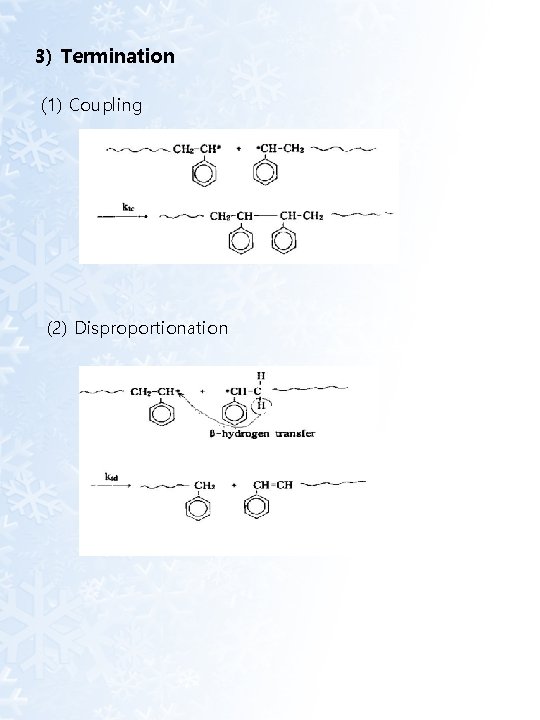
3) Termination (1) Coupling (2) Disproportionation

(3) Coupling vs. Disproportionation 온도가 증가하면 → disproportionation 증가 (because of high activation energy)
![(4) Radical 소멸속도 Rt = (2 ktc +2 ktd) [M∙]2 = 2 kt [M∙]2 (4) Radical 소멸속도 Rt = (2 ktc +2 ktd) [M∙]2 = 2 kt [M∙]2](http://slidetodoc.com/presentation_image/10b9cb0771588e8fd2ccc82c6463c706/image-9.jpg)
(4) Radical 소멸속도 Rt = (2 ktc +2 ktd) [M∙]2 = 2 kt [M∙]2 kt 의 대표값 : 106~108 L/mol·sec (kp보다 훨씬 큰 값) 4) Steady-state approximation ∙ Occurs only after 3 sec ∙ Radical 생성속도 = 소멸속도 (Ri = Rt) 2 f kd [ I ] = 2 kt [M·]2 [M·] = ( f kd [ I ] kt )1/2 대표값 : 10 -9~10 -7 mol/L

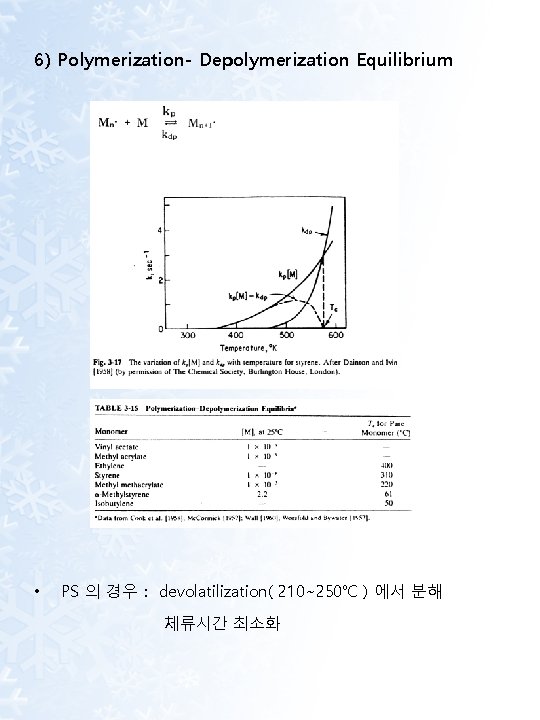
6) Polymerization- Depolymerization Equilibrium • PS 의 경우 : devolatilization( 210~250℃ ) 에서 분해 체류시간 최소화
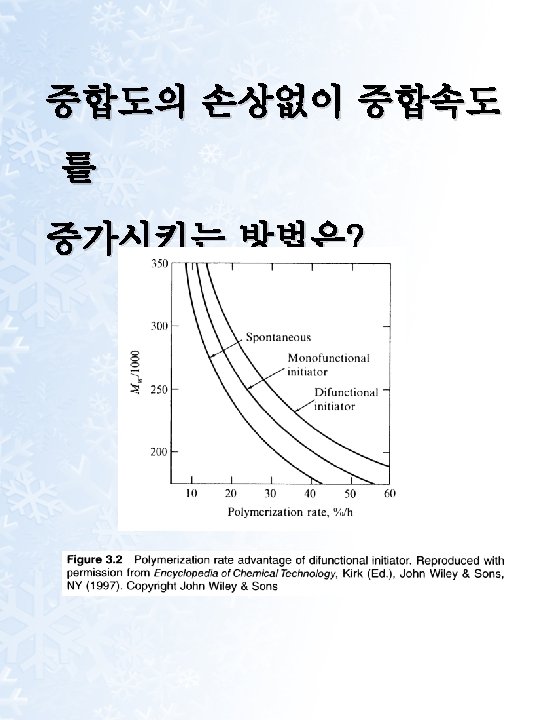
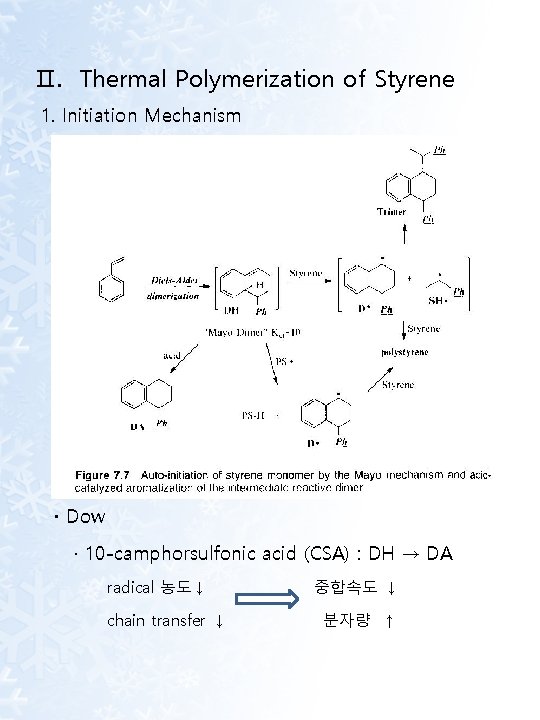
Ⅱ. Thermal Polymerization of Styrene 1. Initiation Mechanism · Dow · 10 -camphorsulfonic acid (CSA) : DH → DA radical 농도↓ chain transfer ↓ 중합속도 ↓ 분자량 ↑
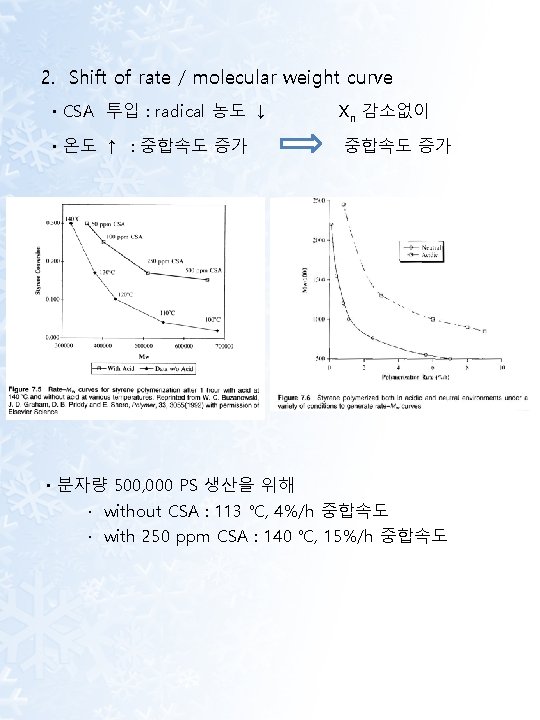
2. Shift of rate / molecular weight curve · CSA 투입 : radical 농도 ↓ Xn 감소없이 · 온도 ↑ : 중합속도 증가 · 분자량 500, 000 PS 생산을 위해 · without CSA : 113 ℃, 4%/h 중합속도 · with 250 ppm CSA : 140 ℃, 15%/h 중합속도
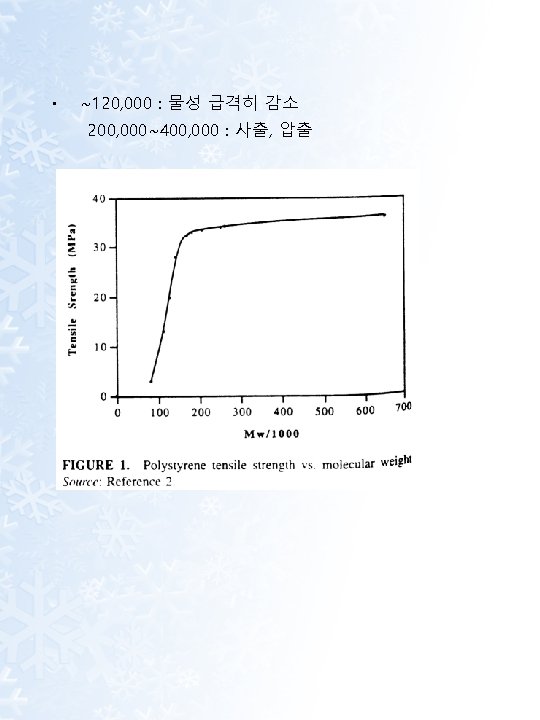
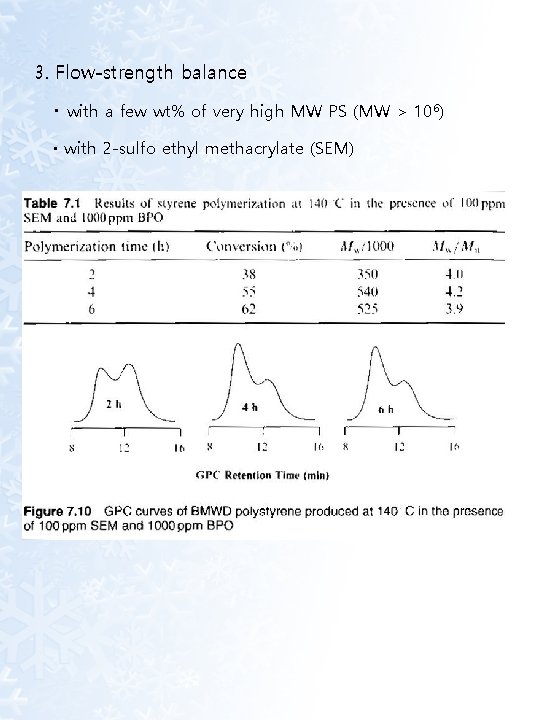
3. Flow-strength balance · with a few wt% of very high MW PS (MW > 106) · with 2 -sulfo ethyl methacrylate (SEM)

Ⅲ. Optimization with Monofunctional Initiators · Multiple initiators BPO ( t 1/2= 1 hr at 91℃ ) TBPB ( t-butyl perbenzoate, t 1/2 = 1 hr at 124 ℃ ) · with temperature profile
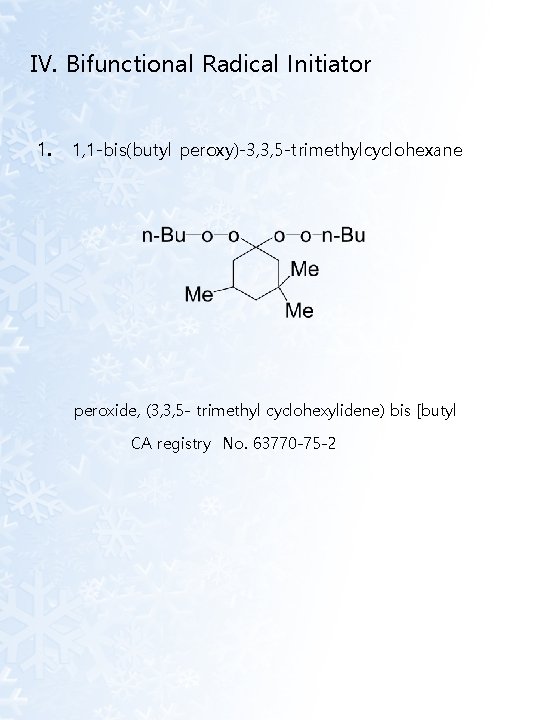
Ⅳ. Bifunctional Radical Initiator 1. 1, 1 -bis(butyl peroxy)-3, 3, 5 -trimethylcyclohexane peroxide, (3, 3, 5 - trimethyl cyclohexylidene) bis [butyl CA registry No. 63770 -75 -2
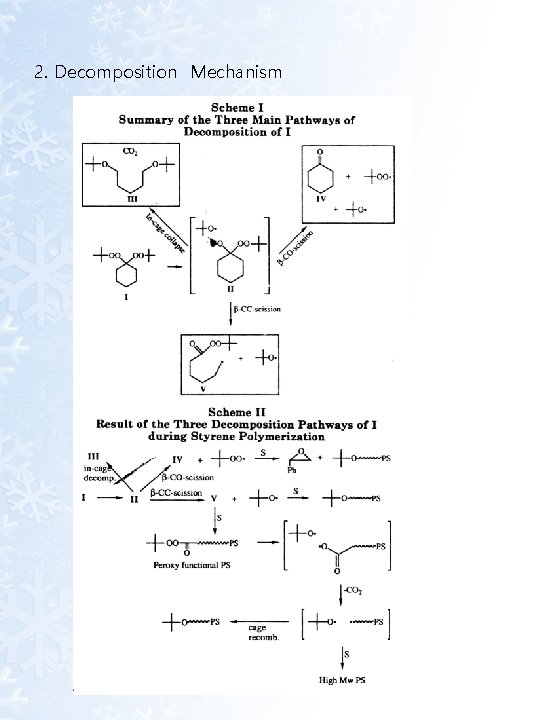
2. Decomposition Mechanism
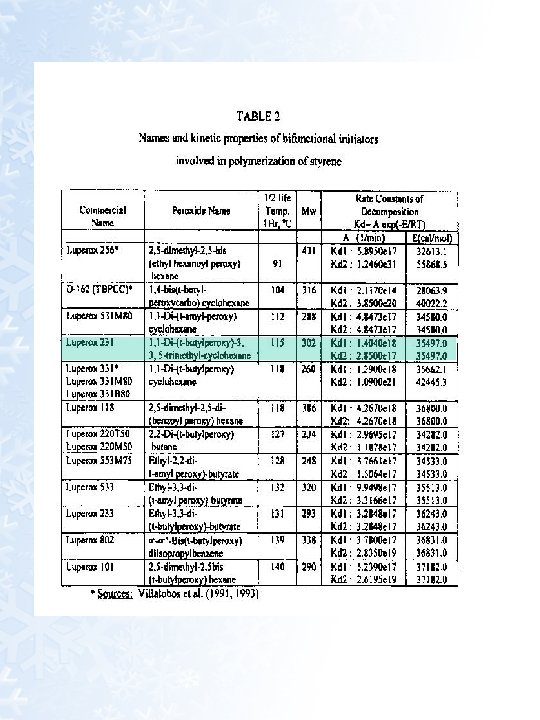

3. BPO vs. 1, 4 - bis(t-butyl peroxycarbo) cyclohexane (D-162) ( most advantaqeous as a substitute for BPO) · BPO 0. 01 M을 사용하여 105℃ 에서 중합하면 : · Cycle time : 8 h · Mw : 250, 000 · MWD: 2. 47 · D-162 0. 005 M을 사용하여 105℃ 에서 중합하면 : · Cycle time : 5~6 h · Mw : 290, 000 · MWD: 2. 70

Ⅴ. Tetrafunctional Radical Initiator 1. 1관능 vs. 4관능 (A. Penlidis et al. , Macromolecular Chemistry and Physics, 204, 436442 (2003)) (A. Penlidis et al. , Macromolecular Reaction Engineering, 1, 209 -221 (2007)) 분자량의 큰 손상없이 중합속도 증대 + branch 형성 ․ t-butylperoxy 2 -ethylhexyl carbonate ․ tetrakis(t-butylperoxy carbonate)
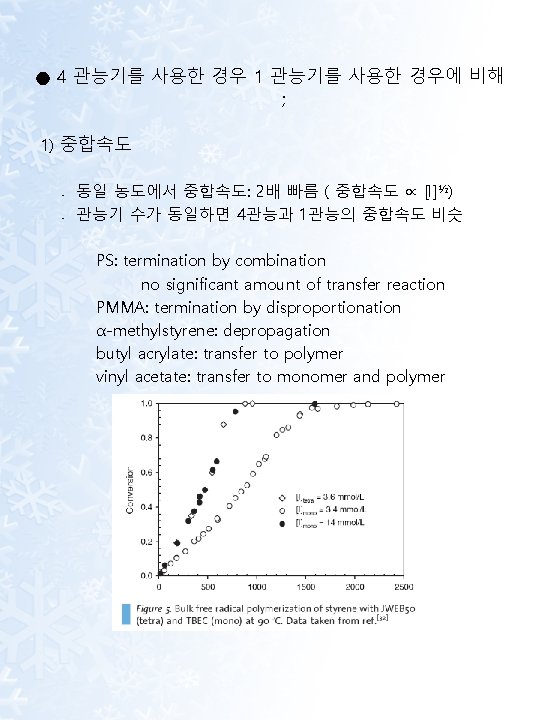
● 4 관능기를 사용한 경우 1 관능기를 사용한 경우에 비해 ; 1) 중합속도 ․ 동일 농도에서 중합속도: 2배 빠름 ( 중합속도 ∝ [I]½) ․ 관능기 수가 동일하면 4관능과 1관능의 중합속도 비슷 PS: termination by combination no significant amount of transfer reaction PMMA: termination by disproportionation α-methylstyrene: depropagation butyl acrylate: transfer to polymer vinyl acetate: transfer to monomer and polymer
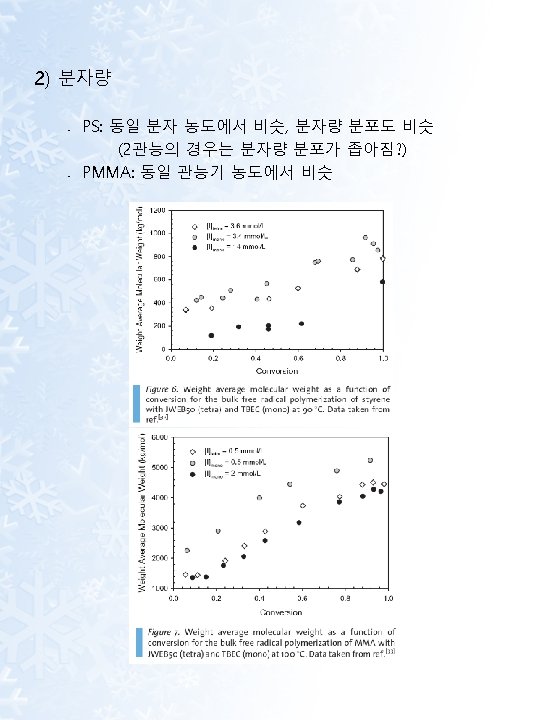
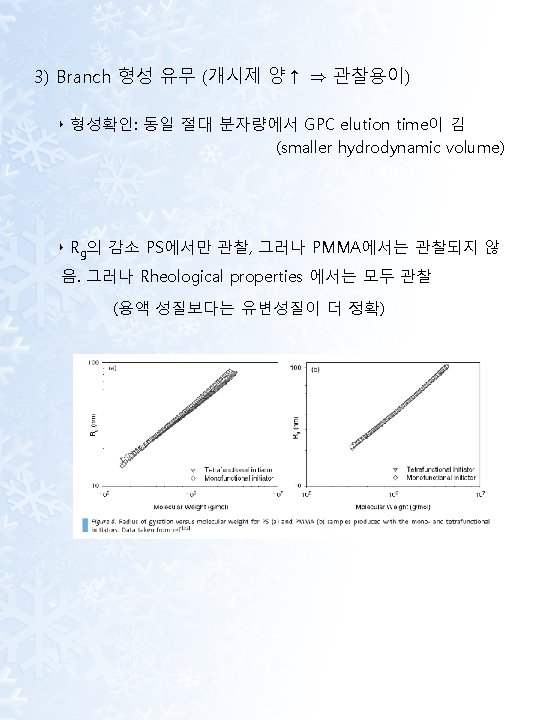
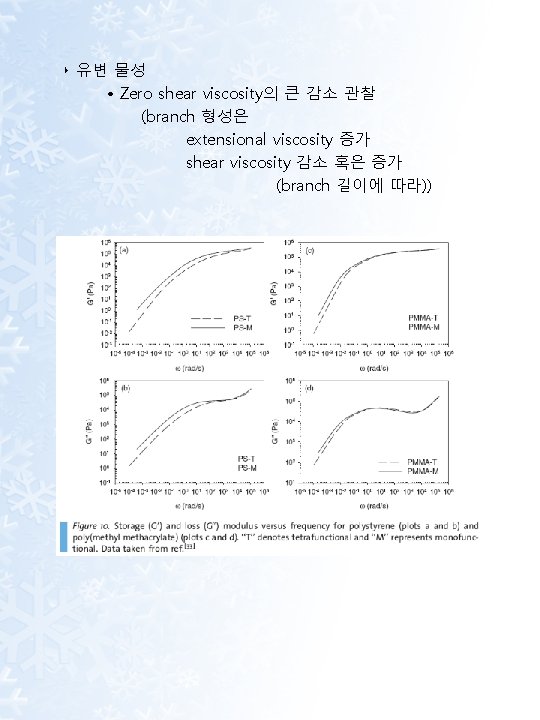
‣ 유변 물성 • Zero shear viscosity의 큰 감소 관찰 (branch 형성은 extensional viscosity 증가 shear viscosity 감소 혹은 증가 (branch 길이에 따라))
3. 2관능 vs. 4관능 (L. Kasehagen et al. , ANTEC, 1837 (2002)) (1) 사용 개시제 • ADF: Luperox 531 M 80, 1, 1 -di(t-amyl peroxy) cyclohexane • BDF: Luperox 331 M 80, 1, 1 -di(t-butyl peroxy) cyclohexane • TFP: Luperox JWEB 50
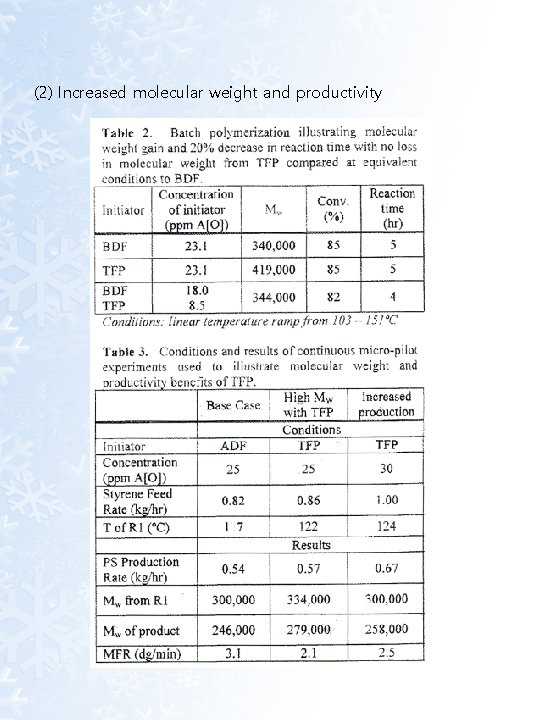
(2) Increased molecular weight and productivity
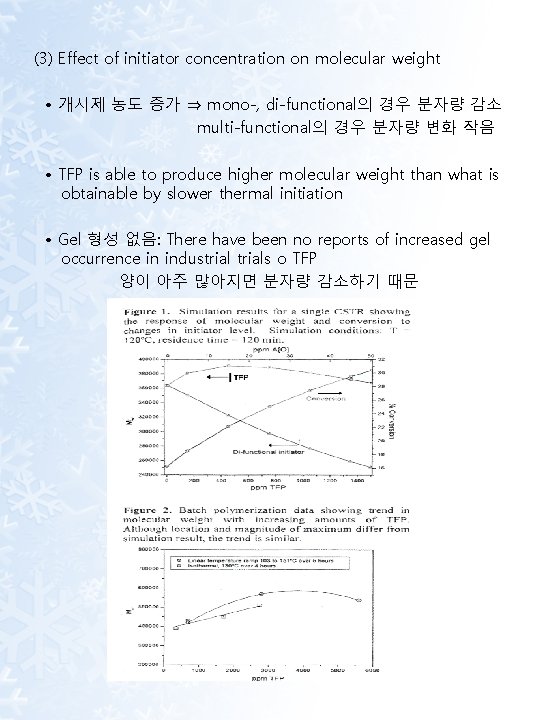
(3) Effect of initiator concentration on molecular weight • 개시제 농도 증가 ⇒ mono-, di-functional의 경우 분자량 감소 multi-functional의 경우 분자량 변화 작음 • TFP is able to produce higher molecular weight than what is obtainable by slower thermal initiation • Gel 형성 없음: There have been no reports of increased gel occurrence in industrials o TFP 양이 아주 많아지면 분자량 감소하기 때문
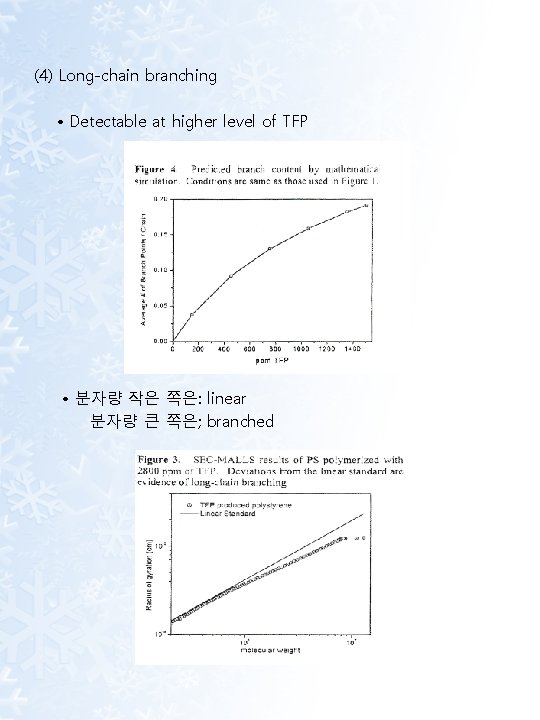
(4) Long-chain branching • Detectable at higher level of TFP • 분자량 작은 쪽은: linear 분자량 큰 쪽은; branched
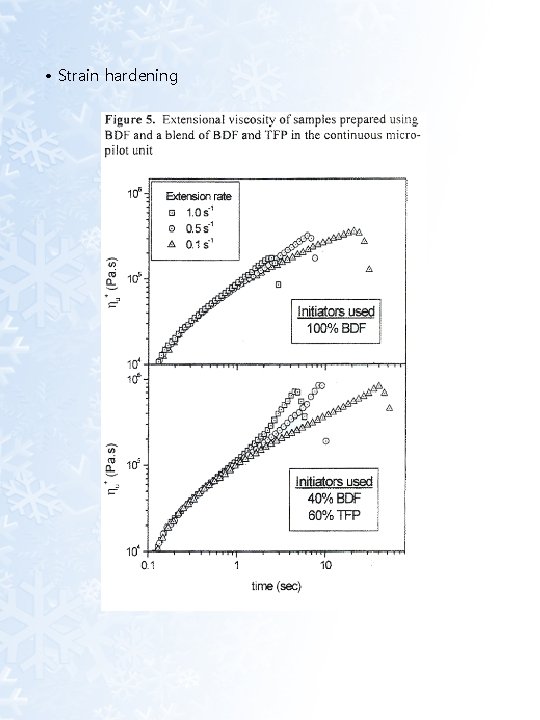
• Strain hardening

Ⅴ. Copolymerization of St and AN 1) Copolymerization Equation
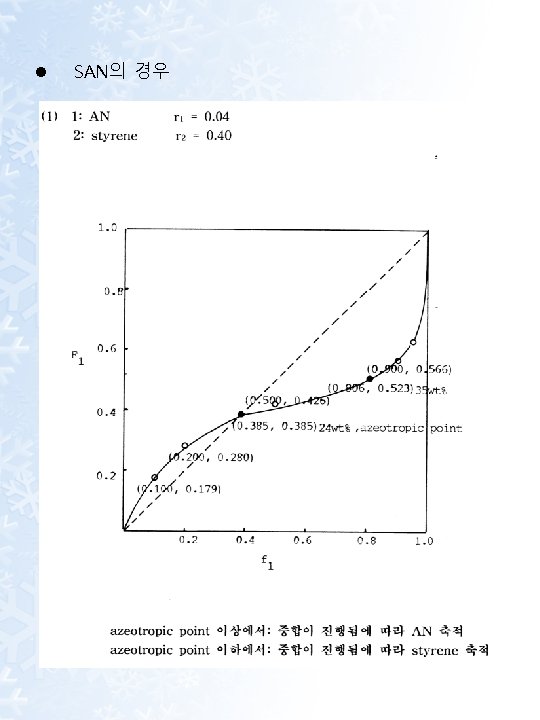

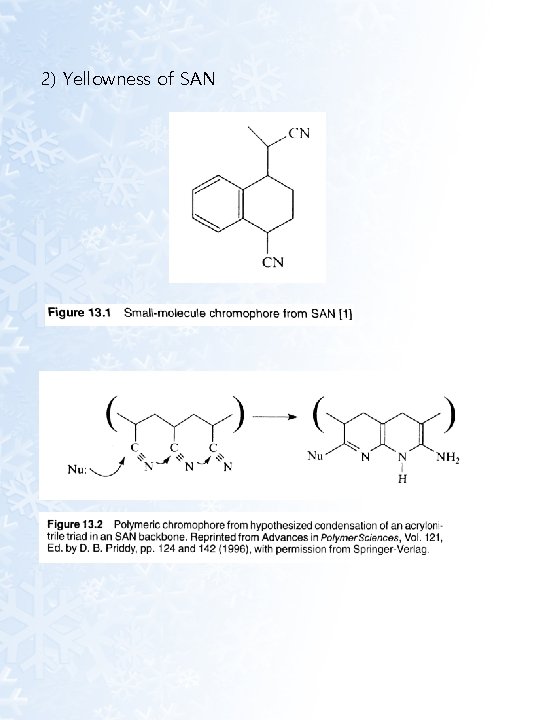
2) Yellowness of SAN
- Slides: 35