POLMEROS Estudiante Constanza Escobar Curso IVB Profesora Marianet
POLÍMEROS Estudiante: Constanza Escobar Curso: IV°B Profesora: Marianet Zerené Asignatura: Química Común
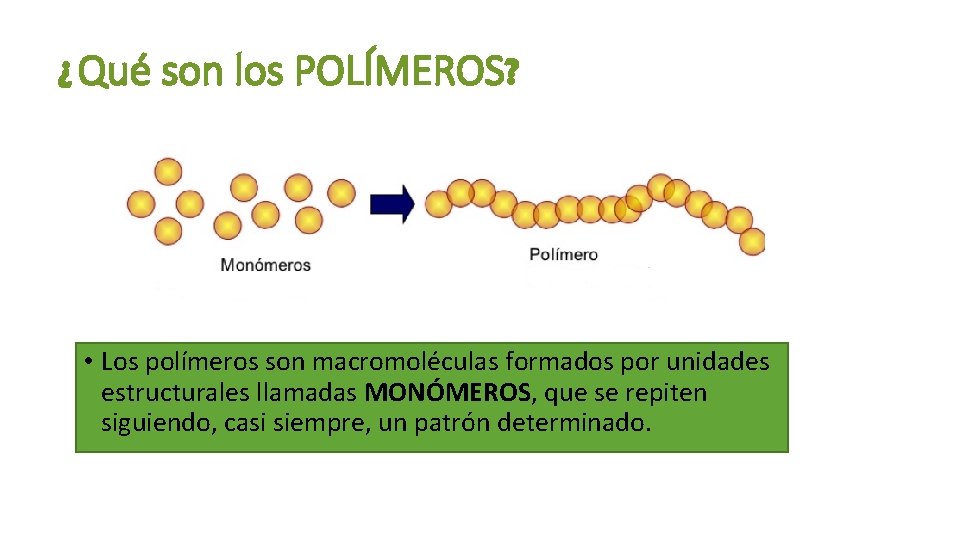
¿Qué son los POLÍMEROS? • Los polímeros son macromoléculas formados por unidades estructurales llamadas MONÓMEROS, que se repiten siguiendo, casi siempre, un patrón determinado.

ORIGEN: 1. 2. 3. 4. 1 2 3 4 BREA: Se obtenía de la brea de los árboles. CAUCHO NATURAL: Pelotas de gaucho usadas por los Incas. BAQUELITA: Primer polímero sintético producido en 1909. PRIMERA GUERRA MUNDIAL: Mucha producción de gaucho sintético en éste periodo.

CARACTERÍSTICAS: BAJO COSTO LIGEREZA NO CONDUCEN LA ELECTRICIDAD BAJA ABSORCIÓN DE HUMEDAD

PROPIEDADES: MECÁNICAS: DUREZA ELONGACIÓN RESISTENCIA FÍSICAS: FIBRAS ELASTÓMEROS PLÁSTICOS COMPORTAMIENTO FRENTE AL CALOR: TERMOPLÁSTICOS TERMOESTABLES

IMPACTO EN EL MEDIO AMBIENTE DEGRADABLES: Diseñado para sufrir un cambio significativo en su estructura química bajo ciertas condiciones ambientales, resultante en la pérdida de algunas de sus propiedades, las cuales pueden ser comprobadas por métodos estándar de verificación de los materiales plásticos y su aplicación en un período determinado de tiempo, el cual determina su clasificación. BIODEGRADABLES: La degradación ocurre por efecto de la acción de microorganismos existentes en la naturaleza tales como bacterias, hongos y algas. OXI-BIODEGRADABLES: Proceso de dos: primero el plástico es modificado por efecto de su reacción con agua, y en segunda instancia las moléculas pequeñas oxidadas son degradadas y se convierten en dióxido de carbón, agua y biomasa. Es muy lento, puede tardar específicamente décadas y tal vez centurias.

CLASIFICACIÓN SEGÚN SU ORIGEN: a) POLÍMEROS NATURALES: son aquellos que forman parte de los seres vivos, como las plantas y animales. EJEMPLOS: Almidón, caucho natural, proteínas y ácidos nucleicos. b) POLÍMEROS SINTÉTICOS: son aquellos polímeros sintetizados a través de procesos químicos en laboratorios o en industrias a partir de materias primas específicas. EJEMPLOS: Caucho vulcanizado, el polietileno y el poliéster. Entre los polímeros naturales y sintéticos no hay grandes diferencias estructurales; ambos están formados por monómeros que se repiten a lo largo de toda la cadena polimérica.
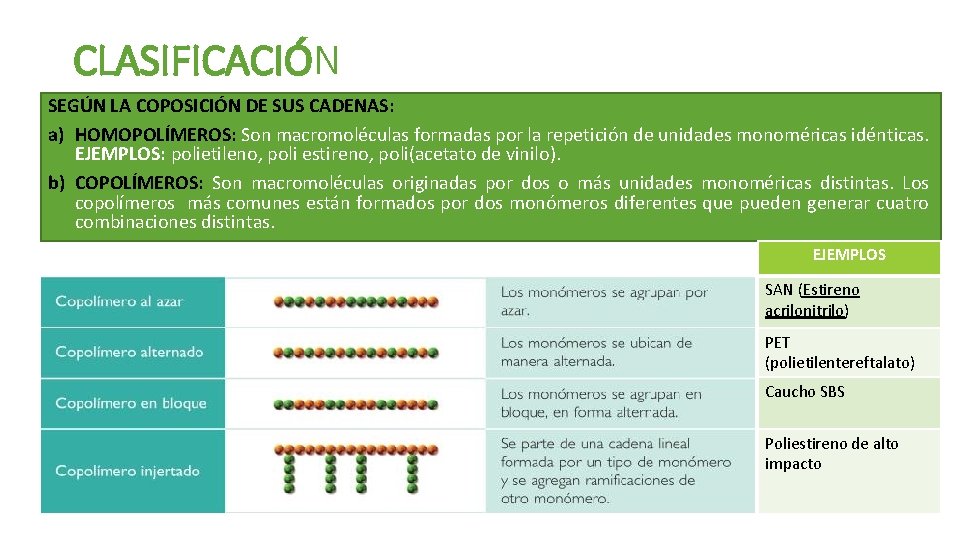
CLASIFICACIÓN SEGÚN LA COPOSICIÓN DE SUS CADENAS: a) HOMOPOLÍMEROS: Son macromoléculas formadas por la repetición de unidades monoméricas idénticas. EJEMPLOS: polietileno, poli estireno, poli(acetato de vinilo). b) COPOLÍMEROS: Son macromoléculas originadas por dos o más unidades monoméricas distintas. Los copolímeros más comunes están formados por dos monómeros diferentes que pueden generar cuatro combinaciones distintas. EJEMPLOS SAN (Estireno acrilonitrilo) PET (polietilentereftalato) Caucho SBS Poliestireno de alto impacto

CLASIFICACIÓN SEGÚN SU ESTRUCTURA: a) LINEALES: Forman una línea recta, de modo que la polimerización ocurre en una sola dirección, pero en ambos sentidos. EJEMPLO: Polipropileno. b) RAMIFICADOS: La polimerización aquí ocurre de una forma tridimensional, lo que quiere decir que los monómeros pueden unirse a otros y formar grandes y diversas figuras. EJEMPLO: Poliestireno. c) ENTRECRUZADOS: Son cadenas lineales adyacentes las cuales se unen transversalmente en varias posiciones mediante enlaces covalentes. EJEMPLOS: Resina fenol-formol, resina melanina-formol, resina urea-formol. d) RETICULADOS: Son cadenas ramificadas en las tres direcciones del espacio. EJEMPLO: Baquelita, Algunos Poliésteres.
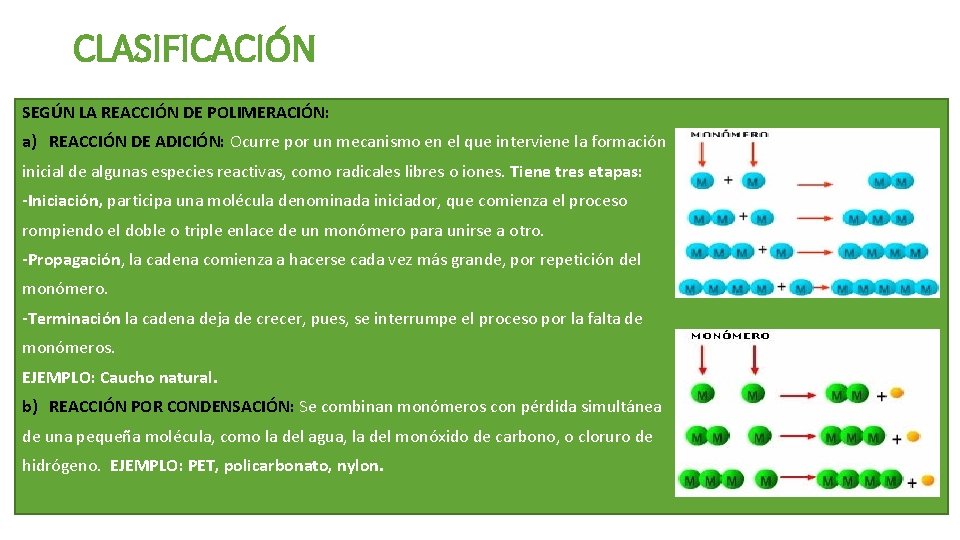
CLASIFICACIÓN SEGÚN LA REACCIÓN DE POLIMERACIÓN: a) REACCIÓN DE ADICIÓN: Ocurre por un mecanismo en el que interviene la formación inicial de algunas especies reactivas, como radicales libres o iones. Tiene tres etapas: -Iniciación, participa una molécula denominada iniciador, que comienza el proceso rompiendo el doble o triple enlace de un monómero para unirse a otro. -Propagación, la cadena comienza a hacerse cada vez más grande, por repetición del monómero. -Terminación la cadena deja de crecer, pues, se interrumpe el proceso por la falta de monómeros. EJEMPLO: Caucho natural. b) REACCIÓN POR CONDENSACIÓN: Se combinan monómeros con pérdida simultánea de una pequeña molécula, como la del agua, la del monóxido de carbono, o cloruro de hidrógeno. EJEMPLO: PET, policarbonato, nylon.

CLASIFICACIÓN POLÍMEROS ORGÁNICOS: Posee en la cadena principal átomos de carbono. EJEMPLO: Pilopirrol. POLÍMEROS ORGANICOS VINÍLICOS: La cadena principal de sus moléculas está formada exclusivamente por átomos de carbono. Incluyen átomos de halógenos (cloro, flúor. . . ) en su composición. EJEMPLO: Polietileno, polipropileno. POLÍMEROS ORGANICOS NO VINÍLICOS: Además de carbono, tienen átomos de oxígeno o nitrógeno en su cadena principal. EJEMPLO: Poliacetal.

CLASIFICACIÓN SEGÚN SU COMPORTAMIENTO AL ELEVAR LA TEMPERATURA: Consiste en calentarlos por encima de cierta temperatura. Según si el material funde y fluye o por el contrario no lo hace se diferencian dos tipos de polímeros: TERMOPLÁSTICOS: Fluyen (pasan al estado líquido) al calentarlos y se vuelven a endurecer (vuelven al estado solido) al enfriarlos. Su estructura molecular presenta pocos (o ningún) entrecruzamientos. EJEMPLO: Policarbonato (PC), polietileno, nylon. TERMOESTABLES: No fluyen, y lo único que conseguimos al calentarlos es que se descompongan químicamente, en vez de fluir. Este comportamiento se debe a una estructura con muchos entrecruzamientos, que impiden los desplazamientos relativos de las moléculas. EJEMPLO: Poliester, baquelita.

POLIMERACIÓN Proceso químico mediante el cual moléculas iguales o distintas se unen entre si, por enlaces covalentes para formar un POLÍMERO.
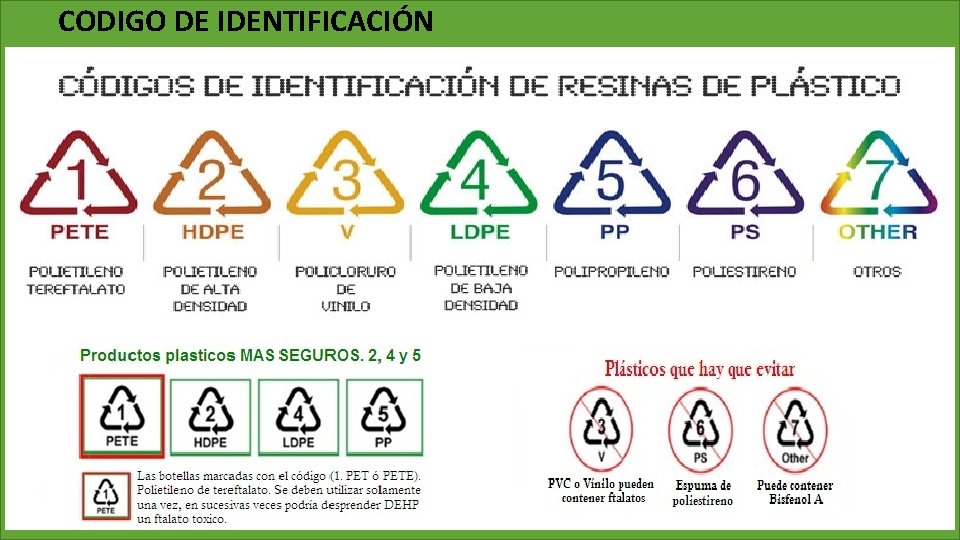
CODIGO DE IDENTIFICACIÓN

POLÍMEROS NATURALES
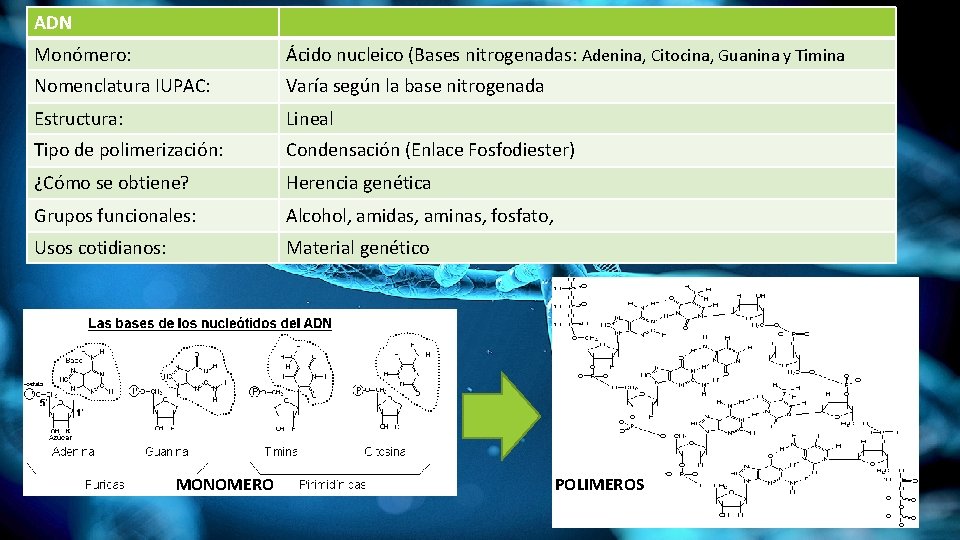
ADN Monómero: Ácido nucleico (Bases nitrogenadas: Adenina, Citocina, Guanina y Timina Nomenclatura IUPAC: Varía según la base nitrogenada Estructura: Lineal Tipo de polimerización: Condensación (Enlace Fosfodiester) ¿Cómo se obtiene? Herencia genética Grupos funcionales: Alcohol, amidas, aminas, fosfato, Usos cotidianos: Material genético MONOMERO POLIMEROS
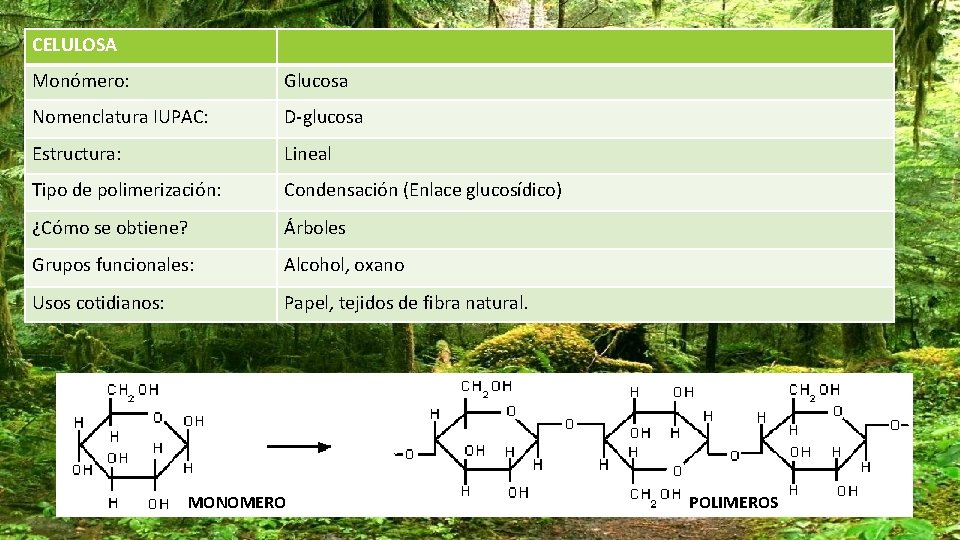
CELULOSA Monómero: Glucosa Nomenclatura IUPAC: D-glucosa Estructura: Lineal Tipo de polimerización: Condensación (Enlace glucosídico) ¿Cómo se obtiene? Árboles Grupos funcionales: Alcohol, oxano Usos cotidianos: Papel, tejidos de fibra natural. MONOMERO POLIMEROS
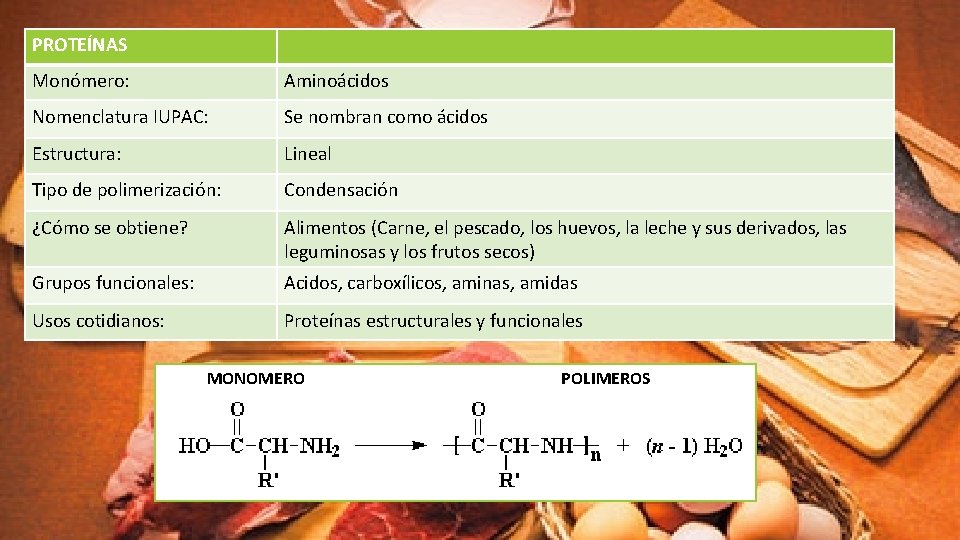
PROTEÍNAS Monómero: Aminoácidos Nomenclatura IUPAC: Se nombran como ácidos Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? Alimentos (Carne, el pescado, los huevos, la leche y sus derivados, las leguminosas y los frutos secos) Grupos funcionales: Acidos, carboxílicos, aminas, amidas Usos cotidianos: Proteínas estructurales y funcionales MONOMERO POLIMEROS
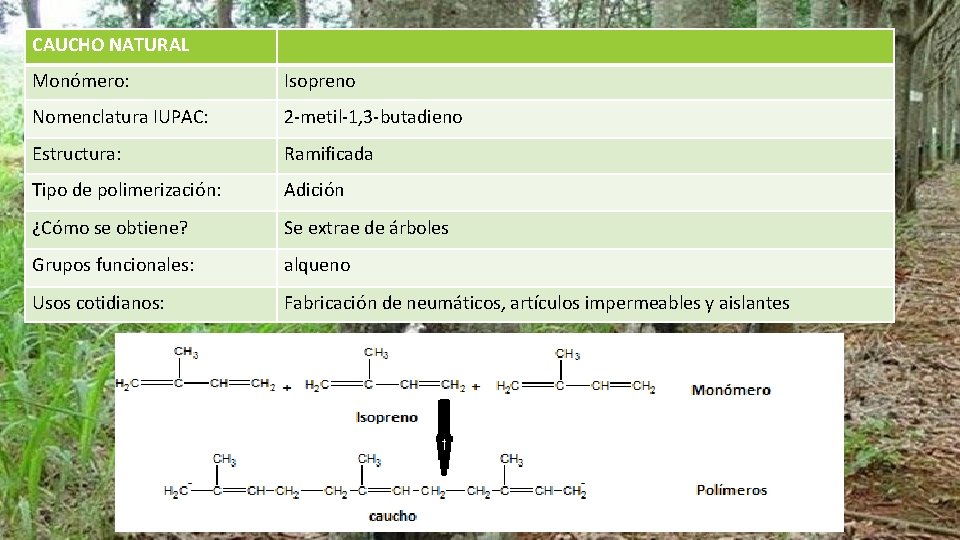
CAUCHO NATURAL Monómero: Isopreno Nomenclatura IUPAC: 2 -metil-1, 3 -butadieno Estructura: Ramificada Tipo de polimerización: Adición ¿Cómo se obtiene? Se extrae de árboles Grupos funcionales: alqueno Usos cotidianos: Fabricación de neumáticos, artículos impermeables y aislantes
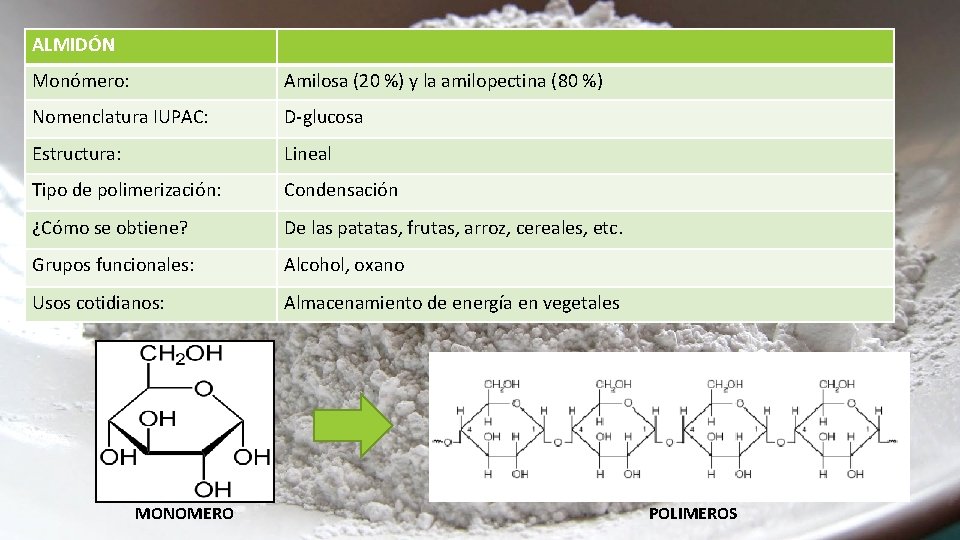
ALMIDÓN Monómero: Amilosa (20 %) y la amilopectina (80 %) Nomenclatura IUPAC: D-glucosa Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? De las patatas, frutas, arroz, cereales, etc. Grupos funcionales: Alcohol, oxano Usos cotidianos: Almacenamiento de energía en vegetales MONOMERO POLIMEROS
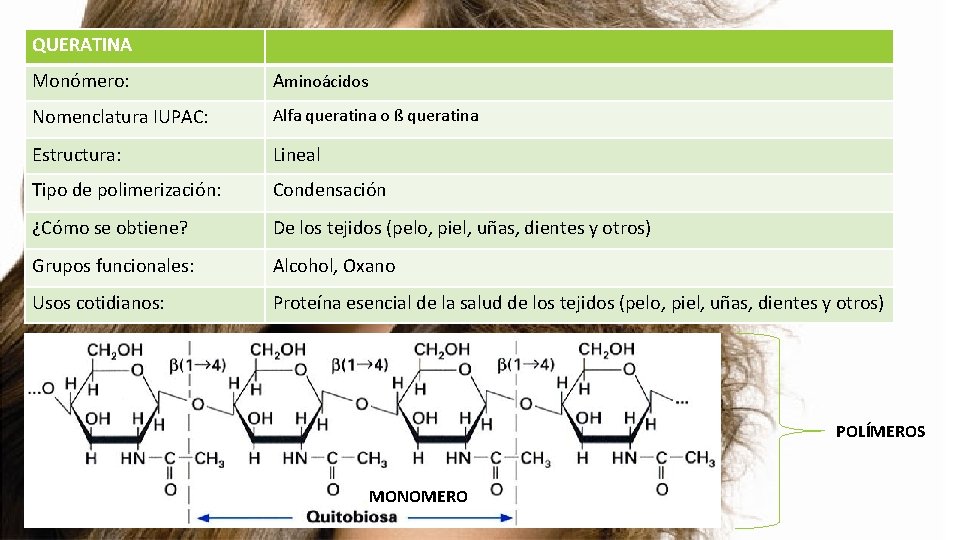
QUERATINA Monómero: Aminoácidos Nomenclatura IUPAC: Alfa queratina o ß queratina Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? De los tejidos (pelo, piel, uñas, dientes y otros) Grupos funcionales: Alcohol, Oxano Usos cotidianos: Proteína esencial de la salud de los tejidos (pelo, piel, uñas, dientes y otros) POLÍMEROS MONOMERO
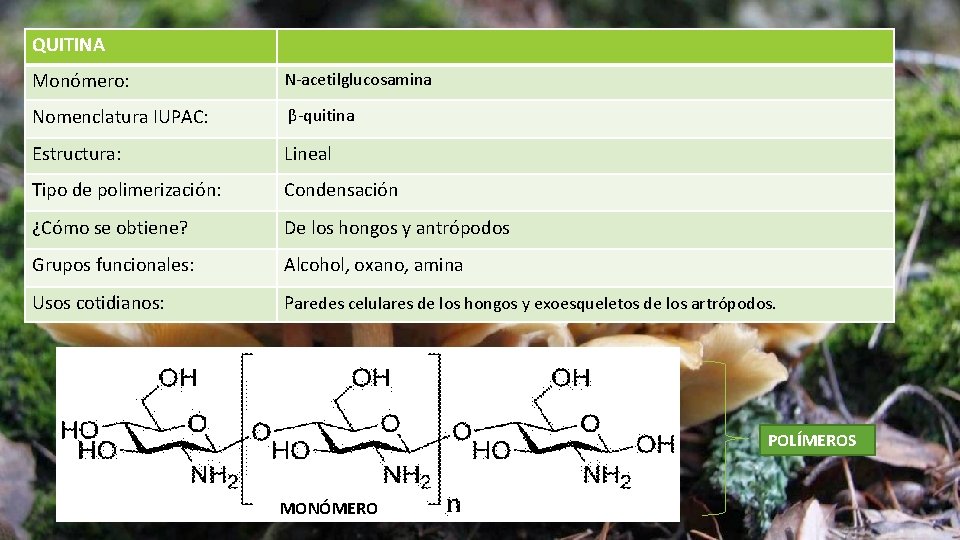
QUITINA Monómero: N-acetilglucosamina Nomenclatura IUPAC: β-quitina Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? De los hongos y antrópodos Grupos funcionales: Alcohol, oxano, amina Usos cotidianos: Paredes celulares de los hongos y exoesqueletos de los artrópodos. POLÍMEROS MONÓMERO
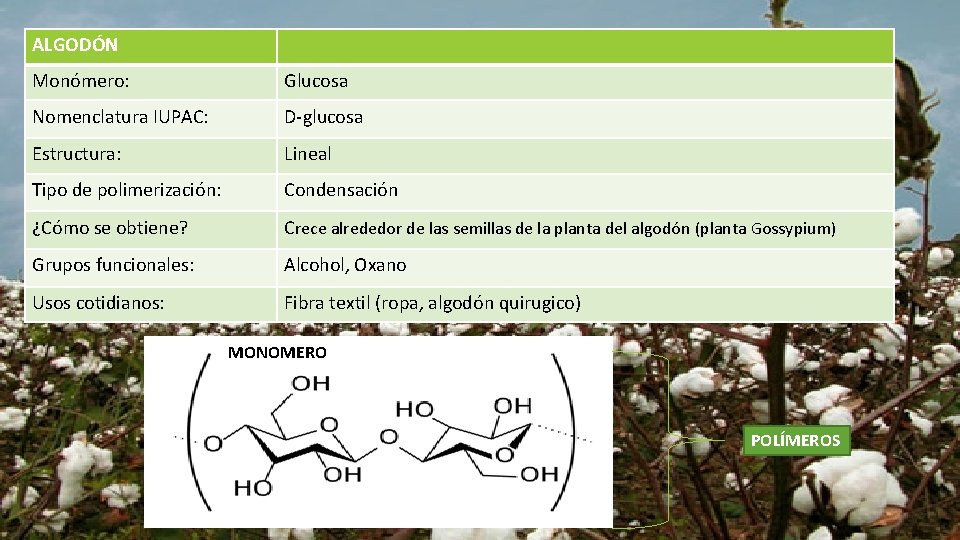
ALGODÓN Monómero: Glucosa Nomenclatura IUPAC: D-glucosa Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? Crece alrededor de las semillas de la planta del algodón (planta Gossypium) Grupos funcionales: Alcohol, Oxano Usos cotidianos: Fibra textil (ropa, algodón quirugico) MONOMERO POLÍMEROS
SEDA Monómero: Amida (Serina, alanina, glicina) Nomenclatura IUPAC: Ácido 2 -amina-3 -hidroxipropanoico (Serina) Estructura: Ramificada Tipo de polimerización: Condensación ¿Cómo se obtiene? Del gusano (bombyx marl) Grupos funcionales: Depende del aminoácido Usos cotidianos: Tejidos y telas

POLÍMEROS SINTÉTICOS
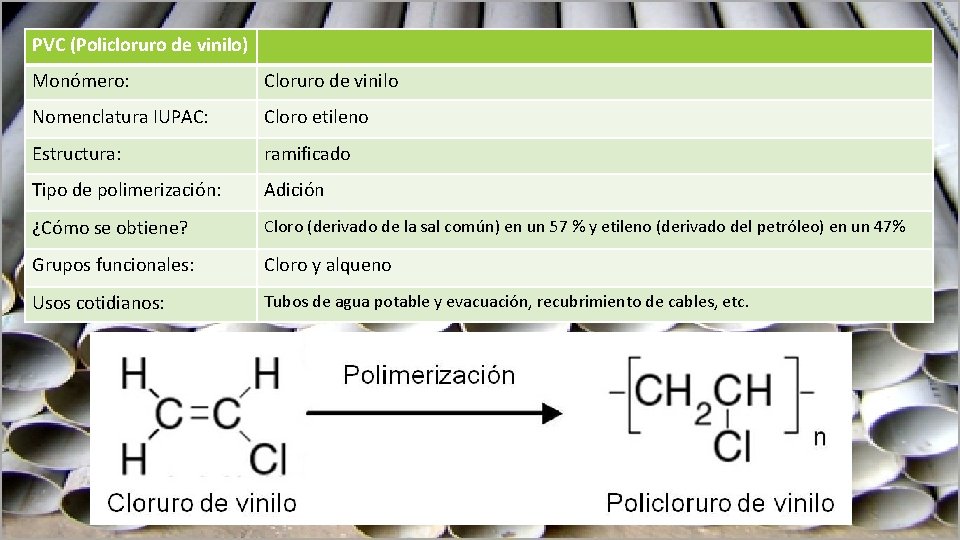
PVC (Policloruro de vinilo) Monómero: Cloruro de vinilo Nomenclatura IUPAC: Cloro etileno Estructura: ramificado Tipo de polimerización: Adición ¿Cómo se obtiene? Cloro (derivado de la sal común) en un 57 % y etileno (derivado del petróleo) en un 47% Grupos funcionales: Cloro y alqueno Usos cotidianos: Tubos de agua potable y evacuación, recubrimiento de cables, etc.
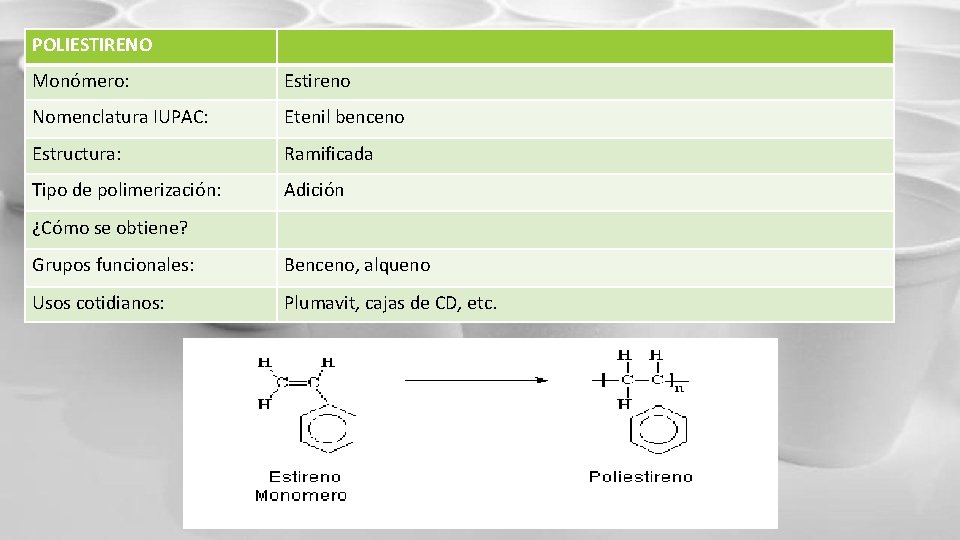
POLIESTIRENO Monómero: Estireno Nomenclatura IUPAC: Etenil benceno Estructura: Ramificada Tipo de polimerización: Adición ¿Cómo se obtiene? Grupos funcionales: Benceno, alqueno Usos cotidianos: Plumavit, cajas de CD, etc.
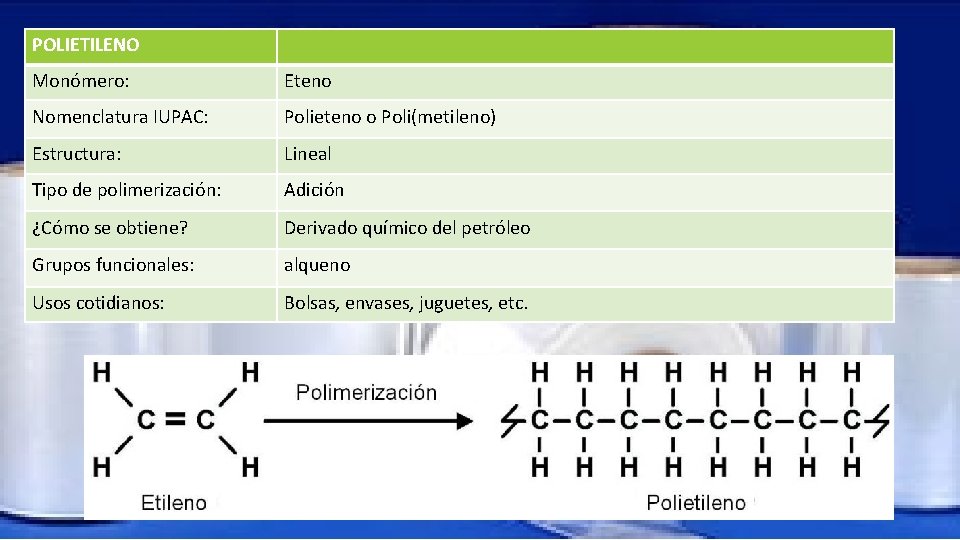
POLIETILENO Monómero: Eteno Nomenclatura IUPAC: Polieteno o Poli(metileno) Estructura: Lineal Tipo de polimerización: Adición ¿Cómo se obtiene? Derivado químico del petróleo Grupos funcionales: alqueno Usos cotidianos: Bolsas, envases, juguetes, etc.

POLIETILENO DE BAJA DENSIDAD Y DE ALTA DENSIDAD POLIETILENO DE BAJA INTENSIDAD: (LDPE o PE-LD) oscila entre 0. 910 a 0. 925 gr/cm 3 y es principalmente amorfo. Puede soportar temperaturas de hasta 80 C°, es muy resistente a los ataques de sustancias químicas, es atóxico, impermeable al agua y poco permeable al vapor de gases, POLIETILENO DE ALTA DENSIDAD: (HDPE) Puede soportar temperaturas de hasta 120 C°. Admite usos más variados, como los contenedores plásticos más gruesos y resistentes; algunos de ellos son los que se usan para detergentes líquidos y otras sustancias corrosivas o peligrosas. También se utilizan para la fabricación de juguetes, protectores corporales como rodilleras o cascos, diversas clases de prótesis y partes de automóviles. Es transparente, rígido y resistente a muchos productos químicos diferentes.
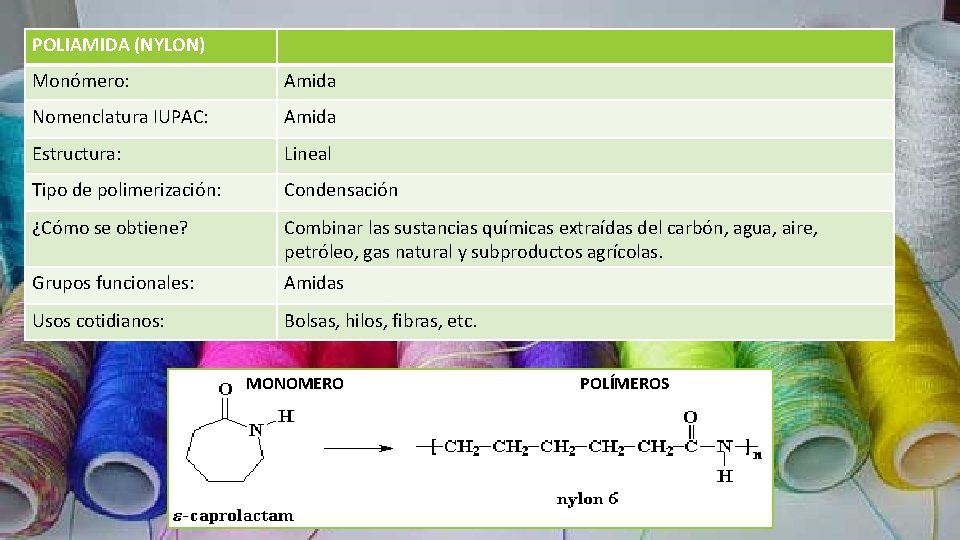
POLIAMIDA (NYLON) Monómero: Amida Nomenclatura IUPAC: Amida Estructura: Lineal Tipo de polimerización: Condensación ¿Cómo se obtiene? Combinar las sustancias químicas extraídas del carbón, agua, aire, petróleo, gas natural y subproductos agrícolas. Grupos funcionales: Amidas Usos cotidianos: Bolsas, hilos, fibras, etc. MONOMERO POLÍMEROS
- Slides: 30