Podstawy farmakokinetyki klinicznej Dziaania niepodane lekw Dr n















































![Rozwiązanie 1. Dawka nasycająca = Vd x Ct x BW/F = 7, 3 [L/kg] Rozwiązanie 1. Dawka nasycająca = Vd x Ct x BW/F = 7, 3 [L/kg]](https://slidetodoc.com/presentation_image_h/8efb12a04cb0559f92f1305da8f62501/image-58.jpg)



























- Slides: 85

Podstawy farmakokinetyki klinicznej. Działania niepożądane leków. Dr n. med. Agnieszka Śliwińska, Klinika Chorób Wewnętrznych, Diabetologii i Farmakologii Klinicznej , Uniwersytet Medyczny w Łodzi

Plan seminarium • • Procesy LADME Parametry farmakokinetyczne Niepożądane działania leków (ADR), efekt uboczny (AE) Rodzaje działań niepożądanych leków Klasyfikacja działań niepożądanych leków wg. Rawlins’a Klasyfikacja FDA leków stosowanych w ciąży Zgłaszanie działań niepożądanych leków

FARMAKOLOGIA nauka o leku FARMAKOKINETYKA wpływ organizmu na lek FARMAKODYNAMIKA wpływ leku na organizm

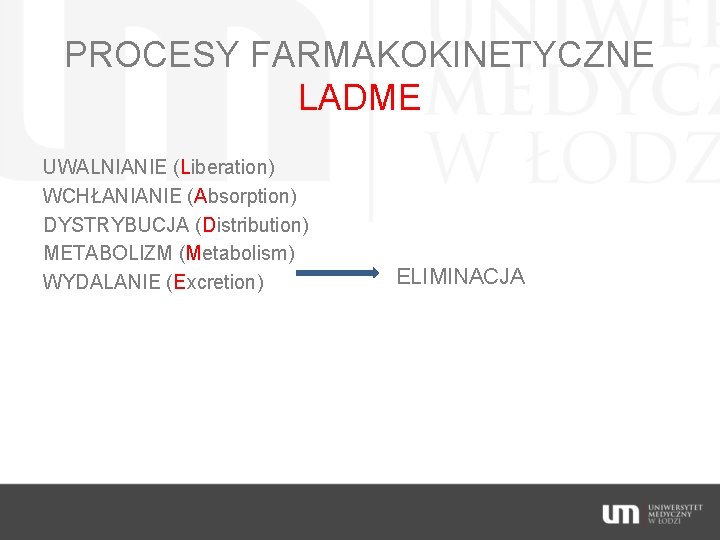
PROCESY FARMAKOKINETYCZNE LADME UWALNIANIE (Liberation) WCHŁANIANIE (Absorption) DYSTRYBUCJA (Distribution) METABOLIZM (Metabolism) WYDALANIE (Excretion) ELIMINACJA

Procesy farmakokinetyczne UWALNIANIE WCHŁANIANIE DYSTRYBUCJA METABOLIZM WYDALANIE

UWALNIANIE Uwalnianie substancji czynnej z preparatu, który został wprowadzony do organizmu, etapy: 1. Rozpad (tabletki, kapsułki) 2. Uwolnienie substancji czynnej z tabletki 3. Rozpuszczenie w płynach ustrojowych Przebieg tych procesów zależy głównie od czynników technologicznych

Procesy farmakokinetyczne UWALNIANIE WCHŁANIANIE DYSTRYBUCJA METABOLIZM WYDALANIE

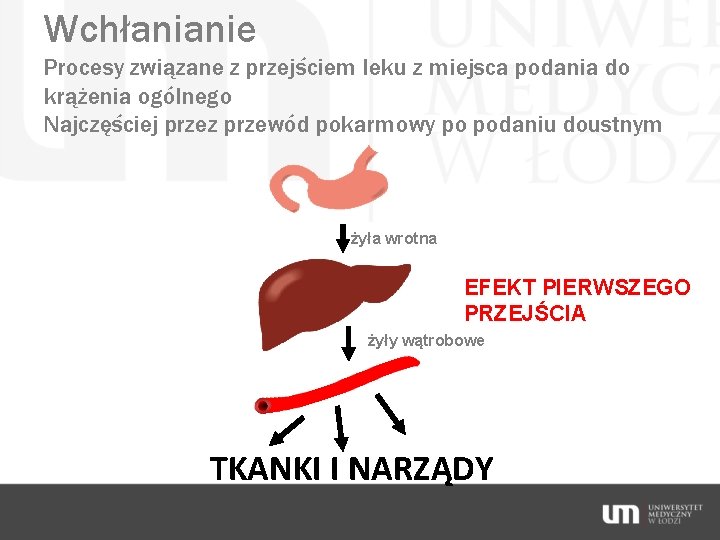
Wchłanianie Procesy związane z przejściem leku z miejsca podania do krążenia ogólnego Najczęściej przez przewód pokarmowy po podaniu doustnym żyła wrotna EFEKT PIERWSZEGO PRZEJŚCIA żyły wątrobowe TKANKI I NARZĄDY

Efekt pierwszego przejścia Intensywność metabolizowania leku w czasie pierwszego przepływu przez wątrobę Może wykluczyć doustną drogę podawania leku lub sprawić, że dawka podawana doustnie jest dużo większa niż równoważna jej dawka podawana dożylnie Drogi podania: – doustna – do tętnicy wątrobowej lub żyły wrotnej – doodbytnicza (częściowo)

Efekt pierwszego przejścia Przykłady leków o dużym efekcie pierwszego przejścia: 1. propranolol, metoprolol, acebutolol 2. nifedypina, werapamil 3. nitrogliceryna 4. ASA, paracetamol 5. petydyna, morfina 6. lidokaina

Wchłanianie Pozostałe drogi podania leku: 1. dożylna 2. podskórna 3. domięśniowa 4. doodbytnicza 5. donosowa 6. podjęzykowa 7. wziewna 8. na skórę 9. do worka spojówkowego

Wchłanianie Czynniki determinujące wybór drogi podania leku: - właściwości fizykochemiczne leku - oczekiwany początek działania leku - docelowe miejsce działania leku - stan ogólny pacjenta - wiek pacjenta

Przechodzenie leków przez błony biologiczne Dyfuzja bierna, ułatwiona, przez pory – rozpuszczalność w tłuszczach – p. H – wielkość cząsteczki Transport aktywny za pośrednictwem nośników Pinocytoza

Dostępność biologiczna (F) (biodostępność) Ułamek dawki substancji leczniczej, który dostaje się w formie aktywnej farmakologicznie do krążenia ogólnego po podaniu pozanaczyniowym oraz szybkość, z jaką ten proces zachodzi

Czynniki determinujące dostępność biologiczną; • droga podania (po podaniu dożylnym = 1 (100%) • właściwości fizykochemiczne preparatu – warunkują szybkość i ilość substancji czynnej uwolnionej z postaci leku (rozpuszczalność, lipofilność, stopień zjonizowania, masa cząsteczkowa, substancje pomocnicze) • stan fizjopatologiczny organizmu (zmiany p. H lub motoryki przewodu pokarmowego, choroby przewodu pokarmowego lub wątroby) • efekt pierwszego przejścia • interakcje pomiędzy lekami lub lekiem i treścią pokarmową w miejscu wchłaniania

Dostępność biologiczna Bezwzględna porównanie badanego leku podanego pozanaczyniowo z tym samym lekiem podanym donaczyniowo Względna D iv. x AUC po. EBA = D po. x AUC iv. porównanie preparatu badanego z preparatem standardowym o znanej dostępności biologicznej Ds x AUCb EBA = Db x AUCs EBA - Extend of Bioavailability s – preparat standardowy b – preparat badany

Podsumowanie 1. Obliczyć biodostępność teofiliny podanej dożylnie (F= 100%) w dawce 80 mg w postaci aminofiliny. Aminofilina ulega we krwi deestryfikacji w wyniku czego powstaje 80% teofiliny (aktywna) oraz 20% etylenodiaminy (nieaktywna). 2. Obliczyć biodostępność leku podanego doustne w dawce 100 mg, z czego wchłonięciu uległo 80% dawki, a w wyniku efektu pierwszego przejścia 20% dawki wchłoniętej uległo zmetabolizowaniu do nieaktywnych metabolitów. 3. W Jakim celu oblicza się względną dostępność biologiczną?

Rozwiązanie 1. F = 80 mg x 0, 8 = 64 mg teofiliny 2. F = 100 mg x 0, 8 = 64 mg 3. Preparaty tego samego leku mogą różnić się biodostępnością w efekcie może dojść do niepowodzenia terapeutycznego (niższa F) lub wystąpienia objawów toksycznych (wyższa F)

Wykorzystując rycinę omów wchłanianie felodypiny

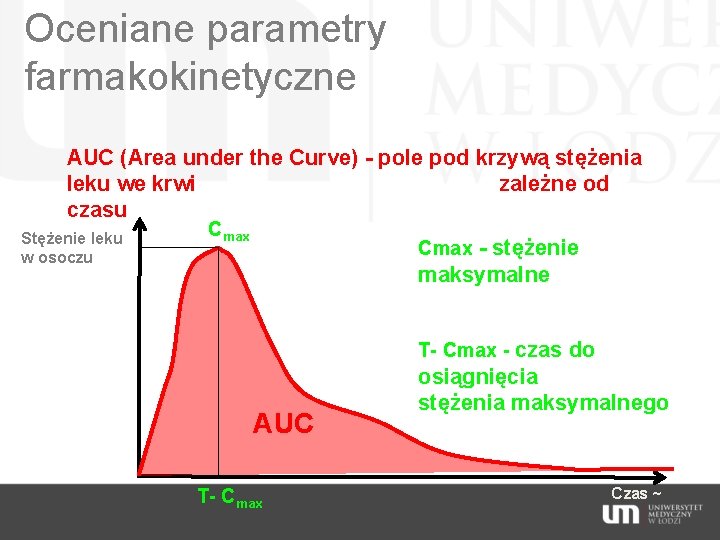
Oceniane parametry farmakokinetyczne AUC (Area under the Curve) - pole pod krzywą stężenia leku we krwi zależne od czasu Stężenie leku w osoczu Cmax - stężenie maksymalne T- Cmax - czas do AUC T- Cmax osiągnięcia stężenia maksymalnego Czas ~

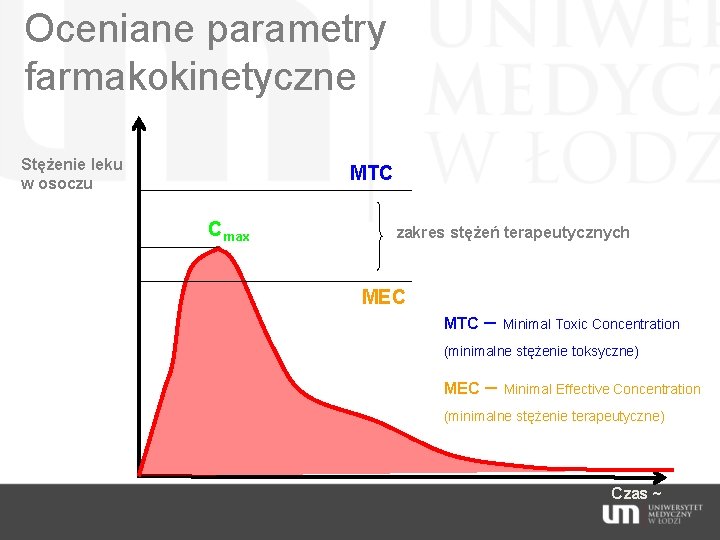
Oceniane parametry farmakokinetyczne Stężenie leku w osoczu MTC Cmax zakres stężeń terapeutycznych MEC MTC – Minimal Toxic Concentration (minimalne stężenie toksyczne) MEC – Minimal Effective Concentration (minimalne stężenie terapeutyczne) Czas ~

Procesy farmakokinetyczne UWALNIANIE WCHŁANIANIE DYSTRYBUCJA METABOLIZM WYDALANIE

Dystrybucja Proces rozmieszczania leku w płynach i tkankach organizmu Czynniki warunkujące dystrybucję: • szybkość przepływu krwi przez poszczególne tkanki (pojęcie kompartmentu) • szybkość transportu przez błony biologiczne • wiązanie z białkami

Kompartment To zespół tkanek, narządów lub płynów ustrojowych, w których lek i jego metabolity są rozmieszczone homogenicznie KOMPARTMENT CENTRALNY (PŁYTKI) Stężenie leku natychmiast osiąga stan równowagi ze stężeniem we krwi KOMPARTMENT TKANKOWY (GŁĘBOKI) Lek osiąga stan równowagi stężeń z kompartmentem centralnym po upływie czasu od zakończenia dystrybucji osocze Tkanka tłuszczowa Skóra Mięśnie Inne tkanki słabiej ukrwione Mózg Serce Wątroba Nerki Erytrocyty Inne tkanki dobrze ukrwione MODEL JEDNOKOMPARTMENTOWY MODEL DWUKOMPARTMENTOWY

Objętość dystrybucji Vd Hipotetyczna objętość płynów ustrojowych, w której po równomiernym rozmieszczeniu lek miałby stężenie takie jak we krwi Vd bezwzględna - wyrażana w litrach Vd względna – wyrażana w litrach/kilogram Vd = A/C A – ilość leku w organizmie [mg] C - stężenie leku we krwi [mg/L]

Objętość dystrybucji znaczenie praktyczne Vd = 5 l - dystrybucja ograniczona jest do krwi Vd = 10 -20 l - przenikanie leku do płynów zewnątrzkomórkowych Vd = 25 -35 l - przenikanie leku do płynów wewnątrzkomórkowych Vd = 40 l - rozmieszczanie we wszystkich płynach organizmu Vd > 100 l - lek silnie kumuluje się w tkankach

Objętość dystrybucji znaczenie praktyczne Obliczenie dawki nasycającej A = Vd x C Dawka nasycająca (Ld) = Vd x Ct x BW Vd – objętość dystrybucji Ct – stężenie terapeutyczne BW – masa ciała w kg F – dostępność biologiczna F

Wiązanie z białkami Odwracalny proces powstawania kompleksu lek-białko Znaczenie kliniczne ma wówczas, gdy stopień wiązania leku z białkami jest większy niż 80% Lek związany z białkami: - jest nieaktywny farmakologicznie - nie może przechodzić przez błony biologiczne - nie ulega metabolizmowi - nie może być wydalony Zmniejszenie stopnia wiązania leku skutkuje: – wzrostem siły działania leku – skróceniem czasu działania leku

Stopień wiązania leku z białkami zależy od: – stężenia leku (wysycenie miejsc wiążących już w zakresie stężeń terapeutycznych dla salicylanów, fenylbutazonu, kwasu walproinowego, prednizolonu) – powinowactwa leku do miejsc wiążących – stężenia białek (wydolność nerek, wątroby, wiek, stan odżywienia itp. . . ) – obecności substancji egzogennych (leki, trucizny środowiskowe) i endogennych (kwasy tłuszczowe, bilirubina, mocznik, hormony) – p. H osocza (spadek wiązania np. barbituranów z białkami w kwasicy)

Przykłady leków o dużym stopniu wiązania z białkami: – – – Pochodne kumaryny Chlorpropamid Fenylobutazon Salicylany Sulfonamidy Penicyliny

Procesy farmakokinetyczne UWALNIANIE WCHŁANIANIE DYSTRYBUCJA METABOLIZM WYDALANIE

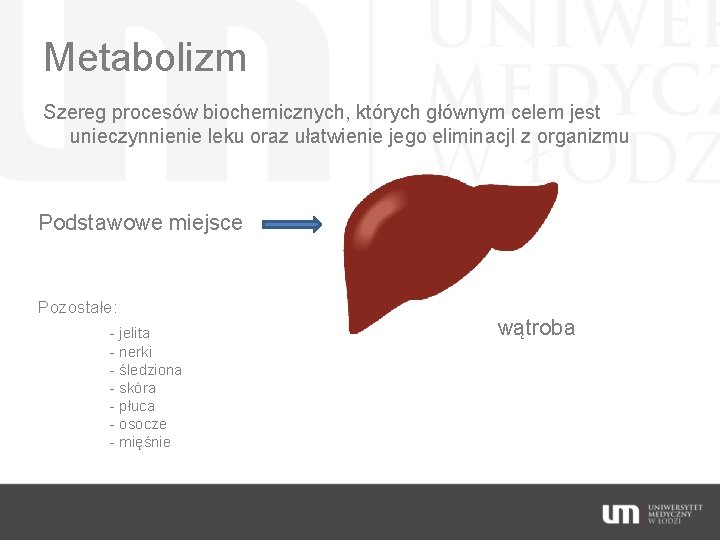
Metabolizm Szereg procesów biochemicznych, których głównym celem jest unieczynnienie leku oraz ułatwienie jego eliminacj. I z organizmu Podstawowe miejsce Pozostałe: - jelita - nerki - śledziona - skóra - płuca - osocze - mięśnie wątroba

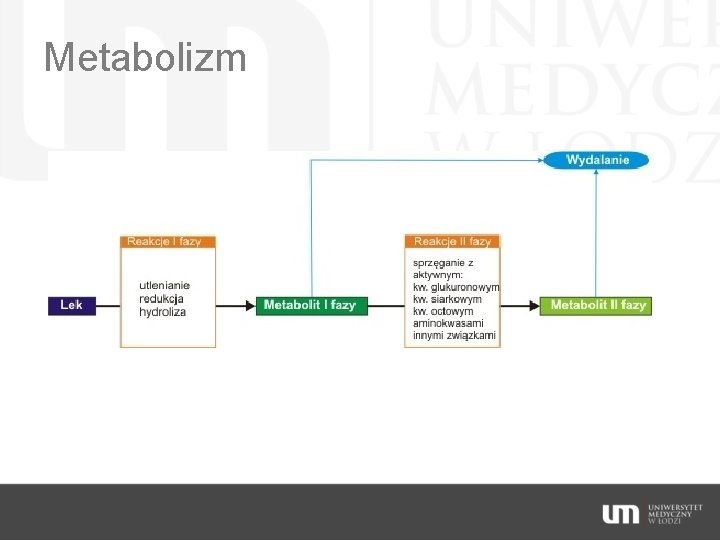
Metabolizm

Metabolizm Procesy I fazy prowadzą do: - inaktywacji leku macierzystego - aktywacji proleku do czynnej farmakologicznie postaci (enalapril) - powstania metabolitu aktywnego farmakologicznie (imipramina) - powstania metabolitu toksycznego (paracetamol) Procesy II fazy prowadzą zwykle do powstania związków nieczynnych farmakologicznie

Czynniki wpływające na metabolizm leków 1. Wiek pacjenta: - Noworodki – niedojrzały układ mikrosomalny - Małe dzieci – przyspieszony metabolizm - Chorzy w wieku podeszłym – zmniejszenie aktywności enzymów mikrosomalnych 1. Płeć (mężczyźni metabolizują szybciej) 2. Stany chorobowe (niewydolność krążenia, marskość wątroby) 3. Interakcje lekowe 4. Czynniki genetyczne

Izoenzymy cytochromu P-450 Najważniejsze: CYP 1 A 2 CYP 2 C 9 CYP 2 C 19 CYP 2 D 6 CYP 2 E 1 CYP 3 A 4 Czynniki warunkujące aktywność izoenzymów: - polimorfizm genetyczny - indukcja i inhibicja

Znaczenie kliniczne indukcji i inhibicji zmiana siły działania stosowanego induktora / inhibitora i innych stosowanych jednocześnie leków Indukcja: → osłabienie siły działania i skrócenie czasu działania w przypadku metabolitów nieaktywnych lub mniej aktywnych → wzrost siły działania w przypadku metabolitów bardziej aktywnych → możliwość działania toksycznego innych stosowanych jednocześnie leków w przypadku odstawienia induktora po uprzedniej korekcji ich dawki

Leki a izoenzymy cytochromu P-450 Inhibitory Cymetydyna Propranolol Erytromycyna Doustne leki antykoncepcyjne Ciprofloksacyna Sok z grapefruita Induktory Alkohol etylowy Barbiturany Nikotyna Rifampicyna

Procesy farmakokinetyczne UWALNIANIE WCHŁANIANIE DYSTRYBUCJA METABOLIZM WYDALANIE

Wydalanie Procesy związane z usuwaniem leku z organizmu Drogi wydalania: – Przez nerki (większość leków) – Z żółcią (makrolidy, glikozydy) – Ze śliną (fenytoina) – Z powietrzem wydychanym (alkohol, środki znieczulenia ogólnego) – Z potem (witamina B 1)

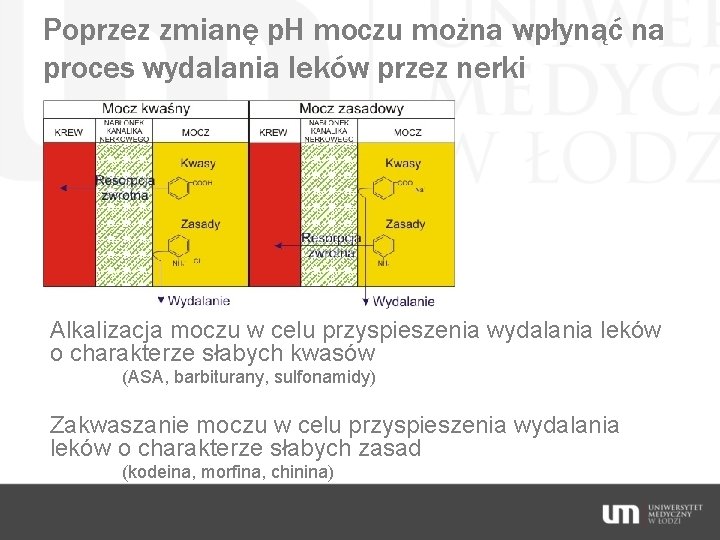
Poprzez zmianę p. H moczu można wpłynąć na proces wydalania leków przez nerki Alkalizacja moczu w celu przyspieszenia wydalania leków o charakterze słabych kwasów (ASA, barbiturany, sulfonamidy) Zakwaszanie moczu w celu przyspieszenia wydalania leków o charakterze słabych zasad (kodeina, morfina, chinina)

Klirens leku (Cl) Objętość osocza całkowicie oczyszczonego z leku w jednostce czasu przez narząd eliminujący ten lek z organizmu Cl = K x Vd Klirens całkowity Cl. T = Cl. R + Cl. H + Cl. X Przykład Propranolol Cl. T=849 ml/min, Cl. H = 840 ml/ml, Cl. R = 8 ml/min

Biologiczny okres półtrwania Czas, po upływie którego stężenie leku we krwi, po zakończonej dystrybucji zmniejsza się o połowę Pozwala określić odstępy dawkowania leków t½ = 0, 693 K t½ = 0, 693 x Vd Cl

Biologiczny okres półtrwania zależy od: – czynniki genetyczne – płeć – wiek – wydolności układu krążenia, wątroby i nerek – stan enzymów mikrosomalnych wątroby

Stała eliminacji (K) Określa szybkość usuwania określonej porcji leku z kompartmentu centralnego jako konsekwencji metabolizmu i wydalania K reprezentuje również frakcję objętości dystrybucji, która zostaje oczyszczona z substancji leczniczej w jednostce czasu K= K – stała eliminacji Cl – klirens leku Vd – objętość dystrybucji Cl Vd

Dawka podtrzymująca Ld = Cl x Cssp x T F Cl - klirens leku Cssp – stężenie stacjonarne leku T - odstęp dawkowania F – dostępność biologiczna

Stężenie stacjonarne Stan równowagi pomiędzy ilością leku wprowadzanego do organizmu i przez niego wydalanego (metabolizm + eliminacja) Uwarunkowane głównie przez podawanie kolejnych dawek leku oraz klirens leku Spadek klirensu może stwarzać ryzyko przedawkowania!!! Jest ono osiągane po 4 -5 okresach t½ od podania pierwszej dawki

Farmakokinetyka Liniowa - szybkość procesów farmakokinetycznych jest proporcjonalna do stężenia leku Nieliniowa - szybkość procesów farmakokinetycznych zmienia się wraz ze zmianą stężenia leku w sposób nieliniowy

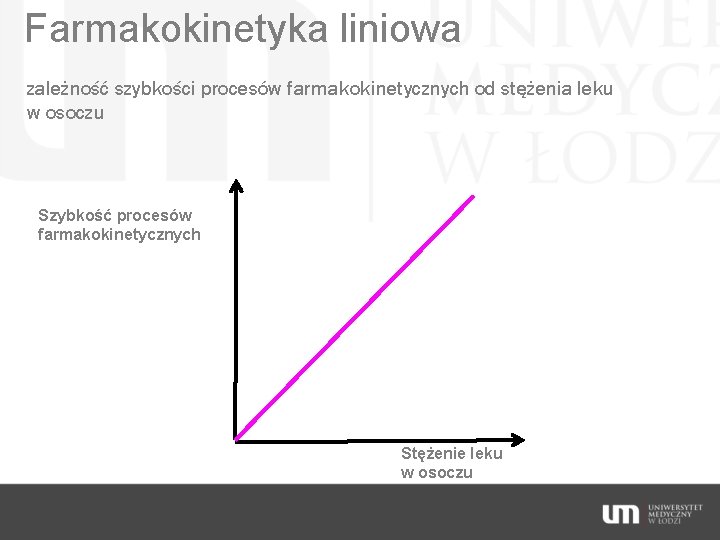
Farmakokinetyka liniowa zależność stężenia leku w osoczu od podanej dawki Stężenie leku w osoczu C 2 C 1 D 2 Podana dawka leku

Farmakokinetyka liniowa zależność szybkości procesów farmakokinetycznych od stężenia leku w osoczu Szybkość procesów farmakokinetycznych Stężenie leku w osoczu

Charakterystyka procesów przebiegających według kinetyki liniowej – t½, Vd, Cl jest stały, niezależny od dawki – AUC jest proporcjonalne do dawki – stężenie w stanie stacjonarnym jest proporcjonalne do dawki

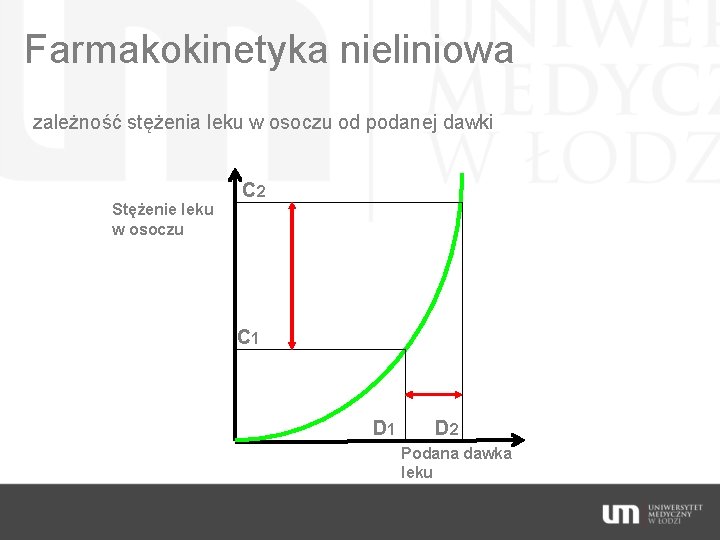
Farmakokinetyka nieliniowa zależność stężenia leku w osoczu od podanej dawki C 2 Stężenie leku w osoczu C 1 D 2 Podana dawka leku

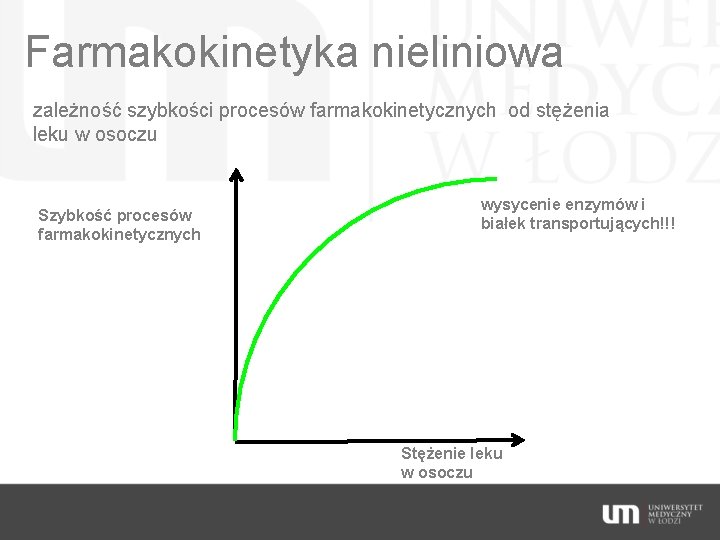
Farmakokinetyka nieliniowa zależność szybkości procesów farmakokinetycznych od stężenia leku w osoczu Szybkość procesów farmakokinetycznych wysycenie enzymów i białek transportujących!!! Stężenie leku w osoczu

Charakterystyka procesów przebiegających według kinetyki nieliniowej – szybkość procesów eliminacji nie jest proporcjonalna do stężenia leku – t½ ulega wydłużeniu wraz ze wzrostem dawki – AUC i stężenie w stanie stacjonarnym nie jest proporcjonalne do ilości leku

Zagrożenia wynikające z kinetyki nieliniowej ! niewielkie zmiany dawkowania mogą prowadzić do ujawnienia działania toksycznego ! eliminacja i osiągnięcie stanu stacjonarnego mogą wydłużać się w sposób nieoczekiwany

Leki podlegające prawom kinetyki nieliniowej – – – – Salicylany Fenytoina Prednizolon Dikumarol Teofilina Winkrystyna TLPD (po przedawkowaniu)

Podsumowanie 1. Obliczyć dawkę nasycającą digoksyny dla mężczyzny o masie 70 kg, mając następujące dane Vd = 7, 3 L/kg, Ct = 1, 5 ng/m. L, F = 0, 62, BW = 70 kg
![Rozwiązanie 1 Dawka nasycająca Vd x Ct x BWF 7 3 Lkg Rozwiązanie 1. Dawka nasycająca = Vd x Ct x BW/F = 7, 3 [L/kg]](https://slidetodoc.com/presentation_image_h/8efb12a04cb0559f92f1305da8f62501/image-58.jpg)
Rozwiązanie 1. Dawka nasycająca = Vd x Ct x BW/F = 7, 3 [L/kg] x 1, 5 [mg/L] x 70 kg / 0, 62 = 1, 2 mg

Działania niepożądane leków

Farmaksologia nauka zajmująca się objawami niepożądanymi działania leków

Działanie niepożądane (ADR adverse drug reaction) Każda szkodliwa i niezamierzona reakcja organizmu występująca po zastosowaniu leku w dawkach przeciętnie stosowanych zgodnie ze wskazaniami (które służą zapobieganiu, diagnozie lub leczeniu)

Efekt uboczny/ zdarzenie niepożądane (AE adverse event) Każda niepożądana reakcja, występująca u pacjenta lub osoby biorącej udział w badaniu klinicznym, niezależnie od tego czy jest uznana za związaną z danym lekiem, czy też nie.

Działanie toksyczne Powstaje w wyniku przedawkowania leku (przekroczenie maksymalnej dawki leczniczej)

Czynniki sprzyjające wystąpieniu ADR - Cechy leku: właściwości fizykochemiczne, farmakokinetyczne, farmakodynamiczne, postać leku, stosowana dawka, częstość i droga podawania oraz interakcje z innymi lekami. - Cechy osobnicze chorego: - fizjologiczne: wiek, płeć, masa ciała, uwarunkowania genetyczne, ciąża, wysiłek fizyczny, sposób odżywiania - patologiczne: choroby współistniejące - uczulenie na leki - stosowanie używek: alkohol, tytoń - szkodliwy wpływ środowiska

Klasyfikacja kliniczna działań niepożądanych Rawlins’a • • • Reakcje typu A Reakcje typu B Reakcje typu C Reakcje typu D Reakcje typu E

Działanie niepożądane leków typu A (drug actions) • • • Przewidywalne - zależne od właściwości farmakologicznych leku Interakcje międzylekowe odwracalne i ustępują już po obniżeniu dawki stanowią 70 -80% wszystkich działań niepożądanych Przykłady: kaszel po zastosowaniu inhibitorów konwertazy angiotensyny.

Działanie niepożądane leków typu B (patient reactions) • Nieprzewidywalne - reakcje niezależne od dawki i mechanizmu działania leku • często o podłożu immunologicznym, o lekkim lub ciężkim przebiegu, nawet zagrażające życiu • Stanowią 20 -25% działań niepożądanych • reakcje alergiczne, które mogą być: – ostre i przenoszone przez immunoglobuliny typu Ig. E lub Ig. G (wstrząs anafilaktyczny, reakcje skórne) – wynikiem procesów autoimmunologicznych (układowy toczeń rumieniowaty) – reakcją typu Arthusa, przenoszoną przez immunoglobuliny Ig. G i Ig. M (do tej grupy należy choroba posurowicza) – wynikiem dziedzicznych skłonności czy cech np. deficyt dehydrogenazy glukozo-6 fosforanowej, nietypowy metabolizm, kumulacja toksycznych metabolitów •

Różnice pomiędzy niepożądanymi działaniami leków typu A i B Typ A Typ B możliwe do przewidzenia nieprzewidywalne zwykle zależne od dawki rzadko zależne od dawki występują często występują rzadko są powodem zgonu związane z wyższą w stosunku do typu A częstością zgonów zmniejszone nasilenie lub ustąpienie po zmniejszeniu dawki zwykle wymagają przerwania podawania leku

Działanie niepożądane leków typu C (not true drug actions) Reakcje występujące często przy podawaniu określonego leku, ale nie można jednoznacznie powiązać ich z tym lekiem Przykłady: zakrzepica u kobiet stosujących hormonalne środki antykoncepcyjne.

Działanie niepożądane leków typu D (retarded actions) Reakcje pojawiające się z opóźnieniem Przykłady: działanie teratogenne talidomidu, uszkodzenie serca po antracyklinach (nawet po 15 latach od zakończenia leczenia)

Działanie niepożądane leków typu E Reakcje występujące po nagłym odstawieniu leku, powodujące zaostrzenie objawów choroby ponad poziom na którym te objawy byłyby, gdyby leku w ogóle nie zastosowano Przykłady: zwiększenie poziomu gastryny prowadzące do wyrzutu HCl w żołądku po odstawieniu antagonistów receptorów H 2 w żołądku

Rodzaje działań toksycznych – Działanie hepatotoksyczne – Działanie nefrotoksyczne – Działanie kardiotoksyczne – Działanie ototoksyczne – Działanie teratogenne – Działanie karcynogenne

Działanie hepatotoksyczne – Uszkodzenie hepatocytów i wątroby najczęściej w wyniku biotransformacji leków zachodzącej przy współudziale cytochromu P 450 – Objawia się podwyższonym stężeniem Asp. AT i Al. AT lub stanem zapalnym – Paracetamol przyjmowany w dawkach przekraczających dawki lecznicze może tworzyć metabolity o silnym działaniu hepatotoksycznym, uszkodzenie wątroby może nastąpić gdy wyczerpane zostaną zasoby glutationu wątrobowego niezbędnego do unieszkodliwienia toksycznego metabolitu Nacetylobenzochinoiminy, proces ten może być nasilony w przypadku równoczesnego podania związków będących induktorami układów enzymatycznych wątroby

Działanie nefrotoksyczne • Nerki jako narząd odpowiedzialny za wydalanie leków lub ich metabolitów w szczególny sposób narażony jest na szkodliwe działanie leków • Objawia się to: zagęszczeniem moczu, zwiększeniem stężenia leku w kanalikach nerkowych • Szkodliwe może byś również krystalizacja leku w wyniku zmiany p. H moczu • Leki wykazujące działanie nefrotoksyczne: – Antybiotyki aminoglikozydowe – jako związki o silnym charakterze zasadowym wiążą się z fosfoinozytolowymi fragmentami błon cewki nerkowej oraz tworząc kompleksy zaburzają czynność komórek i prowadzą do ich martwicy – Diagnostyczne środki cieniujące – zwiększenie radiologicznych środków uszkadza cewke nerkową • Kontrolę funkcji nerek należy prowadzić w przypadku terapii lekami przeciwnowotworowymi, przeciwwirusowymi, immunosuupresyjnymi • Działanie nefrotoksyczne jest zwykle odwracalne

Działanie kardiotoksyczne • • • Wydłużenie odstępu QT w EKG co jest związane z wpływem leków na kanały potasowe w kardiomiocytach, prowadzące do zaburzenia kurczliwości mięśnia sercowego predysponujących do arytmii komorowych, migotania komór i nagłej śmierci Przykłady: leki z grupy fluorochinolonów, antybiotyki makrolidowe, neuroleptyki Antybiotyki antracyklinowe generują tworzenie wolnych rodników hydroksylowych w wyniku przemiany chinonów do hydrochinonów, które powodują peroksydację lipidów i zaburzają czynność błon komórkowych (wpływ na wymianę Na+ i Ca 2+). Wzrost stężenia Ca 2+ wewnątrz kardiomiocytów zaburza kurczliwość i rytm serca

Działanie ototoksyczne • • • Degeneracja komórkowa lub upośledzenie czynności ucha wewnętrznego Antybiotyki aminoglikozydowe (gentamycyna, streptomycyna, tobramycyna) tworzą trwale kompleksy, które zaburzają funkcję komórek nabłonka zmysłowego ślimaka w wyniku ich kumulacji w limfie ucha środkowego (może pojawić się już po kilku dniach leczenia) Cytostatyki, szczególnie związki platyny również uszkadzają narząd słuchu ( nawet u 30% leczonych)

Działanie rakotwórcze (Działanie karcynogenne ) • może wystąpić dopiero po dłuższym okresie utajenia • leki rakotwórcze: niektóre środki cieniujące, leki stosowane w nadczynności tarczycy, cytostatyki, uretany, sulfonamidy, izoniazyd, estrogeny i gryzeofulwina – karcynogeny genotoksyczne (mutageny) - działają bezpośrednio na DNA, pobudzają transformację nowotworową przez zmiany w protoonkogenach lub genach supresorowych. – karcynogeny epigenetyczne - nie powodują uszkodzeń genetycznych lecz zwiększają prawdopodobieństwo wystąpienia nowotworu w wyniku nieprawidłowego różnicowania komórek

Działanie embriotoksyczne, embriopatie – w okresie organogenezy zarodka (okres embrionalny do 60 dnia ciąży), – ciężkie uszkodzenia i/lub obumarcie płodu – leki embriotoksyczne: cytostatyki, talidomid – inne czynniki: niedobór kwasu foliowego, różne związki chemiczne

Działanie teratogenne ("potworotwórcze" od teratos - potwór), fetopatie • w okresie rozwoju płodu (okres płodowy - od 60 dnia ciąży do porodu) • Uszkodzenie płodu i powstanie ciężkich wrodzonych wad rozwojowych • leki teratogenne: cytostatyki, leki przeciwpadaczkowe, retinoidy, alkohol (najczęstsza przyczyna!), antybiotyki (penicylina, tetracykliny), sulfonamidy, talidomid (środek nasenny).

Zwiększone ryzyko poronienia występuje po zastosowaniu prostaglandyn, alkaloidów sporyszu i środków wywołujących znieczulenie ogólne

Zgłaszanie działań niepożądanych – Zgłoszenia spontaniczne od przedstawicieli zawodów medycznych – Okresowe raporty firm farmaceutycznych dotyczące bezpieczeństwa produktu leczniczego

Zgłaszanie działań niepożądanych • Jest obowiązkiem każdego pracownika opieki zdrowotnej, jak również farmaceuty • Zobowiązują do tego następujące akty prawne: – Ustawa z dnia 5 grudnia 1996 o zawodzie lekarza, – Ustawa z dnia 6 września 2001 Prawo Farmaceutyczne, – Rozporządzenie Ministra Zdrowia z dnia 17 lutego 2003 w sprawie monitorowania bezpieczeństwa produktów leczniczych, – Dyrektywa Unii Europejskiej 2001/83/EC • Działanie niepożądane powinno być zgłoszone podmiotowi odpowiedzialnemu za wprowadzenie na rynek leku lub substancji, a w przypadku niemożności jego ustalenia do Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych • Zgłoszenia krajowe są następnie przekazywane do międzynarodowej bazy danych, która mieści się w Uppsali w Szwecji

Żółta Karta

Formularz CIOMS

Okresowe raporty firm dotyczące bezpieczeństwa (PSUR – Periodic Safety Update Report) – Przez pierwsze 2 lata – co 6 miesięcy – Przez następne 3 lata – co 12 miesięcy – Następnie ewentualnie co 5 lat przy odnowieniu rejestracji
 Lekw
Lekw Lekw
Lekw Synergizm addycyjny
Synergizm addycyjny Lekw
Lekw Lekw
Lekw Lekw
Lekw Płomień kinetyczny
Płomień kinetyczny Vhdl automat
Vhdl automat Podstawy fizykochemii spalania
Podstawy fizykochemii spalania Osnowa dokumentu
Osnowa dokumentu Teoretyczne podstawy informatyki
Teoretyczne podstawy informatyki Podstawy kryptografii
Podstawy kryptografii Teoretyczne podstawy informatyki
Teoretyczne podstawy informatyki Monitorowanie realizacji podstawy programowej
Monitorowanie realizacji podstawy programowej Realizacja podstawy programowej w edukacji wczesnoszkolnej
Realizacja podstawy programowej w edukacji wczesnoszkolnej Wzór na pole powierzchni całkowitej graniastosłupa
Wzór na pole powierzchni całkowitej graniastosłupa Studnia potencjału
Studnia potencjału Język sql - podstawy zapytań
Język sql - podstawy zapytań Menisk
Menisk Spalanie bezpłomieniowe żarzenie
Spalanie bezpłomieniowe żarzenie Bpmn podstawy
Bpmn podstawy Podstawy miernictwa elektrycznego
Podstawy miernictwa elektrycznego Podstawy projektowania i implementacji baz danych
Podstawy projektowania i implementacji baz danych Podstawy savoir vivre
Podstawy savoir vivre Zasada prac przygotowanych belka
Zasada prac przygotowanych belka Program do tworzenia stron html
Program do tworzenia stron html Monitorowanie podstawy programowej wzór
Monitorowanie podstawy programowej wzór Spis liter cyfr i innych znaków danego kroju pisma
Spis liter cyfr i innych znaków danego kroju pisma Edukacja formalna i nieformalna
Edukacja formalna i nieformalna Php podstawy
Php podstawy Slidetodoc
Slidetodoc Podstawy akustyki
Podstawy akustyki Warunki realizacji podstawy programowej
Warunki realizacji podstawy programowej Podstawy hydrauliki
Podstawy hydrauliki Podstawy sztucznej inteligencji
Podstawy sztucznej inteligencji Maria dems
Maria dems Najnowsza podstawa programowa z religii
Najnowsza podstawa programowa z religii