Pitanje zato ova buba moe da hoda po

Pitanje: zašto ova buba može da hoda po površini vode? Odgovor: Na granici između vode i vazduha postoji uređen sloj molekula vode povezanih međusobno i sa molekulima u unutrašnjosti vodoničnim vezama. Stoga se voda ponaša kao da je prekrivena nevidljivim filmom koji je otporan na razvlačenje i kidanje. Površinski napon je mera teškoće da se površina tečnosti razvuče ili iskida. Buba ima relativno malu masu ravnomerno raspoređenu po velikoj površini. Stoga njena težina ne prevazilazi površinski napon vode i buba hoda po površini.

Pitanje: zašto mali predmeti plivaju po površini vode? Odgovor: Veličina objekta ne određuje da li će on plivati ili tonuti. Mali predmeti će tonuti u vodu ako je masa skoncentrisana na malu površinu tj. kada je pritisak tako veliki da vodonične veze na površini vode ne mogu da ga nadvladaju.
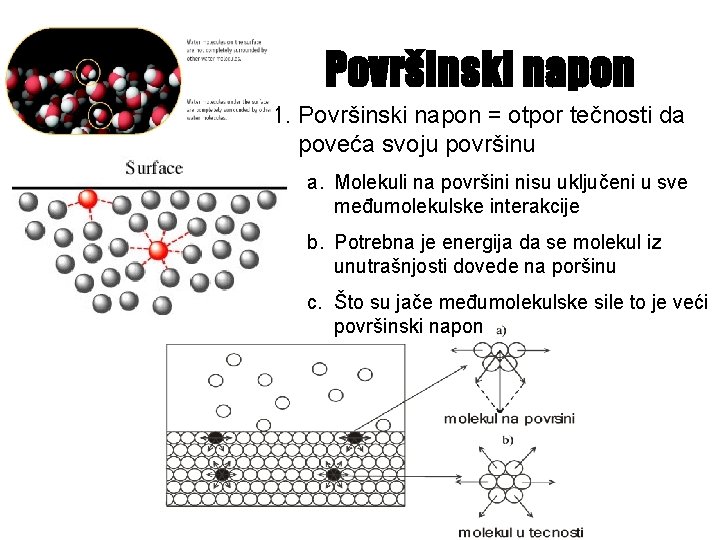
Površinski napon 1. Površinski napon = otpor tečnosti da poveća svoju površinu a. Molekuli na površini nisu uključeni u sve međumolekulske interakcije b. Potrebna je energija da se molekul iz unutrašnjosti dovede na poršinu c. Što su jače međumolekulske sile to je veći površinski napon

Površina tečnosti: Površinski napon Tečnosti imaju jedinstvenu osobinu da zauzimaju oblik koji ima za datu zapreminu minimalnu površinu v. Najmanji odnos površina-zapremina: sferna kapljica v. Maksimalan broj molekula iz čitave zapremine interaguje sa susednim molekulima v. Druge sile mogu da se suprotstavljaju tendenciji za zauzimanje idealnog oblika (npr. gravitacija izdužuje sferu pri formiranju kapljice, formiraju se okeani, jezera i sl. )
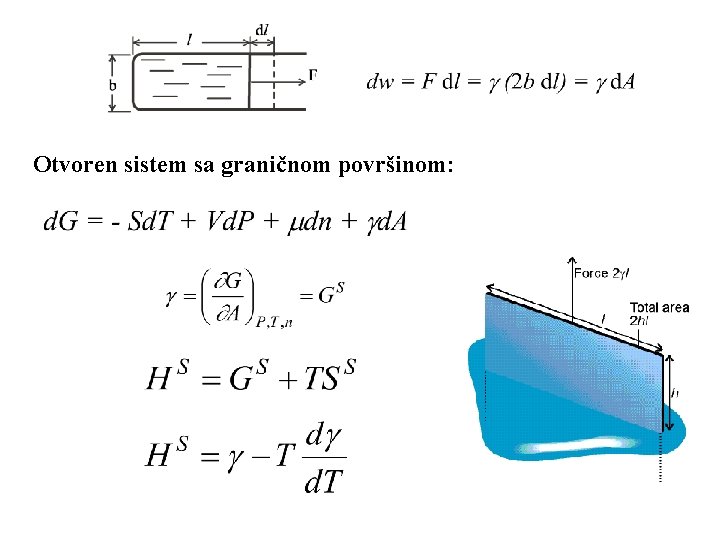
Otvoren sistem sa graničnom površinom:

Helmholz-ova i Gibbs-ova energija se koriste za izražavanje količine rada potrebnog za promenu površine. Pri različitim uslovima, d. A i d. G odgovaraju radu izvršenom pri promeni površine sistema za d. A: Øpri konstantnom pritisku P i T: d. G= d. A gde je konstanta proporcionalnosti, , poznata kao povišinski napon, a ima jedinice: J m-2 ili N m-1(pošto je 1 J =1 N m). ØPri konstantnoj zapremini V i T: d. A= d. A Promena Gibsove slobodne energije pri beskonačno maloj promeni temperature, pritiska, količine supstancije i površine je: d. G = - Sd. T + Vd. P + dn + d. A površinska Gibsova slobodna energija površinska entalpija

Ugao dodira
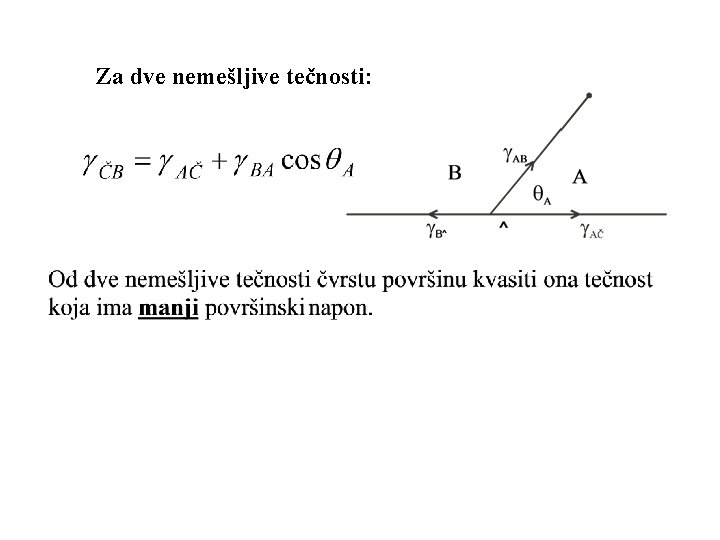
Za dve nemešljive tečnosti:
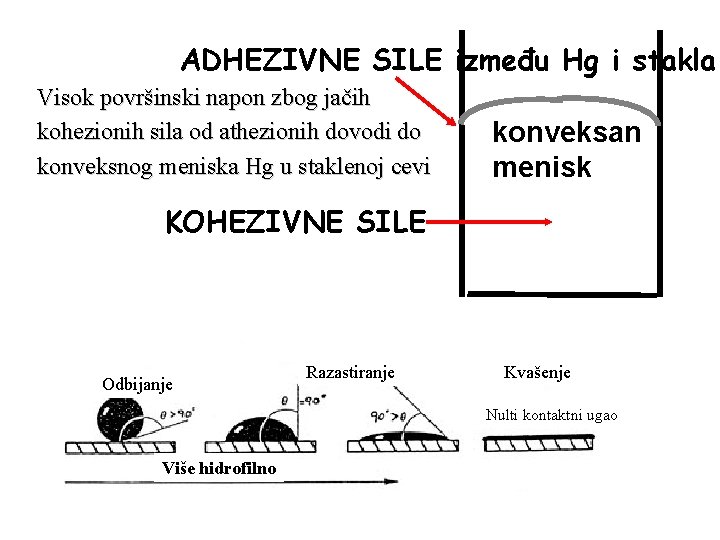
ADHEZIVNE SILE između Hg i stakla Visok površinski napon zbog jačih kohezionih sila od athezionih dovodi do konveksnog meniska Hg u staklenoj cevi konveksan menisk KOHEZIVNE SILE Odbijanje Razastiranje Kvašenje Nulti kontaktni ugao Više hidrofilno

Athezioni rad Kohezioni rad

Ugao dodira Athezioni rad tečnosti po jedinici površine kontakta je: odakle je ugao dodira: c>0, wad> lg-tečnost kvasi površinu c<0, wad< lg-tečnost ne kvasi površinu Za živu c=1400, tako da je wad/ lg=0, 23, što znači mali athezioni rad između žive i stakla, zbog jakih kohezionih sila u živi. Ugao dodira za kerozin je 260 a za vodu 00 (ako je površina stakla idealno čista).

Adhezione i kohezione sile na površini
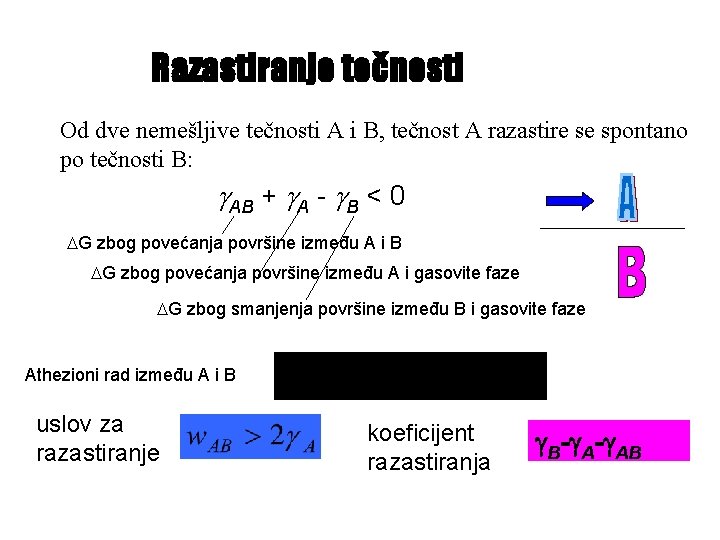
Razastiranje tečnosti Od dve nemešljive tečnosti A i B, tečnost A razastire se spontano po tečnosti B: AB + A - B < 0 G zbog povećanja površine između A i B G zbog povećanja površine između A i gasovite faze G zbog smanjenja površine između B i gasovite faze Athezioni rad između A i B uslov za razastiranje koeficijent razastiranja B- A- AB
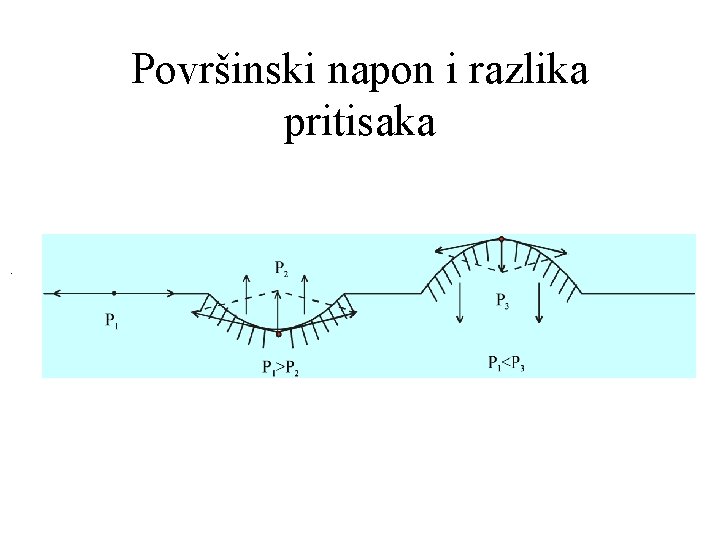
Površinski napon i razlika pritisaka .

Krive površine Površina za datu zapreminu tečnosti može biti smanjena formiranjem krive površine, kao kod mehura. Posledice zakrivljenosti površine su: 1. Napon pare tečnosti zavisi od zakrivljenosti površine 2. Pritisak ispod površine zavisi od njene zakrivljenosti-kapilarnost Balon: oblast u kojoj je para zarobljena tankim filmom koji ima dve površine Mehur-šupljina: parom ispunjena šupljina u tečnosti-jedna površina Kapljica: mala zapremina tečnosti u ravnoteži sa okružujućom parom
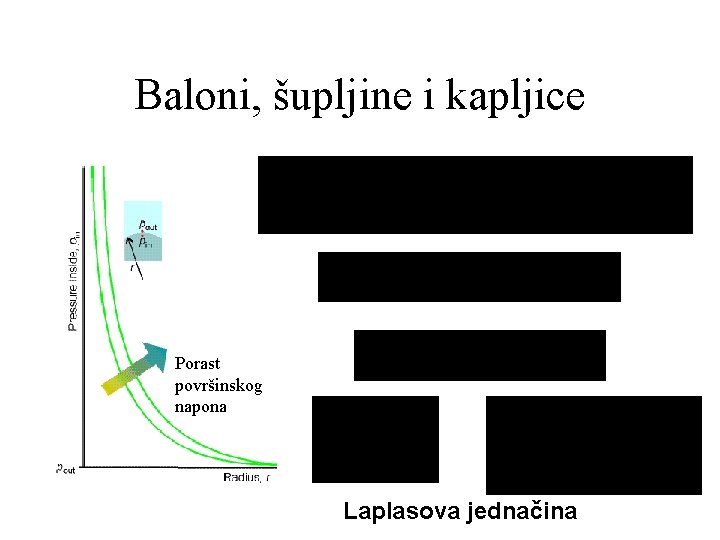
Baloni, šupljine i kapljice mmmmmm mmmmmm mmm Porast mmm površinskog mmm napona mmm Laplasova jednačina

Površinski napon i razlika pritisaka Laplasova jednačina: pritisak na konkavnoj strani dodirne površine P 2 veći je od pritiska sa konveksne strane P 1: P 2 P 1 Razlika u pritisku opada na nulu kada je radijus krivine beskonačan (ravna površina) Unutar zakrivljenih površina malog radijusa krivine pritisak je veliki u odnosu na spoljnji pritisak

Oblici mehura Najmanja površina za datu zapreminu tečnosti je sfera. Oblik br. strana zapremina površina (cm 3) (cm 2) tetraedar 4 16, 4 46, 5 kocka 6 16, 4 38, 7 oktaedar 8 16, 4 36, 9 dodekadear 12 16, 4 34, 3 ikosaedar 20 16, 4 33, 2 sfera 16, 4 31, 2
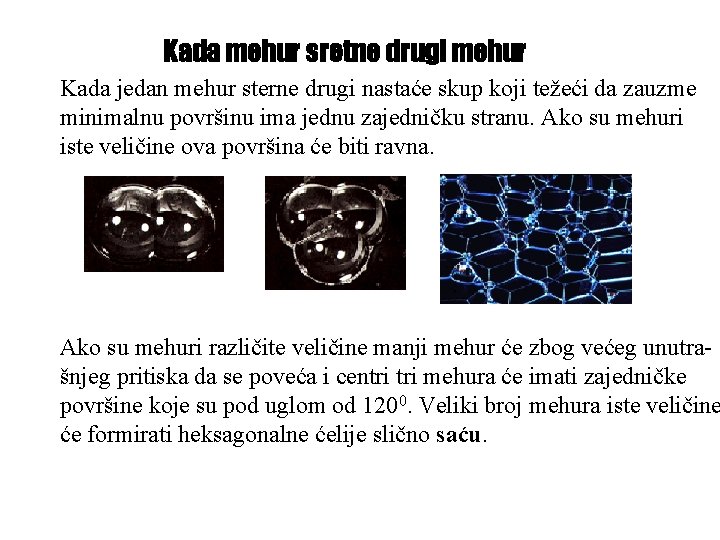
Kada mehur sretne drugi mehur Kada jedan mehur sterne drugi nastaće skup koji težeći da zauzme minimalnu površinu ima jednu zajedničku stranu. Ako su mehuri iste veličine ova površina će biti ravna. Ako su mehuri različite veličine manji mehur će zbog većeg unutrašnjeg pritiska da se poveća i centri mehura će imati zajedničke površine koje su pod uglom od 1200. Veliki broj mehura iste veličine će formirati heksagonalne ćelije slično saću.
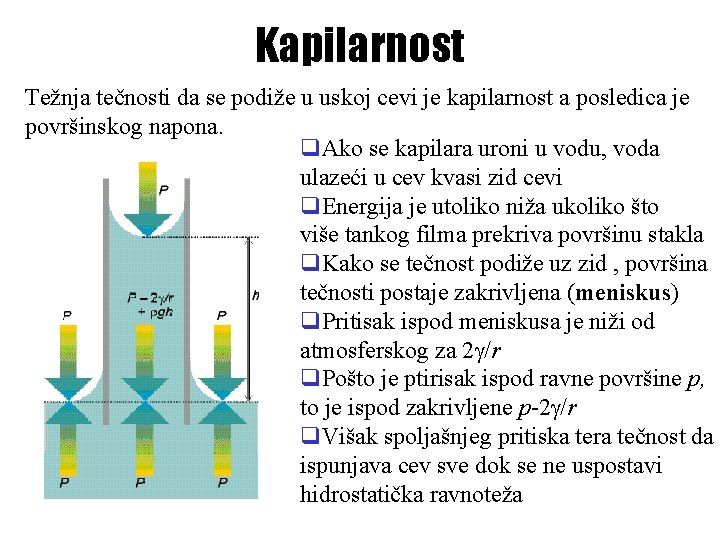
Kapilarnost Težnja tečnosti da se podiže u uskoj cevi je kapilarnost a posledica je površinskog napona. q. Ako se kapilara uroni u vodu, voda ulazeći u cev kvasi zid cevi q. Energija je utoliko niža ukoliko što više tankog filma prekriva površinu stakla q. Kako se tečnost podiže uz zid , površina tečnosti postaje zakrivljena (meniskus) q. Pritisak ispod meniskusa je niži od atmosferskog za 2 /r q. Pošto je ptirisak ispod ravne površine p, to je ispod zakrivljene p-2 /r q. Višak spoljašnjeg pritiska tera tečnost da ispunjava cev sve dok se ne uspostavi hidrostatička ravnoteža
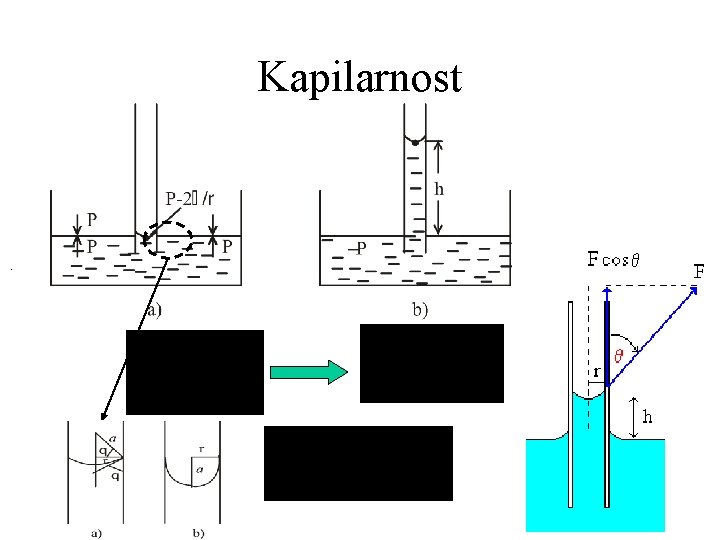
Kapilarnost .

Kapilarno podizanje Pritisak stuba tečnosti gustine je: bb ovaj pritisak uravnotežava razliku pritiska 2 /r, pa je visina stuba bb tečnosti u kapilari: bb bb Primer: Ako se voda na 250 C (gustine 0, 9971 g/cm 3) podiže u cevi radijusa 0, 20 mm za 7, 36 cm površinski napon vode je:
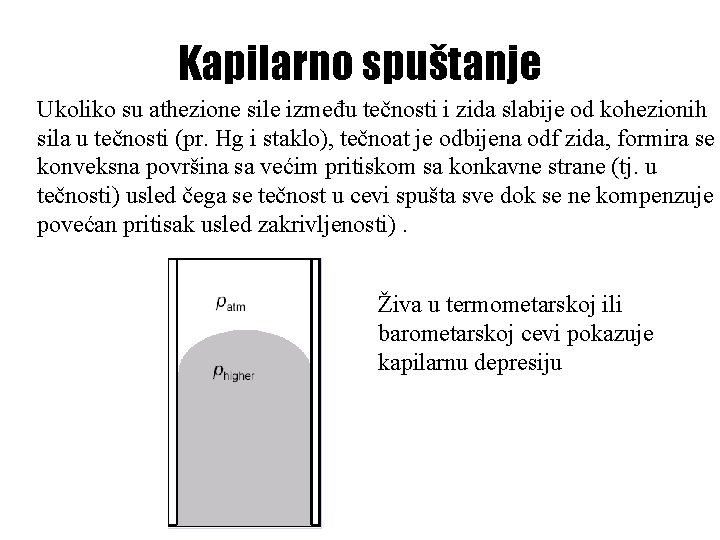
Kapilarno spuštanje Ukoliko su athezione sile između tečnosti i zida slabije od kohezionih sila u tečnosti (pr. Hg i staklo), tečnoat je odbijena odf zida, formira se konveksna površina sa većim pritiskom sa konkavne strane (tj. u tečnosti) usled čega se tečnost u cevi spušta sve dok se ne kompenzuje povećan pritisak usled zakrivljenosti). Živa u termometarskoj ili barometarskoj cevi pokazuje kapilarnu depresiju

Meniscus vode i žive

Kapilarno dejstvo Kohezione sile nasuprot gravitacionih Kretanje vode naviše uz hromatografski papir zavisi od H-veza između H 2 O i OH grupa celuloze. Problem : Naći primenu kapilarnog dejstva u prirodi i laboratoriji

Primer biljnog soka u drveću Da li se sok u drveću podiže usled kapilarnosti i koliko? Pretpostavimo da je sok uglavnom voda ( = 103 kgm-3), kontaktni ugao je 0 , radijus kapilara je 2, 5 x 10 -5 m. Za vodu je = 7, 28 x 10 -2 Nm-1

Pritisak u kapilarama drveta se može meriti ovim uređajem (5 -50 atm)
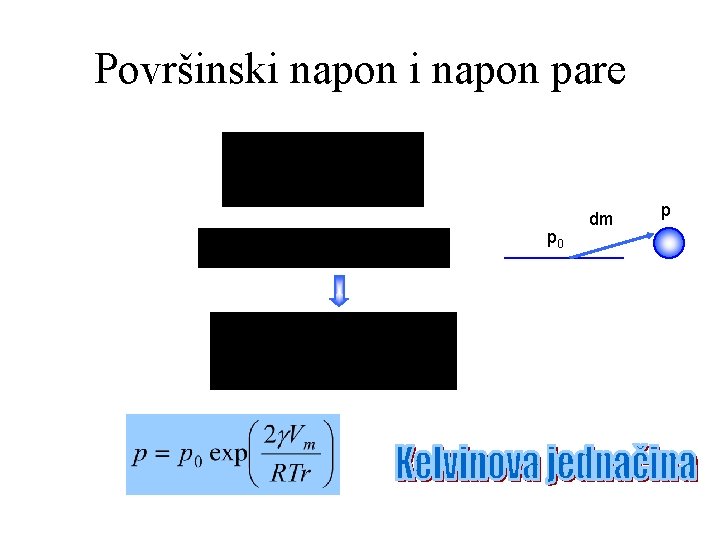
Površinski napon pare p 0 dm p
Nukleacije Za kapljicu radijusa 1 m ili 1 nm odnos p/p 0 prezasićeno je 1, 003 ili 3 (mada u poslednjem slučaju kapljica sadrži svega 10 molekula u dijametru i pitanje je koliko važi primena Kelvinove jednačine) što je malo ali može imati ozbiljne posledice u praksi. Razmotrimo formiranje oblaka: üTopal, vlažan vazduh se penje naviše üTemperatura opada i u nekom momentu će para postati termodinamički nestabilna, postojaće težnja ka kondenzaciji üRojevi molekula vode se skupljaju u tako male kapljice da one imaju povećan napon pare i umesto da se kondenzuju one isparavaju tj. ostaju u stanju presićene pare (težnja ka kondenzaciji je nadvladana težnjom ka isparavanju usled povećanog napona pare iznad krive površ. )

Nukleacije-2 Postoje dva mehanizma formiranje oblaka: v. Dovoljno veliki broj molekula se skuplja u kapljicu čije su dimenzije tolike da da je težnja ka isparavanju zanemarljivo mala (spontana nukleacija)-mala verovatnoća da se ovo dogodi vČestice prašine ili druge materije predstavljaju centre nukleacije za koje se lepe molekuli vode tako da se formiraju dovoljno velike kapljice koje su termodinamički stabilne i dešava se kondenzacija Tečnosti mogu biti pregrejane iznad tačke ključanja ili prehlađene ispod tačke mržnjenja-termodinamički stabilna faza se ne formira-na račun kinetičke stabilizacije u odsustvu centara nukleacije v. Maglena komora-veoma čista superzasićena smeša vodene pare i vazduha, do kondenzacije ne dolazi sve dok kroz komoru ne proleti elementarna čestica koja vrši jonizaciju na svom putu.
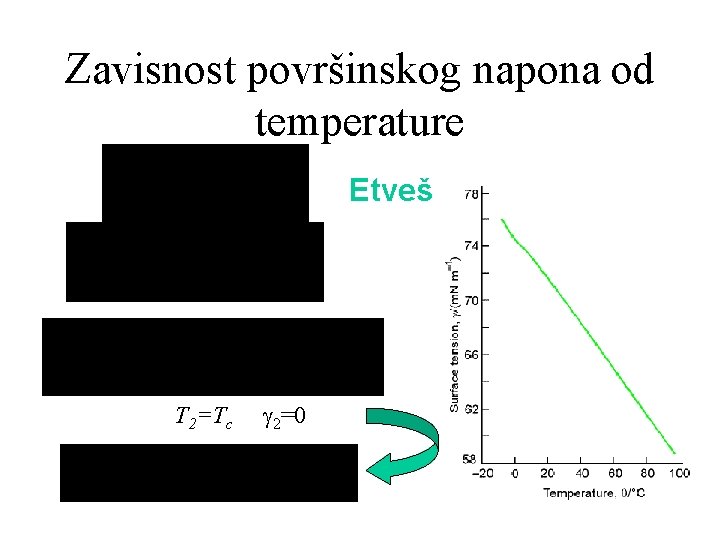
Zavisnost površinskog napona od temperature Etveš T 2=Tc 2=0 nn nn nn

Zavisnost površinskog napona od temperature-nastavak Druge empirijske jednačine: Remzi i Šilds Vand der Vals
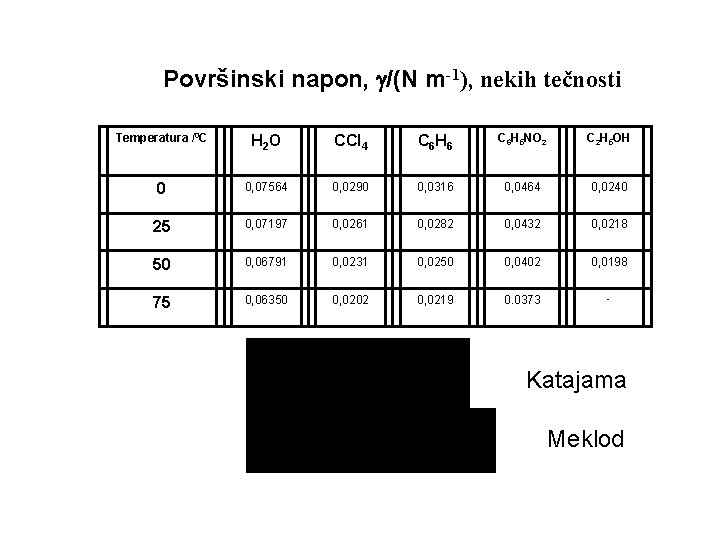
Površinski napon, /(N m-1), nekih tečnosti Temperatura /0 C H 2 O CCl 4 C 6 H 6 C 6 H 5 NO 2 C 2 H 5 OH 0 0, 07564 0, 0290 0, 0316 0, 0464 0, 0240 25 0, 07197 0, 0261 0, 0282 0, 0432 0, 0218 50 0, 06791 0, 0231 0, 0250 0, 0402 0, 0198 75 0, 06350 0, 0202 0, 0219 0. 0373 - Katajama Meklod

VISKOZNOST je težnja za otporom tečnosti proticanju. Da li očekujete da će glicerol imati veću ili manju viskoznost od etanola? Etanol Glicerol Otpor proticanju je rezultat nekoliko faktora, uključujući međumolekulske interakcije, oblik i veličinu molekula.

Veličina i viskoznost • Koji molekul bi lakše isticao iz boce? • Koji bi pokazivao veće trenje? • Kako to utiče na viskoznost?

Viskoznost tečnosti Viskoznost predstavlja otpor kojim se pojedini slojevi tečnosti suprostavljaju kretanju jednog u odnosu na drugi, odnosno to je vrsta unutrašnjeg trenja koja dovodi do protoka fluida konstanom brzinom. Voda Sirup § Koja suspstancija ima veću viskoznost? § Kako se to može meriti? Koeficijent viskoznosti, , brojno jednak sili koja između slojeva jedinične površine, održava jedinični gradijent brzine

Njutnov zakon Njutn je pokazao da je viskozna sila srazmerna površini slojeva, A, između kojih se pri rastojanju od dx održava konstana razlika brzina dv, tako da Njutnov zakon za viskoznu silu glasi: Tečnosti koje se pokoravaju Njutnovom zakonu pri laminarnom protoku su Njutnovske ili normalne tečnosti.
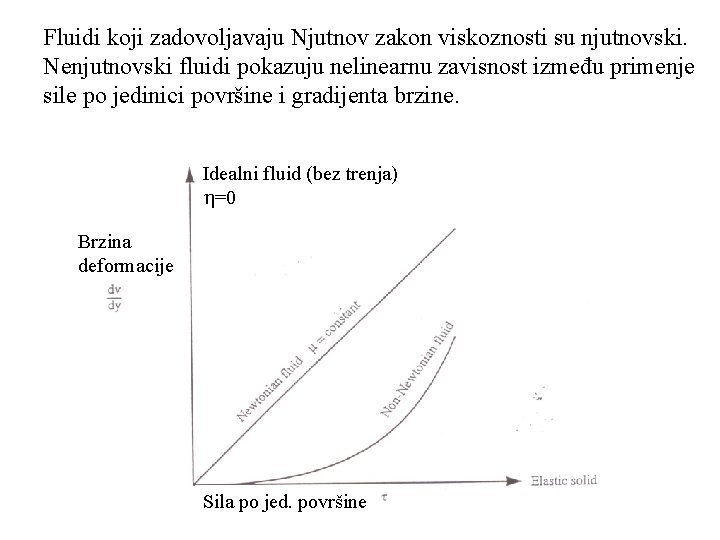
Fluidi koji zadovoljavaju Njutnov zakon viskoznosti su njutnovski. Nenjutnovski fluidi pokazuju nelinearnu zavisnost između primenje sile po jedinici površine i gradijenta brzine. Idealni fluid (bez trenja) =0 Brzina deformacije Sila po jed. površine

1. Dinamička viskoznost: trenje između slojeva fluida koji klize jedan preko drugog: Jedinica za dinamičku viskoznost je poaz: 1 P= 0, 1 Pa s a dimenzije su: m l - 1 t - 1 Recipročna vrednost viskoznosti je fluidnost, =1/ , koja pokazuje lakoću kojom tečnost teče.
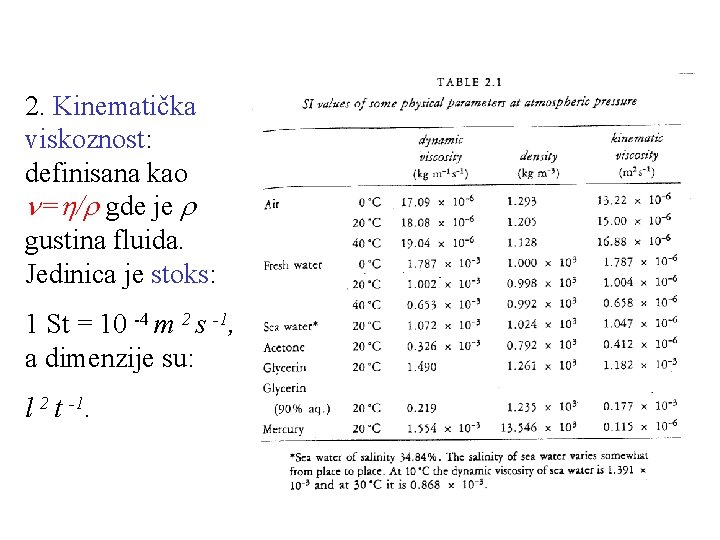
2. Kinematička viskoznost: definisana kao = / gde je gustina fluida. Jedinica je stoks: 1 St = 10 -4 m 2 s -1, a dimenzije su: l 2 t -1.

Viskoznost je osobina fluida da se suprostavljaju sili. Ovaj otpor zavisi od kohezionih sila i prenosa momenta. Tečnosti dominiraju kohezione sile viskoznost opada sa temperaturom Gasovi dominira prenos momenta (sudarima) viskoznost raste sa porastom temperature
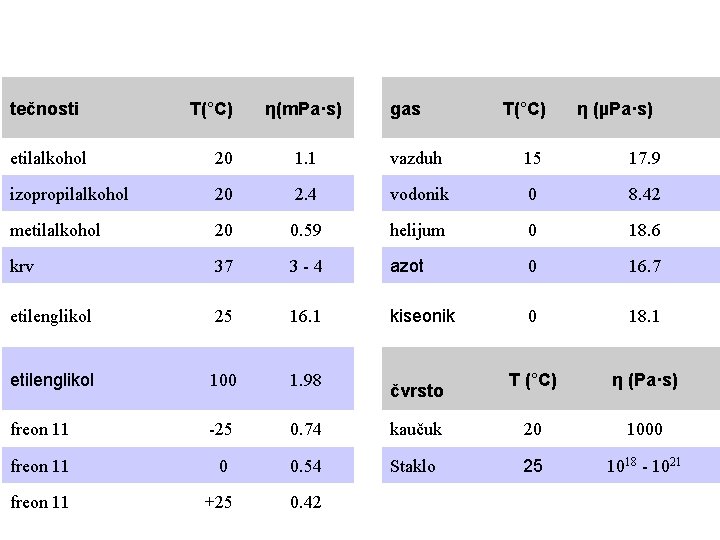
tečnosti T(°C) η(m. Pa·s) etilalkohol 20 1. 1 izopropilalkohol 20 2. 4 metilalkohol 20 0. 59 krv 37 etilenglikol gas T(°C) η (µPa·s) vazduh 15 17. 9 vodonik 0 8. 42 helijum 0 18. 6 3 - 4 azot 0 16. 7 25 16. 1 kiseonik 0 18. 1 etilenglikol 100 1. 98 T (°C) η (Pa·s) freon 11 -25 - 0. 74 kaučuk 20 1000 freon 11 0 0. 54 Staklo 25 1018 - 1021 freon 11 +25+ 0. 42 čvrsto
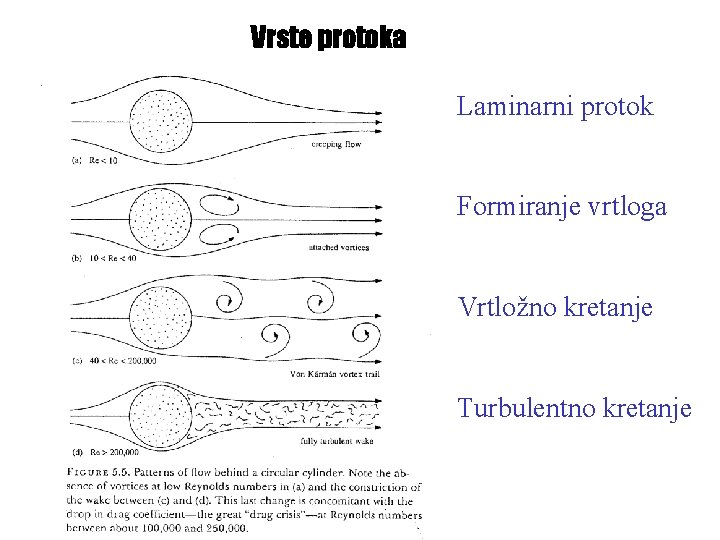
Vrste protoka Laminarni protok Formiranje vrtloga Vrtložno kretanje Turbulentno kretanje

3. Tipovi protoka fluida: (a) Idealni protok (Re= beskonačno) Re = ρ u dp/η mmmm i. Ovo je najbolji tip protoka u teoriji jer sve komponente putuju istom brzinom kroz sredinu tako da svi stižu u isto vreme do kraja cevi i nema širenja toka. ii. Ali, ovaj tip protoka se ne javlja u praksi i služi samo kao model da se razumeju faktori koji utiču na protok.
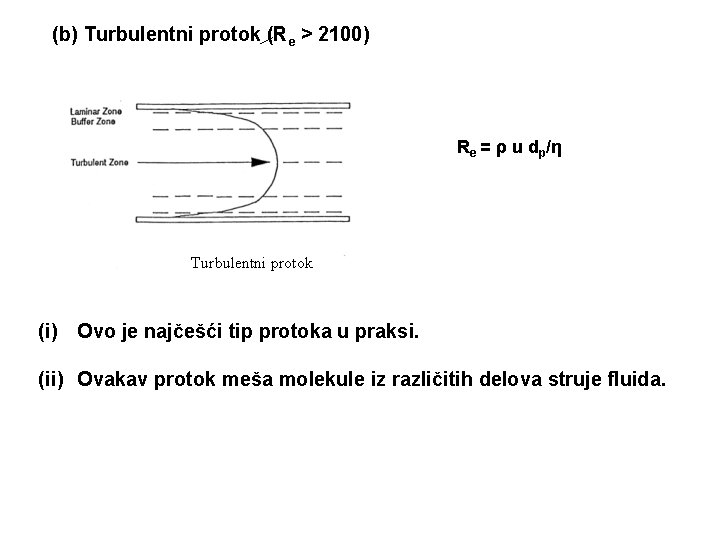
(b) Turbulentni protok (Re > 2100) Re = ρ u dp/η Turbulentni protok (i) Ovo je najčešći tip protoka u praksi. (ii) Ovakav protok meša molekule iz različitih delova struje fluida.

(c) Laminarni (parabolični) protok (Re < 2100) Re = ρ u dp/η (i) Ovo je najuobičajeniji tip protoka i vidi se npr. kod hromatografije. (ii) Brzina kojom putuju molekuli može da se poveže sa njihovim položajem u struji paraboličnom jednačinom tipa. ux = umax (1 -x 2/r 2)

Laminarni i Turbulentni protok Reynolds 1883 Niske brzine Laminarni protok Protok Velike brzine Turbulentan protok Laminarni protok- kada viskozne sile dominiraju - viskozni protok Prelaz je iznenadan Prelazna tačka U = srednja brzina fluida kroz cev d = dijametar cevi Jedinice: 2200 bezdimenziono i poznato kao Reynolds-ov broj

Jednakost Reynolds-ovih brojeva za dva protoka garantuje da su njihove fizičke karakteristike iste!!! Turbulentan protok a ne laminaran dovodi do mešanja toplote, gasova, hrane i dr. u vodi što je od značaja za održavanje života u akva svetu

Poazejev zakon Posmatra se stacionarno proticanje nestišljivog fluida kroz cev pod dejstvom konstantne razlike pritiska. Dr. Jean Leonard Marie Poiseuille
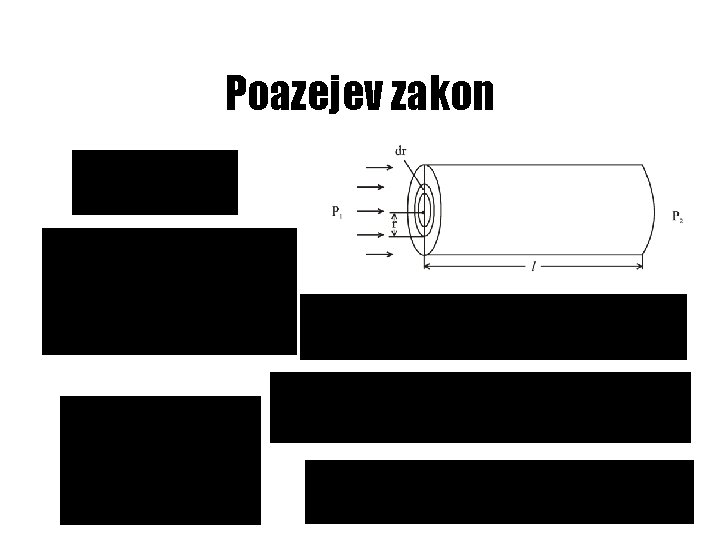
Poazejev zakon

Stoksov zakon Sila na sferu radijusa a koja se kreće brzinom v kroz tečnost viskoznosti je: F = 6 va Potisak Viskozna sila U F Dijametar = 2 a Težina, W Tečnost, l U stanju ravnoteže nema ubrzanja: U-W+F=0
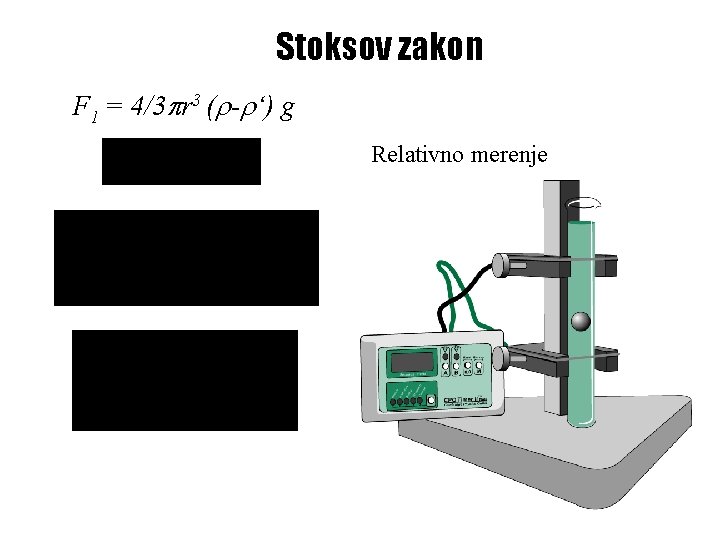
Stoksov zakon F 1 = 4/3 r 3 ( - ‘) g Relativno merenje
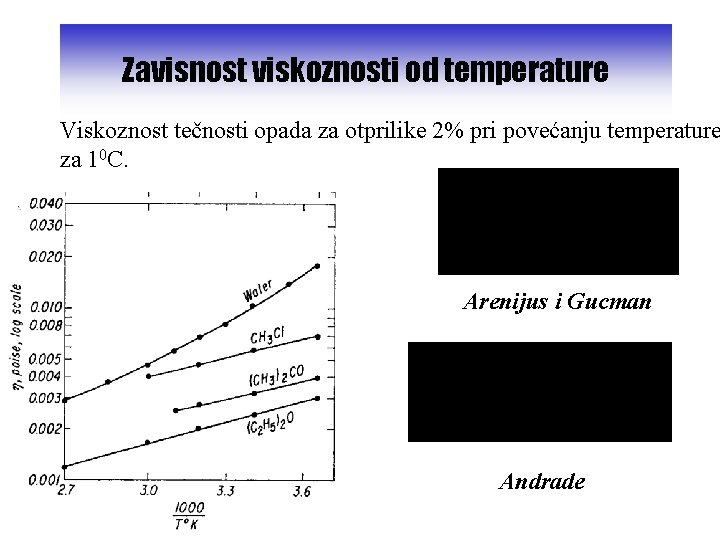
Zavisnost viskoznosti od temperature Viskoznost tečnosti opada za otprilike 2% pri povećanju temperature za 10 C. Arenijus i Gucman Andrade

Zavisnost viskoznosti od temperature i pritiska = k Vc Vc=3 b vsp - b Bačinski Van der Vals zapremina “rupa”-šupljina Dinamička viskoznost je obrnuto srazmerna tapremini šupljina!

Ajringova teorija viskoznosti Da bi molekul A 2 prešao u položaj A 2’ mora biti savladano privlačenje susednog molekula B 2 tj. mora biti savladana pot. barijera . Molekul može imati termalnu energiju da savlada potencijalnu barijeru ali će biti ista verovatnoća da se molekul kreće i nalevo i nadesno. Ako deluje sila f nadesno termalna energija neophodna za kretanje nadesno je smanjena i doći će do termalno aktiviranog protoka nadesno. Deo molekula koji imaju minimalno enrgiju je exp(- /k. T). Da bi molekul prešao na položaj A 2’ mora se stvoriti vakancija u tečnosti.

Ajringova teorija viskoznosti Može se pokazati da je koeficijent viskoznosti, uzimajući u obzir Ajringovu teoriju, dat kao: gde je vm efektivna zapremina koju zauzimaju molekuli, a je energija aktivacije za proticanje tečnosti. /NA=E je molarna energija aktivacije. Ova energija je uporedljiva sa latentnom toplotom isparavanja. Pošto u tečnosti već ima slobodnog prostora to je:

Zavisnost viskoznosti od pritiska Sa povećanjem pritiska viskoznost raste, pri višim pritiscima taj porast je veći nego pri nižim pritiscima. U odsustvu spoljašnjeg pritiska viskoznost je: Ako se primeni pritisak P rad potreban za stvaranje šupljine je povećan za PVh gde je Vh zapremina šupljine. Termalna energija za aktivirani protok je: Nađeno je eksperimentalno da je Vh 0, 15·Vm za proste tečnosti i približno Vh 0, 05·Vm za tečne metale.

Zavisnost viskoznosti od temperature i pritiska kod gasova i tečnosti Fluid Uticaj T Uticaj P gasovi raste kao T 1/2 opada kao nema tečnosti raste kao

Da bi se odredila unutrašnja viskoznost: - Merimo sp kao funkciju koncentracije makromolekula. - Izračunavamo sp/C za svaku koncentraciju. - Ekstrapolišemo vrednost na C = 0.
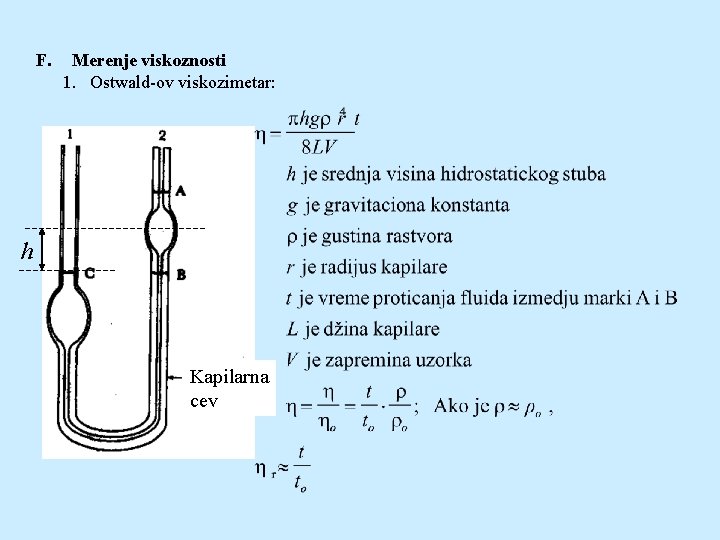
F. Merenje viskoznosti 1. Ostwald-ov viskozimetar: h Kapilarna cev
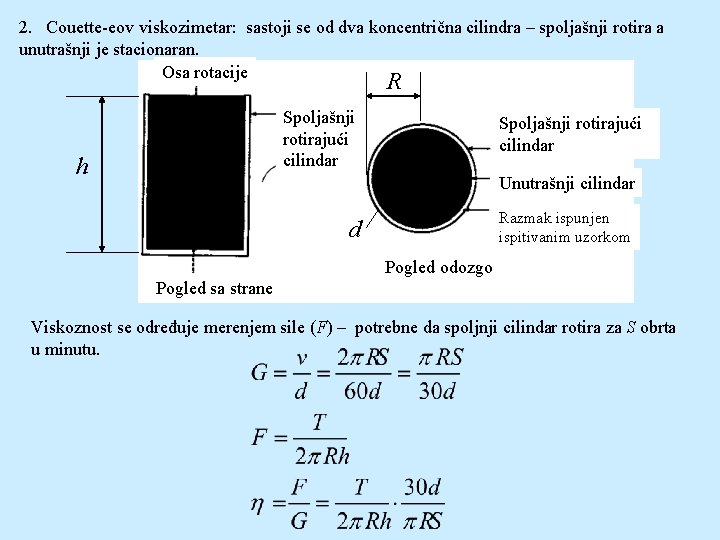
2. Couette-eov viskozimetar: sastoji se od dva koncentrična cilindra – spoljašnji rotira a unutrašnji je stacionaran. Osa rotacije R Spoljašnji rotirajući cilindar h Spoljašnji rotirajući cilindar Unutrašnji cilindar Razmak ispunjen ispitivanim uzorkom d Pogled odozgo Pogled sa strane Viskoznost se određuje merenjem sile (F) – potrebne da spoljnji cilindar rotira za S obrta u minutu.
- Slides: 61