Pillole di chimica Legge Boyle Giovanni Casavecchia Ripasso

Pillole di chimica: Legge Boyle Giovanni Casavecchia

Ripasso: Il modello particellare della materia Il modello particellare descrive la materia come costituita da particelle sferiche in continuo movimento Le particelle di un solido sono molto vicine tra loro sono tenute insieme dalle intense forze di coesione non sono libere di muoversi, ma vibrano attorno alla propria posizione – questo conferisce al solido una forma e un volume definiti Capitolo 7 Le leggi dei gas 2

In un liquido le forze di coesione sono più deboli le particelle hanno maggiore libertà di movimento – pur avendo un volume definito, i liquidi assumono la forma del recipiente che li contiene In un aeriforme le forze di coesione sono molto deboli le particelle sono libere di muoversi e di allontanarsi fino a riempire tutto lo spazio disponibile – gli aeriformi non hanno né un volume proprio né una forma definita Capitolo 7 Le leggi dei gas 3

Gli aeriformi: gas e vapori Gli aeriformi non hanno né volume né forma definiti sono rarefatti sono comprimibili sono in grado di espandersi sono in grado di diffondere velocemente Capitolo 7 Le leggi dei gas 4

1 Un modello per i gas La teoria cinetica e il gas perfetto Secondo la teoria cinetica dei gas a) le particelle del gas sono in costante, rapido e disordinato movimento tra un urto e l’altro, si muovono lungo traiettorie rettilinee b) urtando contro le pareti del recipiente le particelle rimbalzano e cambiano direzione ed esercitano una forza sulla parete La pressione è la forza che le molecole del gas esercitano sull’area unitaria di una superficie Capitolo 7 Le leggi dei gas 5

1 Un modello per i gas c) l’energia cinetica delle particelle è associata al movimento degli atomi e delle molecole ed è direttamente proporzionale alla temperatura del gas d) gli urti delle particelle contro le pareti del recipiente sono elastici – l’energia prima e dopo l’urto è la stessa e) il volume delle particelle è trascurabile rispetto al volume totale del gas – questo spiega la comprimibilità dei gas Un gas che si comporta come previsto dalla teoria cinetica è detto gas ideale (o perfetto) Quando il gas si trova a temperature molto basse o a pressioni molto alte, il modello non è più valido Capitolo 7 Le leggi dei gas 6

2 Le leggi dei gas e il volume molare Legge di Boyle Analizzando i risultati di alcuni esperimenti sui gas Boyle si accorse che se la pressione aumenta, il volume diminuisce le due grandezze sono inversamente proporzionali il prodotto della pressione per il volume è costante Capitolo 7 Le leggi dei gas 7
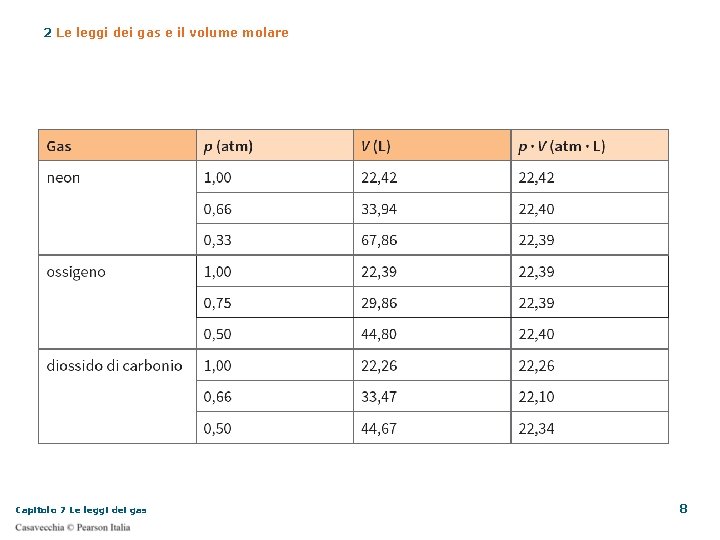
2 Le leggi dei gas e il volume molare Capitolo 7 Le leggi dei gas 8
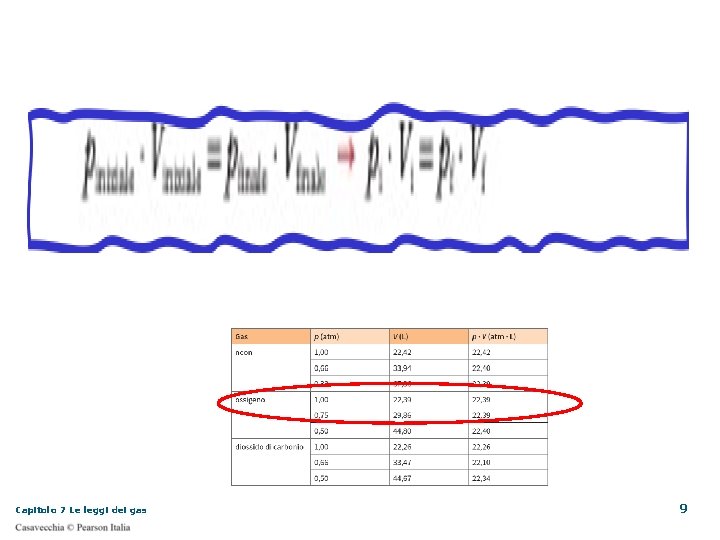
Capitolo 7 Le leggi dei gas 9
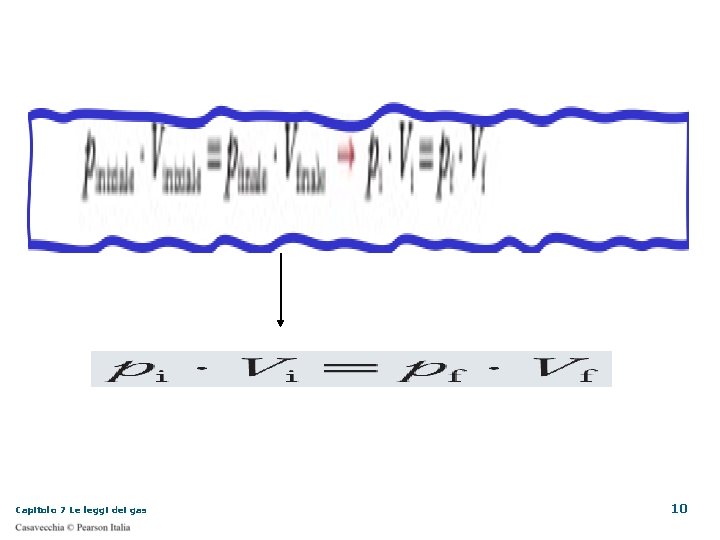
Capitolo 7 Le leggi dei gas 10
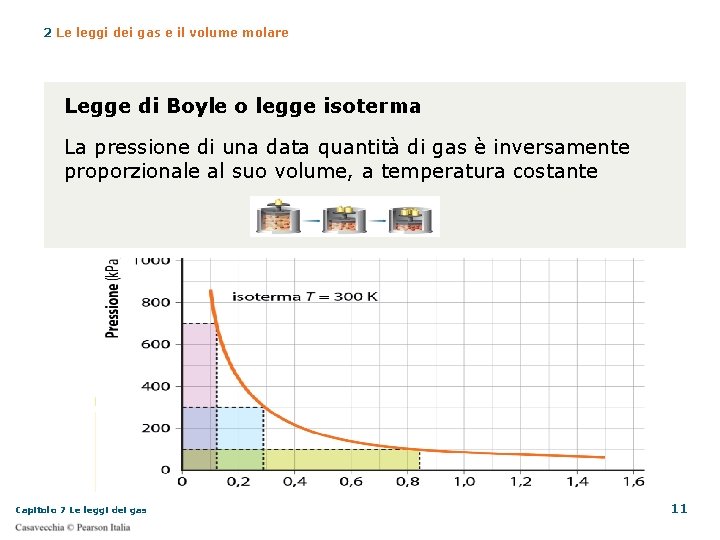
2 Le leggi dei gas e il volume molare Legge di Boyle o legge isoterma La pressione di una data quantità di gas è inversamente proporzionale al suo volume, a temperatura costante Capitolo 7 Le leggi dei gas 11

2 Le leggi dei gas e il volume molare Se rappresentiamo pressione e volume in un grafico cartesiano, otteniamo una iperbole equilatera, chiamata isoterma Capitolo 7 Le leggi dei gas 12
- Slides: 12