Pilhas comerciais Pilha seca pilha de Leclanch O






















- Slides: 32

Pilhas comerciais Pilha seca (pilha de Leclanché) O recipiente é constituído de Zn, atuando como ânodo. Há um papelão poroso que separa o zinco dos demais materiais. O eletrodo central é de grafita, e atua como cátodo. Existe uma pasta úmida que fica entre os eletrodos que apresenta Zn. Cl 2 e NH 4 Cl. O cátodo é envolvido por uma camada de Mn. O 2 A voltagem fornecida por essa pilha é 1, 5 V. Semi reações: Zn 2+ + 2 e 2 Mn. O 2 + H 2 O + 2 e- Mn 2 O 3 + 2 OHNH 4+ + OH- NH 3 + H 2 O A amônia se acumula ao redor do bastão de grafite, agindo como uma camada isolante, reduzindo a voltagem da pilha. A pilha cessará quando todo Mn. O 2 for consumido.

Pilha alcalina É um aprimoramento da pilha de leclanché. É uma pilha seca de Zn e Mn. O 2, a solução eletrolítica é base forte (KOH). (Em leclanché utiliza-se NH 4 Cl e Zn. Cl 2) Sua voltagem também é de 1, 5 V, porém sua duração é cinco vezes maior que a pilha seca de Leclanché. - KOH não forma uma camada isolante -O zinco não fica muito tempo exposto ao meio ácido (NH 4+)

Pilha de lítio O ânodo é feito de metal lítio e o cátodo é de Mn. O 2 ou cloreto de sulfurila (SOCl 2). As pilhas de lítio apresentam uma alta voltagem: 3, 4 V.

Pilhas recarregáveis As pilhas não-recarregáveis, que são aquelas utilizadas uma vez e depois são descartadas, estas são chamadas de pilhas primárias. Nessas pilhas os materiais de oxidação e de redução não permanecem no ânodo e no cátodo, por isso é impossível reverter a situação. As pilhas recarregáveis são aquelas que depois de utilizadas pode ser recarregadas e utilizadas novamente, estas são chamadas de pilhas secundárias. Nessas pilhas os materiais de oxidação ficam no ânodo e os materiais de redução permanecem no cátodo, sendo possível inverter as reações.

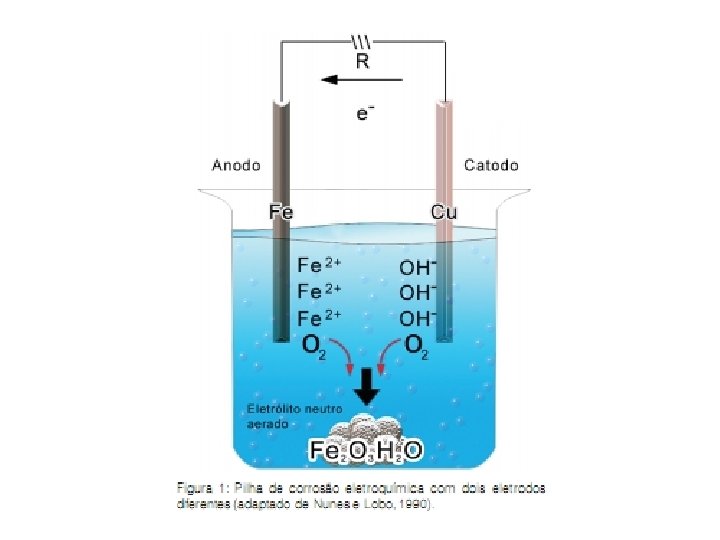
Corrosão É um processo resultante da ação do meio sobre um determinado material, causando sua deterioração. É um fenômeno que está associado à ferrugem que é aquela camada de cor marrom-avermelhada que geralmente se forma em superfícies metálicas. A ferrugem nada mais é do que o desgaste sofrido pelas construções que representam os sinais de reações químicas. Este fenômeno não ocorre somente com metais mas também com outros materiais dentre eles os polímeros orgânicos, o concreto, eletrodomésticos, grades, instalações industriais, automóveis, etc.

Formação da Ferrugem Reação anódica (oxidação): Fe ---> Fe 2+ + 2 e– Reação catódica (redução): 2 H 2 O + 2 e– ---> H 2 + 2 OH– (2) (1) Neste processo, os íons Fe 2+ migram em direção à região catódica, enquanto os íons OH - direcionam-se para a anódica. Em uma região intermediária, ocorre a formação do hidróxido ferroso: Fe 2+ + 2 OH– ---> Fe (OH)2 (3) 3 Fe(OH)2 ---> Fe 3 O 4 + 2 H 2 O + H 2 (4)

Em meio com baixo teor de oxigênio, o hidróxido ferroso sofre a seguinte transformação: 3 Fe(OH)2 ---> Fe 3 O 4 + 2 H 2 O + H 2 (4) Caso o teor de oxigênio seja elevado 2 Fe(OH)2 + H 2 O + 1/2 O 2 ---> 2 Fe(OH)3 (5) 2 Fe(OH)3 ---> Fe 2 O 3. H 2 O + 2 H 2 O (6) Produto final da corrosão (ferrugem): Fe 3 O 4 (coloração preta) Fe 2 O 3. H 2 O (coloração alaranjada ou castanho- avermelhada).


Ataque do concreto por agente externo Essa corrosão também afeta a estabilidade e durabilidade das estruturas, sendo muito rápida e progressiva. Fatores: mecânicos (vibrações e erosão), físicos (variação de temperatura), biológicos (bactérias) ou químicos (em geral ácidos e sais).

Como minimizar os efeitos da corrosão? Os processos mais empregados para a prevenção da corrosão a proteção catódica e anódica, os revestimentos e os inibidores de corrosão. A proteção catódica é a técnica que transforma a estrutura metálica que se deseja proteger em uma pilha artificial, evitando, assim, que a estrutura se deteriore (Dutra e Nunes, 1987).

A proteção de uma superfície metálica Um procedimento possível para proteger o ferro da corrosão em ambientes nos quais estejam exposto à agua e a O 2 é a galvanização. Galvanizar o ferro ou o aço consiste em revesti-lo com zinco metálico (como se fosse uma fina camada de tinta) para evitar sua corrosão. O zinco foi escolhido por ser um redutor mais forte que o ferro. Zn 2+ + 2 e- Zn Eo = -0, 76 V Fe 2+ + 2 e- Fe Eo = -0, 44 V O zinco também atua, com relação ao ferro, como se fosse o ânodo de uma pilha.

Se o ferro galvanizado fosse “riscado” e exposto ao ar e a umidade, ele estaria sujeito a ser oxidado a Fe 2+. Este seria imediatamente reduzido pelo zinco, impedindo o aparecimento da ferrugem. Zn(s) + Fe 2+(aq) Fe(s) + Zn 2+(aq) Como o Zn tem mais facilidade para se oxidar ( pois tem menor Eored) ele tende a se oxidar preferencialmente, mesmo que o Fe esteja exposto.

Se a película protetora de Zn for danificada e o ferro estiver exposto, o Zn atuará como metal de sacrifício, ou seja, um metal propositadamente colocado em contato com o ferro para que seja oxidado em lugar dele, preservando-o.

O escurecimento de um objeto de prata se deve à formação de uma película de Ag 2 S, na qual a prata está oxidada (Ag+). A limpeza pode ser reduzindo-se Ag+ a Ago. 4 Ag (s) + 2 H 2 S (g) + O 2 (g) 2 Ag 2 S (s) + 2 H 2 O (l) Talher Poluente do ar depósito preto Para limpeza, utiliza-se pastas ou soluções que apresentem alumínio em pó. Eo red Al 3+/Alo -1, 68 V Eo red Ag+/ Ago +0, 80 V

ELETRÓLISE

Pode-se dizer que ELETRÓLISE é o fenômeno de decomposição de uma substância pela ação de uma CORRENTE ELÉTRICA A eletrólise ocorre com soluções onde existam íons ou com substâncias iônicas fundidas

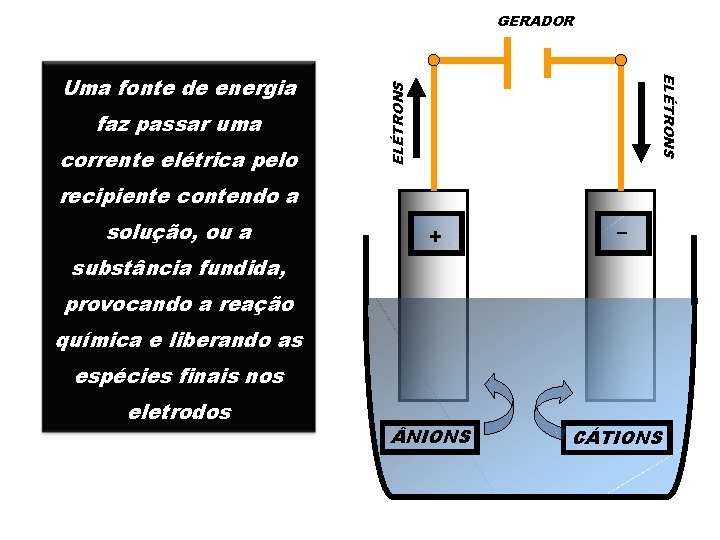
GERADOR corrente elétrica pelo ELÉTRONS faz passar uma + – ELÉTRONS Uma fonte de energia recipiente contendo a solução, ou a + – substância fundida, provocando a reação química e liberando as espécies finais nos eletrodos NIONS CÁTIONS

Podemos dividir a eletrólise em ÍGNEA e AQUOSA ELETRÓLISE ÍGNEA Ocorre com a substância iônica na fase líquida (fundida) ELETRÓLISE AQUOSA Ocorre quando o eletrólito se encontra dissolvido na ÁGUA

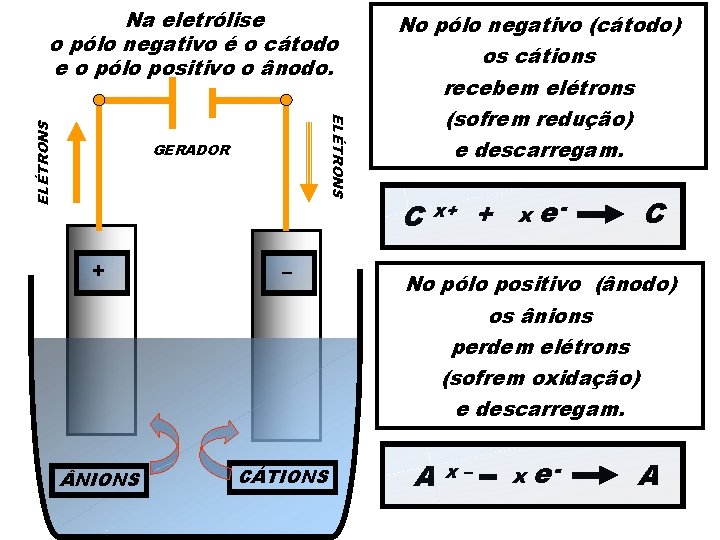
Na eletrólise o pólo negativo é o cátodo e o pólo positivo o ânodo. ELÉTRONS – ELÉTRONS + GERADOR + – NIONS CÁTIONS No pólo negativo (cátodo) os cátions recebem elétrons (sofrem redução) e descarregam. C x+ + x e- C No pólo positivo (ânodo) os ânions perdem elétrons (sofrem oxidação) e descarregam. A x– x e- A

Eletrólise ígnea do CLORETO DE SÓDIO ( Na. Cl ) No estado fundido teremos os íons sódio (Na+) e cloreto (Cl–) + 2 e – 2 Na Pólo negativo: 2 Na+ 2 Cl – – 2 e – Cl 2 Pólo positivo: Reação global: 2 Na+ + 2 e 2 Cl – – – 2 e– 2 Na Cl 2 2 Na. Cl 2 Na + Cl 2

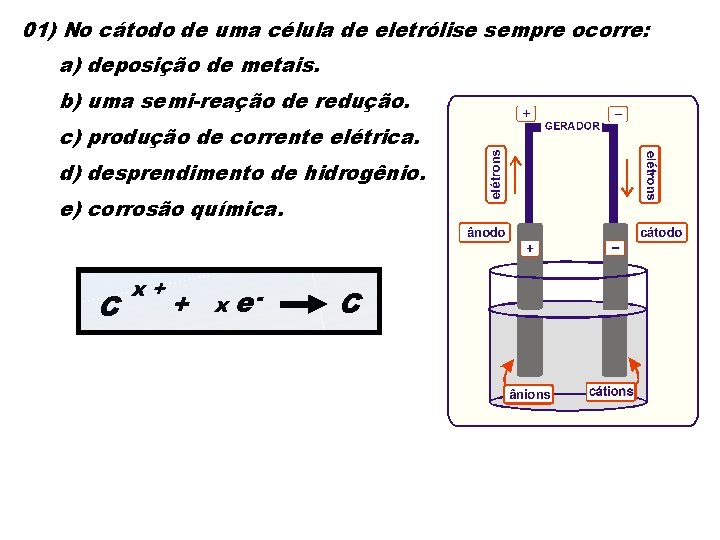
01) No cátodo de uma célula de eletrólise sempre ocorre: a) deposição de metais. b) uma semi-reação de redução. c) produção de corrente elétrica. d) desprendimento de hidrogênio. e) corrosão química. C x+ + x e- C

02) A eletrólise de cloreto de sódio fundido produz sódio metálico e gás cloro. Nesse processo, cada íon: a) sódio recebe dois elétrons. b) cloreto recebe um elétron. c) sódio recebe um elétron. d) cloreto perde dois elétrons. e) sódio perde um elétron. Na + Cl – Pólo negativo: 2 Na+ Pólo positivo: 2 Cl – + 2 e – 2 Na – 2 e – Cl 2

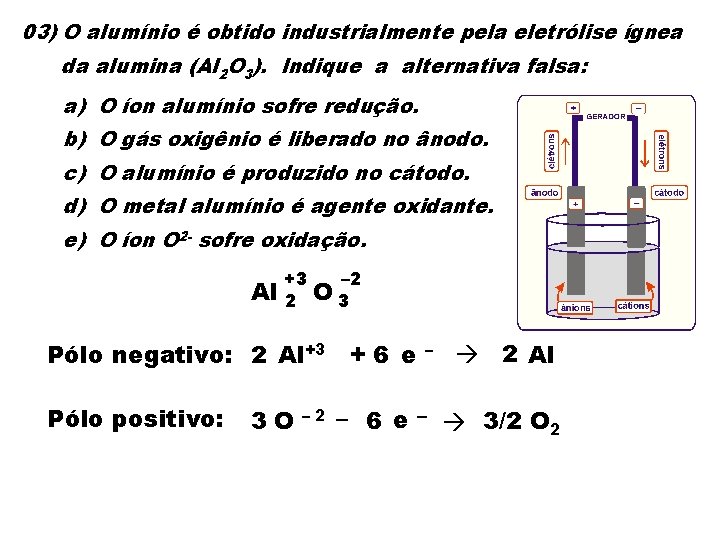
03) O alumínio é obtido industrialmente pela eletrólise ígnea da alumina (Al 2 O 3). Indique a alternativa falsa: a) O íon alumínio sofre redução. b) O gás oxigênio é liberado no ânodo. c) O alumínio é produzido no cátodo. d) O metal alumínio é agente oxidante. e) O íon O 2 - sofre oxidação. Al +3 – 2 2 O 3 Pólo negativo: 2 Al+3 + 6 e Pólo positivo: 3 O – 2 Al – 6 e – 3/2 O 2

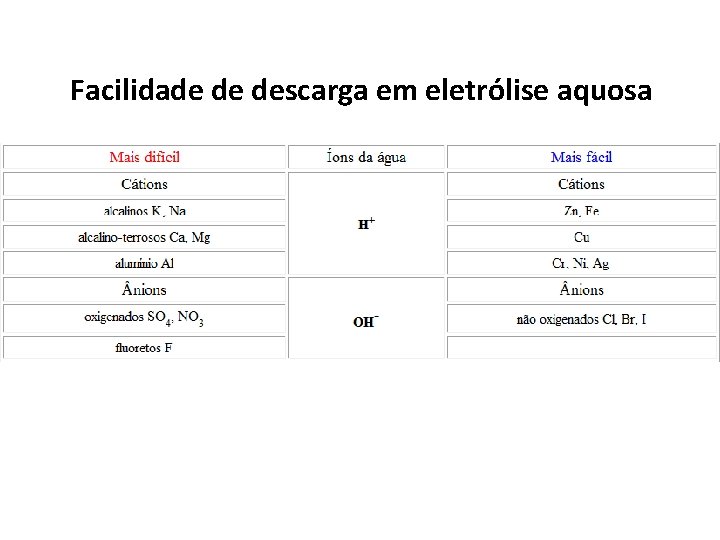
Na eletrólise aquosa teremos a presença de “ DOIS CÁTIONS “ e “ DOIS NIONS “ Neste caso teremos que observar a “ ORDEM DE DESCARGA DOS ÍONS ”

Facilidade de descarga em eletrólise aquosa

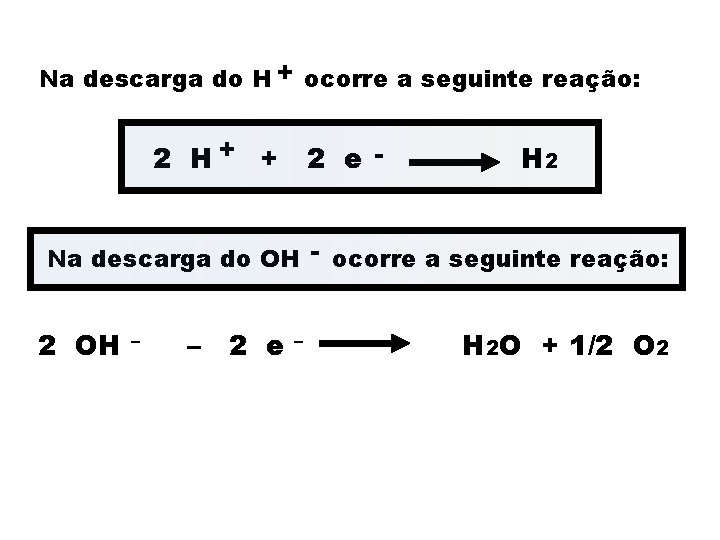
Na descarga do H + ocorre a seguinte reação: 2 H+ + 2 e - H 2 Na descarga do OH - ocorre a seguinte reação: 2 OH – – 2 e – H 2 O + 1/2 O 2

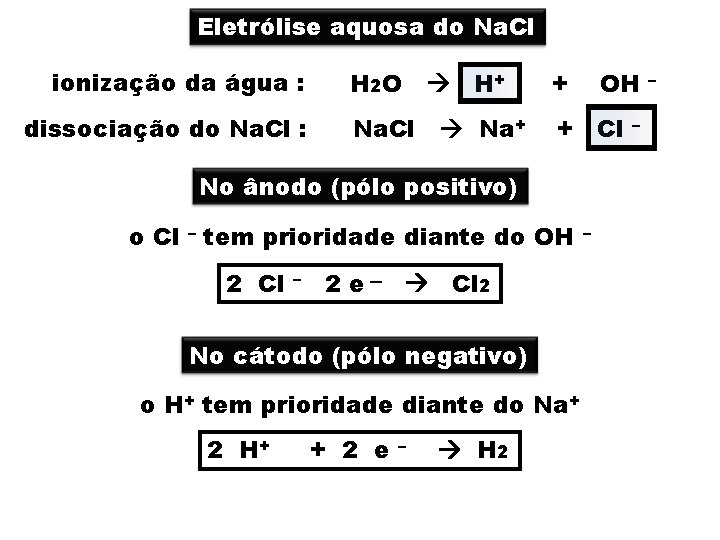
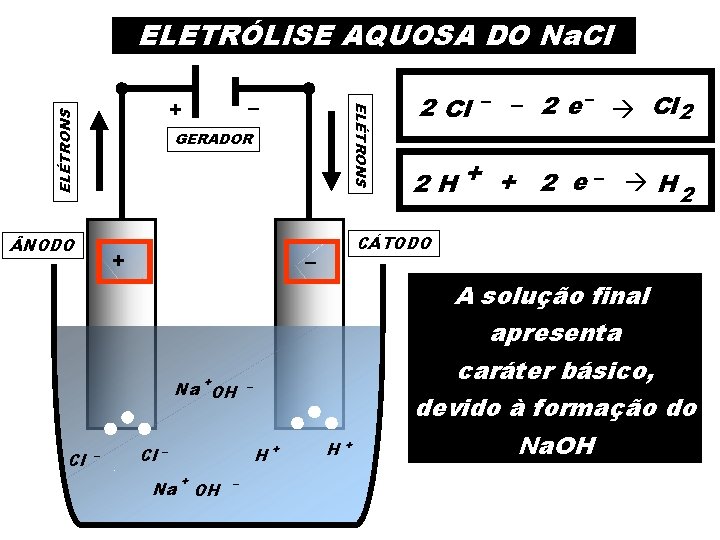
Eletrólise aquosa do Na. Cl ionização da água : dissociação do Na. Cl : H 2 O Na. Cl H+ Na+ + OH + Cl No ânodo (pólo positivo) o Cl – tem prioridade diante do OH 2 Cl – 2 e – Cl 2 No cátodo (pólo negativo) o H+ tem prioridade diante do Na+ 2 H+ + 2 e – H 2 – – –

NODO : 2 Cl – – 2 e – Cl 2 CÁTODO : 2 H + + 2 e – H 2 ficam na solução os íons Na+ e OH tornando a mesma básica devido á formação do Na. OH –

ELETRÓLISE AQUOSA DO Na. Cl ELÉTRONS GERADOR NODO + + – Na – H+ Cl – + OH – 2 Cl – – 2 e – Cl 2 2 H + + 2 e – H 2 CÁTODO – Na OH Cl ELÉTRONS – + H + A solução final apresenta caráter básico, devido à formação do Na. OH

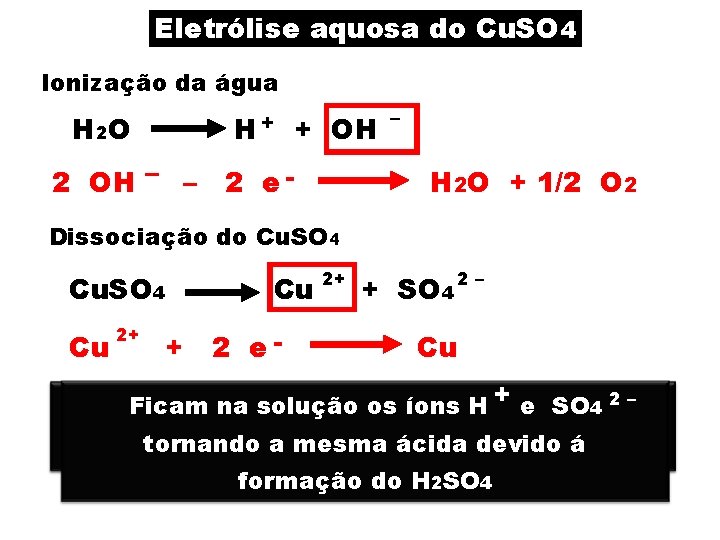
Eletrólise aquosa do Cu. SO 4 Ionização da água H 2 O H+ + OH 2 OH – – 2 e - – H 2 O + 1/2 O 2 Dissociação do Cu. SO 4 Cu 2+ Cu + 2 e- 2+ + SO 4 2– Cu + e SO 4 2 – Ficam na solução os íons H ânodo (pólo positivo)oaíon oxidrila tem No. No cátodo (pólo negativo) cúprico tem tornando a mesma ácida devido á prioridade diante do do sulfato prioridade diante H+ formação do H 2 SO 4

01) Quando se faz passar uma corrente elétrica através de uma solução aquosa de iodeto de potássio pode-se verificar que: a) ocorre migração de K+ para o ânodo e I – para o cátodo. b) ocorre migração do H+ para o cátodo e I – para o ânodo. c) a solução torna-se ácida devido à formação de HI. d) a solução permanece neutra devido à formação de H 2 e I 2. e) há formação de I 2 no cátodo. ionização da água : H 2 O dissociação do KI : KI Pólo negativo: (cátodo) 2 H Pólo positivo: (ânodo) 2 I – H + + OH OH–– K K++ + I – + + 2 e– H 2 – 2 e– I 2 Ficam na solução

02) Na eletrólise de uma solução aquosa diluída de ácido sulfúrico: a) Quais são os gases produzidos? Ionização da água: H 2 O H+ + OH – Ionização do ácido sulfúrico: H 2 SO 4 Pólo negativo: 2 H + (cátodo) Pólo positivo: (ânodo) 2 OH – – 2 2 H + + SO 4 + 2 e – H 2 – 2 e – 1/2 O 2 + H 2 O b) O que ocorre com a concentração da solução? A solução vai ficando CONCENTRADA em H 2 SO 4 c) Escreva a equação global. 2 H + + 2 OH – H 2 + ½ O 2 + H 2 O