PILAS Elabor Esther Flores Cruz OBJETIVO Al finalizar
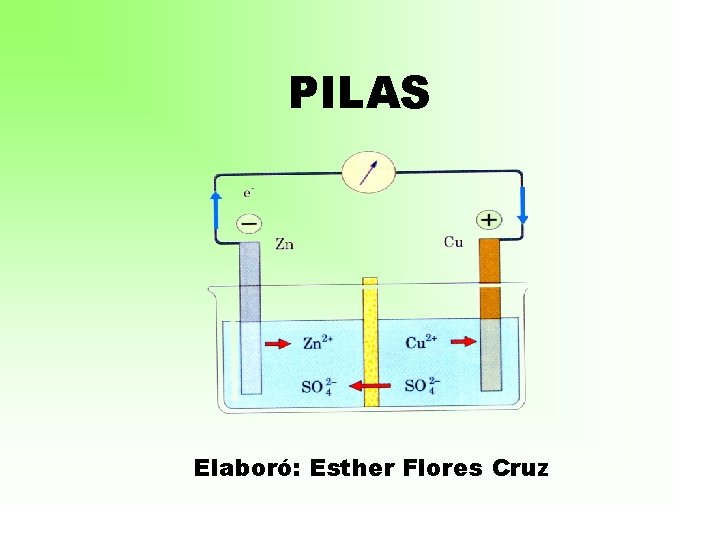
PILAS Elaboró: Esther Flores Cruz

OBJETIVO Al finalizar esta sesión el alumno identificará los elementos de una pila y determinará su potencial o fuerza electromotriz (fem).

ANTECEDENTES §Electroquímica §Reacción redox §Pila §Reacción espontánea §Diagrama de predicción de una reacción espontánea

ANTECEDENTES • ELECTROQUÍMICA: la electroquímica es la rama de la Química que estudia la conversión entre la energía eléctrica y la energía química

ANTECEDENTES • REACCIÓN REDOX : una reacción redox, llamada también de oxidaciónreducción, es aquella donde se realiza un intercambio de electrones, de manera que una sustancia se oxida y la otra se reduce.

ANTECEDENTES • PILA: una pila (llamada también celda galvánica o voltaica), es aquella en la que una reacción química redox espontánea genera energía eléctrica.

ANTECEDENTES • REACCIÓN ESPONTÁNEA: es una reacción química cuantitativa hacia la formación de los productos, es decir, se desplaza hacia la derecha.

ANTECEDENTES Diagrama de predicción de una reacción espontánea Aumento de la fuerza oxidante Ox 1 Red 1 Ox 2 Eo(V) Red 2 Aumento de la fuerza reductora

ANTECEDENTES Semirreacciones Ox 2 + ne Red 1 Red 2 reacción de reducción Ox 1 + ne reacción de oxidación Donde ne es el número de electrones intercambiados en cada semirreacción.

ANTECEDENTES Reacción global espontánea Ox 2 + Red 1 Ox 1 + Red 2

ANTECEDENTES Para calcular el potencial o fuerza electromotriz (fem) de la pila o celda, aplicamos la expresión siguiente : Eo celda= Eo reducción – Eo oxidación Donde Eo reducción es el potencial estándar de la especie que se reduce y Eo oxidación el potencial estándar de la especie que se oxida.

METODOLOGÍA DE RESOLUCIÓN Para la resolución de los ejercicios se recomienda: • Consultar la tabla de potenciales estándar de reducción a 25(o. C), de las sustancias involucradas en la reacción química(cuando la información no es proporcionada). • En un diagrama de predicción de reacción química espontánea anotar los valores de potenciales estándar de las sustancias.

METODOLOGÍA DE RESOLUCIÓN • La reacción química espontánea se lleva a cabo entre la sustancia más oxidante con la sustancia más reductora. • Se identifica entonces la semirreacción de oxidación de la sustancia, así como la semirreacción de reducción de la otra especie involucrada.

METODOLOGÍA DE RESOLUCIÓN • Para calcular el potencial o fem de la pila, se sustituyen los valores de los potenciales estándar de las sustancias de la reacción redox espontánea, en la expresión correspondiente.

Ejercicios resueltos Se presentan dos ejercicios resueltos y al finalizar la explicación, se proponen cuatro ejercicios para resolver por el alumno.

Ejercicio resuelto Calcule el potencial de la pila (celda) a 25(o. C) de acuerdo a la reacción redox espontánea siguiente: Cu 2+(ac) + Zn(s) Cu(s) + Zn 2+(ac) Resolución: de la reacción se observa Cu 2+(ac) + 2 e Zn(s) Cu(s) Zn 2+(ac) + 2 e reacción de reducción reacción de oxidación

Ejercicio resuelto Eo celda = Eo reducción –Eo oxidación Sustituyendo los valores de potencial estándar de reducción de las especies de la reacción, tenemos: Eo celda =[ 0. 34(V) ] – [-0. 76(V)] Eo celda = 1. 10(V)

EJERCICIO RESUELTO Prediga si la siguiente reacción procederá espontáneamente, y si es así, calcule el potencial de la pila generada a 25(o. C). Fe 3+(ac) + V 2+(ac) Fe 2+(ac) + V 3+ (ac)

EJERCICIO RESUELTO Potenciales especies: estándar de reducción Eo Fe 3+/Fe 2+ = 0. 77(V) Eo V 3+/V 2+ = -0. 255(V) de las

EJERCICIO RESUELTO Diagrama para identificar la espontaneidad de la reacción química 3+ Fe -0. 255 0. 77 V V Fe 3+ (ac) V 2+(ac) 2+ + 1 e Fe 3+ Eo(V) 2+ Fe 2+(ac) reacción de reducción V 3+(ac) + 1 e reacción de oxidación
![EJERCICIO RESUELTO Eo celda= Eo reducción - Eooxidación Eocelda=[ 0. 77(V)] - [ -0. EJERCICIO RESUELTO Eo celda= Eo reducción - Eooxidación Eocelda=[ 0. 77(V)] - [ -0.](http://slidetodoc.com/presentation_image_h/98ce5458df543d4cbc7d97097222f89d/image-21.jpg)
EJERCICIO RESUELTO Eo celda= Eo reducción - Eooxidación Eocelda=[ 0. 77(V)] - [ -0. 255(V) ] Eocelda=1. 025(V)

EJERCICIOS PROPUESTOS Prediga si las siguientes reacciones procederan espontáneamente a 25(o. C), de ser así calcule la fem de la pila o celda generada. Consulte la tabla de potenciales estándar de reducción. a) Sn 2+(ac) + Fe(s) Sn(s) + Fe 2+(ac) b) Cr(s) + Ag 1+(ac) Cr 3+(ac) + Ag(s) c)
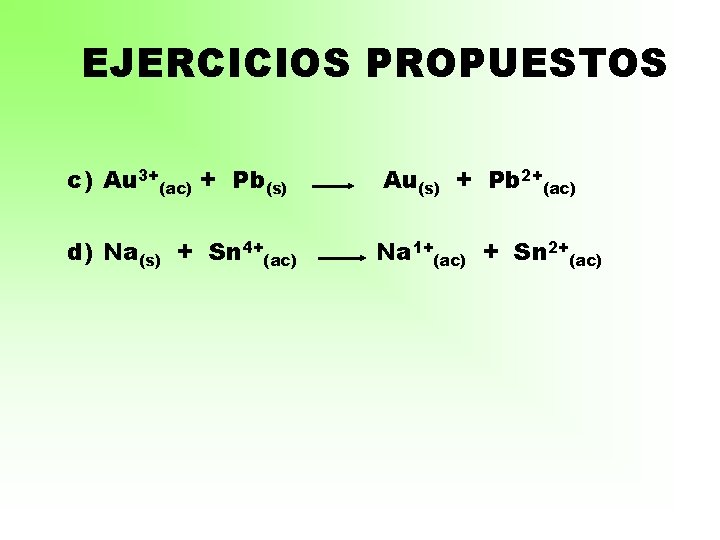
EJERCICIOS PROPUESTOS c) Au 3+(ac) + Pb(s) d) Na(s) + Sn 4+(ac) Au(s) + Pb 2+(ac) Na 1+(ac) + Sn 2+(ac)

BIBLIOGRAFÍA §Chang, Raymond Chemistry Mc. Graw-Hill U. S. A. 1997. §Mortimer, Charles Química Grupo Editorial Iberoamérica México, 1983
- Slides: 24