PI PI L LHA H AS Luigi Galvani







- Slides: 17

PI PI L LHA H AS

Luigi Galvani (1737 -1798) Em 1780, ao dissecar uma rã, Galvani notou que a perna da rã se encolhia, quando o bisturi tocava os nervos. Galvani suspeitou que houvesse eletricidade

Laboratório de Galvani Luigi Galvani

Volta discorda de Galvani, concluindo que a eletricidade provinha do contato entre metais. Alessandro Volta (1745 -1827)

Alessandro Volta A pilha de Volta usava 3 discos: zinco, cobre e papelão embebido em solução ácida. Em uma reação eletroquímica, o zinco perde elétrons para a solução e o cobre os recebe. O nome pilha é usado até hoje e decorre do empilhamento dos discos.

Volta e Napoleão


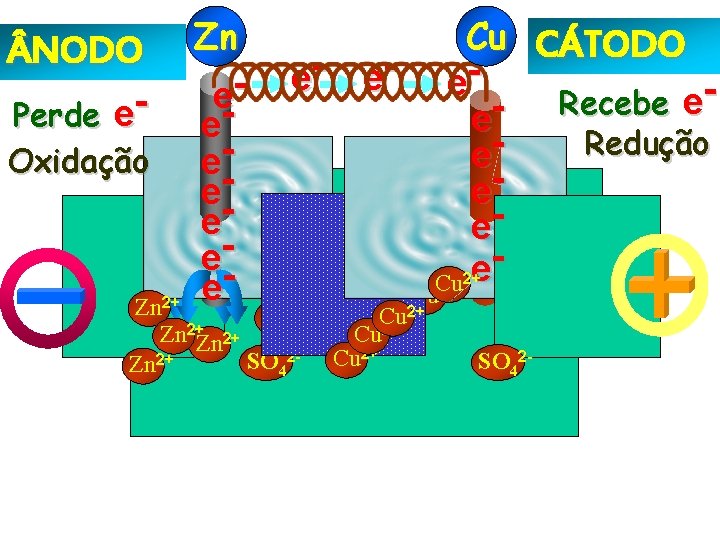
NODO Perde e- Oxidação Zn e-ee ee- e- Zn 2+ 2+ Zn Zn 2+ SO 42 Zn 2+ e- Cu CÁTODO e. Recebe e e. Redução eeee 2+ Cu Cu 2+ SO 42 -

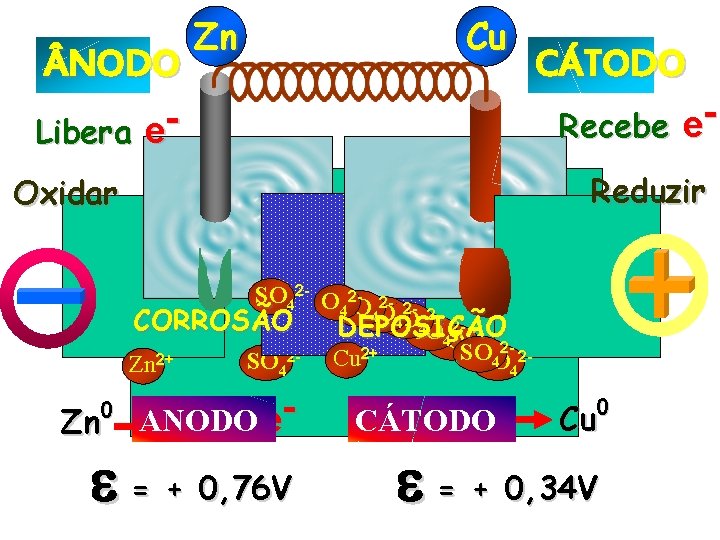
NODO Libera e- Zn Cu CÁTODO Recebe e. Reduzir Oxidar 2 - 2 - 2 SOSO 2 - 24 4 OSO 4 SO 24 SO 4 4 CORROSÃO 2 DEPOSIÇÃO SOSO 4 2 - 24 2+ SO 22+ Cu 4 2 SO 4 SO Zn 4 Zn ANODO Zn +2 e 0 2+ = + 0, 76 V e 2 Cu CÁTODO 2+ 0 Cu = + 0, 34 V

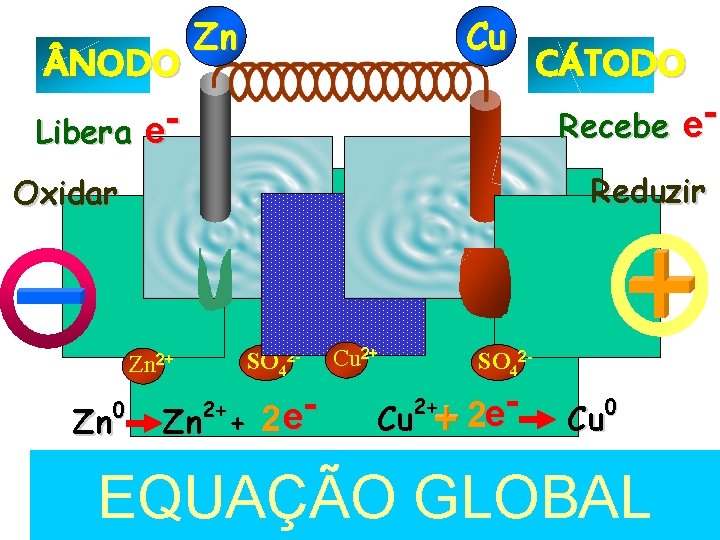
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 0 Zn Cu 2+ e 2 Zn + SO 42 - 2+ 2+ Cu 2 e- 0 Cu E = E + E EQUAÇÃO GLOBAL oxi red 0 Zn CÁTODO 2+ Cu 2+ Zn 0 Cu

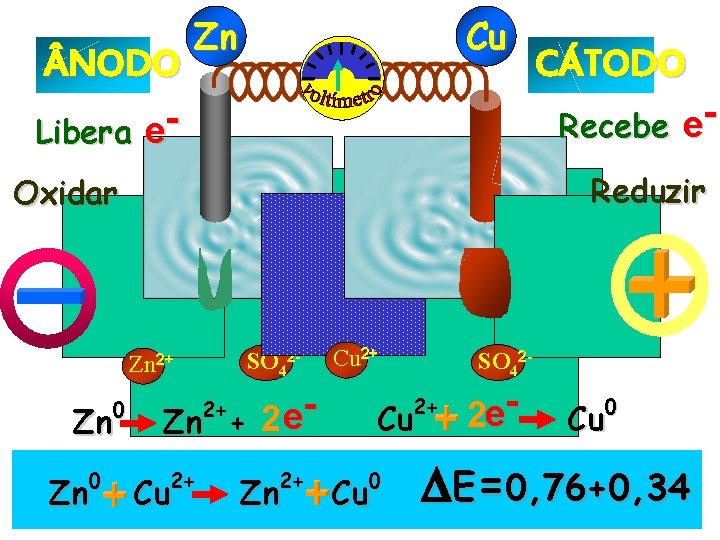
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 0 Zn CÁTODO Cu 2+ e 2 Zn + 2+ 2+ 2+ Cu 2+ Zn SO 42 - Cu 0 Cu 2 e- 0 Cu E=0, 76+0, 34

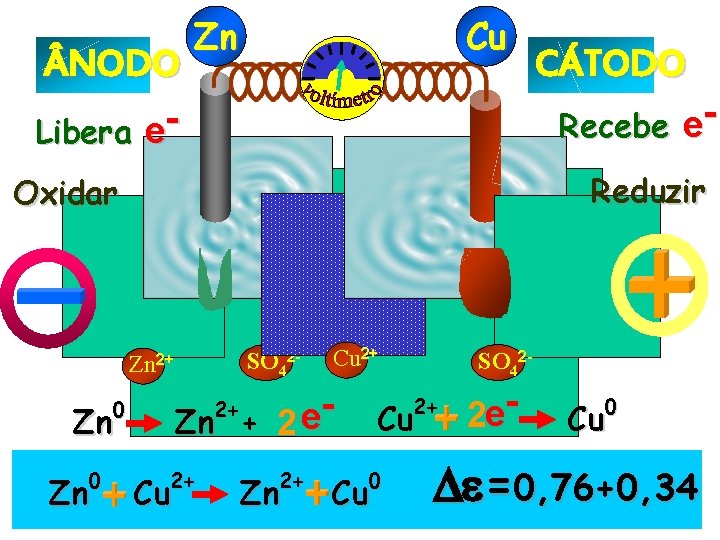
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 2+ Cu 2+ Zn SO 42 - 2+ 2+ Zn Zn Cu 2+ e Zn + 2 0 0 CÁTODO Cu 0 Cu 2 e- 0 Cu =0, 76+0, 34

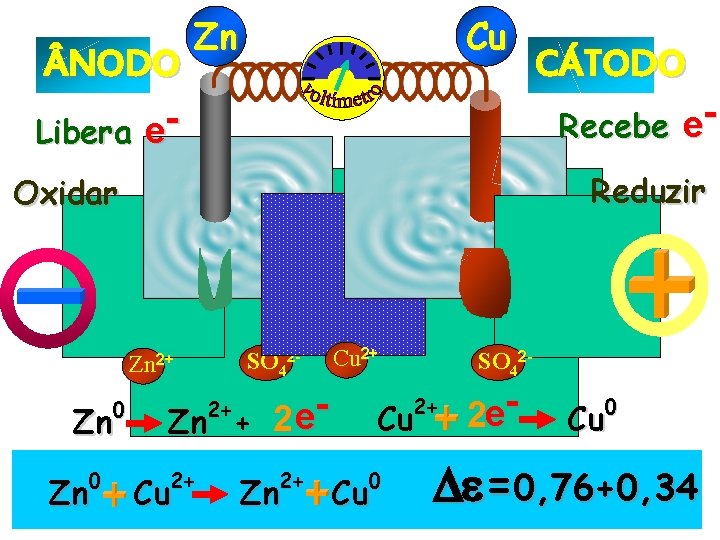
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 0 Zn CÁTODO Cu 2+ e 2 Zn + 2+ 2+ 2+ Cu 2+ Zn SO 42 - Cu 0 Cu 2 e- 0 Cu =0, 76+0, 34

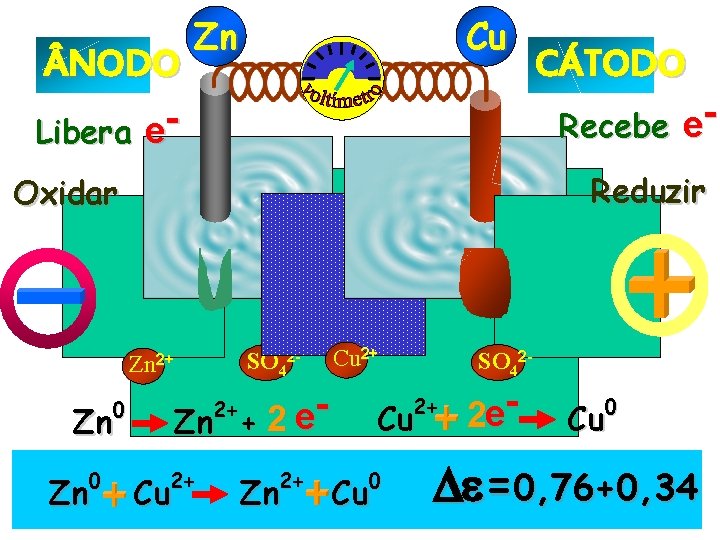
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 2+ Cu 2+ Zn SO 42 - 2+ 2+ Zn Zn Cu 2+ e 2 Zn + 0 0 CÁTODO Cu 0 Cu 2 e- 0 Cu =0, 76+0, 34

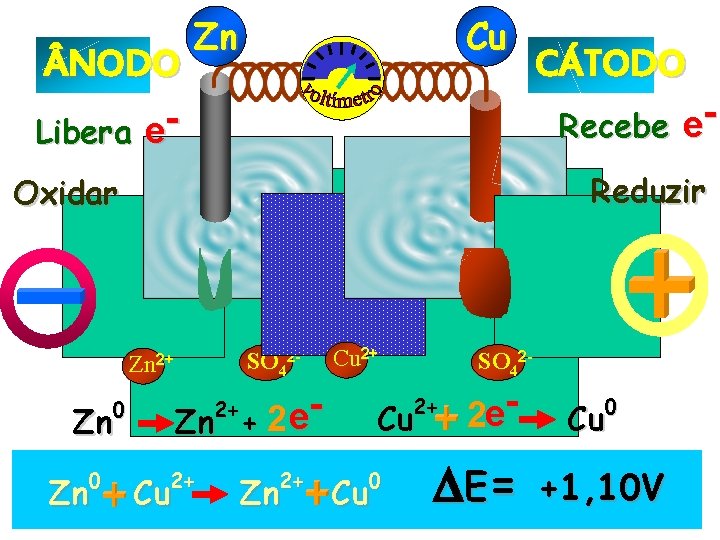
NODO Libera e- Zn Cu Recebe e. Reduzir Oxidar SO 42 - Zn 2+ 2+ Cu 2+ Zn SO 42 - 2+ 2+ Zn Zn Cu 2+ e 2 Zn + 0 0 CÁTODO Cu 0 Cu 2 e- E= 0 Cu +1, 10 V

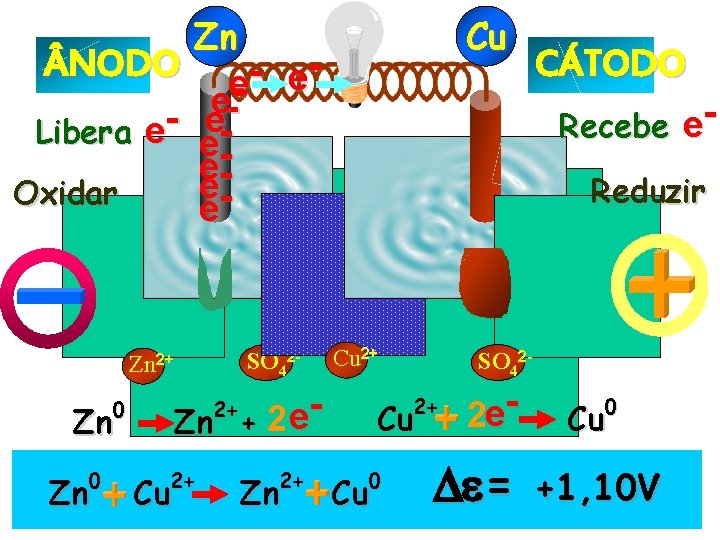
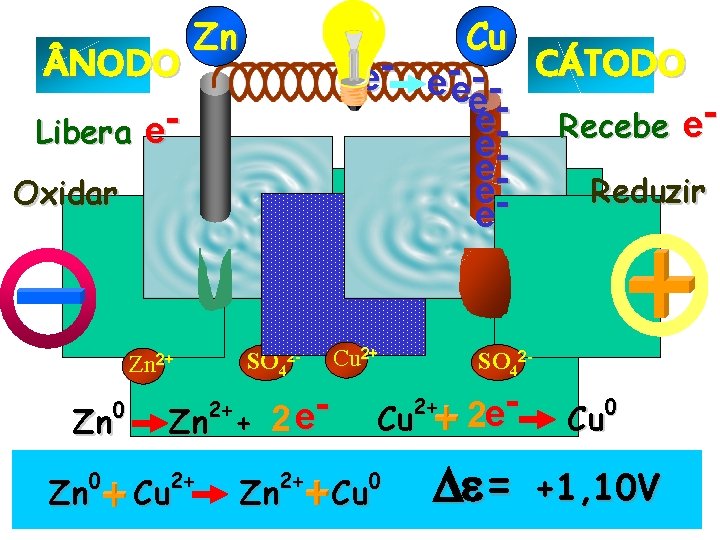
NODO Libera e. Oxidar Zn e e e-eeeee SO 42 - Zn 2+ Zn Reduzir Cu 2+ 2+ Cu 2+ Zn SO 42 - 2+ 2+ Zn CÁTODO Recebe e- e 2 Zn + 0 0 Cu Cu 0 Cu 2 e- = 0 Cu +1, 10 V

NODO Libera e- Zn Cu CÁTODO e e e- ee- Recebe eee. Reduzir ee Oxidar SO 42 - Zn 2+ 0 Zn Cu 2+ e 2 Zn + 2+ 2+ 2+ Cu 2+ Zn SO 42 - Cu 0 Cu 2 e- = 0 Cu +1, 10 V