Phng gio dc Kin x ng Bi 13

Phßng gi¸o dôc KiÕn x ¬ng
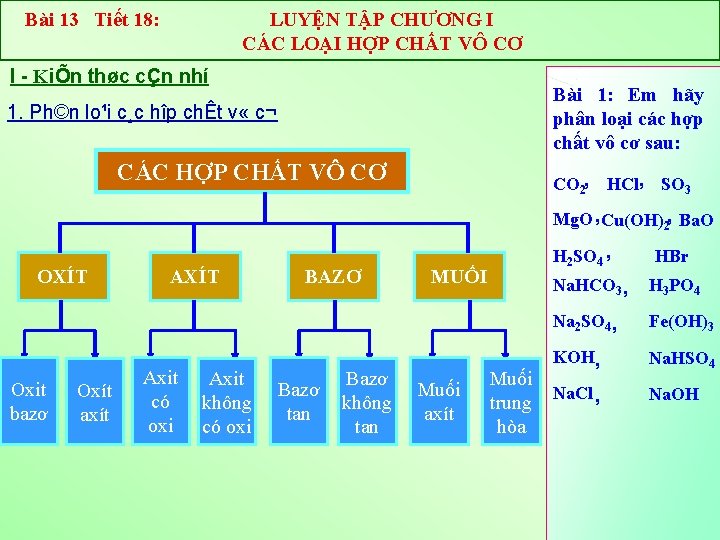
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí Bài 1: Em hãy phân loại các hợp chất vô cơ sau: 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ CÁC HỢP CHẤT VÔ CƠ CO 2, HCl, SO 3 Mg. O , Cu(OH)2, Ba. O OXÍT Oxit bazơ Oxít axít AXÍT Axit có oxi Axit không có oxi BAZƠ Bazơ tan Bazơ không tan H 2 SO 4 , MUỐI Muối axít Muối trung hòa HBr Na. HCO 3, H 3 PO 4 Na 2 SO 4, Fe(OH)3 KOH, Na. HSO 4 Na. Cl , Na. OH

Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ 2. Tính chất hóa học của các loại hợp chất vô cơ

Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ Bài 2. Hãy chọn những chất thích hợp điền vào (…) các phương trình hóa học cho mỗi loại hợp chất: Nhóm 1 Nhóm 2 1. Oxit 2. Baz¬ a) Oxit baz¬ +n íc… baz¬ ; b) Oxit baz¬ + axit … muèi + n íc ; b) Baz¬ +oxit…axit muèi + n íc ; c) Oxit axit + n íc. . . axit ; a) Baz¬ + axit … muèi + n íc ; c) Baz¬ +muèi … muèi + baz¬ ; t 0 d) Oxit axit + baz¬ … muèi + n íc ; d) Baz¬ … oxit baz¬ + n íc ; Nhóm 4 e) Oxit axit + oxit baz¬ muèi … 4. Muèi Nhóm 3 3. Axit a) Muèi + axit … axit + muèi ; a) Axit + kim…lo¹i muèi + hi®ro ; b) Muèi + baz¬ … muèi + baz¬ ; b) Axit + baz¬ … muèi + n íc ; c) Muèi + muèi … muèi + muèi ; c) Axit + oxir…baz¬ muèi + n íc ; d) Muèi + kim … lo¹i muèi + kim lo¹i ; t 0 NhiÒu chÊt d) Axit + muèi … muèi + axit ; e) Muèi … míi
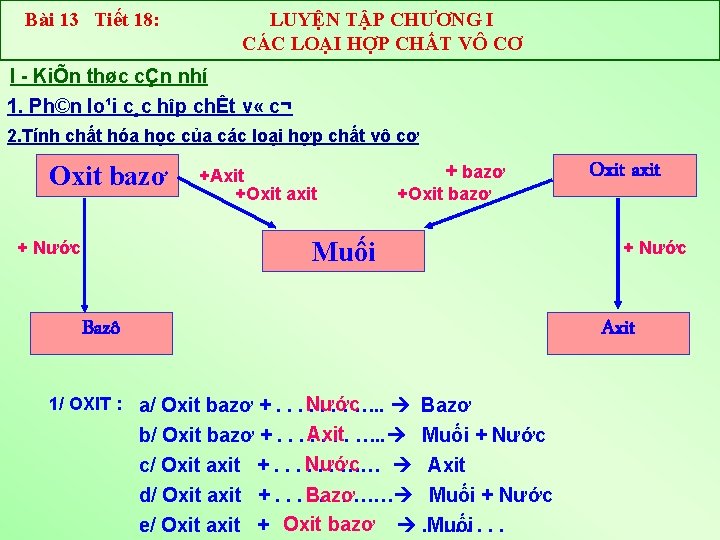
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ 2. Tính chất hóa học của các loại hợp chất vô cơ Oxit bazơ +Axit +Oxit axit + bazơ +Oxit bazơ Muối + Nước Bazô Oxit axit + Nước Axit 1/ OXIT : a/ Oxit bazơ +. . . Nước. . …. . Bazơ b/ Oxit bazơ +. . . Axit. . …. . Muối + Nước c/ Oxit axit +. . . Nước. . . …… Axit d/ Oxit axit +. . . Bazơ. . …… Muối + Nước e/ Oxit axit + Oxit bazơ . Muối. . . .
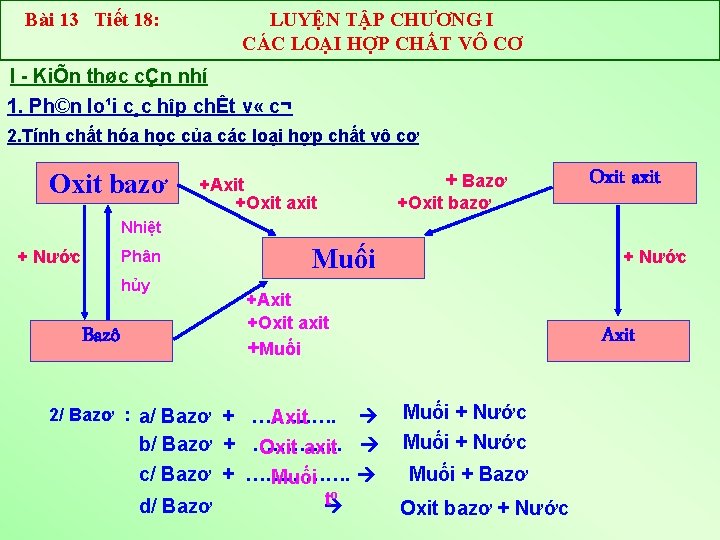
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ 2. Tính chất hóa học của các loại hợp chất vô cơ Oxit bazơ + Bazơ +Axit +Oxit axit +Oxit bazơ Oxit axit Nhiệt + Nước Phân hủy Bazô Muối +Axit +Oxit axit +Muối 2/ Bazơ : a/ Bazơ + …………. Axit b/ Bazơ + …………. . Oxit axit c/ Bazơ + ……………. Muối d/ Bazơ + Nước o t Axit Muối + Nước Muối + Bazơ Oxit bazơ + Nước
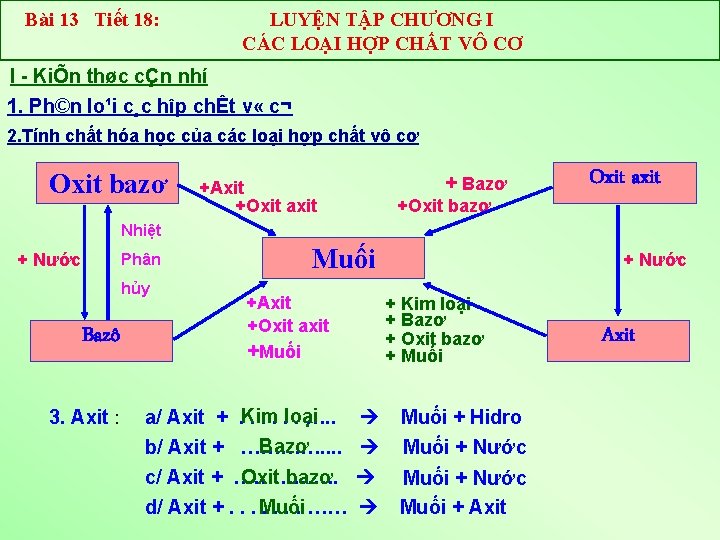
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ 2. Tính chất hóa học của các loại hợp chất vô cơ Oxit bazơ + Bazơ +Axit +Oxit axit +Oxit bazơ Oxit axit Nhiệt + Nước Phân hủy Bazô 3. Axit : Muối +Axit +Oxit axit +Muối a/ Axit +. Kim. . loại. …. . Bazơ b/ Axit + …………. . c/ Axit + ……………. Oxit bazơ d/ Axit +. . . Muối. . …… + Nước + Kim loại + Bazơ + Oxit bazơ + Muối + Hidro Muối + Nước Muối + Axit
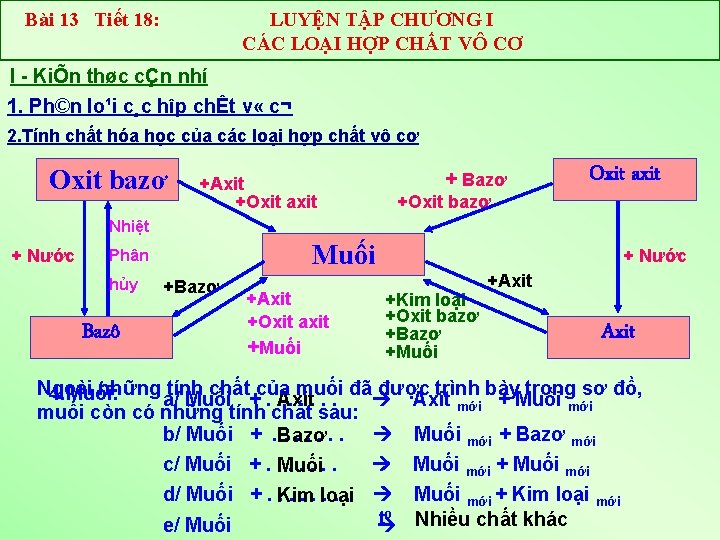
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí 1. Ph©n lo¹i c¸c hîp chÊt v « c¬ 2. Tính chất hóa học của các loại hợp chất vô cơ Oxit bazơ +Axit +Oxit axit + Bazơ +Oxit bazơ Oxit axit Nhiệt + Nước Muối Phân hủy Bazô +Bazơ +Axit +Oxit axit +Muối + Nước +Kim loại +Oxit bazơ +Bazơ +Muối +Axit Ngoài những tính chất của muối đã được trình bày trong sơ đồ, 4. Muối: a/ Muối +. . Axit. . . Axit mới + Muối mới muối còn có những tính chất sau: b/ Muối +. Bazơ. . . Muối mới + Bazơ mới c/ Muối +. . Muối. . . Muối mới + Muối mới d/ Muối +. Kim. . loại. . . Muối mới + Kim loại mới to Nhiều chất khác e/ Muối
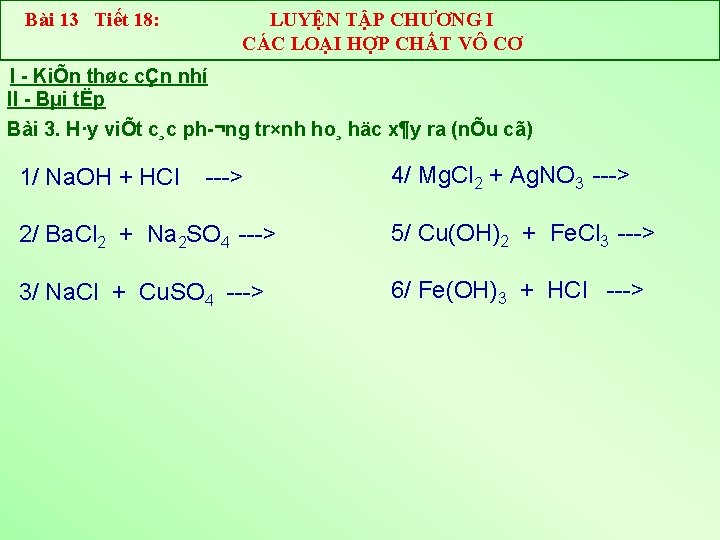
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ I KiÕn thøc cÇn nhí II Bµi tËp Bài 3. H·y viÕt c¸c ph ¬ng tr×nh ho¸ häc x¶y ra (nÕu cã) 1/ Na. OH + HCl > 4/ Mg. Cl 2 + Ag. NO 3 > 2/ Ba. Cl 2 + Na 2 SO 4 > 5/ Cu(OH)2 + Fe. Cl 3 > 3/ Na. Cl + Cu. SO 4 > 6/ Fe(OH)3 + HCl >
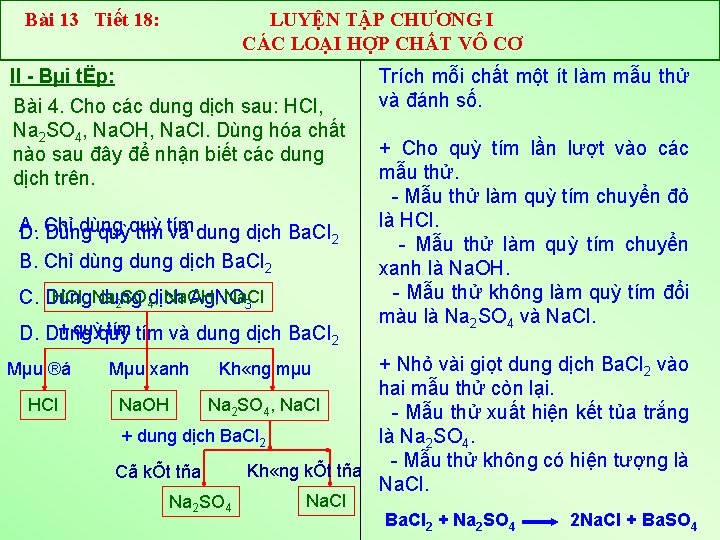
Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ II Bµi tËp: Bài 4. Cho các dung dịch sau: HCl, Na 2 SO 4, Na. OH, Na. Cl. Dùng hóa chất nào sau đây để nhận biết các dung dịch trên. A. dùng D. Chỉ Dùng quỳquỳ tím. và dung dịch Ba. Cl 2 B. Chỉ dùng dung dịch Ba. Cl 2 HCl, Na. OH, Na. Cl C. Dùng dung dịch Ag. NO 2 SO 4 3 + quỳquỳ tím và dung dịch Ba. Cl D. Dùng 2 Mµu ®á HCl Trích mỗi chất một ít làm mẫu thử và đánh số. + Cho quỳ tím lần lượt vào các mẫu thử. Mẫu thử làm quỳ tím chuyển đỏ là HCl. Mẫu thử làm quỳ tím chuyển xanh là Na. OH. Mẫu thử không làm quỳ tím đổi màu là Na 2 SO 4 và Na. Cl. + Nhỏ vài giọt dung dịch Ba. Cl 2 vào hai mẫu thử còn lại. Na. OH Na 2 SO 4, Na. Cl Mẫu thử xuất hiện kết tủa trắng + dung dịch Ba. Cl 2 là Na 2 SO 4. Mẫu thử không có hiện tượng là Kh «ng kÕt tña Cã kÕt tña Na. Cl. Mµu xanh Kh «ng mµu Na 2 SO 4 Na. Cl Ba. Cl 2 + Na 2 SO 4 2 Na. Cl + Ba. SO 4

Bài 13 Tiết 18: LUYỆN TẬP CHƯƠNG I CÁC LOẠI HỢP CHẤT VÔ CƠ II Bµi tËp: Bµi tËp 5: Hoµ tan hoµn toµn 9, 2 g hçn hîp gåm Mg, Mg. O b» ng dung dÞch HCl d. Sau ph¶n øng thu ® îc 1, 12 l khÝ hi®ro (ë ®ktc). a. ViÕt ph ¬ng tr×nh hãa häc. b. TÝnh phÇn tr¨m theo khèi l îngmçi chÊt trong hçn hîp ban ®Çu. Tãm t¾t: Cho 9, 2 g hh Mg + HCl d Mg. O a. ViÕt PTHH b. TÝnh %Mg, %Mg. O 1, 12 lÝt H 2 (®ktc) C¸c b íc gi¶i phÇn b TÝnh Dùa vµo => TÝnh % Mg => %Mg. O =>

HƯỚNG DẪN VỀ NHÀ 1. ¤n tËp tÝnh chÊt ho¸ häc cña c¸c lo¹i hîp chÊt v « c¬. (Dùa vµo s¬ ®å mèi liªn hÖ). 2. Làm các bài tập 1, 2, 3, sgk/ 43 3. T×m hiÓu bµi thùc hµnh: “TÝnh chÊt hãa häc cña Baz¬ vµ muèi”

Bµi tËp 3: (SGK trang 43) Trén mét dung dÞch cã hoµ tan 0, 2 mol Cu. Cl 2 víi mét dung dÞch cã hoµ tan 20 g Na. OH. Läc hçn hîp c¸c chÊt sau ph¶n øng, ® îc kÕt tña vµ n íc läc. Nung kÕt tña ®Õn khi khèi l îng kh «ng ®æi. a, ViÕt c¸c ph ¬ng tr×nh ho¸ häc. b, TÝnh khèi l îng chÊt r¾n thu ® îc sau khi nung. c, TÝnh khèi l îng c¸c chÊt tan cã trong n íc läc. - Đề bài cho: số mol của Cu. Cl 2 = 0, 2 mol m. Na. OH= 20 g n. Na. OH = 20/40 = 0, 2 mol a/ Phương trình: (1) 1 mol 2 mol (2) 1 mol b/ Khối lượng chất rắn sau khi nung là khối lượng của Cu. O. Lập tỉ lệ để so sánh số mol của Cu. Cl 2 và Na. OH Số mol chất dư. Số mol của Cu(OH)2 tính dựa vào số mol chất thiếu. - Từ phương trình (1) và (2) Số mol Cu. O = số mol Cu(OH)2 Khối lượng Cu. O c/ Khối lượng các chất trong nước lọc gồm Na. Cl và Na. OH dư hoặc Cu. Cl 2 dư
Trò chơi chọn số 1 2 3 4 5 6 7 8 1. 2. 3. 4. 5. 6. 7. 8. Dung Có Hợp Ure chất dịch dùng loại nào chất phân Khí thuốc sau nào bón đây thử sau hóa có nào đây tác sau tác tạo dụng chỉ dụng đây ra chứa khử mưa để được nhận 1 chua axit. trong với biết cho dd 3 sai? nguyên dd đất Na. OH? Na. Cl trồng tố Dung dịch H Cu(OH) Si. O Có làm quì loại quì tím hợp hóa chất xanh. vô Đúng cơ Đúng hay sai? Có 8 thể ôlà số được cho 2 học đội chơi. đỏ. 2 chia 3đều 2 mấy dinh dưỡng chính nào của thực vật. - Nếu chọn ô nào thì phải trả lời câu hỏi tương ứng của ô đó. Trả lời sai a) CO b) b) CH c) SO d)Kali Ca. O O 2 a) a) Quì Nitơ tím Ba. Cl photpho c) Na. Cl Ag. NO c) d) dd. Cu. SO 4 b) loại c c) aa) c d đúng sẽ được trả lời có 2 HCl 4 Cu. Cl 2điểm. b dd a) Ba. Cl b) SAI c)dd KNO d) Na. Cl b) Ca. Cl 4 2 10 điểm, 222 sai không 3 3 -Trong 8 ô có 3 ô màu đỏ và 5 ô màu xanh. Nếu chọn trúng ô màu đỏ sẽ được cộng thêm 10 điểm. - Đội nào có tổng điểm cao đội đó thắng.

TROØ CHÔI: ÑOÄI NAØO LÀ NHÀ VÔ ĐỊCH XANH ÑOÛ Câu 1 Câu 5 Câu 2 Câu 6 Câu 3 Câu 7 Câu 4 Câu 8 Dung dịch chất nào sau đây tác dụng được với dd Na. OH Ure là loại phân bón hóa học chỉ chứa 1Đúng trong 3 nguyên Có mấy loại hợp chất vô cơ Có Dung thể dùng dịch thuốc H Cu(OH) Si. O làm nào quì sau tím đây hóa để đỏ. xanh. nhận biết Đúng hay dd sai hay Na. Cl saitố nào sau đây tạo ra mưa axit. 2 khí 3 thử 2 làm Hợp chất nào sau đây có tác dụng khử chua cho đất trồng dinh dưỡng chính nào của thực vật. SAI Ba. Cl d) c) Na. Cl a) CO 2 b) dd b) CH c)Na. Cl d) O 42 loại sai b) Cu. Cl a) a) Quì tím Ba. Cl c)c)dd. KNO Ag. NO d) Kali dd. Cu. SO 3 SO 4 photpho 2 24 b) d) Ca. O 2 3 3 a) Nitơ HCl b) Ca. Cl c) 2

- Slides: 16