PHARMACOGENETIQUE Jean Baptiste Woillard UMR Inserm S 850

PHARMACOGENETIQUE Jean Baptiste Woillard UMR Inserm S 850 Pharmacologie, Toxicologie et Pharmacovigilance, CHU Limoges Pharmacologie médicale, Faculté de Médecine de Limoges No conflict of interest to declare 1

Définition et objectifs de la pharmacogénétique La pharmacogénétique étudie l’influence de la séquence d’ADN (variabilité génétique) sur la réponse aux médicaments : • Explique une partie de la variabilité inter-individuelle : • • • d’ordre pharmacocinétique : variations génétiques concernant l’expression ou l’activité des protéines impliquées dans le métabolisme ou le transport des médicaments d’ordre pharmacodynamique : variations concernant les gènes codant pour des récepteurs ou autres protéines cibles des M. 2

Définition et objectifs de la pharmacogénétique Objectifs • • • mettre au point des tests de dépistage génétique permettant d’identifier les sujets répondeurs et non répondeurs à un médicament donné Identifier les sujets à risque de survenue d’un événement indésirable pour un médicament donné Prévoir la dose la plus adaptée à chaque individu pour un médicament donné 3

Pharmacogénétique : une discipline récente ? • Pythagore (510 av. J-C) à propos du favisme : « ce qui peut être nourriture pour certains, peut être poison violent pour d’autres » • 1959, Friedrich Vogel définit le terme « pharmacogénétique = bases héréditaires de la variabilité des effets des M. » 4
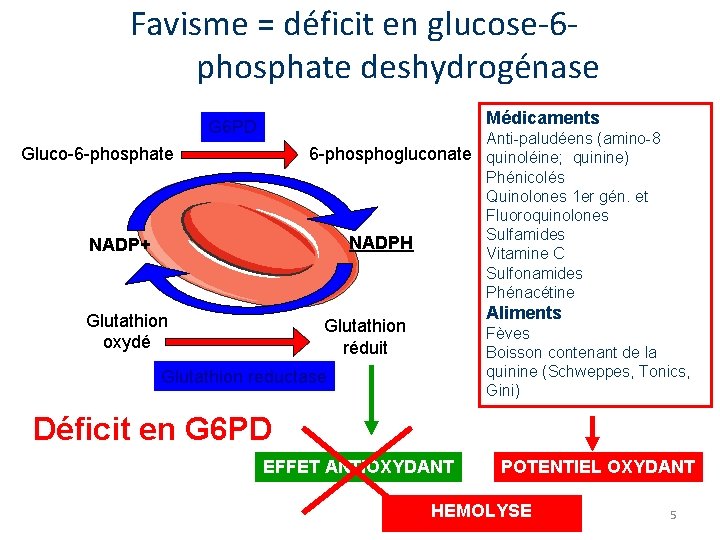
Favisme = déficit en glucose-6 phosphate deshydrogénase Médicaments G 6 PD Anti-paludéens (amino-8 6 -phosphogluconate quinoléine; quinine) Phénicolés Quinolones 1 er gén. et Fluoroquinolones Sulfamides NADPH Vitamine C Sulfonamides Phénacétine Gluco-6 -phosphate NADP+ Glutathion oxydé Aliments Glutathion réduit Fèves Boisson contenant de la quinine (Schweppes, Tonics, Gini) Glutathion reductase Déficit en G 6 PD EFFET ANTIOXYDANT POTENTIEL OXYDANT HEMOLYSE 5

Notions de génétique en pharmacogénétique Rappel de génétique moléculaire • Le génome humain – ~ 3 milliards de paires de bases – 20 000 – 25 000 gènes – 2% du génome codant pour des protéines • Séquence comportant des variations génétiques • • ~ 10 millions de paires de base Un gène sur trois a des variations fréquentes 6

Polymorphismes génétiques • • • Différence de la séquence d’ADN à une position donnée (gène), pour des individus d’une même espèce Un gène est dit polymorphe lorsqu'il existe, dans une population, sous plusieurs formes chez au moins 1% des individus. NB. Polymorphisme ≠ mutation q Mutations (variations pathologiques) • Rare (< 1%) • Diagnostique de maladie génétique • Implications physiopathologiques et/ou thérapeutiques q Polymorphismes (variations neutres) • > 1% de la population. • Permet la cartographie physique du génome, l’identification des individus • susceptibilité individuelle aux médicaments 7

Polymorphismes génétiques • Macrolésions – Remaniement concernant l’intégralité du gène – Fusion, duplication, ou délétion du gène – Peu fréquent Exemple : duplication du cytochrome P 450 2 D 6 ADN Gène « normal » CYP 2 D 6*1 ou 2 D 6*2 ARNm aagggacta… Gène dupliqué CYP 2 D 6*1 x 2 ou 2 D 6*2 x 2 aagggacta… Protéine 8

Polymorphismes génétiques • Microlésions – Remaniement concernant une à quelques bases nucléotidiques – Trois types de microlésions : • • • Insertion (ajout d’un à quelques nucléotides) Délétion (disparition d’un à quelques nucléotides) Substitution (Single Nucleotide Polymorphism : « SNP » ) Très fréquent (un SNP / 100 à 1000 paires de base soit au total, 11. 8 millions de SNP référencés – Conséquences variables • • Modification de la séquence protéique Modification de l’expression protéique 9
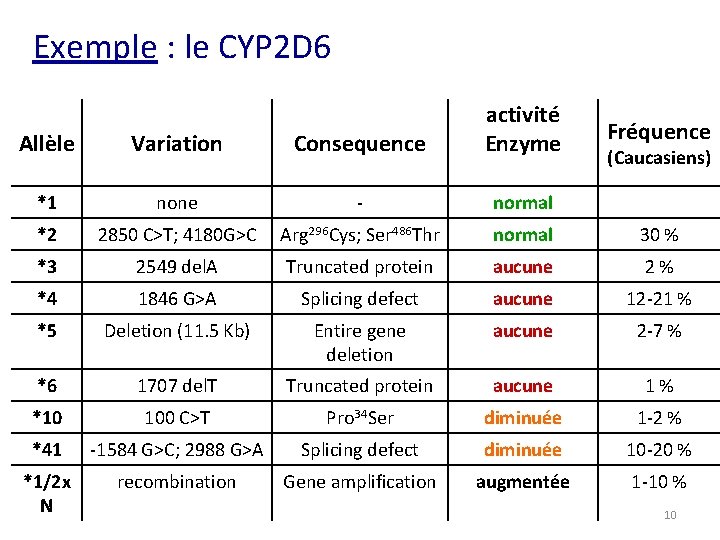
Exemple : le CYP 2 D 6 Allèle Variation Consequence activité Enzyme *1 none - normal *2 2850 C>T; 4180 G>C Arg 296 Cys; Ser 486 Thr normal 30 % *3 2549 del. A Truncated protein aucune 2 % *4 1846 G>A Splicing defect aucune 12 -21 % *5 Deletion (11. 5 Kb) Entire gene deletion aucune 2 -7 % *6 1707 del. T Truncated protein aucune 1 % *10 100 C>T Pro 34 Ser diminuée 1 -2 % *41 -1584 G>C; 2988 G>A Splicing defect diminuée 10 -20 % *1/2 x N recombination Gene amplification augmentée 1 -10 % Fréquence (Caucasiens) 10
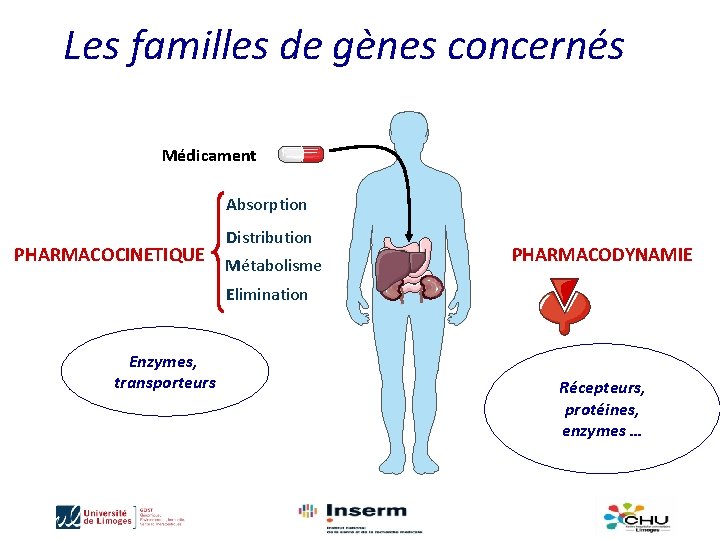
Les familles de gènes concernés Médicament Absorption PHARMACOCINETIQUE Distribution Métabolisme PHARMACODYNAMIE Elimination Enzymes, transporteurs Récepteurs, protéines, enzymes … 11
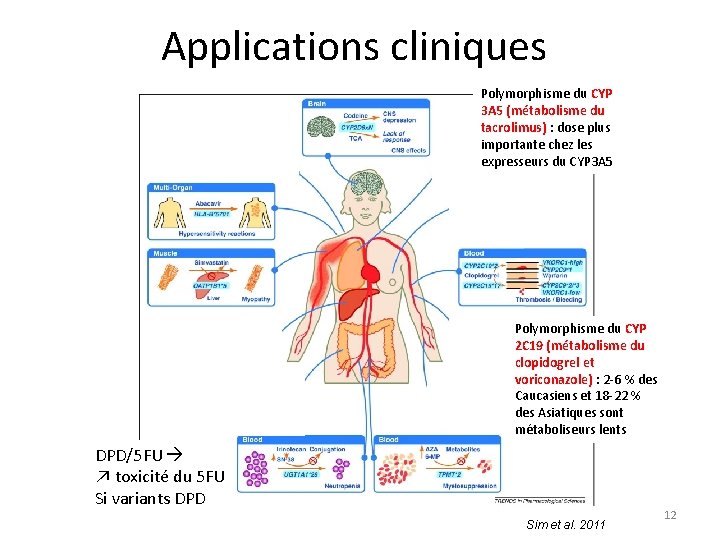
Applications cliniques Polymorphisme du CYP 3 A 5 (métabolisme du tacrolimus) : dose plus importante chez les expresseurs du CYP 3 A 5 Polymorphisme du CYP 2 C 19 (métabolisme du clopidogrel et voriconazole) : 2 -6 % des Caucasiens et 18 -22 % des Asiatiques sont métaboliseurs lents DPD/5 FU ↗ toxicité du 5 FU Si variants DPD Sim et al. 2011 12

Exemple : tacrolimus/CYP 3 A 5 • 80 % des M. sont transformés par les mono-oxygénases hépatiques (dont les cytochromes P 450) • CYP 3 A 5*3 protéine tronquée = non expresseur du CYP 3 A 5 (=85% des caucasiens) • Expresseur besoin d’une dose 2 X pour atteindre le même C 0 • 0. 15 mg/kg b. i. d. vs • 0. 075 mg/kg b. i. d. Zheng et al CPT 2012 Thervet et al CPT 2010
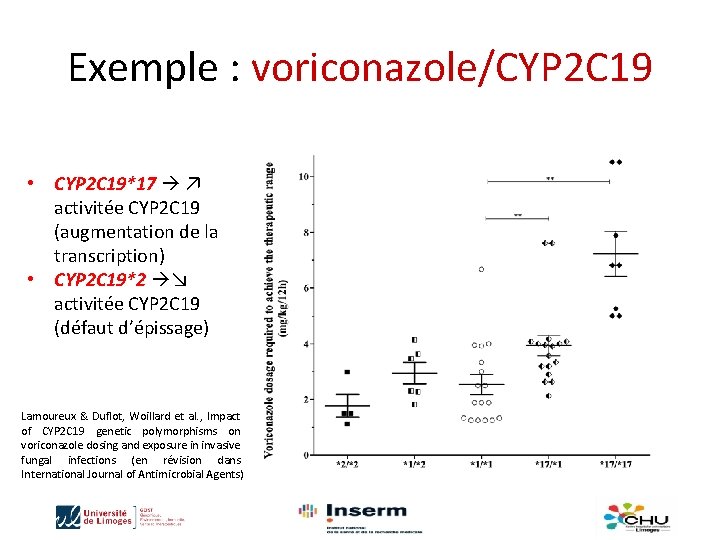
Exemple : voriconazole/CYP 2 C 19 • CYP 2 C 19*17 ↗ activitée CYP 2 C 19 (augmentation de la transcription) • CYP 2 C 19*2 ↘ activitée CYP 2 C 19 (défaut d’épissage) Lamoureux & Duflot, Woillard et al. , Impact of CYP 2 C 19 genetic polymorphisms on voriconazole dosing and exposure in invasive fungal infections (en révision dans International Journal of Antimicrobial Agents)

Exemple toxicogénétique
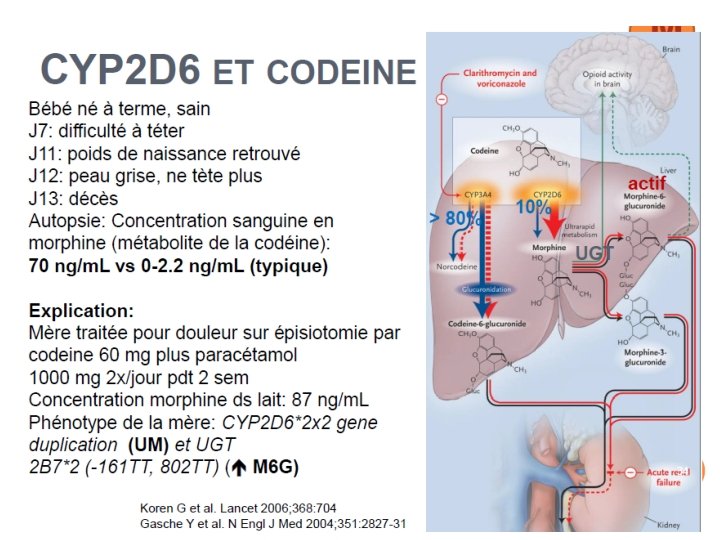
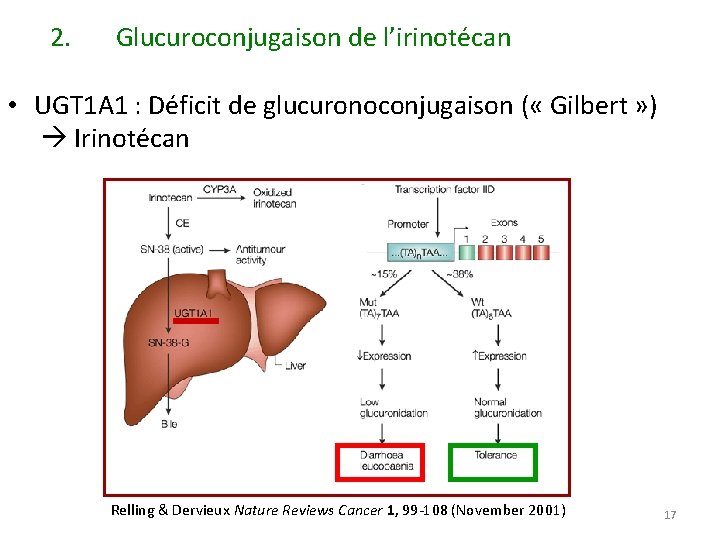
2. Glucuroconjugaison de l’irinotécan • UGT 1 A 1 : Déficit de glucuronoconjugaison ( « Gilbert » ) Irinotécan Relling & Dervieux Nature Reviews Cancer 1, 99 -108 (November 2001) 17
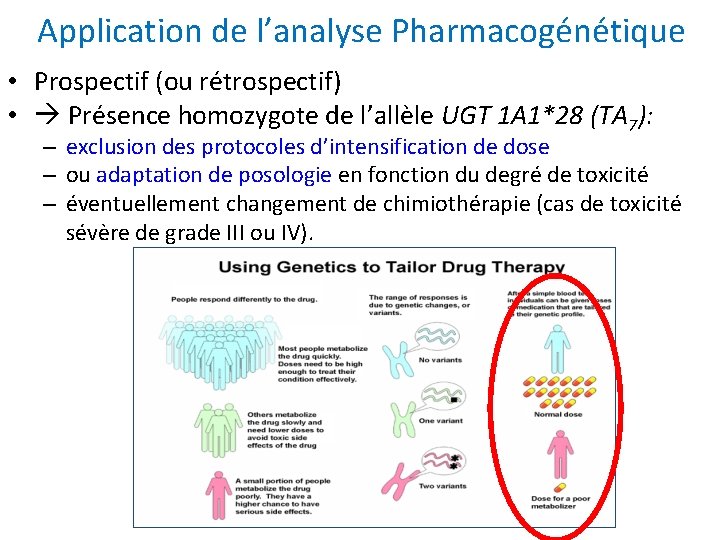
Application de l’analyse Pharmacogénétique • Prospectif (ou rétrospectif) • Présence homozygote de l’allèle UGT 1 A 1*28 (TA 7): – exclusion des protocoles d’intensification de dose – ou adaptation de posologie en fonction du degré de toxicité – éventuellement changement de chimiothérapie (cas de toxicité sévère de grade III ou IV).
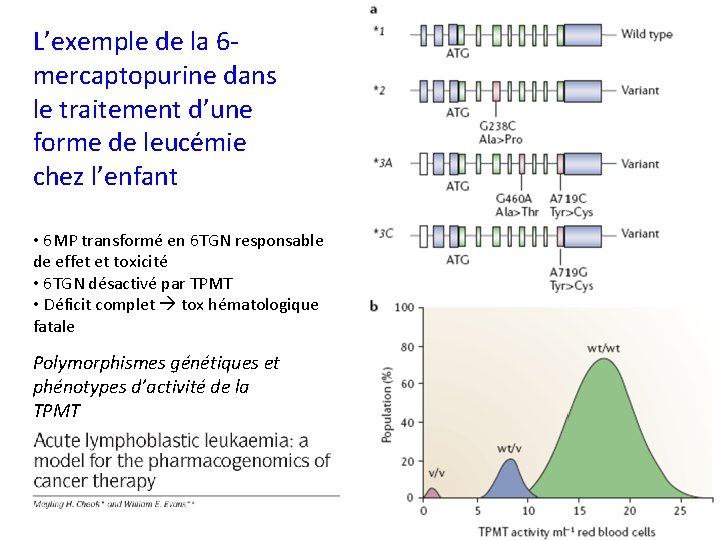
L’exemple de la 6 mercaptopurine dans le traitement d’une forme de leucémie chez l’enfant • 6 MP transformé en 6 TGN responsable de effet et toxicité • 6 TGN désactivé par TPMT • Déficit complet tox hématologique fatale Polymorphismes génétiques et phénotypes d’activité de la TPMT
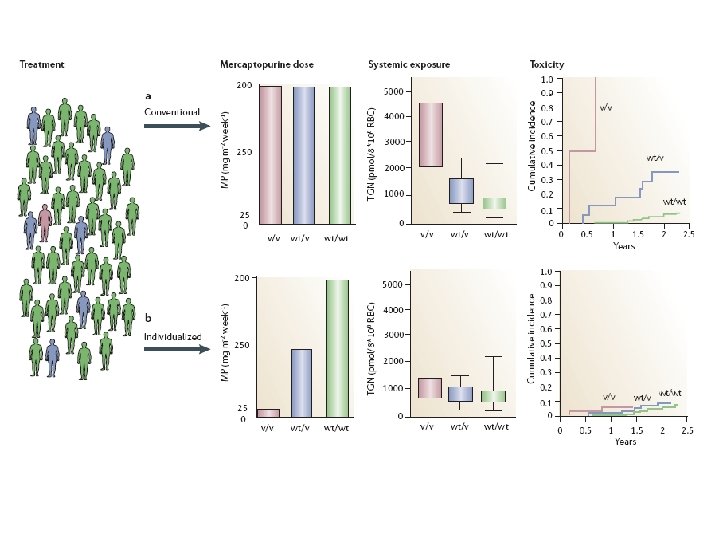

• Conséquences des polymorphismes indésirables rapide Ann Biol Clin 2004, 62, Allorge et Loriot 21

Identification du phénotype • Déterminer son génotype par techniques de génétique moléculaire • Administrer des médicaments tests (spécifiques de l’isoforme) doser le M. et son métabolite calculer le rapport métabolique (concentration du métabolite/concentration du produit parent). • Doser et adapter les thérapeutiques habituelles (attitude pragmatique) … si le risque vital n’est pas engagé. 22

Type d’études en pharmacogénétique – Les approches gène(s) candidat(s) : • hypothèse mécanistique impliquant le(s) gène(s) étudié(s) dans le phénotype d’intérêt. • nombre de SNPs étudié limité • étude par haplotype si les SNPs sont en déséquilibre de liaison – Les approches pan-génomiques ou GWAS (Genome Wide Association Study) • utilisation des puces à ADN ou NGS. • s’intéressent à la variabilité de l’intégralité du génome, sans hypothèse biologique. • grand nombre de polymorphismes testés nombre de sujets suffisant pour garantir une puissance statistique correcte.

Conclusion « ce qu’il faut retenir » • Polymorphismes génétique fréquents ≠ mutation • Expliquent en partie la variabilité inter-individuelle • Avant d’envisager un problème lié à un polymorphisme, recher la présence en réalisant un dosage • d’une interaction médicamenteuse • d’un problème d’observance • ou d’absorption • Nombreuses applications, le séquençage haut débit ouvrant la porte à de nouvelles identifications
- Slides: 24