Pharmacocintique et Pharmacodynamie Introduction Alain BousquetMlou Ecole Nationale

Pharmacocinétique et Pharmacodynamie Introduction Alain Bousquet-Mélou Ecole Nationale Vétérinaire de Toulouse Laboratoire de Physiologie-Pharmacologie-Thérapeutique UMR 1331 TOXALIM Equipe Pharmacocinétique Pharmacodynamie & Modélisation Vet. Agro. Sup – 22 octobre 2014 1
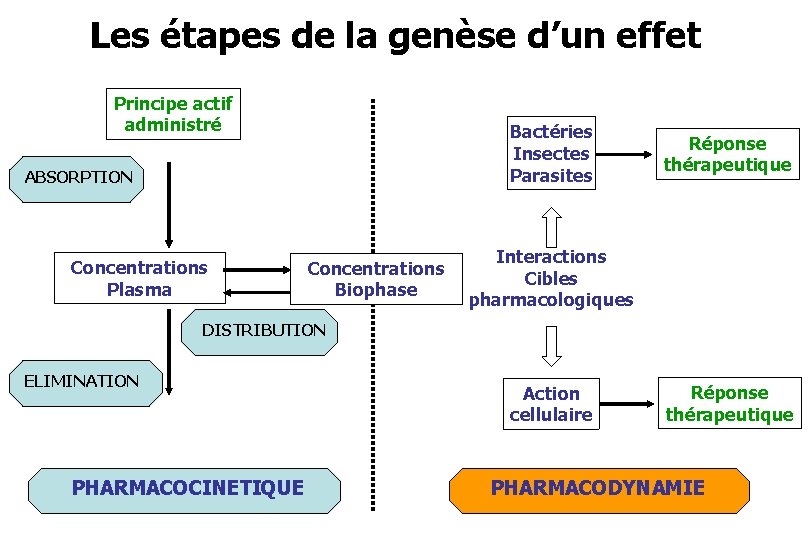
Les étapes de la genèse d’un effet Principe actif administré Bactéries Insectes Parasites ABSORPTION Concentrations Plasma Concentrations Biophase Réponse thérapeutique Interactions Cibles pharmacologiques DISTRIBUTION ELIMINATION PHARMACOCINETIQUE Action cellulaire Réponse thérapeutique PHARMACODYNAMIE
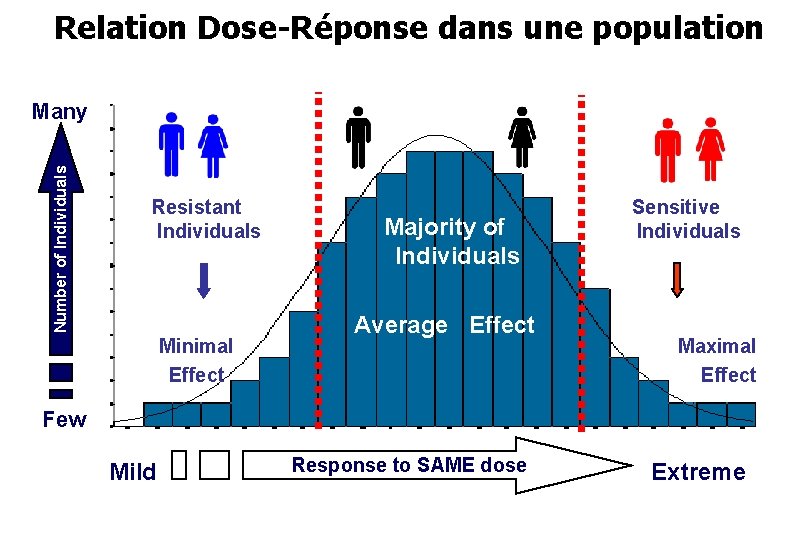
Relation Dose-Réponse dans une population Number of Individuals Many Resistant Individuals Minimal Effect Majority of Individuals Average Effect Sensitive Individuals Maximal Effect Few Mild Response to SAME dose Extreme
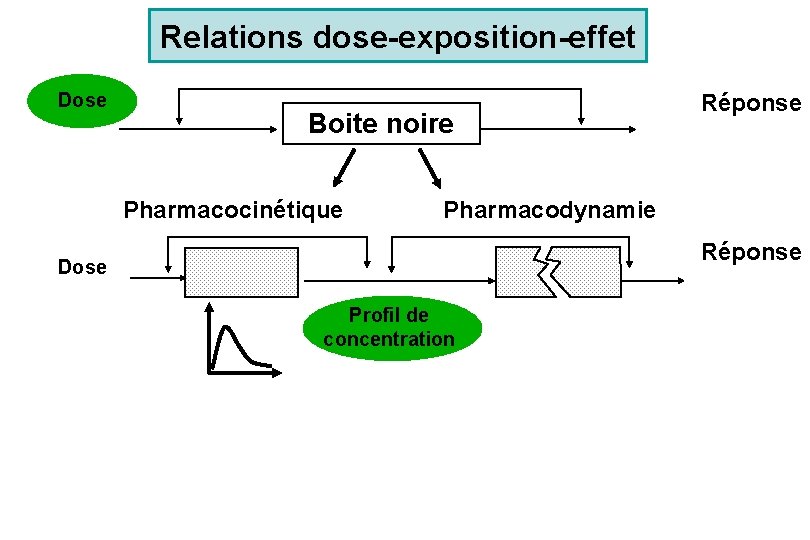
Relations dose-exposition-effet Dose Boite noire Pharmacocinétique Réponse Pharmacodynamie Réponse Dose Profil de concentration
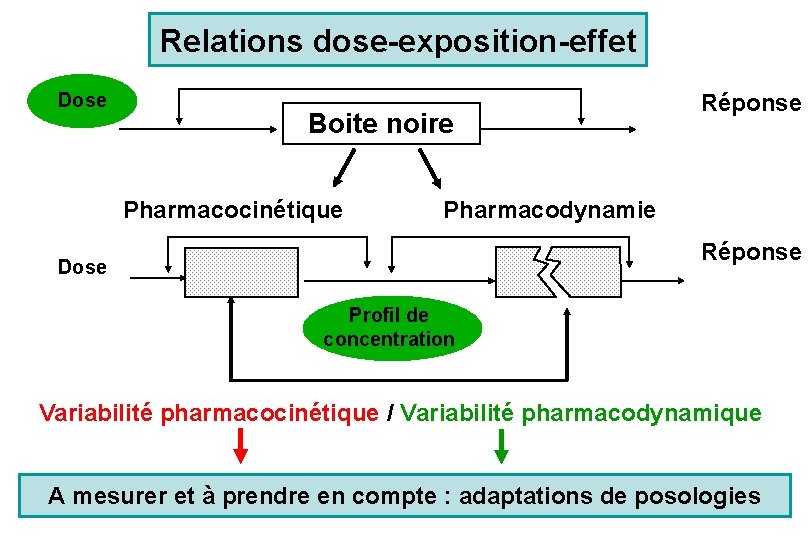
Relations dose-exposition-effet Dose Boite noire Pharmacocinétique Réponse Pharmacodynamie Réponse Dose Profil de concentration Variabilité pharmacocinétique / Variabilité pharmacodynamique A mesurer et à prendre en compte : adaptations de posologies
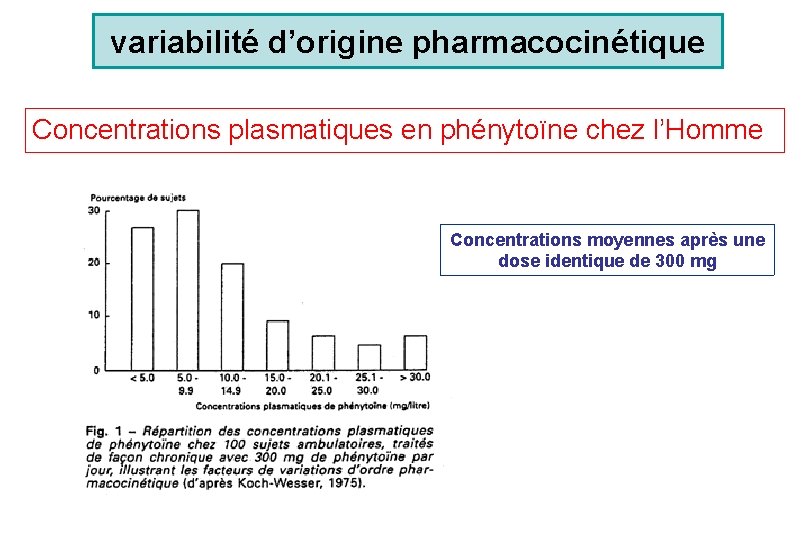
variabilité d’origine pharmacocinétique Concentrations plasmatiques en phénytoïne chez l’Homme Concentrations moyennes après une dose identique de 300 mg
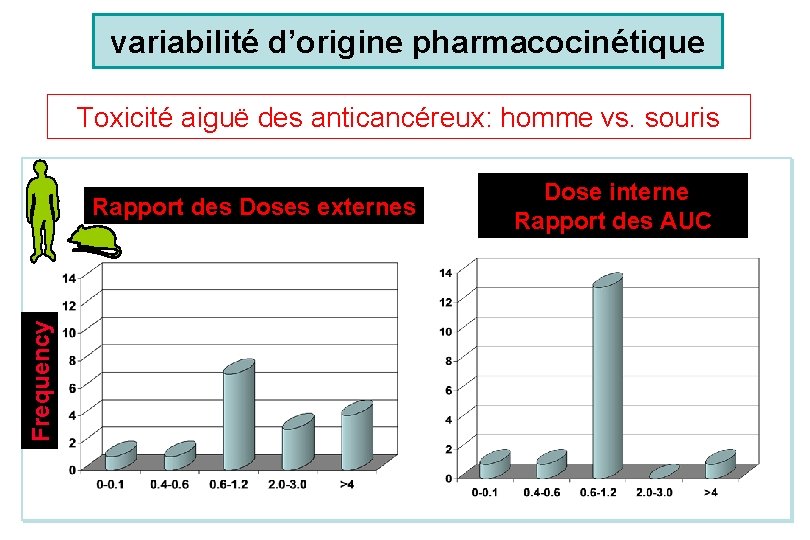
variabilité d’origine pharmacocinétique Toxicité aiguë des anticancéreux: homme vs. souris Frequency Rapport des Doses externes Dose interne Rapport des AUC
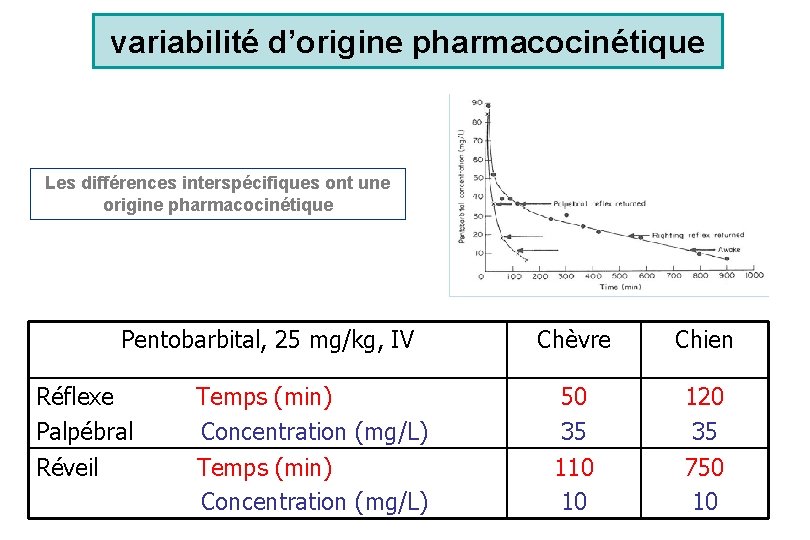
variabilité d’origine pharmacocinétique Les différences interspécifiques ont une origine pharmacocinétique Pentobarbital, 25 mg/kg, IV Chèvre Chien Réflexe Palpébral Temps (min) Concentration (mg/L) 50 35 120 35 Réveil Temps (min) Concentration (mg/L) 110 10 750 10

Les objectifs de la quantification des processus PK et PD n Quantification des effets des médicaments (PD) Relier l’intensité d’un effet avec la concentration du principe actif ¨ Objectif : déterminer la gamme de concentrations (l’exposition) associée à un effet ¨ n Quantification des processus ADME (PK) Relier la quantité de principe actif administré/ingéré aux concentrations sanguines et tissulaires ¨ Objectif : déterminer les doses externes qui conduisent à une exposition donnée ¨
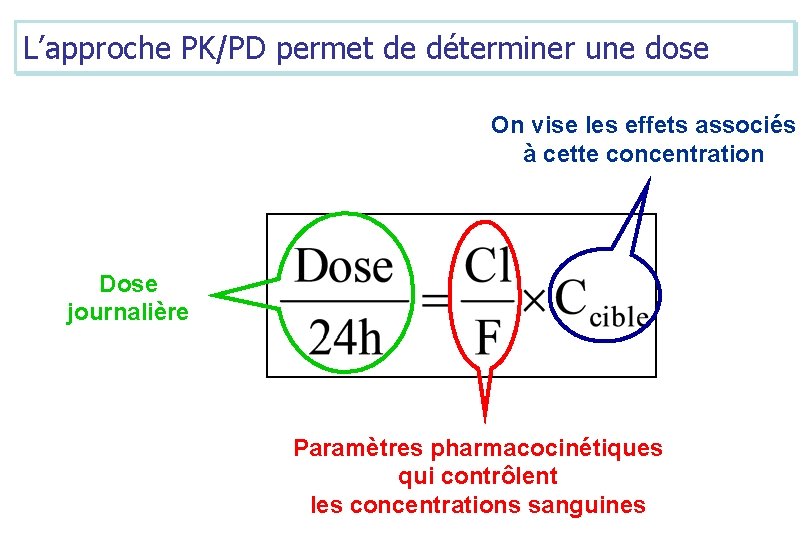
L’approche PK/PD permet de déterminer une dose On vise les effets associés à cette concentration Dose journalière Paramètres pharmacocinétiques qui contrôlent les concentrations sanguines

Extrapolation des doses Extrapolation in vitro/in vivo et interspécifique des paramètres pharmacocinétiques 11

Objectif de l’extrapolation des paramètres PK : obtenir la même exposition plasmatique 12
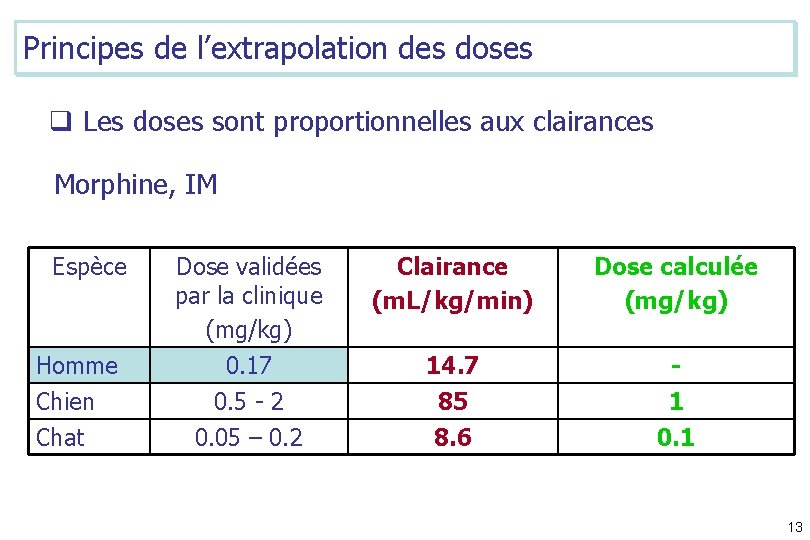
Principes de l’extrapolation des doses q Les doses sont proportionnelles aux clairances Morphine, IM Espèce Dose validées par la clinique (mg/kg) Clairance (m. L/kg/min) Dose calculée (mg/kg) 0. 17 14. 7 - Chien 0. 5 - 2 85 1 Chat 0. 05 – 0. 2 8. 6 0. 1 Homme 13

Principes de l’extrapolation des doses q Quelle posologie pour le kétoprofène chez la chèvre ? : 3 mg/kg/24 h ? Cl = 0. 17 L/kg/h Cl = 0. 74 L/kg/h Dose. CP = 13 mg/kg/24 h 14

Principes de l’extrapolation des doses q Quelle posologie pour le kétoprofène chez la chèvre ? : 3 mg/kg/24 h ? Cl = 0. 17 L/kg/h ? ? q Première dose chez l’Homme (FDIM) ? Extrapolation de la clairance 15

Extrapolation de la clairance q Extrapolation interspécifique : l’approche allométrique 16
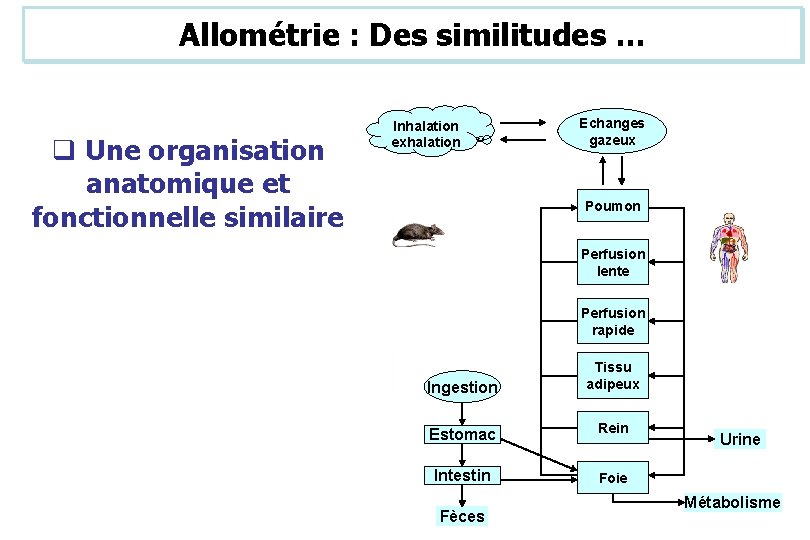
Allométrie : Des similitudes … q Une organisation anatomique et fonctionnelle similaire Inhalation exhalation Echanges gazeux Poumon Perfusion lente Perfusion rapide Ingestion Tissu adipeux Estomac Rein Intestin Foie Fèces Urine Métabolisme
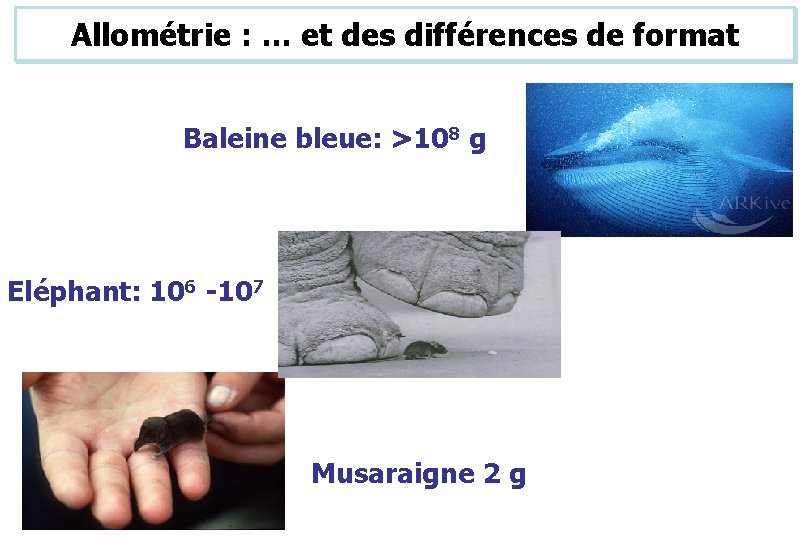
Allométrie : … et des différences de format Baleine bleue: >108 g Eléphant: 106 -107 Musaraigne 2 g
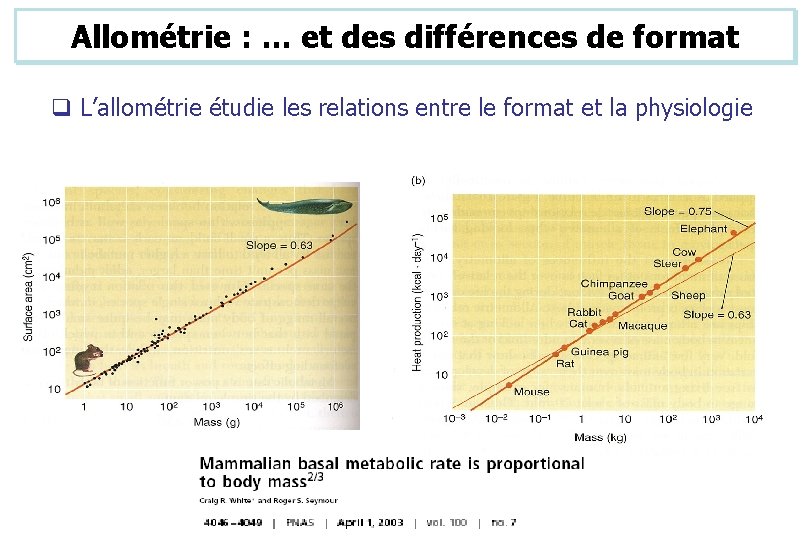
Allométrie : … et des différences de format q L’allométrie étudie les relations entre le format et la physiologie

q Allométrie : des processus physiologiques aux clairances Homme 20

Déterminants physiologiques des clairances q Débits physiologiques q Débits sanguins des organes, débit cardiaque q DFG q Liaison aux protéines plasmatiques q La fraction libre : fu q Capacités intrinsèques des systèmes épurateurs q. Clairance intrinsèque : Clint 21
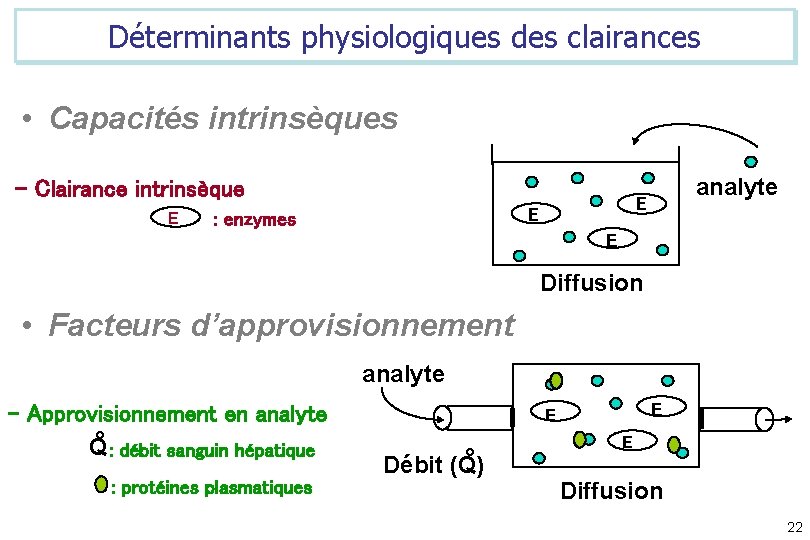
Déterminants physiologiques des clairances • Capacités intrinsèques - Clairance intrinsèque E E E : enzymes analyte E Diffusion • Facteurs d’approvisionnement analyte - Approvisionnement en analyte ° : débit sanguin hépatique Q : protéines plasmatiques E E ° Débit (Q) E Diffusion 22

Médicaments à coefficients d’extraction FORTS q Débits physiologiques q Débits sanguins des organes, débit cardiaque q DFG q Liaison aux protéines plasmatiques q La fraction libre : fu q Capacités intrinsèques des systèmes épurateurs q. Clairance intrinsèque : Clint 23
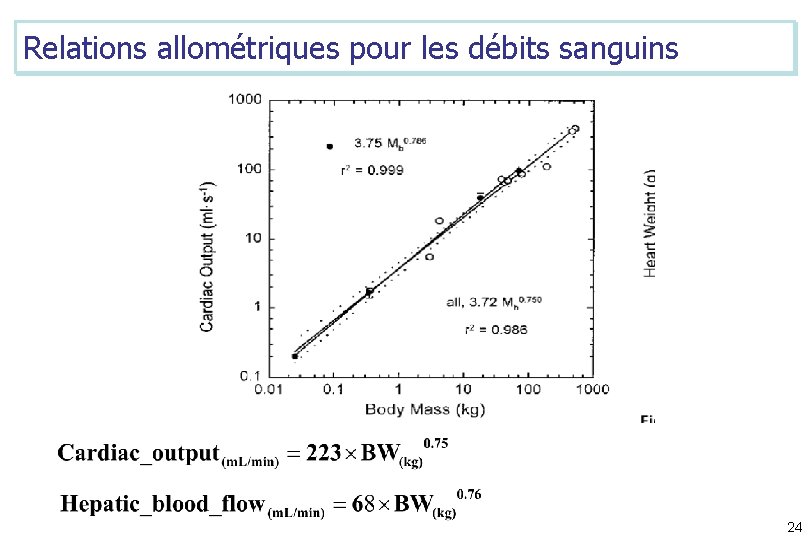
Relations allométriques pour les débits sanguins 24

Relations allométriques pour les clairances 25

Relations allométriques pour les doses 26
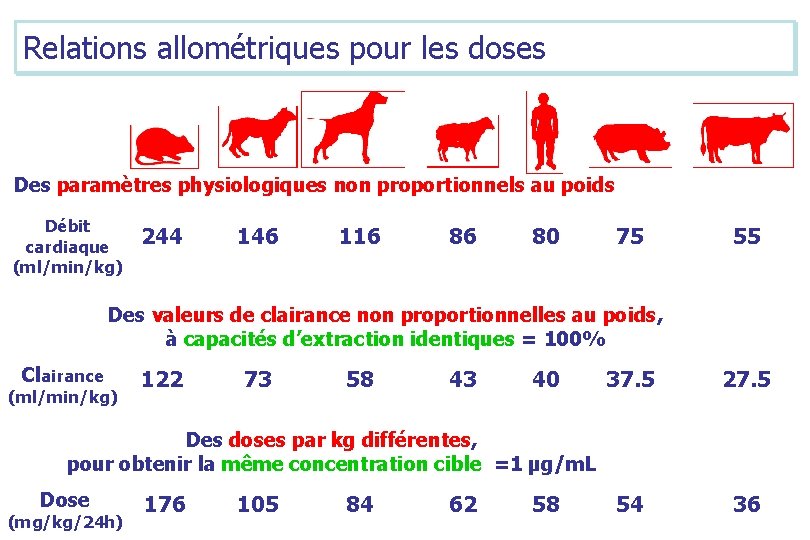
Relations allométriques pour les doses Des paramètres physiologiques non proportionnels au poids Débit cardiaque (ml/min/kg) 244 146 116 86 80 75 55 Des valeurs de clairance non proportionnelles au poids, à capacités d’extraction identiques = 100% Clairance (ml/min/kg) 122 73 58 43 40 37. 5 27. 5 54 36 Des doses par kg différentes, pour obtenir la même concentration cible =1 µg/m. L Dose (mg/kg/24 h) 176 105 84 62 58

Relations allométriques pour les doses • Loi des surfaces (doses exprimées par m 2) – b = 0. 67 – extrapolation de la première dose chez l’Homme – standardisation des doses en cancérologie, en pédiatrie (intraspécifique)

Guidance for Industry: Estimating the Maximum Safe Starting Dose in Initial Clinical Trials for Therapeutics in Adult Healthy Volunteers
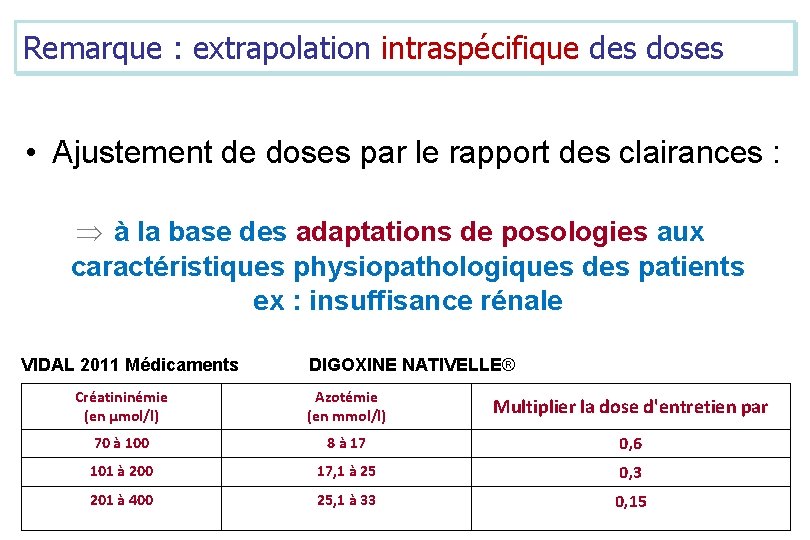
Remarque : extrapolation intraspécifique des doses • Ajustement de doses par le rapport des clairances : Þ à la base des adaptations de posologies aux caractéristiques physiopathologiques des patients ex : insuffisance rénale VIDAL 2011 Médicaments DIGOXINE NATIVELLE® Créatininémie (en µmol/l) Azotémie (en mmol/l) Multiplier la dose d'entretien par 70 à 100 8 à 17 0, 6 101 à 200 17, 1 à 25 0, 3 201 à 400 25, 1 à 33 0, 15

Remarque : extrapolation intraspécifique des doses • Ajustement de doses par le rapport des clairances : Þ à la base des adaptations de posologies aux caractéristiques physiopathologiques des patients : ex : insuffisance rénale Þ à la base des études de pharmacocinétique de population : identifier les caractéristiques individuelles associées à des variations de la clairance et quantifier ce lien

Médicaments à coefficients d’extraction FAIBLES q Débits physiologiques q Débits sanguins des organes, débit cardiaque q DFG q Liaison aux protéines plasmatiques q La fraction libre : fu q Capacités intrinsèques des systèmes épurateurs q. Clairance intrinsèque : Clint 32

Médicaments à coefficients d’extraction FAIBLES q Liaison aux protéines plasmatiques q Pas de relation avec le poids corporel q Capacités intrinsèques q Particularités d’espèces indépendantes du poids 33

Métabolisme hépatique: enzymes de phase I q L’Homme est un cas particulier Clairance du diazepam
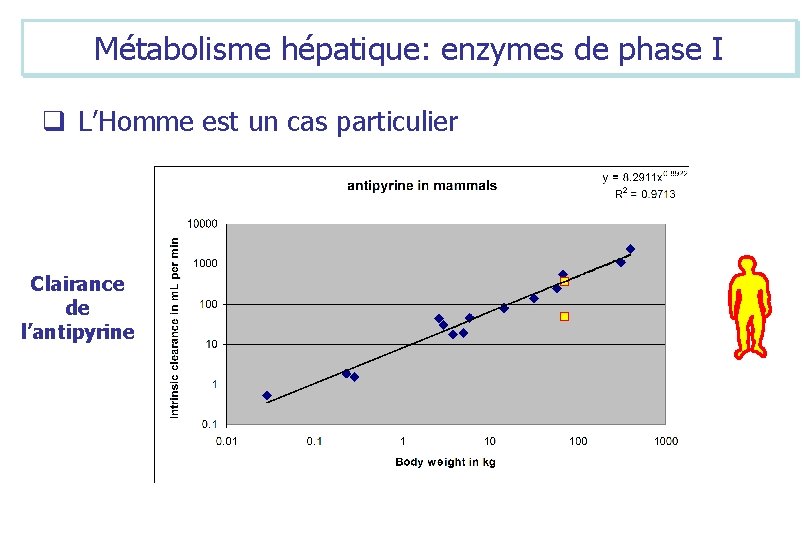
Métabolisme hépatique: enzymes de phase I q L’Homme est un cas particulier Clairance de l’antipyrine
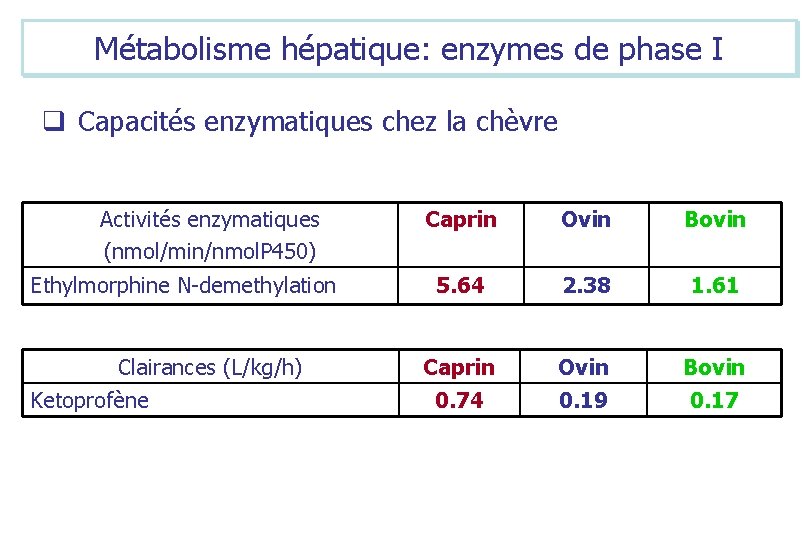
Métabolisme hépatique: enzymes de phase I q Capacités enzymatiques chez la chèvre Activités enzymatiques (nmol/min/nmol. P 450) Ethylmorphine N-demethylation Clairances (L/kg/h) Ketoprofène Caprin Ovin Bovin 5. 64 2. 38 1. 61 Caprin Ovin Bovin 0. 74 0. 19 0. 17

Métabolisme hépatique: enzymes de phase I q Capacités enzymatiques chez la chèvre q Régime alimentaire : peigneur vs brouteur q Espèce “mineure” q Posologies des bovins : sous-dosages fréquents q Résistance aux ivermectines

Métabolisme hépatique: enzymes de phase II q Des espèces avec des déficits des capacités de conjugaison Espèce Réaction de conjugaison Groupements cibles Etat de la réaction Chien, Renard Acétylation Ar-NH 2 Absent Chat Lion, Lynx glucuronidation -OH, -COOH -NH 2, =NH, -SH Présent, peu rapide Porc Sulfatation Ar-OH Ar-NH 2 Présent, faible q Sulfamides q Aspirine, paracétamol, morphine

Extrapolation de la clairance q Extrapolation interspécifique : l’approche allométrique q Extrapolation in vitro/in vivo 39

Extrapolation in vitro / in vivo de la clairance hépatique 40
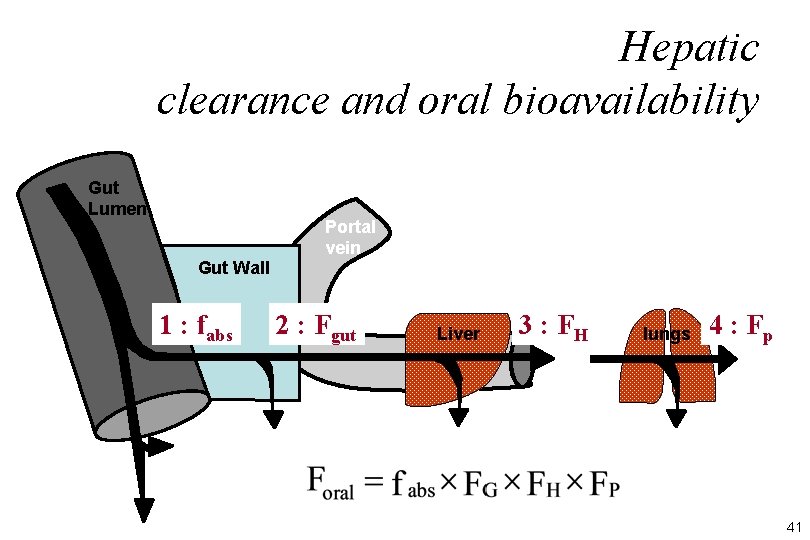
Hepatic clearance and oral bioavailability Gut Lumen Gut Wall 1 : fabs Portal vein 2 : Fgut Liver 3 : FH lungs 4 : Fp 41

Can a new drug be developed for oral route ? • Components of oral bioavailability – Absorption and first-pass effects 42

Hepatic clearance : from in vitro to in vivo • Clearance models • Hepatic clearance • Intrinsic clearance • In vitro systems to study drug metabolism • In vitro intrinsic clearance 43

Models of hepatic clearance ° Cl. H = f (QH ; fu ; Clint) • Intrinsic clearance of unbound drug, Clint : – ability of the liver to eliminate a drug when there is no “supplying” limitation ° • Hepatic blood flow, QH ; unbound fraction, fu : – parameters governing supply of the drug to enzymes in the classical hepatic clearance models 44

Availability of in vitro systems • Purified enzymes • Subcellular fractions – S 9, microsomes • Hepatocytes – Suspensions, primary cultures • Liver slices 45
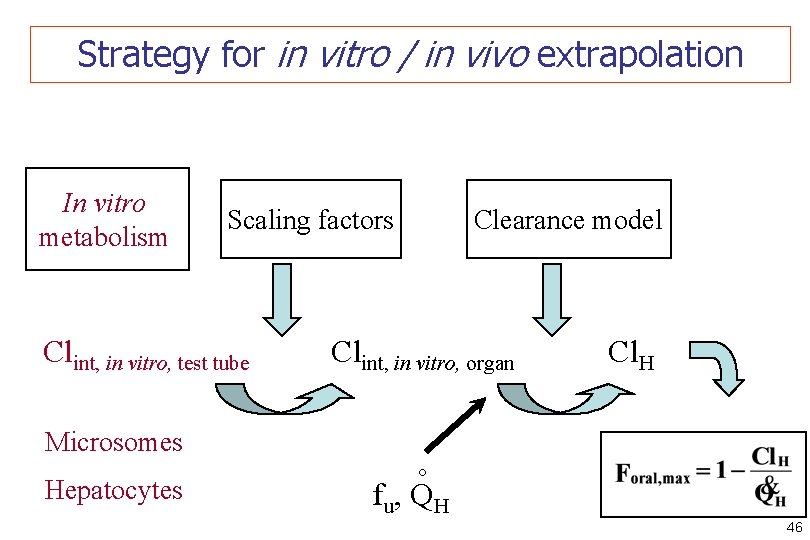
Strategy for in vitro / in vivo extrapolation Scaling factors Clint, in vitro, test tube Microsomes Hepatocytes Clearance model Clint, in vitro, organ Cl. H ° In vitro metabolism fu, QH 46
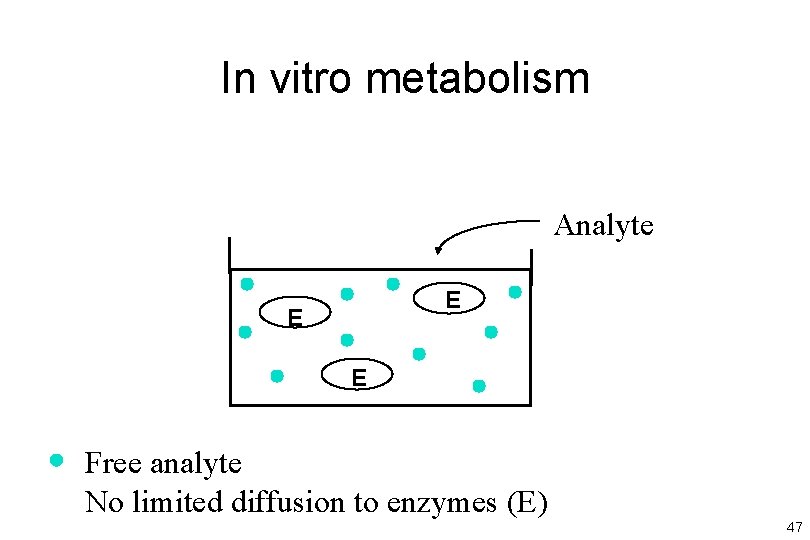
In vitro metabolism Analyte E E E Free analyte No limited diffusion to enzymes (E) 47

In vitro intrinsic clearance • Quantification of metabolism –Rate : amount per unit time • Michaelis-Menten kinetics 48
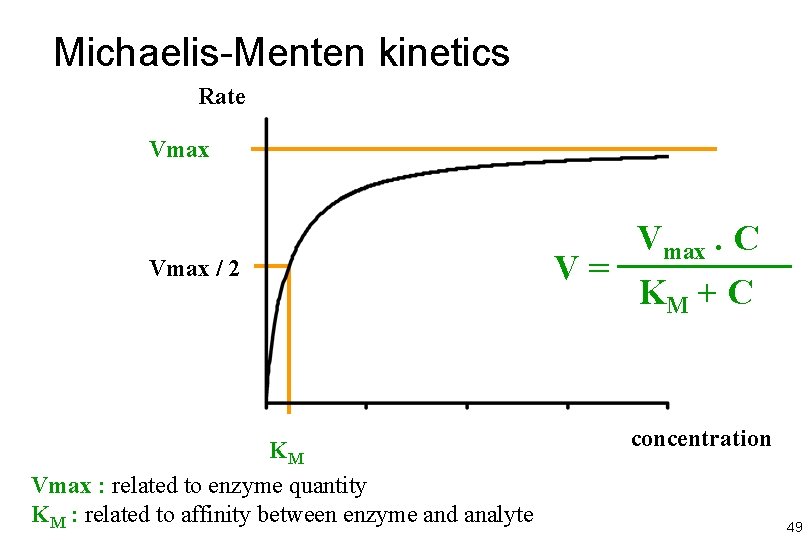
Michaelis-Menten kinetics Rate Vmax / 2 KM Vmax : related to enzyme quantity KM : related to affinity between enzyme and analyte Vmax. C V= KM + C concentration 49
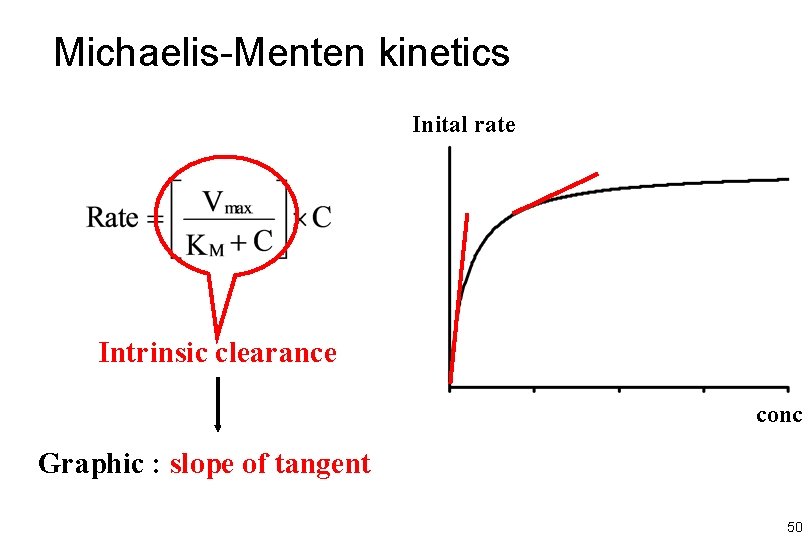
Michaelis-Menten kinetics Inital rate Intrinsic clearance conc Graphic : slope of tangent 50
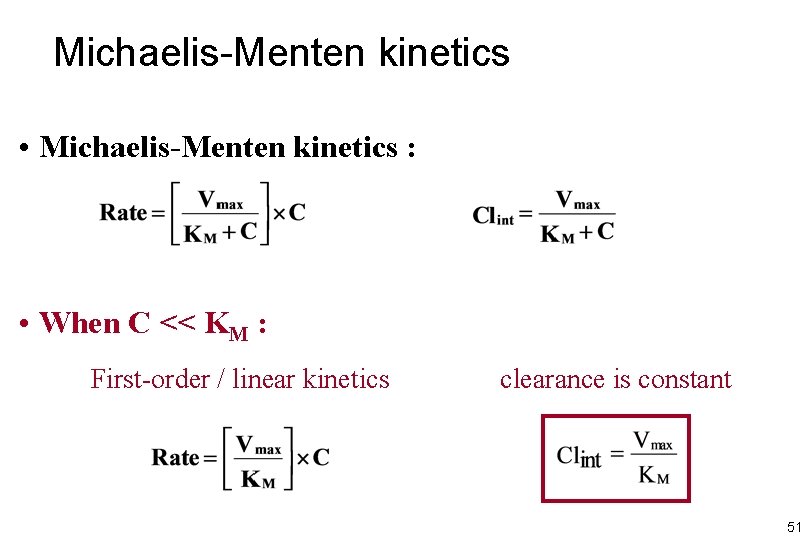
Michaelis-Menten kinetics • Michaelis-Menten kinetics : • When C << KM : First-order / linear kinetics clearance is constant 51
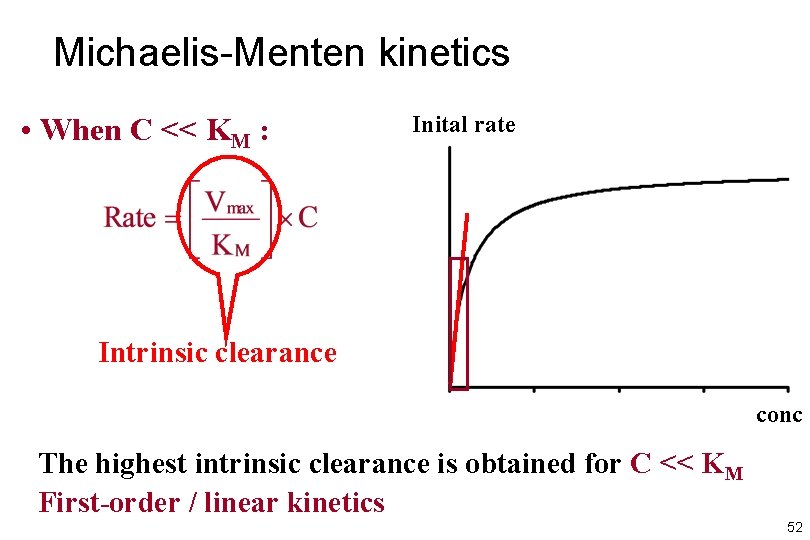
Michaelis-Menten kinetics • When C << KM : Inital rate Intrinsic clearance conc The highest intrinsic clearance is obtained for C << KM First-order / linear kinetics 52
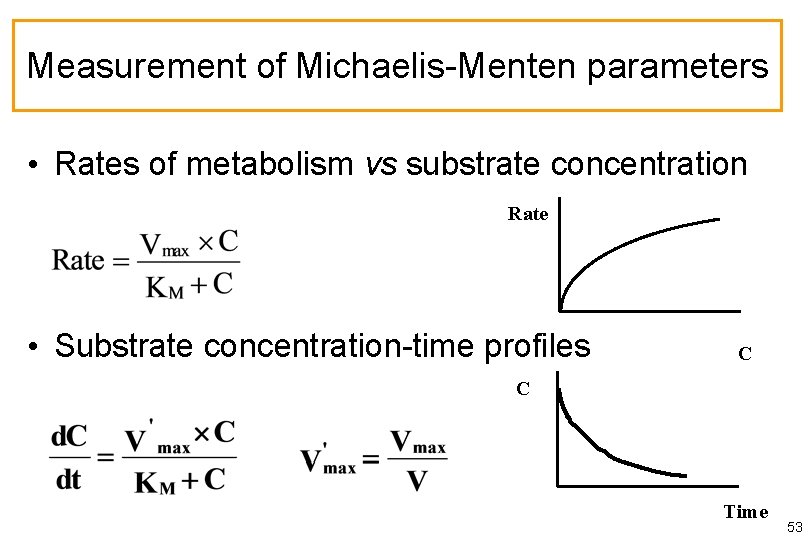
Measurement of Michaelis-Menten parameters • Rates of metabolism vs substrate concentration Rate • Substrate concentration-time profiles C C Time 53
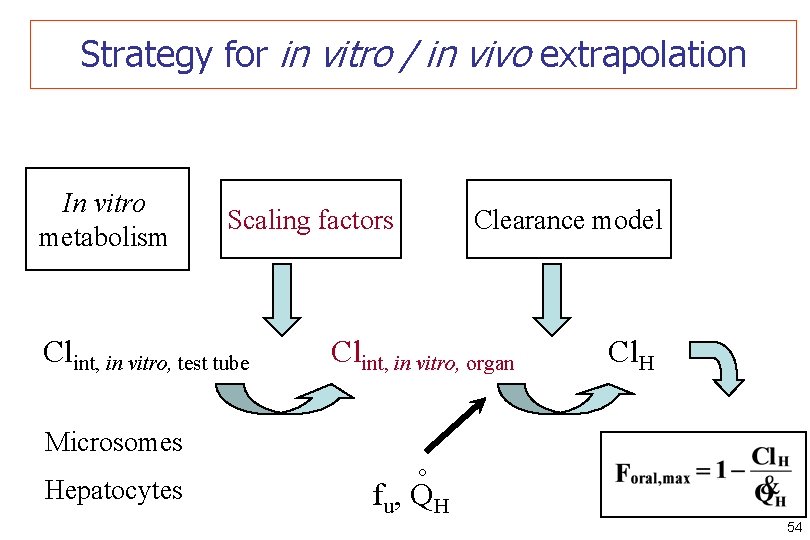
Strategy for in vitro / in vivo extrapolation Scaling factors Clint, in vitro, test tube Microsomes Hepatocytes Clearance model Clint, in vitro, organ Cl. H ° In vitro metabolism fu, QH 54

Scaling factors • From test tube to liver : quantitative relationship Clint, in vitro, test tube Clint, in vitro, organ – Clint, in vitro, organ = SF x Clint, in vitro • From test tube to liver : chemical environment – experimental in vitro conditions vs in vivo situation – not taken into account by scaling factors 55
Scaling factors • Hepatic microsomes – µL / min / mg microsomal protein • Hepatocytes – µL / min / 106 cells 56
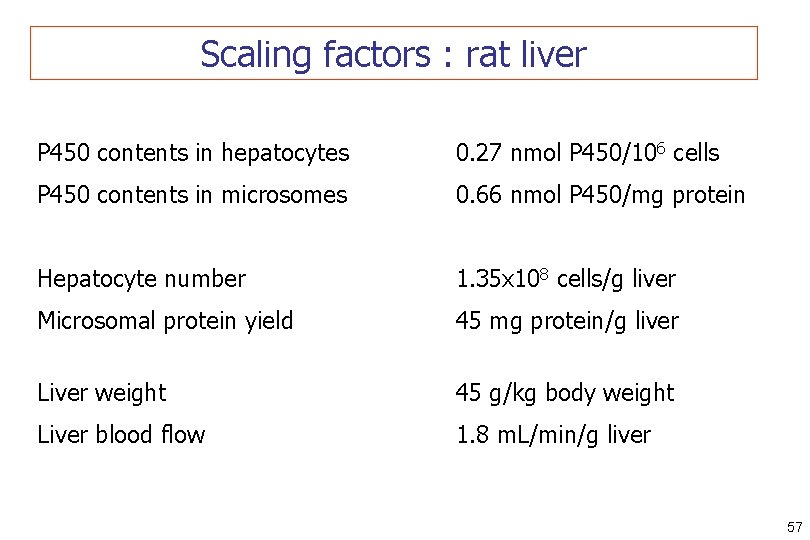
Scaling factors : rat liver P 450 contents in hepatocytes 0. 27 nmol P 450/106 cells P 450 contents in microsomes 0. 66 nmol P 450/mg protein Hepatocyte number 1. 35 x 108 cells/g liver Microsomal protein yield 45 mg protein/g liver Liver weight 45 g/kg body weight Liver blood flow 1. 8 m. L/min/g liver 57
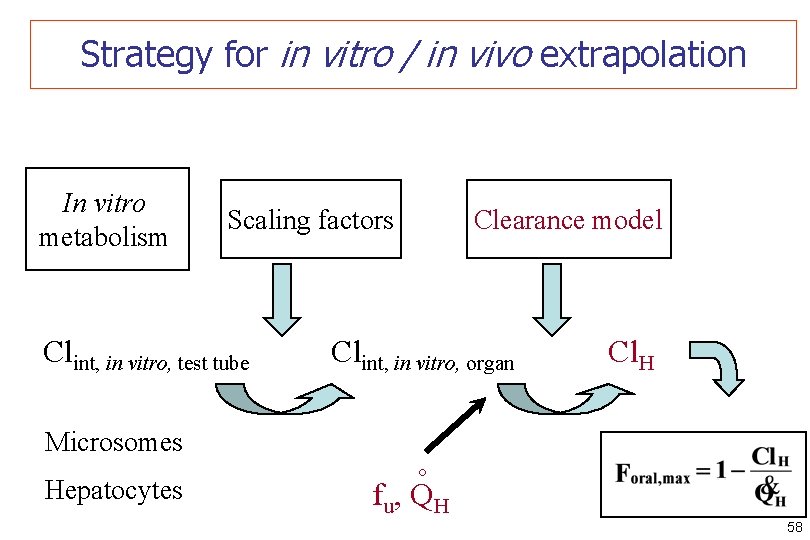
Strategy for in vitro / in vivo extrapolation Scaling factors Clint, in vitro, test tube Microsomes Hepatocytes Clearance model Clint, in vitro, organ Cl. H ° In vitro metabolism fu, QH 58

Models of hepatic clearance click ° Cl. H = f (QH ; fu ; Clint) • Assumptions : – only free drug crosses plasma membranes – rapid equilibrium between blood and hepatocytes – no active transport • Example : Well stirred model 59
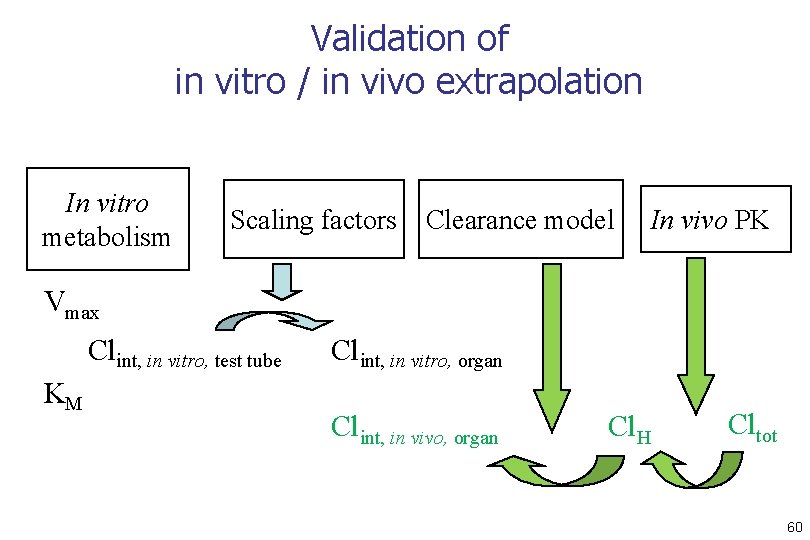
Validation of in vitro / in vivo extrapolation In vitro metabolism Scaling factors Clearance model In vivo PK Vmax Clint, in vitro, test tube KM Clint, in vitro, organ Clint, in vivo, organ Cl. H Cltot 60

Validation of in vitro / in vivo extrapolation • In vivo pharmacokinetic studies – Intravenous administration – Plasma concentration - time profile – Urinary excretion of unchanged drug (Xu) 61

Validation of in vitro / in vivo extrapolation • In vivo pharmacokinetic studies – In vivo intrinsic clearance (homogeneous model) 62
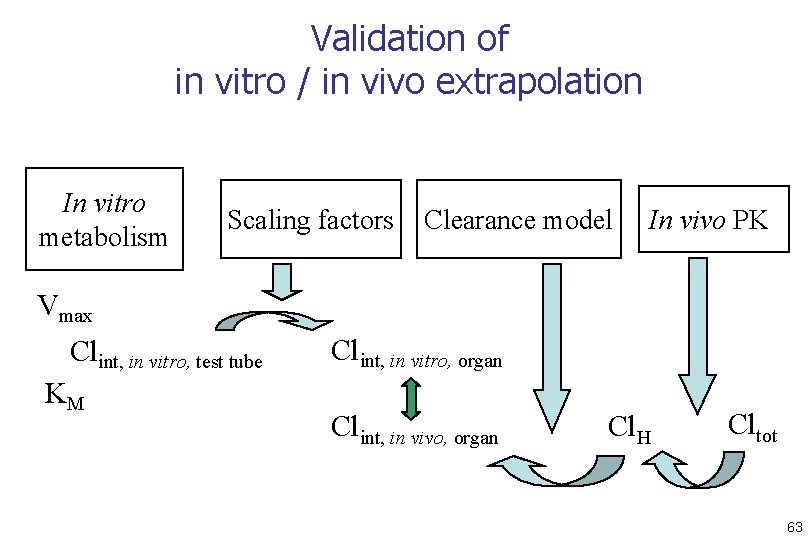
Validation of in vitro / in vivo extrapolation In vitro metabolism Scaling factors Clearance model In vivo PK Vmax Clint, in vitro, test tube KM Clint, in vitro, organ Clint, in vivo, organ Cl. H Cltot 63
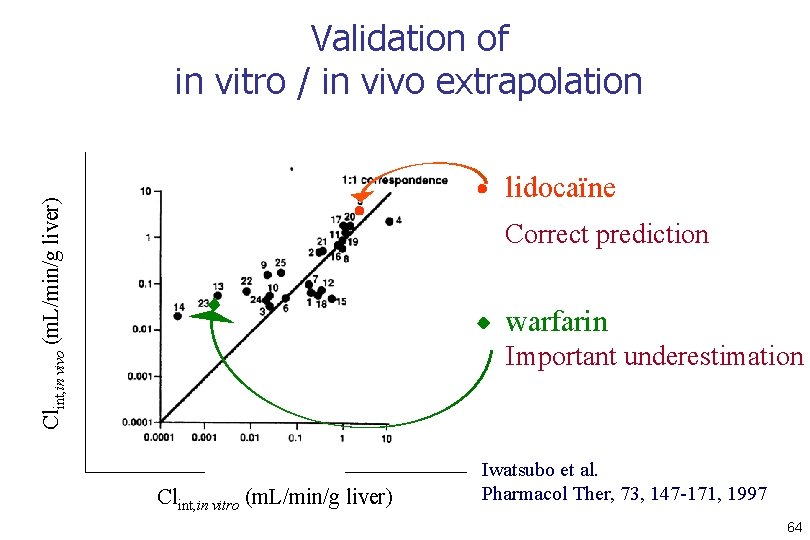
Validation of in vitro / in vivo extrapolation Clint, in vivo (m. L/min/g liver) lidocaïne Correct prediction warfarin Important underestimation Clint, in vitro (m. L/min/g liver) Iwatsubo et al. Pharmacol Ther, 73, 147 -171, 1997 64

Reasons for discrepancies between Clint, in vitro and Clint, in vivo • Extra-hepatic metabolism • Drug transport through membranes – Slow equilibrium between blood and hepatocytes – Presence of active transport • Interindividual variability – Intrinsic : genetic polymorphism / P 450 identification – Extrinsic : liver sample handling / scaling factors 65
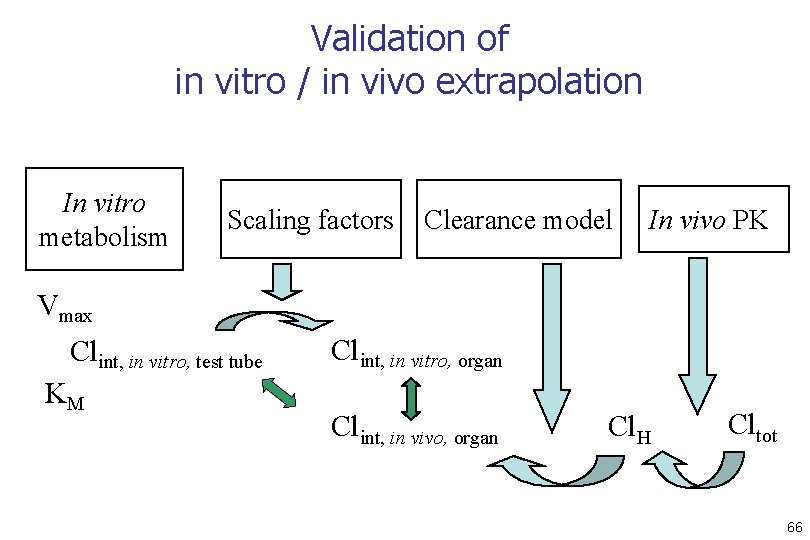
Validation of in vitro / in vivo extrapolation In vitro metabolism Scaling factors Clearance model In vivo PK Vmax Clint, in vitro, test tube KM Clint, in vitro, organ Clint, in vivo, organ Cl. H Cltot 66
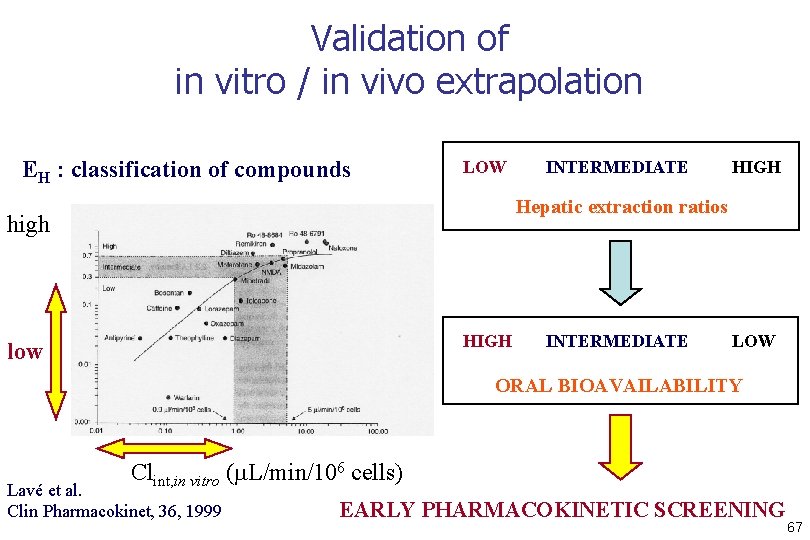
Validation of in vitro / in vivo extrapolation EH : classification of compounds LOW INTERMEDIATE HIGH Hepatic extraction ratios high HIGH low INTERMEDIATE LOW ORAL BIOAVAILABILITY Clint, in vitro (m. L/min/106 cells) Lavé et al. Clin Pharmacokinet, 36, 1999 EARLY PHARMACOKINETIC SCREENING 67
- Slides: 67