Ph Beaune Biochimie B HEGP INSERM U 490

Ph. Beaune Biochimie B HEGP, INSERM U 490 Qu ’est-ce que la Pharmacogénétique? Facteurs génétiques / effets des médicaments Effets: pharmacologiques, secondaires, toxiques; Réponse: Répondeurs / non Répondeurs
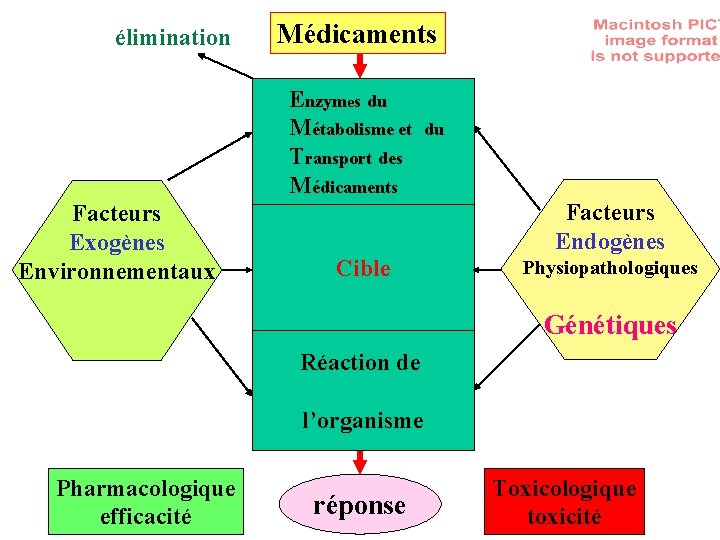
élimination Médicaments Enzymes du Métabolisme et du O des Transport r Médicaments Facteurs Exogènes Environnementaux g a Cible ni s m Réaction de e Facteurs Endogènes Physiopathologiques Génétiques l’organisme Pharmacologique efficacité réponse Toxicologique toxicité

Coûts et incidence des effets délétères des médicaments ADE: « Adverse drug events » , gravité? 2, 7 milliards de prescriptions annuelles aux USA(coût 100 milliards $) Incidence, fragmentaire, variable: - 0, 6 à 0, 7 ADE / 100 patients admis à l’hôpital (Colorado, Utah, NY); - 2 à 30 ADE / 100 si définition plus large; - FDA 1 à 10%. - fatal 0, 13 à 0, 32 %(Lazarou 1998) Coûts humains: USA: 106 000 décès / an 4ème à 6ème cause de mort (1994, Lazarou 1998). Coûts financiers: - 1, 6 à 50 milliards $ en coûts hospitaliers (5, 2); - jusqu ’à 76, 6 milliards $ en incluant les autres coûts de santé (12, 2). 50% due à mauvaise utilisation des médicaments Lazarou et coll. 1998, JAMA 279: 1200 -05. Report on Adverse drug events, general accouting office, 2000
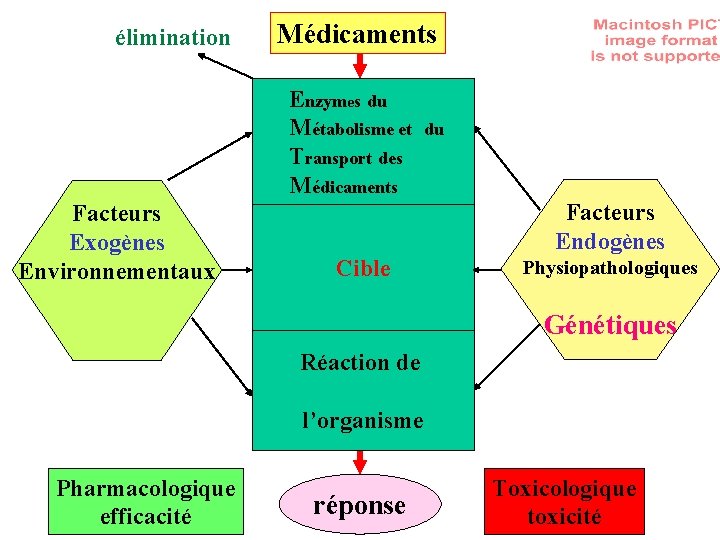
élimination Médicaments Enzymes du Métabolisme et du O des Transport r Médicaments Facteurs Exogènes Environnementaux g a Cible ni s m Réaction de e Facteurs Endogènes Physiopathologiques Génétiques l’organisme Pharmacologique efficacité réponse Toxicologique toxicité

Caractéristiques générales des Enzymes du métabolisme et du transport des médicaments - nombreux enzymes, nombreux isoenzymes ( redondance) - spécificité de substrats relative et chevauchante (redondance) - grande variabilité d’expression: - génétique - environnementale - tissulaire - physiopathologique
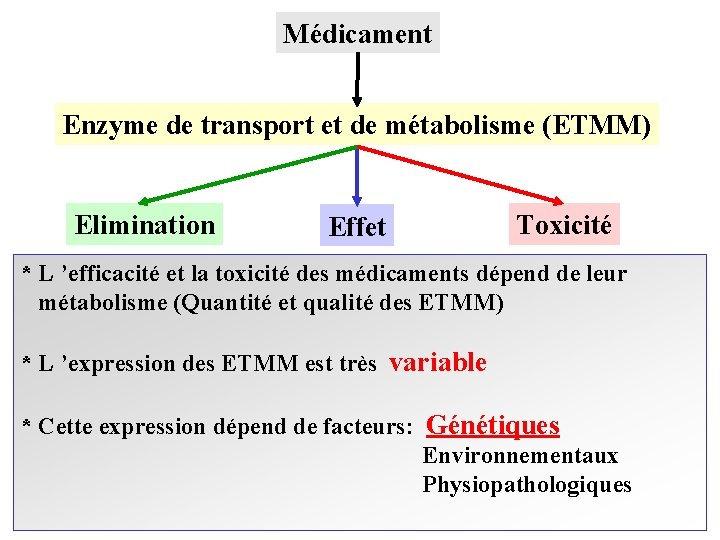
Médicament Enzyme de transport et de métabolisme (ETMM) Elimination Effet Toxicité * L ’efficacité et la toxicité des médicaments dépend de leur métabolisme (Quantité et qualité des ETMM) * L ’expression des ETMM est très variable * Cette expression dépend de facteurs: Génétiques Environnementaux Physiopathologiques

Polymorphismes génétiques - Deux phénotypes reproductibles au moins: * métaboliseurs rapides, (intermédiaires, ultra-rapides), lents - Phénotype le moins fréquent: * 1% < fréquence < 50% - Origine génétique : * ADN, analyse de familles - ! variabilité aussi due aussi à d’autres facteurs
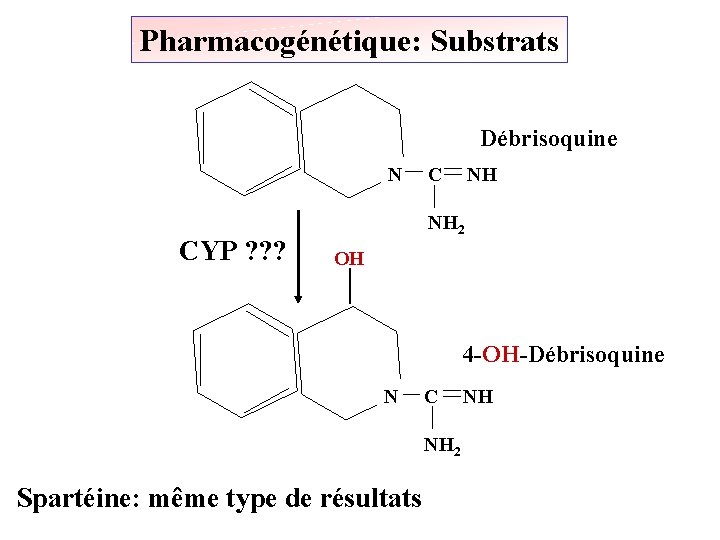
Pharmacogénétique: Substrats Débrisoquine N C NH CYP ? ? ? NH 2 OH 4 -OH-Débrisoquine N C NH 2 Spartéine: même type de résultats
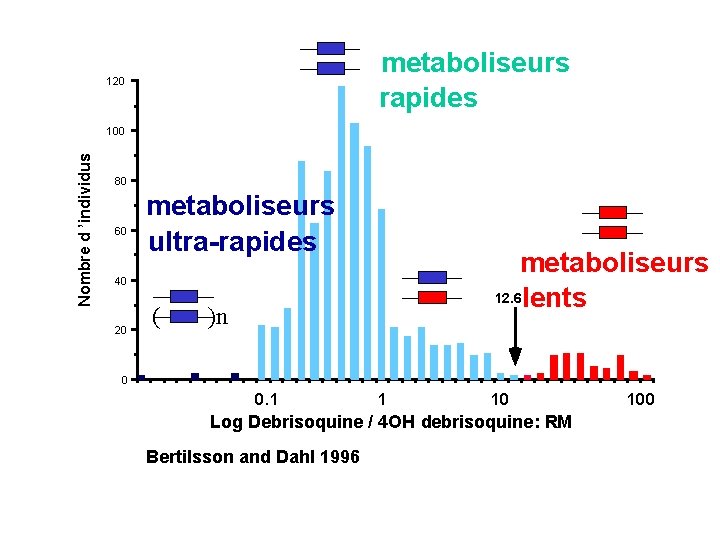
. metaboliseurs rapides 120 Nombre d ’individus 100 80 60 metaboliseurs ultra-rapides metaboliseurs 12. 6 lents 40 20 ( )n 0 0. 1 1 10 Log Debrisoquine / 4 OH debrisoquine: RM Bertilsson and Dahl 1996 100

Déficits génétiques en enzymes du métabolisme des médicaments CYP 1 A 1(induction ~ 10%) CYP 1 B 1 (%) CYP 2 A 6* (5%) CYP 2 C 9 (3%) CYP 2 C 18 (? ) CYP 2 C 19 (5 -20%) CYP 2 D 6* (5 -7%) CYP 2 E 1(>1%) CYP 3 A 4/5 (? ) DPD (<<1 %) GSTM 1* (50%) GSTT 1 (10 -20%) GSTP 1 (10%) UGT 1 A 1 (5 -10%) UGT 1 A 7 NA�T 1 NAT 2 (50%) EH (<5%) TPMT(<1%) Mdr 1 (25%) * : gènes pour lesquels une duplication est connue

INTERET DE LA PHARMACOGENETIQUE *Les variations du métabolisme /transport ont des conséquences: - pharmacocinétiques - pharmacodynamiques - toxiques * Le rôle du métabolisme / transport est important quand: - la fenêtre thérapeutique est étroite - l’efficacité est difficile à évaluer rapidement * Il est possible de prédire la capacité métabolique - génotypage - phénotypage

Phénotype: - activité réelle - quantifiable - mise en oeuvre plus difficile - variations (xénobiotiques, pathologies) - pas permanent Génotype: - facile - permanent - pas quantifiable - pas activité réelle

![Conséquences de la variabilité génétique métaboliseur lent Effet sur [médicament] [médi] Phénotype Conséquence clinique Conséquences de la variabilité génétique métaboliseur lent Effet sur [médicament] [médi] Phénotype Conséquence clinique](http://slidetodoc.com/presentation_image/518e5ceccd835c58e16e80a7169445d2/image-14.jpg)
Conséquences de la variabilité génétique métaboliseur lent Effet sur [médicament] [médi] Phénotype Conséquence clinique Index thérapeutique • toxicité métaboliseur rapide [médi] tps Index thérapeutique • efficacité thérapeutique Index thérapeutique. • inefficacité thérapeutique métaboliseur ultrarapide [médi] tps

Déficits génétiques en enzymes du métabolisme des xénobiotiques CYP 1 A 1(induction ~ 10%) CYP 2 A 6* (5%) CYP 2 C 9 (3%) CYP 2 C 18 (? ) CYP 2 C 19(5 -20%) CYP 2 D 6* (5 -7%) CYP 2 E 1(>1%) CYP 3 A 4/5 (? ) GSTM 1* (50%) GSTT 1 (10 -20%) GSTP 1 (10%) UGT 1 A 1 (5 -10%) NAT 2 (50%) EH (<5%) TPMT(<1%) * : gènes pour lesquels une duplication est connue Les fréquences varient selon les populations: ethnopharmacogénétique

Phénotype: - activité réelle - quantifiable - mise en oeuvre plus difficile - variations (xénobiotiques, pathologies) - pas permanent Génotype: - facile - permanent - pas quantifiable - pas activité réelle

Conséquences cliniques ? ? ou
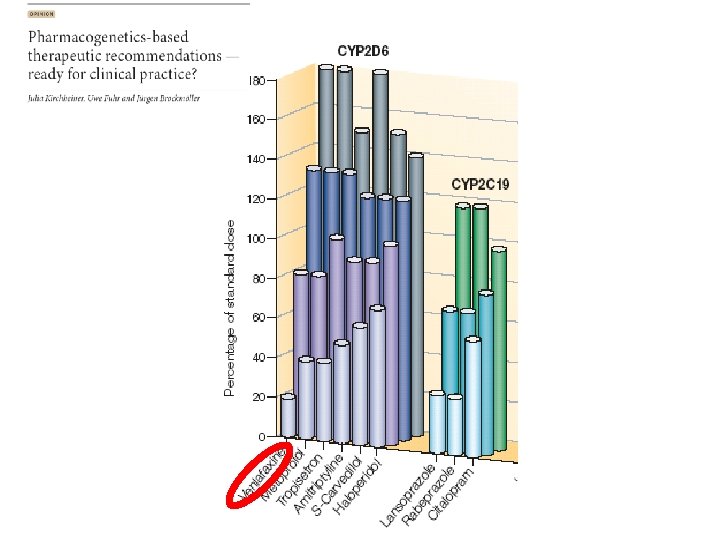
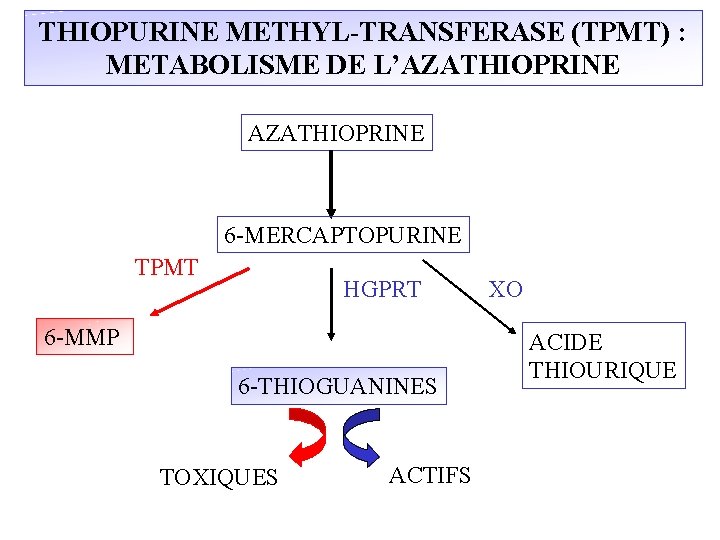
THIOPURINE METHYL-TRANSFERASE (TPMT) : METABOLISME DE L’AZATHIOPRINE 6 -MERCAPTOPURINE TPMT HGPRT 6 -MMP 6 -THIOGUANINES TOXIQUES ACTIFS XO ACIDE THIOURIQUE
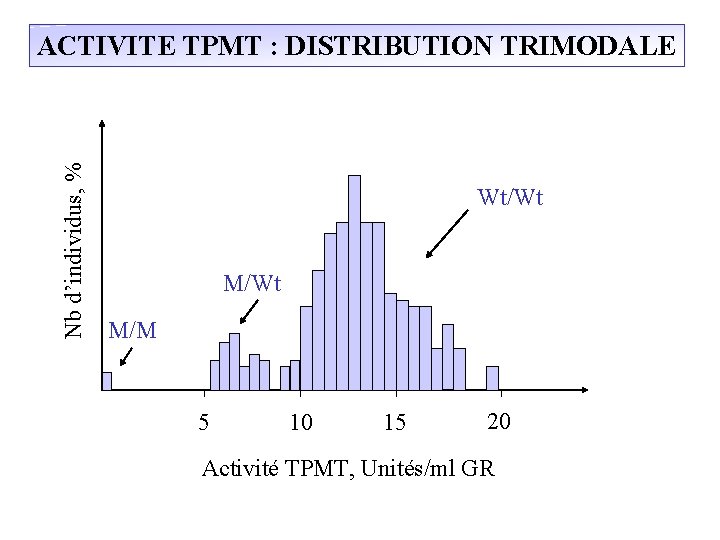
Nb d’individus, % ACTIVITE TPMT : DISTRIBUTION TRIMODALE Wt/Wt M/M 5 10 15 20 Activité TPMT, Unités/ml GR
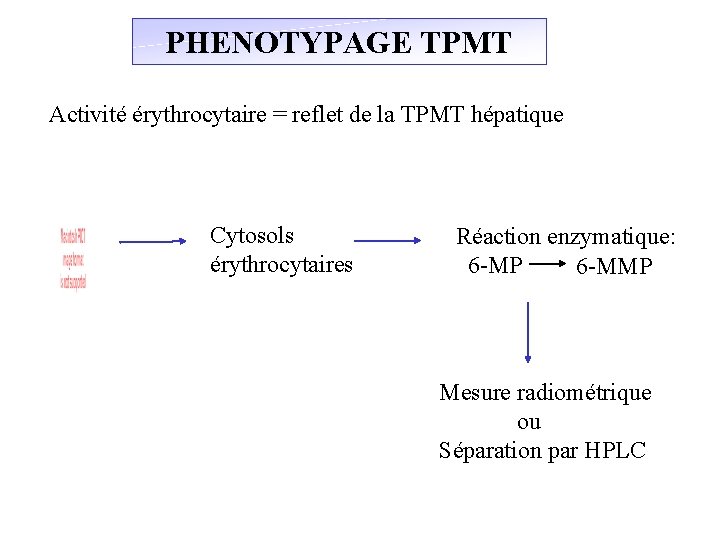
PHENOTYPAGE TPMT Activité érythrocytaire = reflet de la TPMT hépatique Cytosols érythrocytaires Réaction enzymatique: 6 -MP 6 -MMP Mesure radiométrique ou Séparation par HPLC
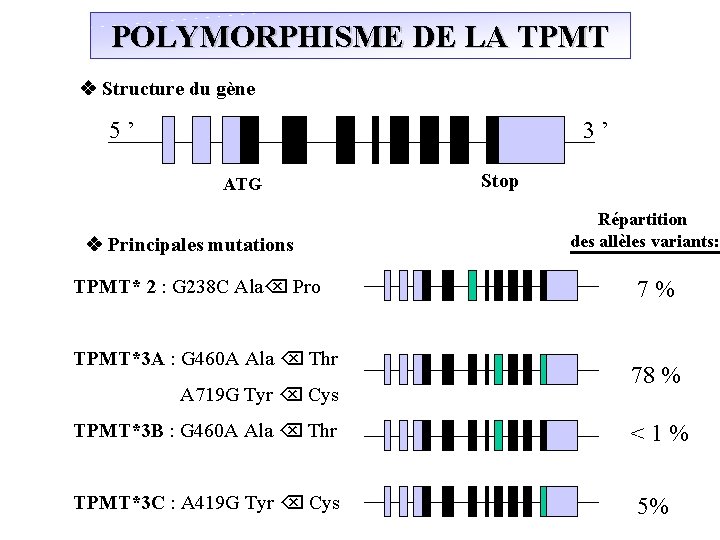
POLYMORPHISME DE LA TPMT Structure du gène 5 ’ 3 ’ Stop ATG Répartition des allèles variants: Principales mutations TPMT* 2 : G 238 C Ala Pro 7 % TPMT*3 A : G 460 A Ala Thr A 719 G Tyr Cys TPMT*3 B : G 460 A Ala Thr TPMT*3 C : A 419 G Tyr Cys 78 % < 1 % 5%
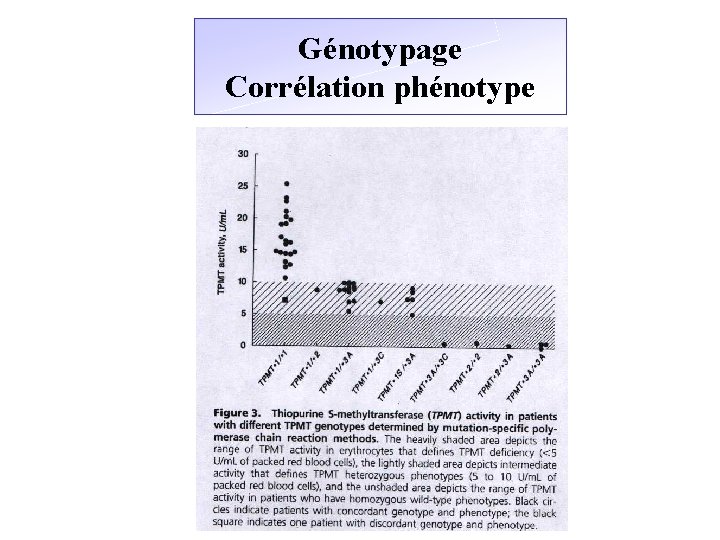
Génotypage Corrélation phénotype
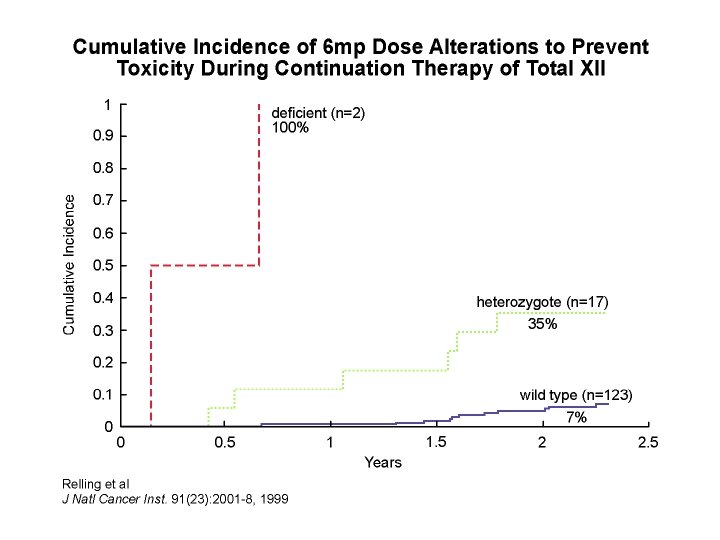
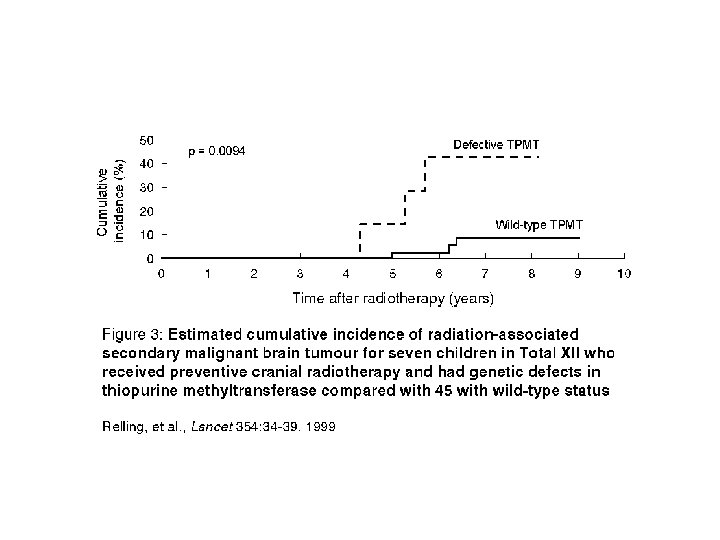

CORRELATION PHENOTYPE / GENOTYPE: dépistage du déficit en TPMT * Corrélation > 90% : prédiction du phénotype par le génotype ==> Il existe d’autres mutations qui ne sont pas recherchées * Prédiction de la toxicité hématologique: phénotypage confirmation par génotypage * Conséquences cliniques: - contre-indication de l’Aza chez les sujets déficients - diminution des doses chez les individus intermédiaires - augmentation des doses chez les sujets très rapides?
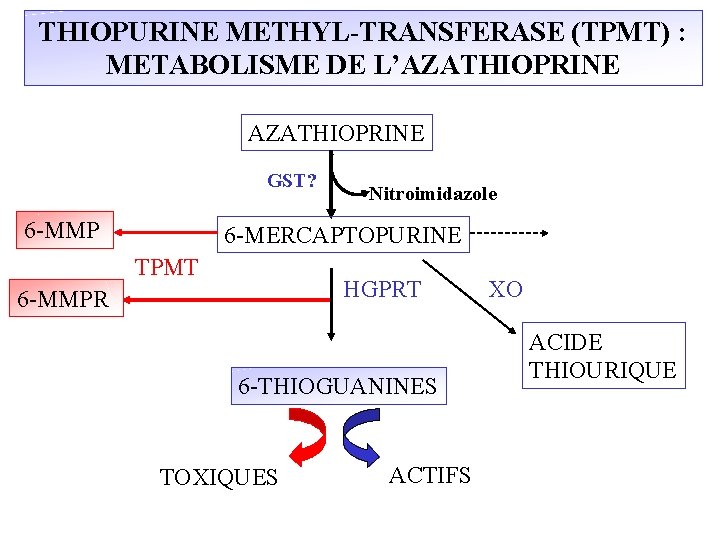
THIOPURINE METHYL-TRANSFERASE (TPMT) : METABOLISME DE L’AZATHIOPRINE GST? 6 -MMP Nitroimidazole 6 -MERCAPTOPURINE TPMT HGPRT 6 -MMPR 6 -THIOGUANINES TOXIQUES ACTIFS XO ACIDE THIOURIQUE

Maladies inflammatoires intestinales - AZA / 6 MP: 55% à 67 % répondent à la thérapeutique - Remplacement par 6 MP: * 77 % non répondeurs répondent quand changement AZA ---> 6 MP. - Augmentation des doses: * 27 % répondeurs augmentation 6 -TGN * non-répondeurs pas d ’augmentation 6 MP augmentation 6 MMPR
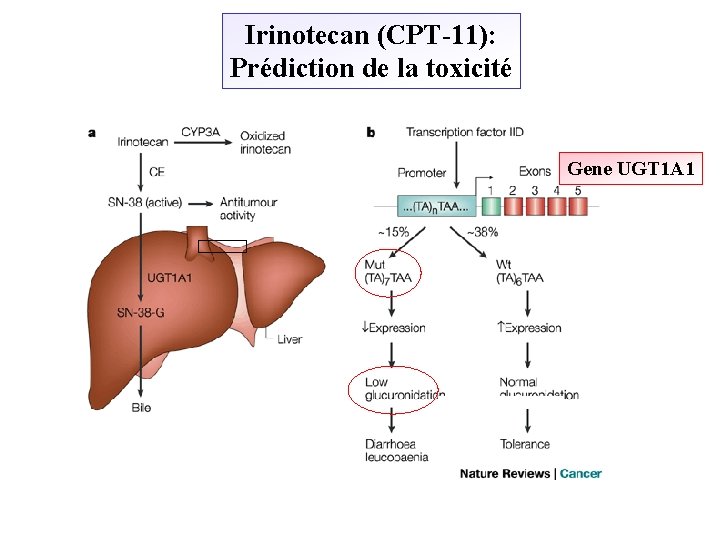
Irinotecan (CPT-11): Prédiction de la toxicité Gene UGT 1 A 1
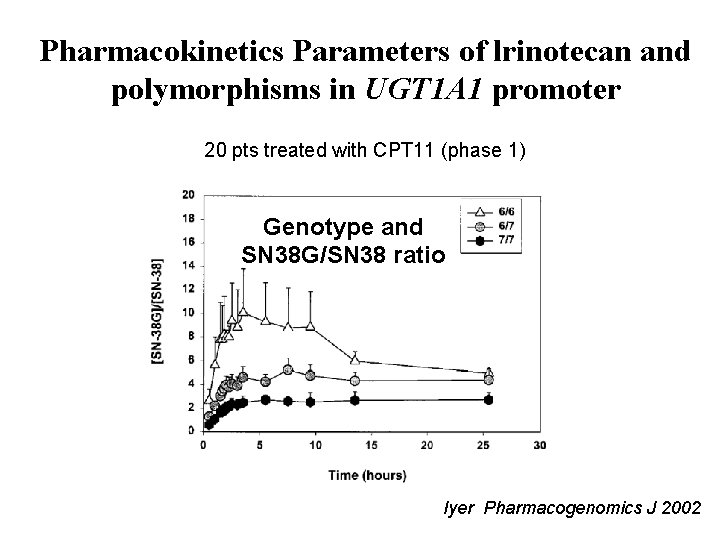
Pharmacokinetics Parameters of lrinotecan and polymorphisms in UGT 1 A 1 promoter 20 pts treated with CPT 11 (phase 1) Genotype and SN 38 G/SN 38 ratio Iyer, Pharmacogenomics J 2002
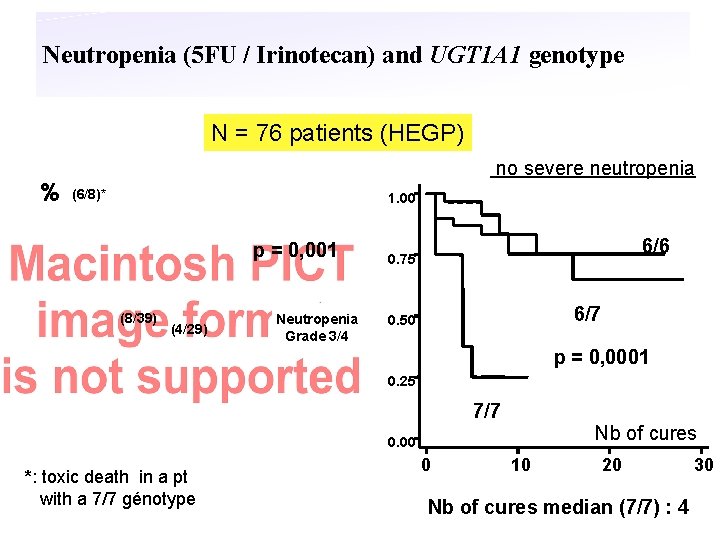
Neutropenia (5 FU / Irinotecan) and UGT 1 A 1 genotype N = 76 patients (HEGP) % no severe neutropenia (6/8)* 1. 00 p = 0, 001 (4/29) Neutropenia Grade 3/4 (8/39) 6/6 0. 75 6/7 0. 50 p = 0, 0001 0. 25 7/7 Nb of cures 0. 00 *: toxic death in a pt with a 7/7 génotype 0 10 20 30 Nb of cures median (7/7) : 4
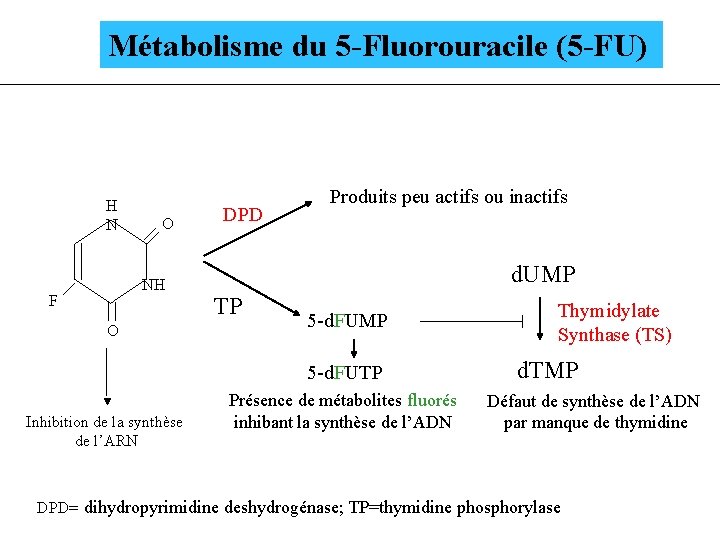
Métabolisme du 5 -Fluorouracile (5 -FU) H N O NH F O DPD Produits peu actifs ou inactifs d. UMP TP 5 -d. FUMP 5 -d. FUTP Inhibition de la synthèse de l’ARN Présence de métabolites fluorés inhibant la synthèse de l’ADN Thymidylate Synthase (TS) d. TMP Défaut de synthèse de l’ADN par manque de thymidine DPD= dihydropyrimidine deshydrogénase; TP=thymidine phosphorylase
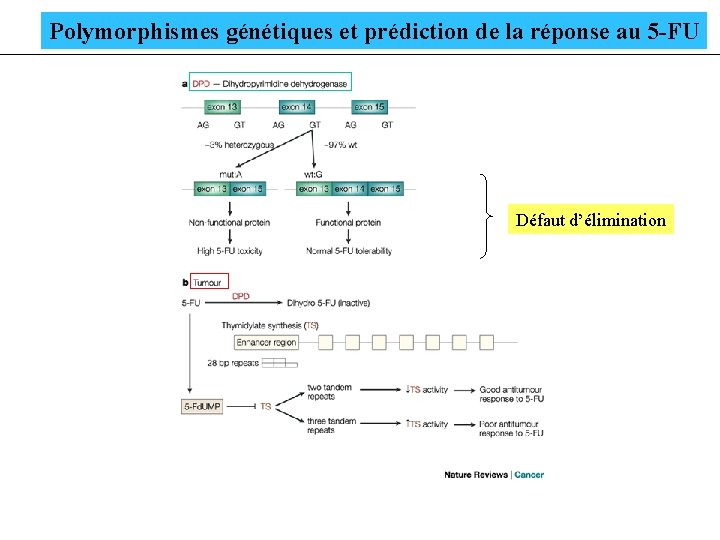
Polymorphismes génétiques et prédiction de la réponse au 5 -FU Défaut d’élimination
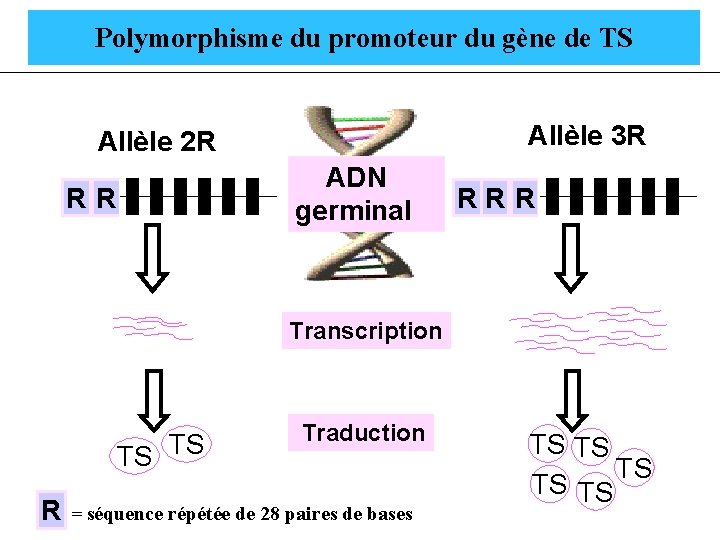
Polymorphisme du promoteur du gène de TS Allèle 3 R Allèle 2 R R R Gène TS ADN germinal R R R Gène TS Transcription TS TS R Traduction = séquence répétée de 28 paires de bases TS TS TS

Toxicité de l’association 5 -FU / irinotécan et polymorphismes du promoteur de la thymidylate synthase (TS) % (4/11) p = 0, 02 (5/33) (0/19) Génotype TS Lecomte, 2004
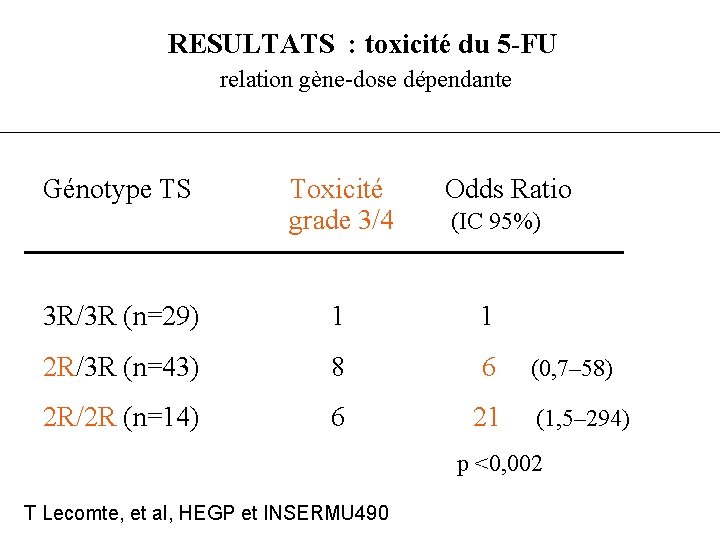
RESULTATS : toxicité du 5 -FU relation gène-dose dépendante Génotype TS Toxicité Odds Ratio grade 3/4 (IC 95%) 3 R/3 R (n=29) 1 1 2 R/3 R (n=43) 8 2 R/2 R (n=14) 6 21 (1, 5– 294) 6 (0, 7– 58) p <0, 002 T Lecomte, et al, HEGP et INSERMU 490

Neurotoxicité chronique à l’Oxaliplatine et polymorphisme de GST-P 1 64 pts inclus et génotypés pour le polymorphisme de GSTP 1(Ile 105 Val) Dose cumulée min. de 500 mg/m 2 % (19/39) p = 0, 04 (5/20) (0/5) Génotype GSTP 1

Neurotoxicité chronique à l’Oxaliplatine et polymorphisme de GST-P 1 64 pts inclus et génotypés pour le polymorphisme de GSTP 1(Ile 105 Val) Dose cumulée min. de 500 mg/m 2 % (19/39) p = 0, 04 (5/20) (0/5) Génotype GSTP 1
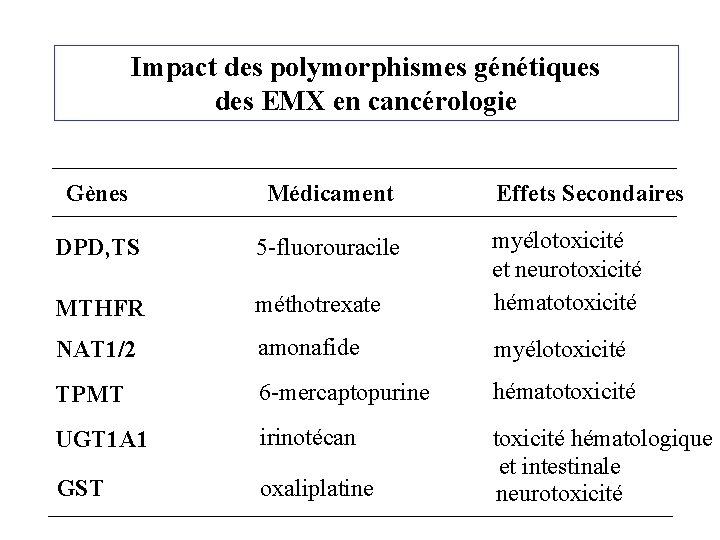
Impact des polymorphismes génétiques des EMX en cancérologie Gènes Médicament Effets Secondaires DPD, TS 5 -fluorouracile MTHFR méthotrexate myélotoxicité et neurotoxicité hématotoxicité NAT 1/2 amonafide myélotoxicité TPMT 6 -mercaptopurine hématotoxicité UGT 1 A 1 irinotécan GST oxaliplatine toxicité hématologique et intestinale neurotoxicité

ORAL ANTICOAGULANT THERAPY First cause of iatrogenic accidents 480 000 to 580 000 treated patients Problems during Vit Kantagonist therapy 3000 deaths per year 17 000 hospitalisations per year
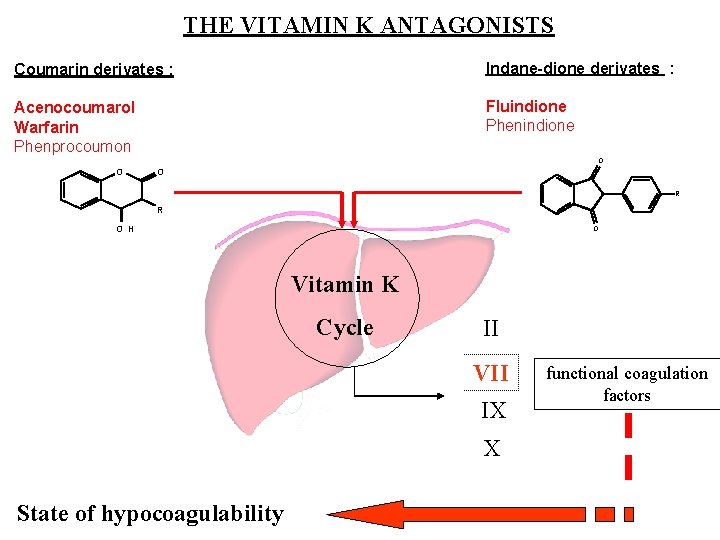
THE VITAMIN K ANTAGONISTS Coumarin derivates : Indane-dione derivates : Acenocoumarol Warfarin Phenprocoumon Fluindione Phenindione O O O R R O H O Vitamin K Cycle II VII IX X State of hypocoagulability functional coagulation factors
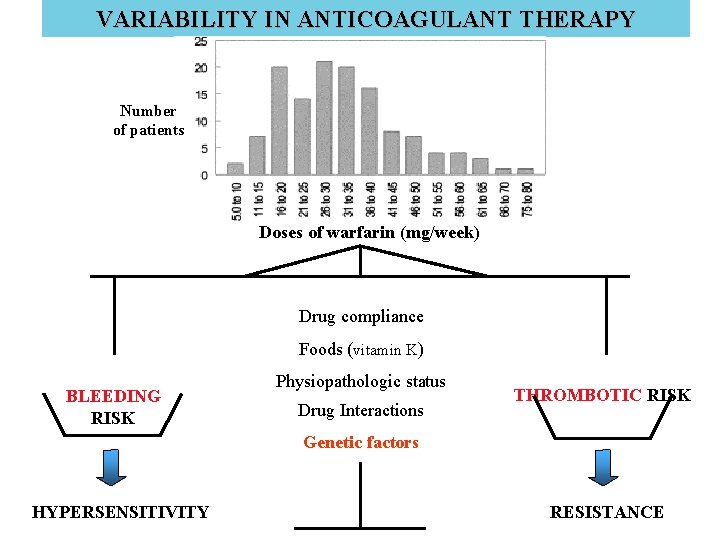
VARIABILITY IN ANTICOAGULANT THERAPY Number of patients Doses of warfarin (mg/week) Drug compliance Foods (vitamin K) BLEEDING RISK Physiopathologic status Drug Interactions THROMBOTIC RISK Genetic factors HYPERSENSITIVITY RESISTANCE
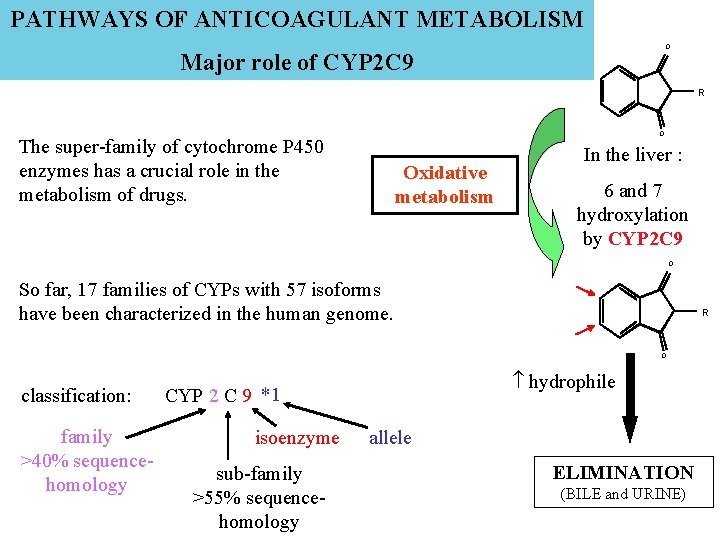
PATHWAYS OF ANTICOAGULANT METABOLISM O Major role of CYP 2 C 9 R O The super-family of cytochrome P 450 enzymes has a crucial role in the metabolism of drugs. Oxidative metabolism In the liver : 6 and 7 hydroxylation by CYP 2 C 9 O So far, 17 families of CYPs with 57 isoforms have been characterized in the human genome. R O classification: family >40% sequencehomology hydrophile CYP 2 C 9 *1 isoenzyme sub-family >55% sequencehomology allele ELIMINATION (BILE and URINE)

FACTORS AFFECTING THE CYP 2 C 9 ACTIVITY âEnvironnemental Variations : inhibition/induction â Genetic Polymorphisms 24 allelic variants http: //www. imm. ki. se/CYPalleles/cyp 2 c 9. htm Allelic variants Allelic frequency Activity CYP 2 C 9*1 0, 79 -0, 86 100 % CYP 2 C 9*2 (Cys 144 Arg) 0, 08 -0, 19 12 % CYP 2 C 9*3 (Leu 359 Ileu) 0, 06 -0, 1 5 % Caucasian populations

CLINICAL IMPLICATIONS OF CYP 2 C 9 POLYMORPHISMS FOR ANTICOAGULANT TREATMENT (1) Bleeding risk Retrospective study including 185 patients with long term warfarin therapy HR of bleeding = 3. 94; CI 95%, 1. 29 -12. 04 Among the carriers of at least one CYP 2 C 9 variant allele (CYP 2 C 9*2 or *3 ) HR : Hazard ratio, established during the initiation phase (90 days) Higashi et al. , JAMA 2002

(2) Mean daily dose of warfarin (mg/day) nd : not detected ; nr : not researched

A study including healthy volunteers (n=230) taking a single oral dose of acenocoumarol To explore the contribution of genetic factors in the variability of pharmacological response (% Factor VII ) Collaborations: Clinical Investigation Center of St Antoine Hospital, Paris, Pr L. Becquemont INSERM Unit 525, Paris, Dr DA Trégouët

CYP 2 C 9 polymorphisms (coding region) and response to acenocoumarol Effect of the CYP 2 C 9*2 and *3 alleles on the AC response (factor VII ratio = D 0/D 24 x 100 ) Genotype distribution in our population : genotype *1/*1 *1/*2 *1/*3 *2/*2 *2/*3 *3/*3 n 143 44 30 4 8 1 P< 0. 001 CYP 2 C 9 *2 NS CYP 2 C 9 *3 14% of the variability

Relationship between CYP 2 C 9 genotype and warfarin dose among 200 Caucasian individuals From Daly and King, 2003 Wide interindividual variability in warfarin dose requirement within the *1/*1 group
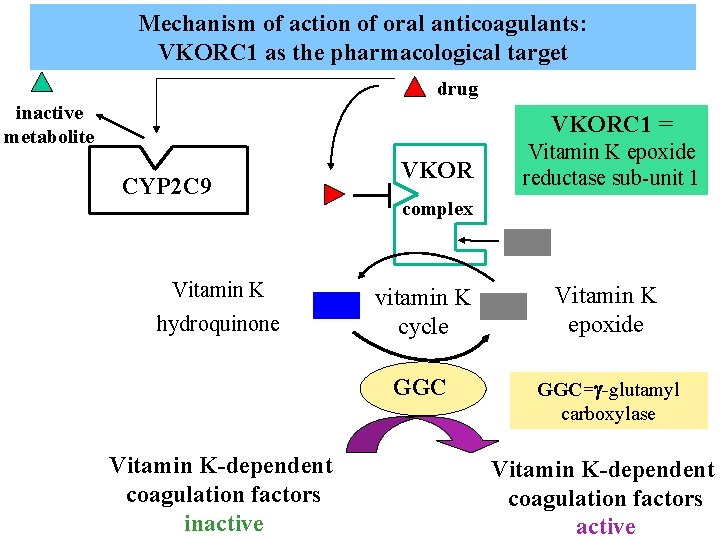
Mechanism of action of oral anticoagulants: VKORC 1 as the pharmacological target drug inactive metabolite VKORC 1 = CYP 2 C 9 Vitamin K hydroquinone Vitamin K-dependent coagulation factors inactive VKOR Vitamin K epoxide reductase sub-unit 1 complex vitamin K cycle Vitamin K epoxide GGC= -glutamyl carboxylase Vitamin K-dependent coagulation factors active

Relation between VKORC 1 SNP 1173 C>T (intron 1) and the warfarin maintenance dose « A polymorphism in VKORC 1 gene is associated with an inter-individual variability in the dose-anticoagulant effect of warfarin » D'Andrea et al. , Blood 2004 CYP 2 C 9 explains 21% of the variability VKORC 1 explains 13% of the variability
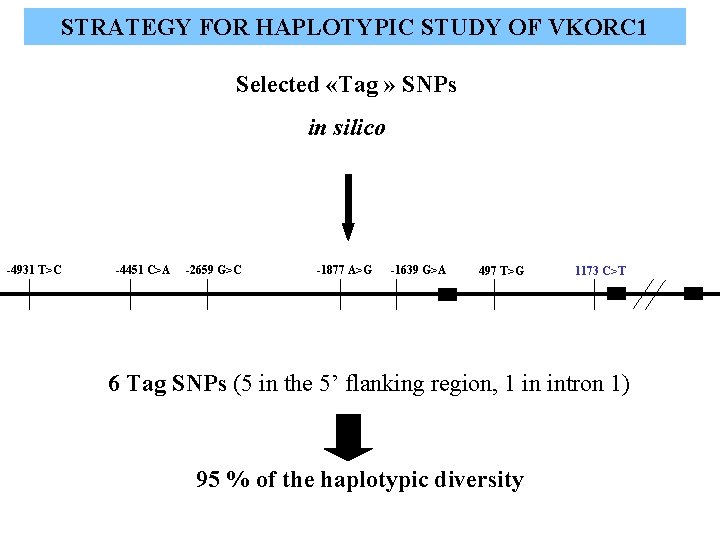
STRATEGY FOR HAPLOTYPIC STUDY OF VKORC 1 Selected «Tag » SNPs in silico -4931 T>C -4451 C>A -2659 G>C -1877 A>G -1639 G>A 497 T>G 1173 C>T 6 Tag SNPs (5 in the 5’ flanking region, 1 in intron 1) 95 % of the haplotypic diversity

VKORC 1 HAPLOTYPE EFFECT ON PHARMACOLOGICAL RESPONSE TO ACENOCOUMAROL *: Factor VII ratio corresponds to the remaining factor VII, expressed as a percentage Compared with baseline value , before acenocoumarol intake 7 haplotypes in our population: SNP -1639 G>A = « haplotype TAG »

EFFECT OF VKORC 1 – 1639 G>A SNP ON THE RESPONSE TO ACENOCOUMAROL P<0. 001 Factor VII ratio (%) VKORC 1 genotype 37% of the variability Bodin et al, Blood 2005

ADDITIVE EFFECT OF VKORC 1 – 1639 G>A AND CYP 2 C 9*3 ON THE RESPONSE TO ACENOCOUMAROL CYP 2 C 9*3 + VKORC 1 G-1639 A = 50% of the variability Factor VII ratio (%) 20% 5% High risk for overanticoagulation

VKORC 1 polymorphisms and warfarin dose requirement Low doses High doses -1639 G>A 25% variance in dose explained From Rieder et al. New England J Med 2005
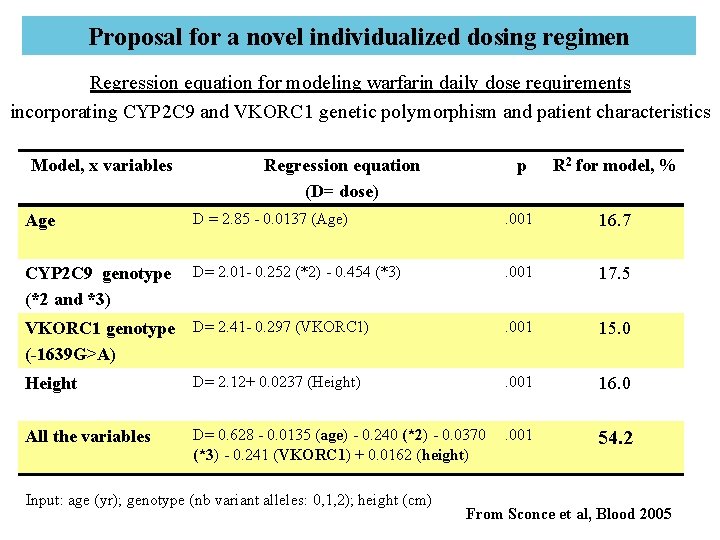
Proposal for a novel individualized dosing regimen Regression equation for modeling warfarin daily dose requirements incorporating CYP 2 C 9 and VKORC 1 genetic polymorphism and patient characteristics Model, x variables Regression equation (D= dose) p R 2 for model, % Age D = 2. 85 - 0. 0137 (Age) . 001 16. 7 CYP 2 C 9 genotype (*2 and *3) D= 2. 01 - 0. 252 (*2) - 0. 454 (*3) . 001 17. 5 VKORC 1 genotype (-1639 G>A) D= 2. 41 - 0. 297 (VKORC 1) . 001 15. 0 Height D= 2. 12+ 0. 0237 (Height) . 001 16. 0 All the variables D= 0. 628 - 0. 0135 (age) - 0. 240 (*2) - 0. 0370 . 001 (*3) - 0. 241 (VKORC 1) + 0. 0162 (height) 54. 2 Input: age (yr); genotype (nb variant alleles: 0, 1, 2); height (cm) From Sconce et al, Blood 2005

RESISTANCE TO ANTICOAGULANT TREATMENT « Mutation in VKORC 1 cause warfarin resistance and multiple coagulation deficiency type 2 » Rost et al. , Nature 2004 4 Rare non-synonymous heterozygous mutations in VKORC 1 causative for warfarin resistance (15 -35 mg/d) Expression studies and VKOR activity measurements in HEK 293 cells Val 29 Leu Val 45 Ala Arg 58 Gly Leu 128 Arg Lower VKOR activity than the wild type Lower sensitivity to warfarin than the wild type ---> resistance
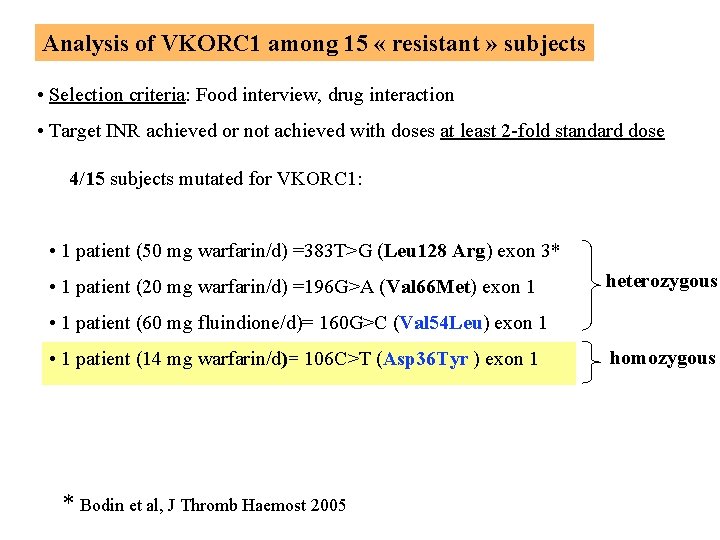
Analysis of VKORC 1 among 15 « resistant » subjects • Selection criteria: Food interview, drug interaction • Target INR achieved or not achieved with doses at least 2 -fold standard dose 4/15 subjects mutated for VKORC 1: • 1 patient (50 mg warfarin/d) =383 T>G (Leu 128 Arg) exon 3* • 1 patient (20 mg warfarin/d) =196 G>A (Val 66 Met) exon 1 heterozygous • 1 patient (60 mg fluindione/d)= 160 G>C (Val 54 Leu) exon 1 • 1 patient (14 mg warfarin/d)= 106 C>T (Asp 36 Tyr ) exon 1 * Bodin et al, J Thromb Haemost 2005 homozygous
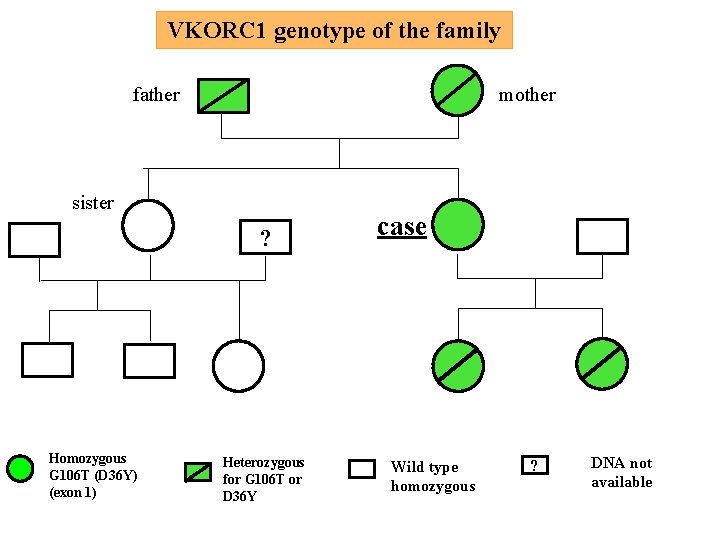
VKORC 1 genotype of the family father mother sister ? Homozygous G 106 T (D 36 Y) (exon 1) Heterozygous for G 106 T or D 36 Y case Wild type homozygous ? DNA not available
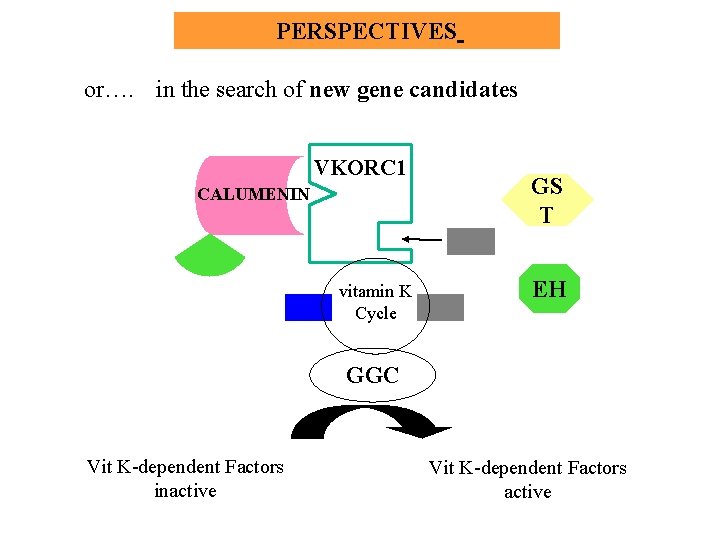
PERSPECTIVES or…. in the search of new gene candidates VKORC 1 CALUMENIN vitamin K Cycle GS T EH GGC Vit K-dependent Factors inactive Vit K-dependent Factors active

Risque de toxicité sévère avec l’irinotecan Risque OR UGT 1 A 1*28 7, 23 Mode d ’administration 4, 52 Sexe (femmes) 2, 45 Le déficit en UGT 1 A 1 augmente le risque de toxicité de l ’irinotecan. A tester: CE, MDR, CYP 3 A 4. Ando et coll. Cancer res. 2000, 60: 6921.
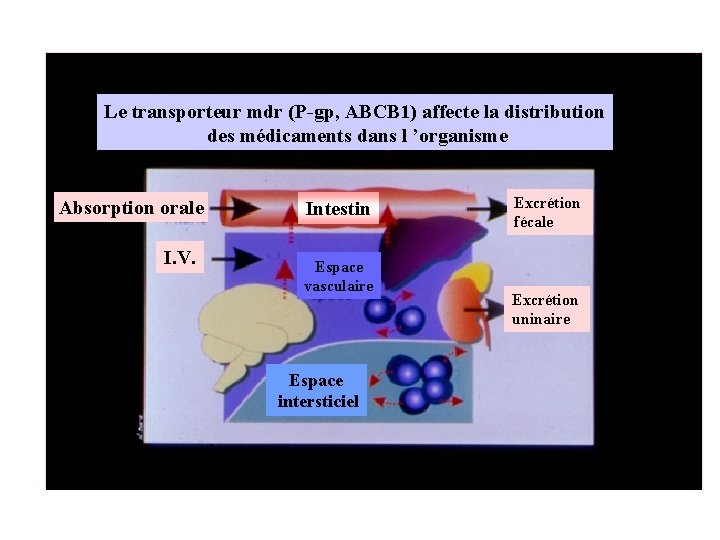
Le transporteur mdr (P-gp, ABCB 1) affecte la distribution des médicaments dans l ’organisme Absorption orale I. V. Intestin Espace vasculaire Espace intersticiel Excrétion fécale Excrétion uninaire

Anti-protéases métabolisées par CYP 3 A 4, UGT? , et transportées par mdr - Traitement anti-HIV (Nelfinavir ou efavirenz + …) - Analyse multivariée augmentation du nb de CD 4+ * à 6 mois TT= 250/µl, CT = 180/µl, CC = 110/µl * RR (>200/µl): mdr 1 TT = 3, 0, charge virale initiale = 7, 1 Fellay et coll. Lancet 2002, 359: 30 -36
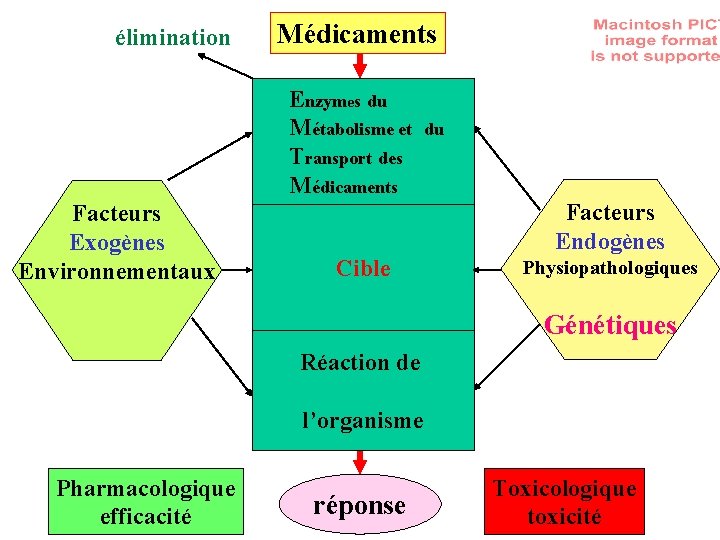
élimination Médicaments Enzymes du Métabolisme et du O des Transport r Médicaments Facteurs Exogènes Environnementaux g a Cible ni s m Réaction de e Facteurs Endogènes Physiopathologiques Génétiques l’organisme Pharmacologique efficacité réponse Toxicologique toxicité
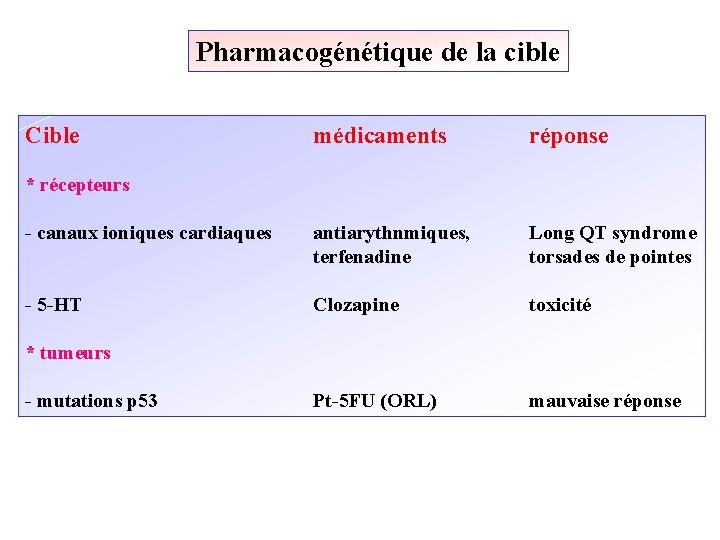
Pharmacogénétique de la cible Cible médicaments réponse - canaux ioniques cardiaques antiarythnmiques, terfenadine Long QT syndrome torsades de pointes - 5 -HT Clozapine toxicité Pt-5 FU (ORL) mauvaise réponse * récepteurs * tumeurs - mutations p 53

Génétique et expression dans la tumeur • 30 patients traités cetuximab pour un cancer colorectal Grade IV – 3 première ligne folfiri – 3 deuxième ligne – 24 troisième ligne • 11 répondeurs (1 réponse complète ) • séquençage KRAS (ex 1), BRAF (ex 11&15), PIK 3 CA (ex 1, ex 2, ex 9, ex 11) • Mesure de l’amplifiaction de EGFR par Chromosome In Situ Hybridation (CISH, F. Penault-Llorca)
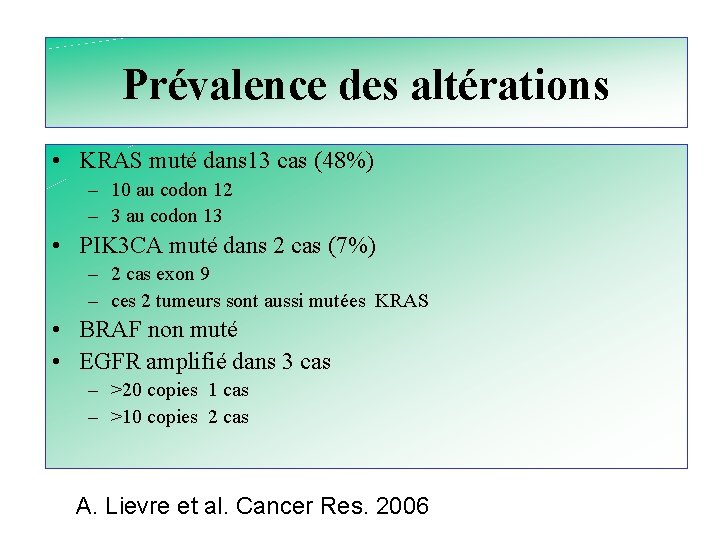
Prévalence des altérations • KRAS muté dans 13 cas (48%) – 10 au codon 12 – 3 au codon 13 • PIK 3 CA muté dans 2 cas (7%) – 2 cas exon 9 – ces 2 tumeurs sont aussi mutées KRAS • BRAF non muté • EGFR amplifié dans 3 cas – >20 copies 1 cas – >10 copies 2 cas A. Lievre et al. Cancer Res. 2006

Response au cétuximab et Mutations KRAS P<0, 0001
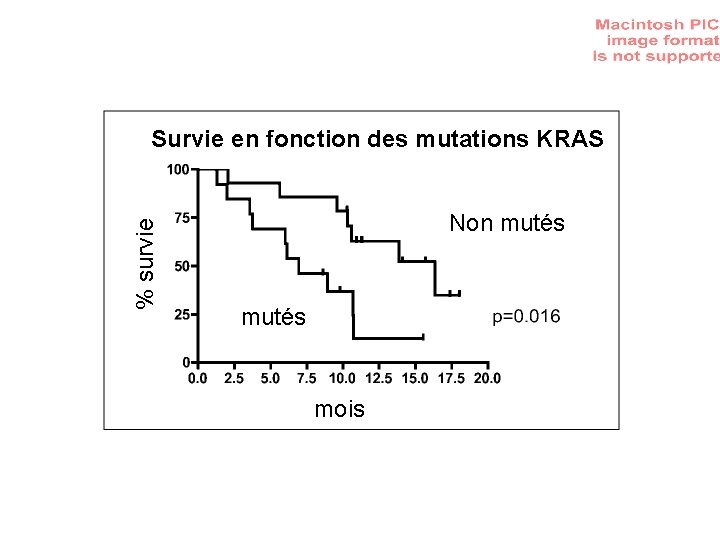
% survie Survie en fonction des mutations KRAS Non mutés mois
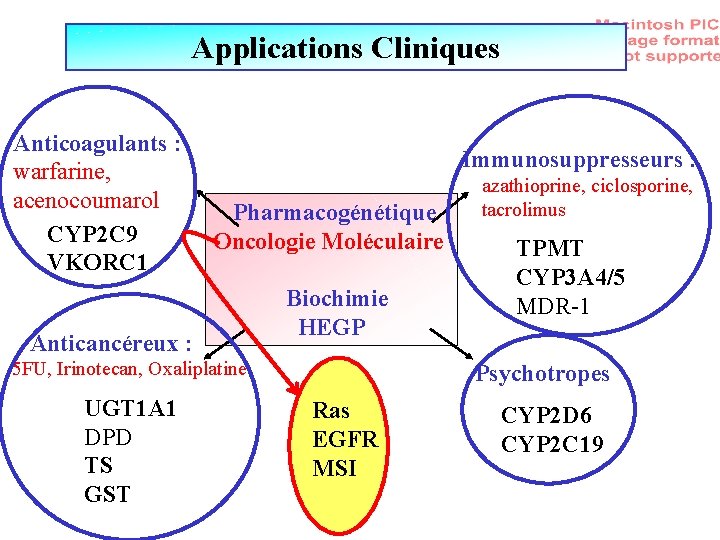
Applications Cliniques Anticoagulants : warfarine, acenocoumarol CYP 2 C 9 VKORC 1 Immunosuppresseurs : Pharmacogénétique Oncologie Moléculaire Anticancéreux : Biochimie HEGP 5 FU, Irinotecan, Oxaliplatine UGT 1 A 1 DPD TS GST azathioprine, ciclosporine, tacrolimus TPMT CYP 3 A 4/5 MDR-1 Psychotropes Ras EGFR MSI CYP 2 D 6 CYP 2 C 19

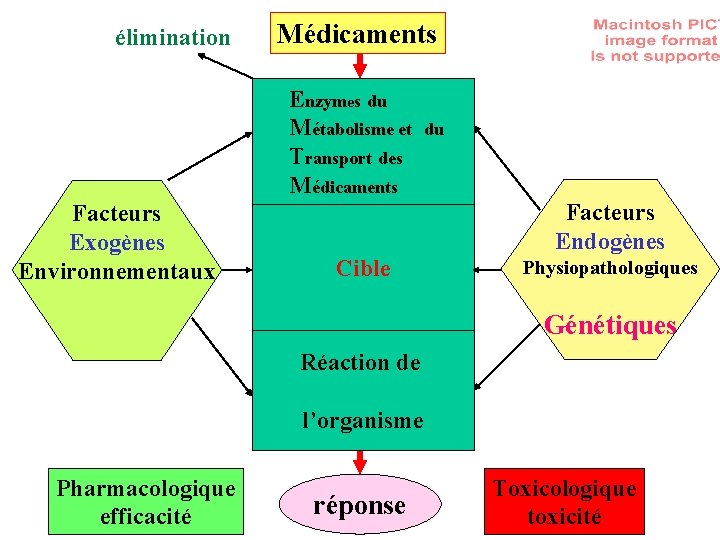
élimination Médicaments Enzymes du Métabolisme et du O des Transport r Médicaments Facteurs Exogènes Environnementaux g a Cible ni s m Réaction de e Facteurs Endogènes Physiopathologiques Génétiques l’organisme Pharmacologique efficacité réponse Toxicologique toxicité

Abacavir Anti-HI, analogue non nucléosidique (Ziagen®) 5% réaction d ’hypersensibilité quelques rares cas---> mort 200 individus suivis - HLA B 5701, C 4 A 6, -DR 7, -DR 3 67 % des intolérants ont cet haplotype 0% des tolérants ont cet haplotype OR 117 - HLA B 5701 78 % des intolérants 2, 4 % des tolérants Valeur prédictive positive 100% et négative 97% Détermination haplotype avant traitement devrait permettre de réduire de 50% les réactions d’hypersensibilité. Mellal et coll. Lancet 2002, Hetherington et coll. Lancet 2002

Conclusions - Influence des variations génétiques sur la réponse aux médicaments * réelle * cliniquement significative - Impact clinique: * validité de l’association * prévalence et sévérité de l ’ADE * possibilité de surveillance * prévalence des polymorphismes * phénotypage et/ou génotypage disponible et coût * interprétation clinico-biologique - génétique - métabolisme
Variability of the target Response to chemotherapy in head and neck cancer - Neo adjuvant chemotherapy (Cis-Pt and 5 FU) in head and neck cancer is efficient in some cases: - ~ 30 % good responders - ~ 30 % partial responders - ~ 30 % non responders - Is it possible to predict the response by analyzing the genome of the tumor? - p 53 mutations

Response to chemotherapy in head and neck cancer Logistic regression Cabelguenne et coll. 2001
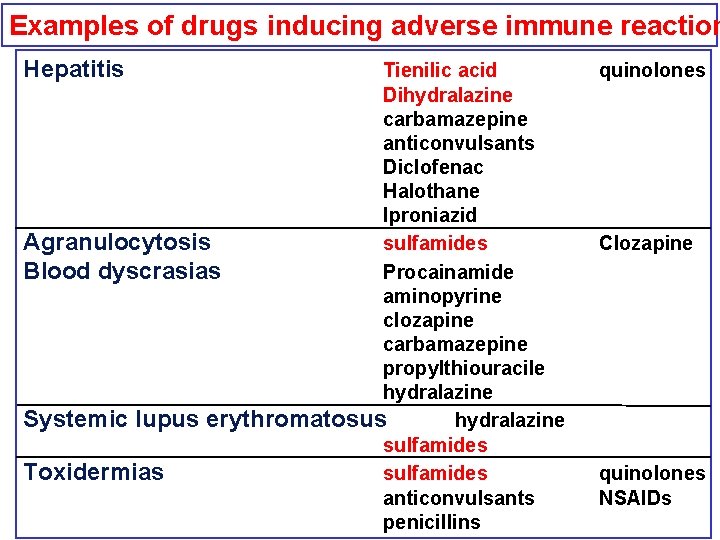
Examples of drugs inducing adverse immune reaction Hepatitis Tienilic acid Dihydralazine carbamazepine anticonvulsants Diclofenac Halothane Iproniazid Agranulocytosis sulfamides Blood dyscrasias Procainamide aminopyrine clozapine carbamazepine propylthiouracile hydralazine Systemic lupus erythromatosus hydralazine sulfamides Toxidermias sulfamides anticonvulsants penicillins quinolones Clozapine quinolones NSAIDs
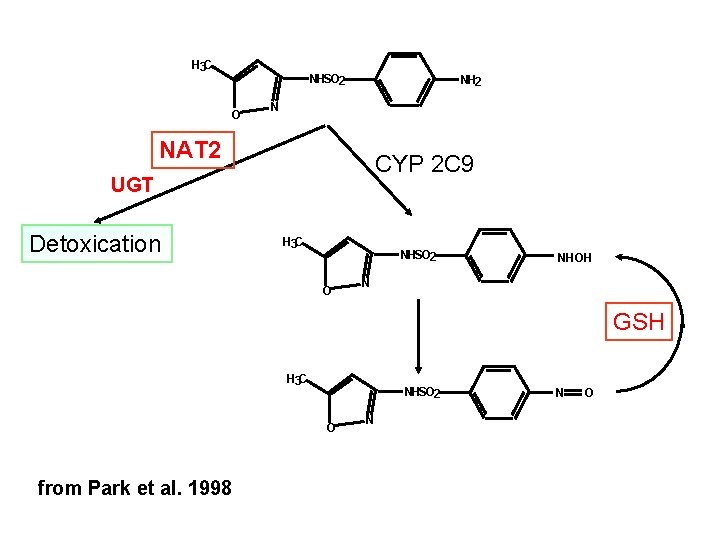
H 3 C NHSO 2 O NH 2 N NAT 2 CYP 2 C 9 UGT Detoxication H 3 C NHSO 2 O NHOH N GSH H 3 C NHSO 2 O from Park et al. 1998 N N O

Toxidermias in AIDS patients treated with sulfamides N - GSTM 1 / - NAT 2 (%) 46 (OR=2. 5) Patients with Tx 41 Patients without Tx 79 25 Total 130 32 Wolkenstein et al. 2000

Fixed drug eruption and sulfamides (trimethoprim/sulfoxasole) - HLA A 30 B 13 Cw 6 more frequent than in control population Oszkaya-Bayazit, J. AM. Acad. Dermatol. 2001 Toxicity of sulfamides linked to - metabolism - immune response - multistep - each factor has influence

Autoantibodies against xenobiotic metabolizing enzymes disease xenobiotic autoantibodies hepatitis agranulocytosis tienilic acid CYP 2 C 9, LKM 2 dihydralazine CYP 1 A 2, LM anticonvulsants CYP? halothane CYP 2 E 1 iproniazide MAO B ? CYP 2 D 6, LKM 1 ? UGT, LKM 3 ? GST clozapine MPO Addison or PGS ? CYP 17, 21, Scc CYP 1 A 2 CYP 2 A 6
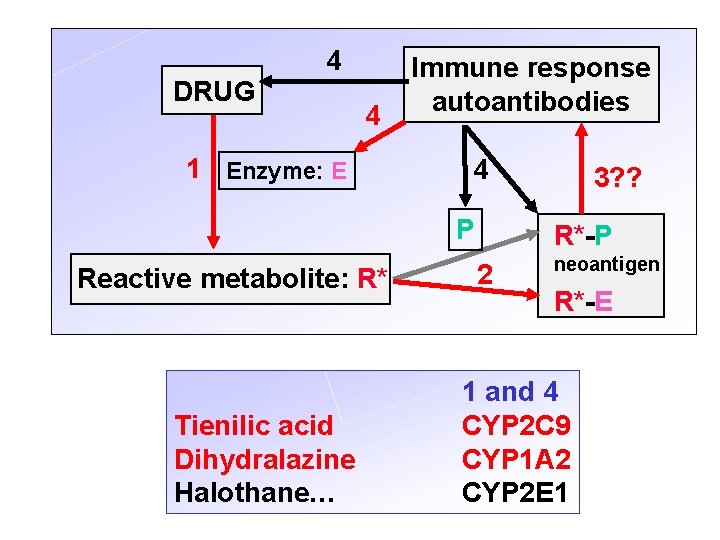
4 DRUG 4 1 Enzyme: E Immune response autoantibodies 4 P Reactive metabolite: R* Tienilic acid Dihydralazine Halothane… 3? ? R*-P 2 neoantigen R*-E 1 and 4 CYP 2 C 9 CYP 1 A 2 CYP 2 E 1
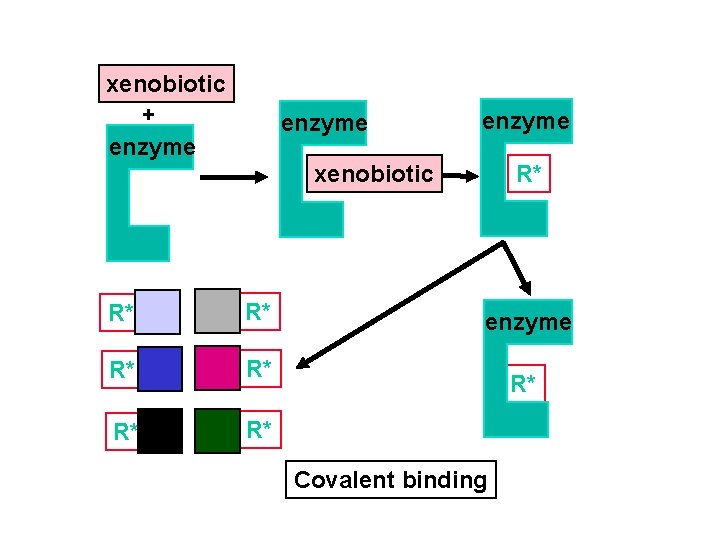
xenobiotic + enzyme xenobiotic R* R* enzyme R* Covalent binding
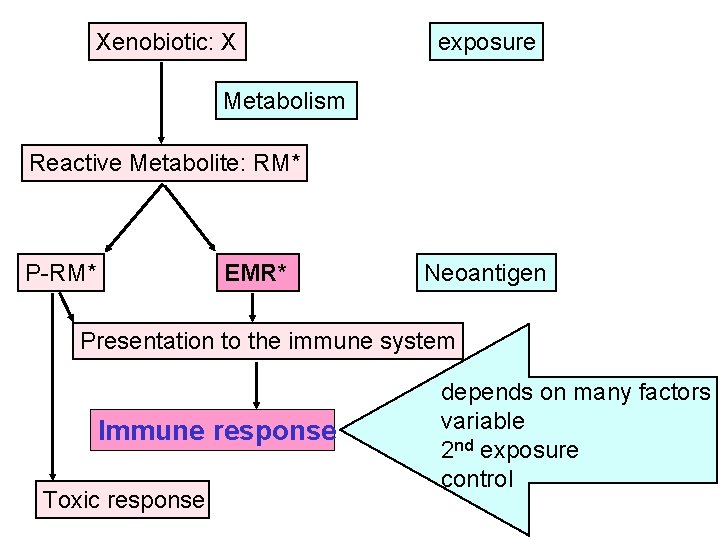
Xenobiotic: X exposure Metabolism Reactive Metabolite: RM* P-RM* EMR* Neoantigen Presentation to the immune system Immune response Toxic response depends on many factors variable 2 nd exposure control
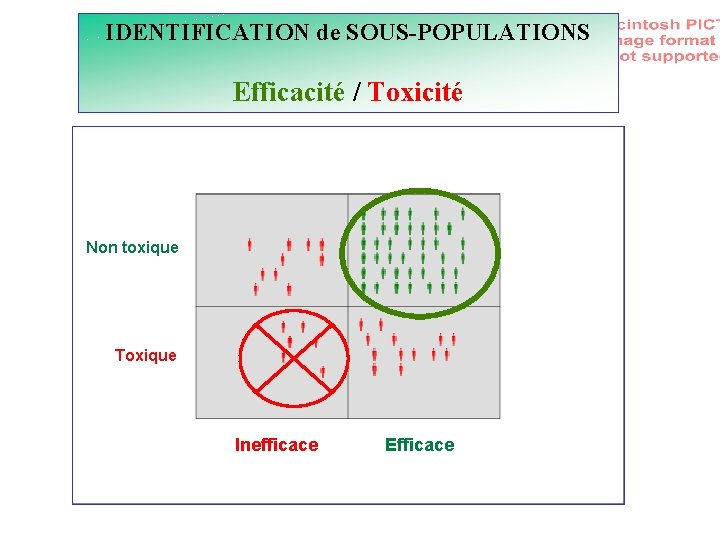
IDENTIFICATION de SOUS-POPULATIONS Efficacité / Toxicité Non toxique Toxique Inefficace Efficace
- Slides: 86