PERYODK CETVELN BAZI GRUPLARI VE ZELLKLER Periyodik cetvel

PERİYODİK CETVELİN BAZI GRUPLARI VE ÖZELLİKLERİ

Periyodik cetvel numaralarına göre tablodur. Bu tabloda birbirine yakın olan toplanmıştır. elementlerin artan atom dizilimini gösteren bir belli kimyasal özellikleri elementler, belli gruplarda � Yatay sütun � Düşey Sütun Periyot : 7 tane periyot vardır Grup : 8 tane a grubu ve 8 tanede b grubu vardır. “b” grubu elementlerine geçiş elementleri denir. Öncelikle inceleyelim: periyodik cetvelin bazı gruplarını
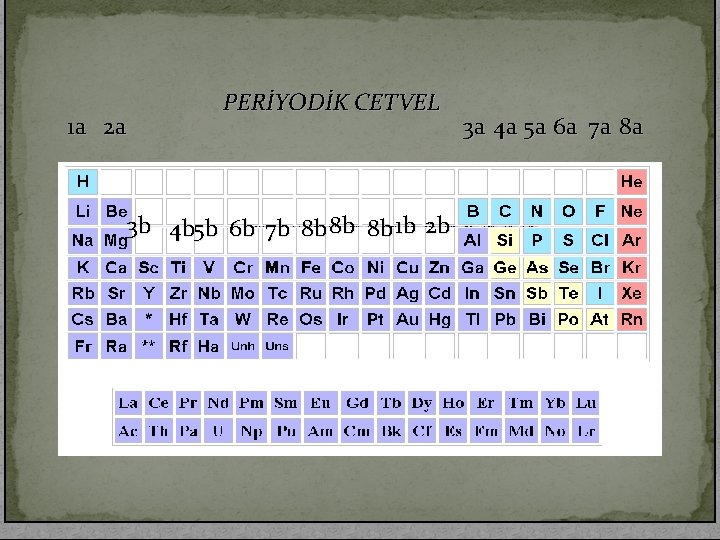
1 a 2 a PERİYODİK CETVEL 3 b 4 b 5 b 6 b 7 b 8 b 8 b 8 b 1 b 2 b 3 a 4 a 5 a 6 a 7 a 8 a

SOYGAZLAR ØPeriyodik cetvelin 8 a grubu elementleridir. ØHe , Ne , Ar , Kr , Xe , Rn bu grubun elementleridir. ØGrupta He dışındaki tüm elementler kararlı elementlerdir. ØErime ve kaynama noktaları çok düşüktür. Grupta yukarıdan aşağıya gidildikçe erime ve kaynama noktaları yükselir.
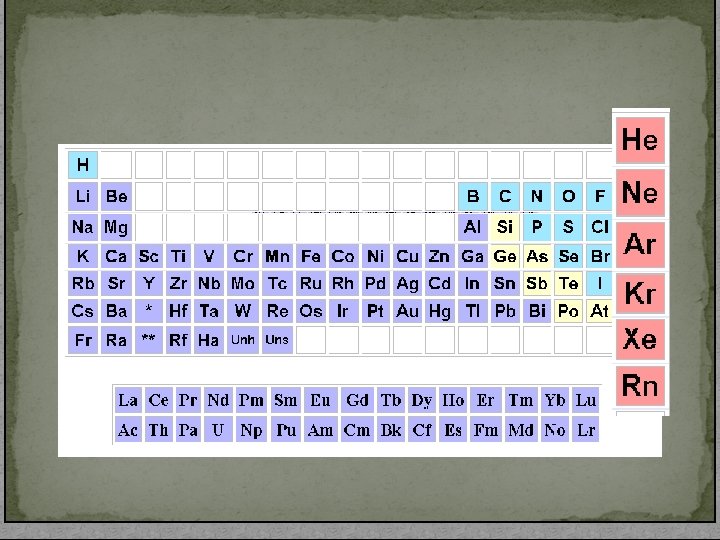

SOYGAZLAR Ø Tümü tek atomlu renksiz gaz halindedir. Ø Yalnız Rd radyoaktif olup çekirdeği dayanaksızdır. Ø Doğada çok az bulunurlar. Ø İyonlaşma enerjileri, sıralarında, en yüksek olan elementlerdir.

ALKALİ METALLER v. Periyodik cetvelin 1 a grubu elementleridir v. Li , Na , K , Rb , Cs , Fr bu grubun elementleridir. v. En yüksek temel enerji düzeylerinde bir elektron vardır. v. Bileşiklerinde ( +1 ) değerlik alırlar. v. Yumuşak, bıçakla kesilebilen, hafif metallerdir. v. Elektrik akımı ve ısıyı iyi iletirler.


ALKALİ METALLER v. Erime ve kaynama noktaları diğer metallerden düşüktür. Grupta yukarıdan aşağıya doğru erime ve kaynama noktaları düşer. vÖzkütleleri düşük olan elementlerdir. vİyonlaşma enerjileri, sıralarında, en düşük olan elementlerdir. v. Tepkime verme yatkınlıkları çok fazladır. v. Doğada daha çok bileşikleri halinde bulunurlar.

v Alkali metaller, havanın oksijeni ile etkileşerek oksit oluştururlar. 2 M(k) +1/2 O 2 ( g) M 2 O(k) v Halojenlerle birleşerek tuzları oluştururlar. 2 M(k) + X 2 2 MX(k) v Su ile hızlı tepkimeye girerler ve hidrojen gazı (H 2) oluştururlar. v 2 M(k) + 2 H 2 O(s) 2 MOH (suda) + H 2 (g)

TOPRAK ALKALİ METALLER ü Periyodik cetveli 2 a grubunda yer alan elementlere toprak alkali metaller adı verilir ü Be , Mg , Ca , Sr , Ba , Ra bu grubun elementleridir. ü Bileşiklerinde +2 değerliklidirler. ü Isı ve elektrik akımını iyi iletirler. ü Alkali metallerden daha sert erime ve kaynama noktaları daha yüksektir. ü İyonlaşma enerjileri alkali yüksektir. metallerden daha


TOPRAK ALKALİ METALLER ü Öz kütleleri de alkali metallerden daha büyüktür ü Oksijenle birleşerek oksitleri oluştururlar. M (k) + ½ O 2 (g) MO(k) ü Halojenlerle birleşerek tuzları oluştururlar. M (k) + Cl 2 (g) MCl 2 (k) ü Su ile tepkimeye girerek hidrojen gazı ( H 2 ) oluştururlar. M (k) + 2 H 2 O (s) M(OH)2 (suda) + H 2 (g)

HALOJENLER ▓ Periyodik cetvelin 7 a grubunda yer alan elementlerdir. ▓ F , Cl , Br , I , At bu grubun elementleridir. ▓ Bileşiklerinde -1 ile +7 arasında çeşitli değerlikler alabilirler. Ancak F bileşiklerinde sadece -1 değerlik alır. ▓ Erime ve kaynama noktaları grupta aşağıdan yukarıya doğru azalır. ▓ Elektron alma istekleri en fazla olan elementlerdir.
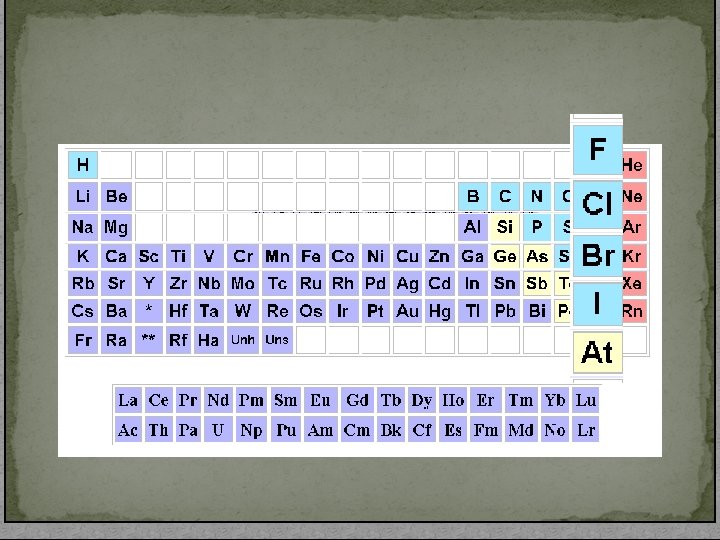

HALOJENLER ▓ Tümü renklidir. ▓ Tümü zehirli ve tehlikelidir. ▓ Element halinde 2 atomlu moleküllerden oluşurlar. (F 2, Cl 2 , Br 2 , I 2 , At 2 ) ▓ At (astatin) doğada bulunmayan, ancak radyoaktif olaylarla oluşan bir elementdir. ▓ Oda koşullarında F ve Cl gaz, Br sıvı, I ise katı haldedir.

ÜÇÜNCÜ SIRA ELEMENTLERİ Periyodik cetvelin üçüncü sırası Na (sodyum) metali ile başlar Ar (argon) soygazı ile biter. Periyodik cetvelin aynı grubundaki elementlerin değerlik elektron sayıları aynı, özellikleri de birbirine benzerdir. Ancak bir sırada bulunan elementlerin başta değerlik elektron sayıları olmak üzere birçok özellikleri farklılık gösterir. Dolayısıyla da Fiziksel ve kimyasal özeliklerde önemli değişiklikler söz konusudur. Buradan sonuç olarak sodyumdan başlayarak argona kadar devam eden elementler birbirlerinden fiziksel ve kimyasal özellikleri bakımından ayrılmışlardır.

DÖRDÜNCÜ SIRA GEÇİŞ ELEMENTLERİ Buraya kadar incelediğimiz gruplar ve sırada değerlik elektronları s ya da p orbitallerinde bulunuyordu. Yani a gruplarındaydı. Geçiş elementlerindeyse değerlik elektronları d orbitallerinde bulunur ve bu elementler 2 a ve 3 a grubu arasında yer alır. Periyodik cetvelin 21 atom numaralı skandiyum ile başlayıp 30 atom numaralı çinko ile biten sıradaki elementler ile bunların altında kalan tüm elementler, geçiş elementleri grubuna girer.
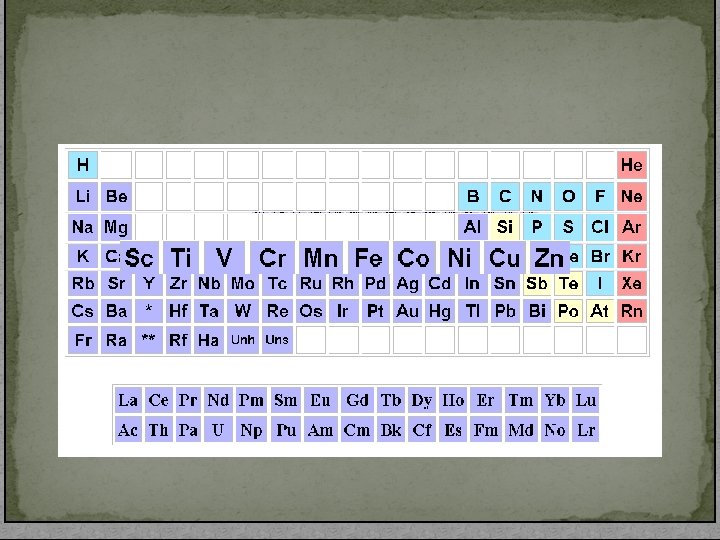

DÖRDÜNCÜ SIRA GEÇİŞ ELEMENTLERİ Ξ Dördüncü sıra geçiş elementleri: Se , Ti , V , Cr , Mn , Ξ Ξ Ξ Fe , Co , Ni , Cu , Zn. Tümü metaldir. 1 a ve 2 a grubu metallerinden farklı olup, sert ve özkütlesi büyük metallerdir. Erime ve kaynama noktaları çok yüksektir. Elektrik akımı ve ısıyı iyi iletirler. Kimyasal tepkimelere yatkınlık bakımından aralarında çok büyük farklılık vardır.

DÖRDÜNCÜ SIRA GEÇİŞ ELEMENTLERİ Ξ 1 a , 2 a , 3 a grubundaki metallerin yalnız bir tür değerliği söz konusuyken geçiş elementlerinin farklı değerlikli birçok bileşikleri vardır. Geçiş elementlerini diğer metalerden farklandıran özellik yalnız s orbitalinden değil, tam dolu olmayan d orbitalininde bileşik oluşturma ile ilgili olmalarıdır. Ξ Periyodik cetvelin altına iki sıra halinde yazılan elementlere İç geçiş Elementleri ya da İçg eçiş Metalleri denir.
- Slides: 21