PERKEMBANGAN TEORI ATOM Indikator Menjelaskan penemuan dan perkembangan

PERKEMBANGAN TEORI ATOM

Indikator Menjelaskan penemuan dan perkembangan stuktur atom, mulai dari teori atom Dalton hingga teori atom modern.
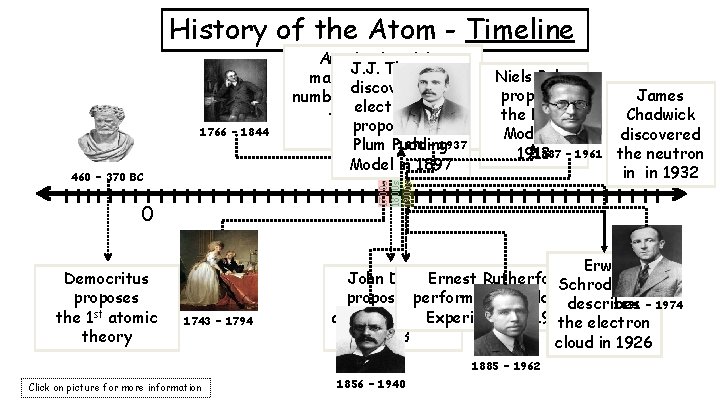
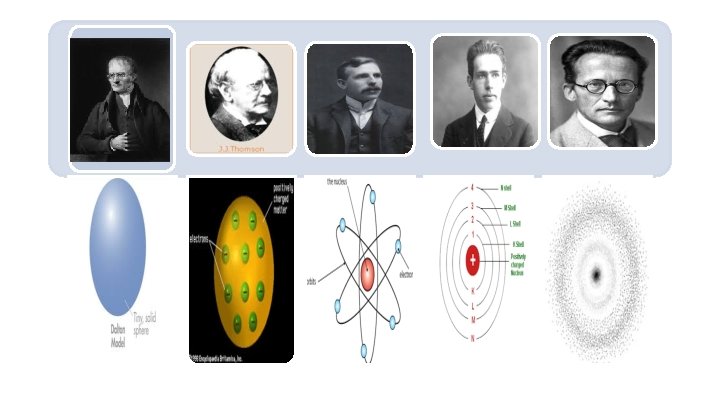
History of the Atom - Timeline 1766 – 1844 1700 s 1800 s 1900 s 460 – 370 BC 0 Democritus proposes the 1 st atomic theory Antoine Lavoisier J. J. Thomson makes a substantial discovers the number of contributions electron and to the field of proposes the Chemistry 1871 – 1937 Plum Pudding Model in 1897 1743 – 1794 Niels Bohr proposes James the Bohr Chadwick Model in discovered 1887 – 1961 the neutron 1913 in in 1932 Erwin Ernest Rutherford John Dalton Schrodinger the Gold Foil proposes performs his 1891 – 1974 describes Experiment in 1909 atomic theory in the electron 1803 cloud in 1926 1885 – 1962 Click on picture for more information 1856 – 1940

Democritus 460 – 370 SM

Teori Atom menurut Democritus : Dengan berdasarkan Observasi di Pantai - - - Atom adalah Materi yang tersusun dari partikel yang tidak bisa dibagi lagi. Terdapat ruang kosong diantara atom-atom Atom berwujud padat Atom bersifat homogen dan tidak punya struktur internal Atom memiliki bentuk, ukuran da berat yang berbeda

Kelemahan Teori Democritus - Tidak dapat menjelaskan sifat-sifat kimia materi - Tidak berdasarkan metode ilmiah

John Dalton (1766 – 1844)

Postulat Dalton Berdasarkan Hukum Kekekalan Massa dan Perbandingan Tetap 1 3 Setiap Unsur terdiri atas partikel yang sudah tidak dapat dibagi lagi yang disebut Atom tidak bisa dihancurkan. Pada reaksi kimia, atom ditata ulang tetapi tidak dipecah 2 4 Atom-atom dari suatu unsur adalah identik. Atom-atom dari unsur yang berbeda sifat berbeda, termasuk mempunyai massa yang berbeda Senyawa terbentuk ketika atom-atom dari dua jenis atau lebih bergabung dengan perbandingan tertentu.

Kelemahan Teori Atom Dalton - Ternyata atom bukanlah sesuatu yang tak terbagi lagi melainkan terdiri dari partikel sub atom. Atom-atom dari unsur yang sama tidak sama dalam segala hal dan unsur yang berbeda juga tidak berbeda dalam segala hal. Hal ini ditunjukkan dengan adanya isotop dan isobar. Melalui reaksi nuklir, atom dari suatu unsur dapat dirubah menjadi atom lain Beberapa unsur tidak terdiri atas atom-atom melainkan molekul - molekul

JJ Thomson (1856 – 1940)
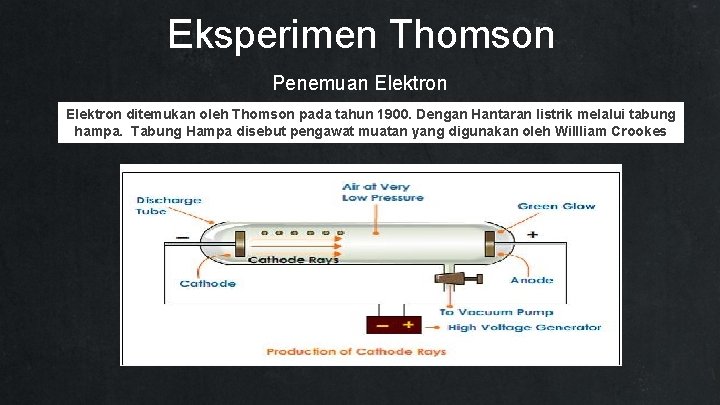
Eksperimen Thomson Penemuan Elektron ditemukan oleh Thomson pada tahun 1900. Dengan Hantaran listrik melalui tabung hampa. Tabung Hampa disebut pengawat muatan yang digunakan oleh Willliam Crookes
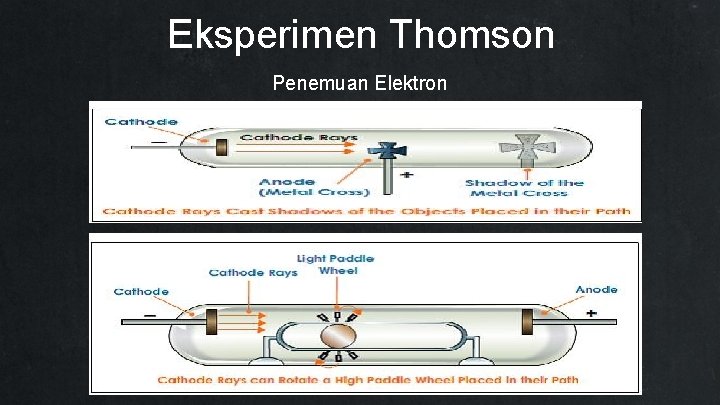
Eksperimen Thomson Penemuan Elektron

Eksperimen Thomson Penemuan Elektron Sinar katoda tersusun dari partikel-partikel yang bermuatan listrik, energetic (memiliki energi kinetik). Partikel ini adalah penyusun (building block) materi dan partikel dasar (fundamental particle) yang disebut Elektron
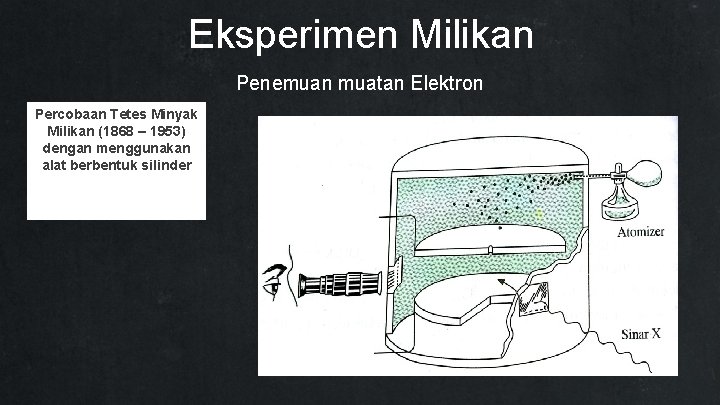
Eksperimen Milikan Penemuan muatan Elektron Percobaan Tetes Minyak Milikan (1868 – 1953) dengan menggunakan alat berbentuk silinder

Eksperimen Milikan Penemuan muatan Elektron Melalui percobaan tersebut, Milikan menemukan bahwa muatan tetes-tetes minyak selalu merupakan kelipatan bulat dari suatu muatan tertentu, yaitu 1, 602 coulomb. Milikan menyimpulkan bahwa muatan tersebut adalah muatan satu elektron. e = 1, 602 x 10 -19 Maka, massa elektron, m = 9, 11 x 10 -28
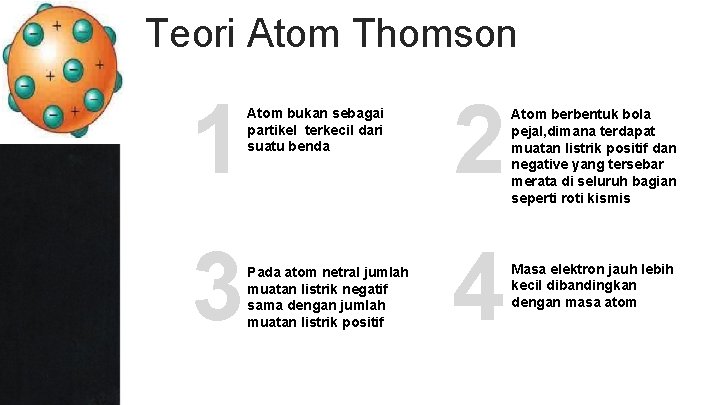
Teori Atom Thomson 1 3 Atom bukan sebagai partikel terkecil dari suatu benda Pada atom netral jumlah muatan listrik negatif sama dengan jumlah muatan listrik positif 2 4 Atom berbentuk bola pejal, dimana terdapat muatan listrik positif dan negative yang tersebar merata di seluruh bagian seperti roti kismis Masa elektron jauh lebih kecil dibandingkan dengan masa atom

Kelemahan Teori Atom Thomson - Tidak dapat menjelaskan kedudukan elektron dalam atom. - Tidak dapat menjelaskan fenomena elektron lepas jika diberi energi seperti tegangan listrik.

Rutherford (1871 – 1937)
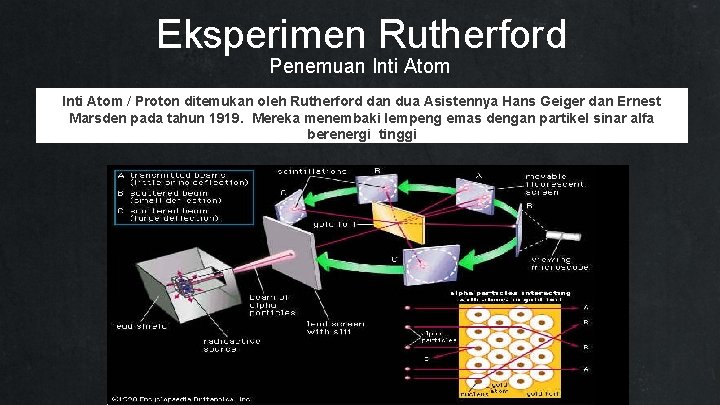
Eksperimen Rutherford Penemuan Inti Atom / Proton ditemukan oleh Rutherford dan dua Asistennya Hans Geiger dan Ernest Marsden pada tahun 1919. Mereka menembaki lempeng emas dengan partikel sinar alfa berenergi tinggi

Eksperimen Rutherford Penemuan Inti Atom Pada tahun 1886 kimiawan bernama Goldstein menemukan partikel yang disebut Proton/inti atom dengan melakukan percobaan dengan sinar tabung katode

Teori Atom Rutherford 1 Atom terdiri atas inti atom yang bermuatan listrik positif, dimana masa atom hampir seluruhnya berada pada inti atom. 3 2 Muatan listrik negatif ( elektron ) terletak sangat jauh dari inti Untuk menjaga kestabilan jarak muatan listrik negatif terhadap inti, maka muatan listrik negatif senantiasa bergerak mengelilingi inti.

Teori Atom Rutherford 1 Atom terdiri atas inti atom yang bermuatan listrik positif, dimana masa atom hampir seluruhnya berada pada inti atom. 3 2 Muatan listrik negatif ( elektron ) terletak sangat jauh dari inti Untuk menjaga kestabilan jarak muatan listrik negatif terhadap inti, maka muatan listrik negatif senantiasa bergerak mengelilingi inti.

Kelemahan Teori Atom Rutherford 1. 2. 3. 4. Teori atom Rutherford ini belum mampu menjelaskan dimana letak elektron dan cara rotasinya terhadap ini atom. Elektron memancarkan energi ketika bergerak, sehingga energi atom menjadi tidak stabil. Tidak dapat menjelaskan spektrum garis pada atom hidrogen (H). Tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan teori fisika, gerakan elektron mengelilingi inti ini disertai pemancaran energi sehingga lama-kelamaan energi elektron akan berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke dalam inti.

Niels Bohr (1885 – 1962)

Kelemahan Teori Atom Bohr • Melanggar asas ketidakpastian Heisenberg karena elektron mempunyai jari-jari dan lintasan yang telah diketahui. • Model atom Bohr mempunyai nilai momentum sudut lintasan ground state yang salah. • Lemahnya penjelasan tentang prediksi spektra atom yang lebih besar. • Tidak dapat memprediksi intensitas relatif garis spektra. • Model atom Bohr tidak dapat menjelaskan struktur garis spektra yang baik. • Tidak dapat menjelaskan efek Zeeman.

Mekanika Kuantum (Erwin Scrondinger 1927)

Teori Atom Mekanika Kuantum Berdasarkan Hipotesis Louis de Broglie dan azas ketidakpastian dari Heisenberg 1 Elektron mempunyai tingkat energi tertentu, posisinya tidak dapat dipastikan. 3 2 Daerah dengan peluang terbesar untuk menemukan elektron disebut Orbital Kebolehjadian menemukan elektron pada suatu titik pada jarak tertentu dari intinya.
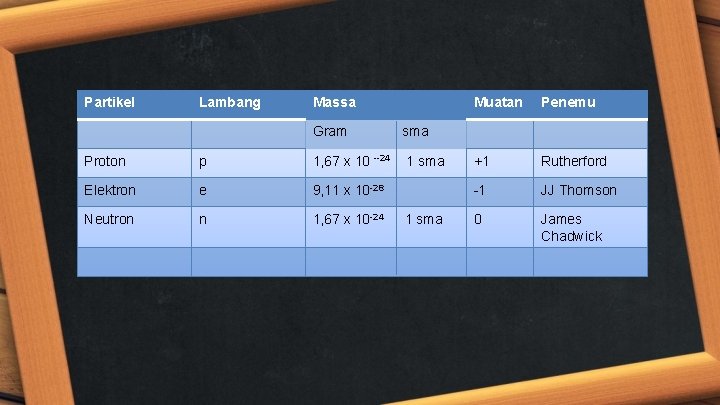
Partikel Lambang Massa Gram Proton p 1, 67 x 10 --24 Elektron e 9, 11 x 10 -28 Neutron n 1, 67 x 10 -24 Muatan Penemu +1 Rutherford -1 JJ Thomson 0 James Chadwick sma 1 sma

Thank you
- Slides: 30