PERIODNI SISTEM ELEMENATA PERIODNI SISTEM ELEMENATA Periodni sistem







- Slides: 8

PERIODNI SISTEM ELEMENATA

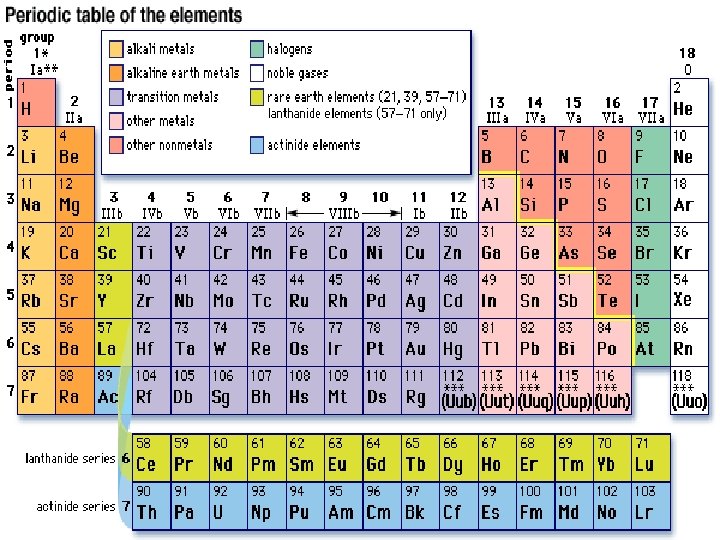
PERIODNI SISTEM ELEMENATA �Periodni sistem elemenata predstavlja prikaz svih poznatih hemijskih elemenata, poredanih po rastućem atomskom broju i elektronskoj konfiguraciji. Elementi su postavljeni tako da su oni sa sličnim hemijskim osobinama svrstani zajedno, u istu glavnu i sporednu grupu, a pored podele po grupama, postoji i podjela po periodama. Periodne sisteme, gotovo identične, nezavisno jedan od drugog razvili su 1869. godine ruski hemičar Dmitrij Ivanovič Mendeljejev(18341907), a samo nekoliko mjeseci kasnije i njemački hemičar Lothar Meyer(1830– 1895).

�Kasnija otkrica o strukturi atoma pokazala su da bi elemente trebalo poredati prema atomskim brojevima tako da svaki naredni element ima jedan proton vise od prethodnog. Postoji 4 vrste elemenata: metali, nemetali, metaloidi i pleneniti gasovi. �U levom uglu periodnog sistema nalaze se metali i oni zauzimaju najveci deo Periodnog sistema elemenata. Desno se nalaze nemetali. Izmedu njih se nalaze metaloidi, elementi koji imaju neka svojstva metala, a neka nemetala. U krajnjem desnom delu Periodnog sistema elemenata nalaze se plemeniti gasovi.

GRUPE I PERIODE �Elementi u periodnom sistemu svrstani su po horizontalnim nivoima (periodama) i vertikalnim nivoima (grupama). � Horizontalni nizovi su energetski nivoi i ima ih 7. �Vertikalni nizovi nazivaju se grupe i ima ih 8 (18). � Broj grupe određuje se na osnovu svih elektrona koji se nalaze na poslednjem energetskom nivou. � Perioda predstavlja najveću vrednost glavnog kvantnog broja.


PERIODNI ZAKON �Periodni zakon (ili zakon periodičnosti, svojstava) kaže da ako hemijske elemente poredamo po rastućoj atomskoj masi (zapravo, tačnije rečeno, po rastućem protonskom broju) i krenemo promatrati fizička i hemijska svojstva elemenata, primeticemo da se ona nakon nekog broja elemenata počinju ponavljati. �Za prva četiri elementa periodi ponavljanja su 8, 8, 18, 32 (za ostale elemente treba odbaciti prvi ili nekoliko prvih članova niza). Tako recimo ako krenemo od elementa helijuma (redni broj 2), idući element koji ima slična svojstva je neon (redni broj 10, a 10 = 2 + 8), pa zatim argon (redni broj 18, a 18 = 2 + 8), pa kripton (redni broj 36, a 36 = 2 + 8 + 18), pa ksenon (redni broj 54, a 54 = 2 + 8 + 18), i konačno radon (redni broj 86, a 86

�Drugim riječima, rednom broju helijuma moramo redom dodavati brojeve 8, 8, 18, 32 i 32 (uoči da zadnji element toga niza još uvijek nije otkriven, odnosno pripravljen!) da bismo dobili redne brojeve njemu sličnih elemenata. Istu stvar uočit ćemo ako krenemo od litijuma i stanemo zapisivati redne (protonske) brojeve elemenata koji su slični litijumu (a to su natrijum, kalijum, rubidijum, cezijum i francijum).

PREZENTACIJU URADIO: STEVANOV TODOR