PERIODNI SISTEM ELEMENATA Ia GRUPA P S E




- Slides: 5

PERIODNI SISTEM ELEMENATA

Ia GRUPA P. S. E. § Ia i VIIa grupa § izučava se posebno § 1 s 1 § lakše prima elektrone nego što ih otpušta § gasovito stanje na sobnoj temperaturi § Ttopljenja= -259. 0 o. C ; Tključanja= -252. 8 o. C § najlakši gas u prirodi § bez boje, ukusa i mirisa § slabo rastvoran u vodi § u obliku dvoatomnog molekula (H 2) § najrasprostranjeniji element u svemiru (60. 40%) Laboratorijsko dobijanje: § u reakciji metala i vodenog rastvora neke kiseline: Zn + 2 HCl Zn. Cl 2 + H 2

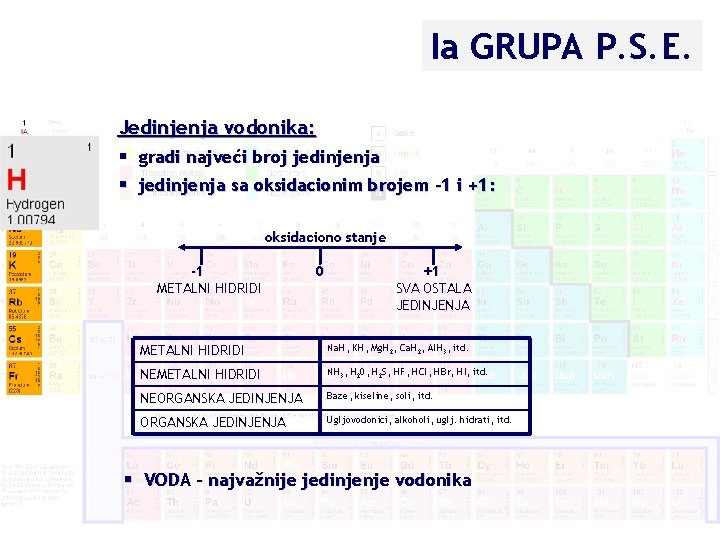
Ia GRUPA P. S. E. Jedinjenja vodonika: § gradi najveći broj jedinjenja § jedinjenja sa oksidacionim brojem -1 i +1: oksidaciono stanje -1 METALNI HIDRIDI 0 +1 SVA OSTALA JEDINJENJA METALNI HIDRIDI Na. H, KH, Mg. H 2, Ca. H 2, Al. H 3, itd. NEMETALNI HIDRIDI NH 3, H 20, H 2 S, HF, HCl, HBr, HI, itd. NEORGANSKA JEDINJENJA Baze, kiseline, soli, itd. ORGANSKA JEDINJENJA Ugljovodonici, alkoholi, uglj. hidrati, itd. § VODA – najvažnije jedinjenje vodonika

- grupa alkalnih metala - Ia GRUPA P. S. E. § ns 1 § niske temp. topljenja i mala gustina § mala tvrdoća § najreaktivniji metali – ne postoje u slobodnom stanju § isključivo +1 oksidaciono stanje u jedinjenjima § burno reaguju sa vodom gradeći odgovarajuće baze § grade hidride, okside, baze i soli: HIDRIDI Me. H OKSIDI Me 2 O BAZE Me. OH SOLI Me. A, Me 2 A, Me 3 A § boje plamen karakterističnim bojama: Li Na K Rb Cs

Ia GRUPA P. S. E. Važnija jedinjenja elemenata Ia grupe P. S. E. : § § § § § Na. Cl – Natrijum hlorid (“kuhinjska so”) Na. OH – Natrijum hidroksid (“masna soda”) Na. HCO 3 – Natrijum hidrogenkarbonat (“soda bikarbona”) Na 2 CO 3 – Natrijum karbonat (“soda”, dekahidrat je “kristalna soda”) Na 2 SO 4 – Natrijum sulfat (dekahidrat je “Glauberova so”) Na. NO 3 – Natrijum nitrat (“čilska šalitra”) KNO 3 – Kalijum nitrat (“šalitra”) KOH – Kalijum hidroksid KCl – Kalijum hlorid. . . i još mnogo, mnogo drugih jedinjenja. . .