Periodick tabuka chemickch prvkov Z Jarovnice 192 Mgr
Periodická tabuľka chemických prvkov ZŠ Jarovnice 192 Mgr. Gabriela Kropuchová

Dmitrij Ivanovič Mendelejev 1834 - 1907 � narodil sa ako sedemnáste dieťa riaditeľa gymnázia v Tobolsku na Sibíri � po skončení gymnázia študoval chémiu a učiteľstvo stal sa profesorom chémie na Petrohradskej univerzite � vytvoril tabuľku s prázdnymi kartičkami a umiestnil v tabuľke všetky vtedy známe chem. prvky bez porušenia periodického zákona = Mendelejevova tabuľka chem. prvkov / r. 1869 � až o niekoľko rokov boli objavované prvky, pre ktoré už bolo v tabuľke miesto - gálium, germánium a scandium
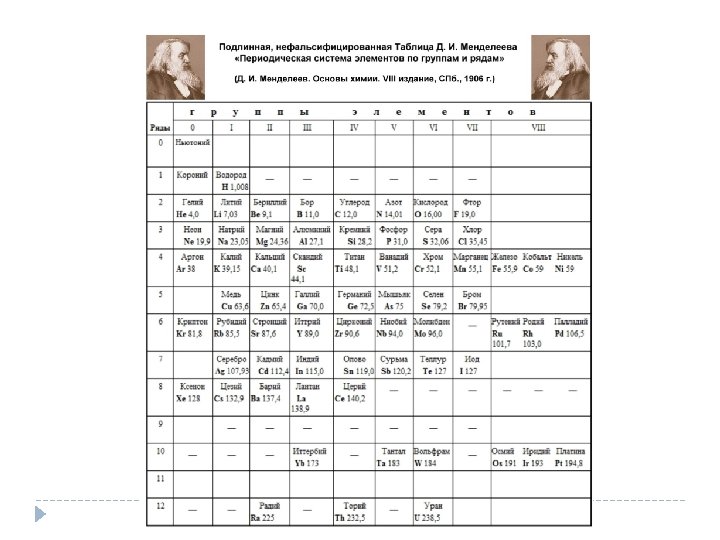

Periodická sústava a periodická tabuľka � Periodická sústava prvkov (PSP) – usporiadanie prvkov podľa ich stúpajúceho protónového čísla do radov a skupín. Periodická tabuľka prvkov (PTP) – grafické znázornenie periodickej sústavy prvkov. � � Každý prvok má v tabuľke svoje okienko, ktoré musí obsahovať: protónové číslo značka prvku atómová relatívna hmotnosť (názov, latinský názov, elektronegativita, teploty varu a topenia, konfigurácia, oxidačné čísla, . . . )
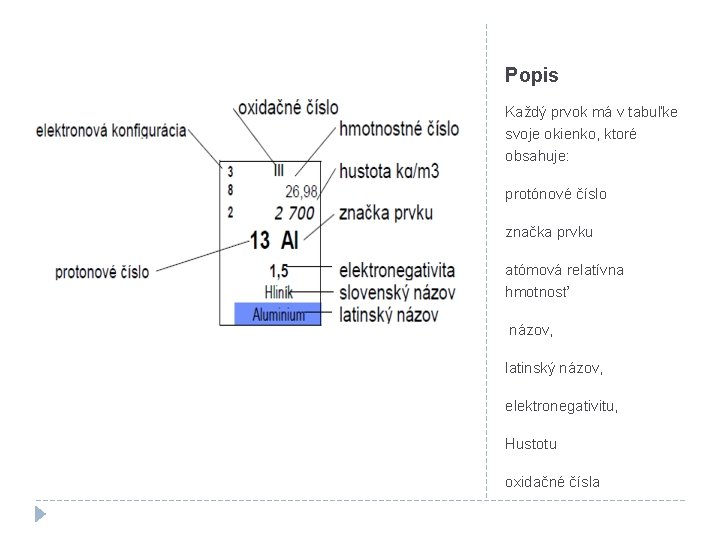
Popis Každý prvok má v tabuľke svoje okienko, ktoré obsahuje: protónové číslo značka prvku atómová relatívna hmotnosť názov, latinský názov, elektronegativitu, Hustotu oxidačné čísla

Periodický zákon Prvky sú v periodickej tabuľke umiestnené postupne podľa narastajúceho počtu protónov , teda podľa protónových čísel prvkov � vlastnosti prvkov v tabuľke sa periodicky menia napr. � elektronegativita

Skupiny � Skupiny – stĺpce prvkov v tabuľke, � označujeme ich arabskými číslicami 1 – 18 (staršie označenie je I. A – VIII. A; I. B – VIII. B). Prvky v jednej skupine majú rovnaký počet valenčných elektrónov a podobné vlastnosti. � Prvky v jednej skupine majú podobné vlastnosti � � Špecifické pomenovanie skupín: 1. skupina – alkalické kovy (okrem H) 2. skupina – kovy alkalických zemín 16. skupina – chalkogény 17. skupina – halogény 18. skupina – vzácne plyny

Periódy � Periódy– riadky prvkov v tabuľke � označujeme ich arabskými číslicami 1 – 7 � Číslo periódy zodpovedá počtu vrstiev, ktoré sú obsadené elektrónmi napr. : 1. perióda H, He – elektróny sú iba na jednej vrstve 2. perióda Li, Be, B, C, N, O, F, Ne - elektróny sú v 2 vrstvách 3. perióda Na, Mg, Al, Si, P, S, Cl, Ar - elektróny sú v 3 vrstvách
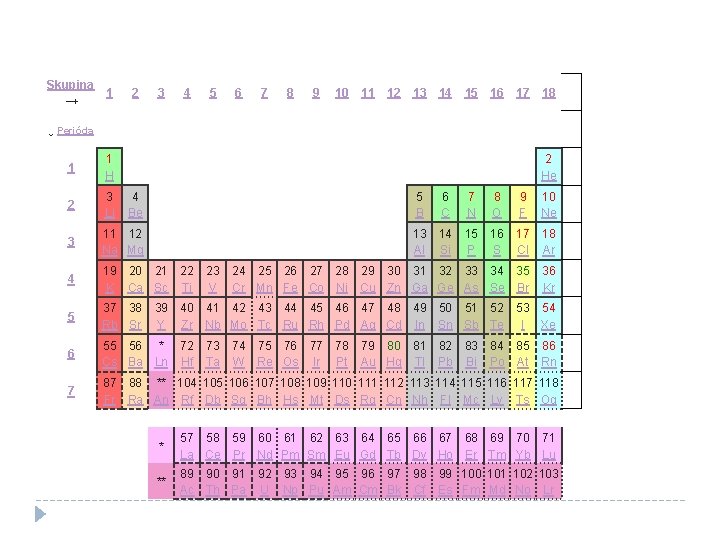
Skupina → 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 ↓ Perióda 1 1 H 2 He 2 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne 3 11 12 Na Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar 4 19 20 21 K Ca Sc 22 Ti 24 25 26 27 28 29 30 31 32 33 34 35 Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br 36 Kr 5 37 38 Rb Sr 40 41 42 43 44 45 46 47 48 49 50 51 52 Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te 6 55 56 * Cs Ba Ln 7 87 88 ** 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 Fr Ra An Rf Db Sg Bh Hs Mt Ds Rg Cn Nh Fl Mc Lv Ts Og 39 Y 72 Hf 23 V 73 Ta 74 75 76 77 W Re Os Ir 53 54 I Xe 78 79 80 81 82 83 84 85 86 Pt Au Hg Tl Pb Bi Po At Rn * 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu ** 89 90 91 92 93 94 95 96 97 Ac Th Pa U Np Pu Am Cm Bk 98 Cf 99 100 101 102 103 Es Fm Md No Lr
- Slides: 10