PERIODICK SOUSTAVA PRVK Tato prezentace vznikla z domcch
























































































































































- Slides: 166

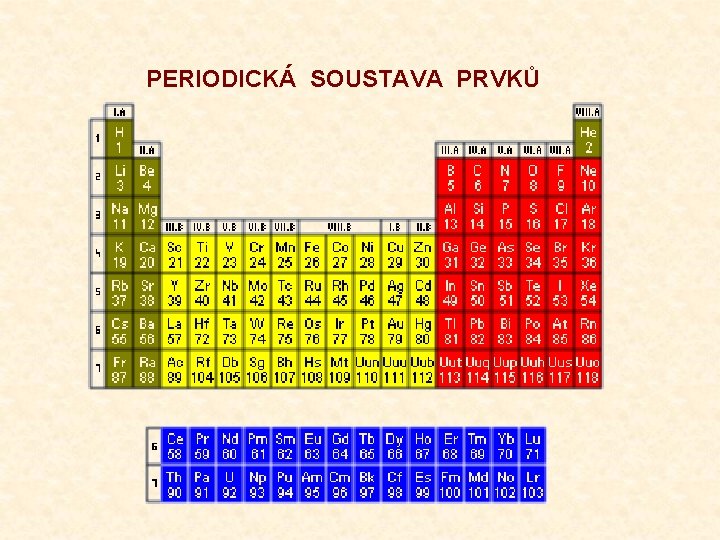
PERIODICKÁ SOUSTAVA PRVKŮ

Tato prezentace vznikla z domácích prací žáků osmého ročníku ZŠ v Komenského ulici v Letohradě a slouží k opakování učiva a získávání informací i pro zvídavé mladší žáky, dospělé jedince nevyjímaje.

Obsah • • Úvod Periodický zákon Chemické prvky periodická soustava prvků Mnemotechnické pomůcky pro zapamatování prvků umístěných v periodické tabulce

Periodický zákon • Chemické prvky jsou seřazeny v periodické soustavě prvků (=PSP) podle vzrůstajícího protonového čísla. Vlastnosti prvků se periodicky mění v závislosti na protonovém čísle. Tato zákonitost se nazývá periodický zákon. • Tabulkovým vyjádření periodického zákona je PSP. Prvky jsou uspořádány do: řad (=period) značí se čísly 1 – 7. Číslo periody určuje počet elektronových vrstev, v nichž jsou elektrony rozmístěny. Poslední vrstva je označována jako valenční. sloupců (=skupin) značí se římskými číslicemi a písmenem I. A – VIII. A a I. B – VIII. B. Číslo skupiny vyjadřuje počet valenčních elektronů. • Prvky se stejným počtem valenčních elektronů mají podobné vlastnosti. • Prvky se rozlišují na kovy, nekovy a polokovy. Zpět na obsah

Periodická soustava prvků I. A – alkalické kovy Li Na K Rb Cs Fr II. A – kovy alkalických zemin Be Mg Ca Sr Ba Ra VII. A – halogeny F Cl Br I At VIII. A – vzácné plyny He Ne Ar Kr Xe Rn Další kovy Ti Cr Fe Co Ni Cu Zn Ag Au Al W Ir Pt Hg Pb Sn Další nekovy C N O H P S Polokov Si Zpět na obsah

Mnemotechnická pomůcka pro zapamatování prvků periodické soustavy • • • druhá řada periodické tabulky prvků: Líbal Bedřich Boženu Celou Nahou O Fuj Nestyda skupina I. a periodické tabulky prvků: Helenu Líbal Na Kolena Robustní Cestář Francek skupina II. a periodické tabulky prvků: Běžela Magda Caňonem Srážela Balvany Ramenem skupina IV. a periodické tabulky prvků: Co Si Germáni Snaží Probodnout? skupina V. a periodické tabulky prvků: Náš Pes Asi Sbaštil Bizona skupina VI. a periodické tabulky prvků: Ó Slečno Sejměte Též Podprsenku skupina VII. a periodické tabulky prvků: Floutek Cleofáš Bručí Iako Atom. skupina VIII. a periodické tabulky prvků: Helena Nechtěla s Arogantním Králem Xenofonem Randit Lanthanoidy: Laciné Ceny Prasat Nedovolily Prométheovi Smést Europu Gdyž Théby Dýchaly Horkou Erotickou Tmou Ybyšku Lučního Zpět na přehled prvků

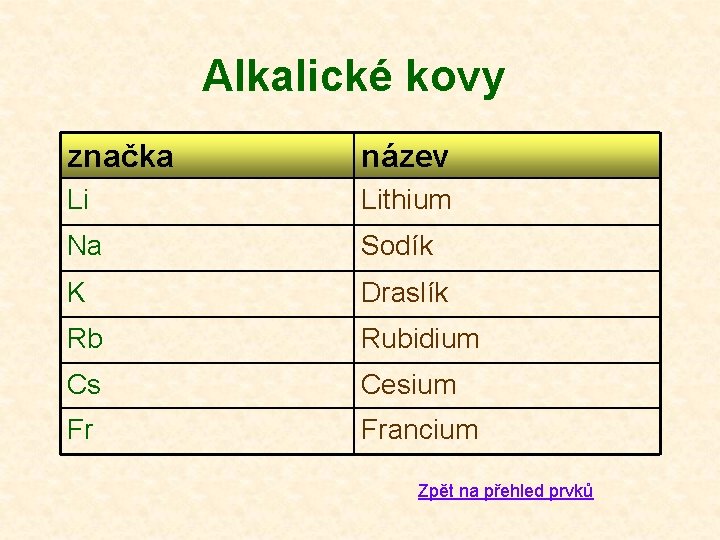
Alkalické kovy značka název Li Lithium Na Sodík K Draslík Rb Rubidium Cs Cesium Fr Francium Zpět na přehled prvků

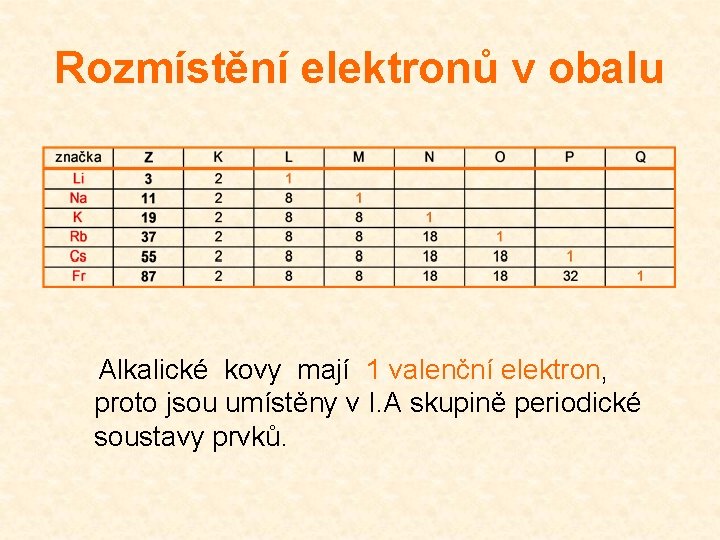
Rozmístění elektronů v obalu Alkalické kovy mají 1 valenční elektron, proto jsou umístěny v I. A skupině periodické soustavy prvků.

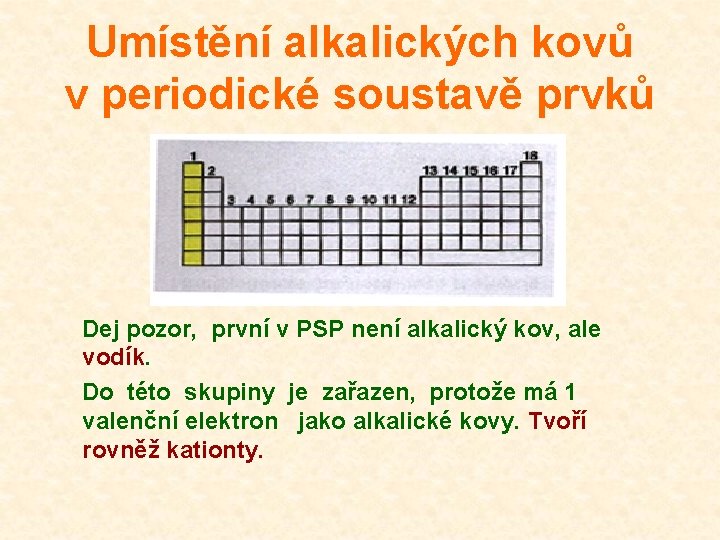
Umístění alkalických kovů v periodické soustavě prvků Dej pozor, první v PSP není alkalický kov, ale vodík. Do této skupiny je zařazen, protože má 1 valenční elektron jako alkalické kovy. Tvoří rovněž kationty.

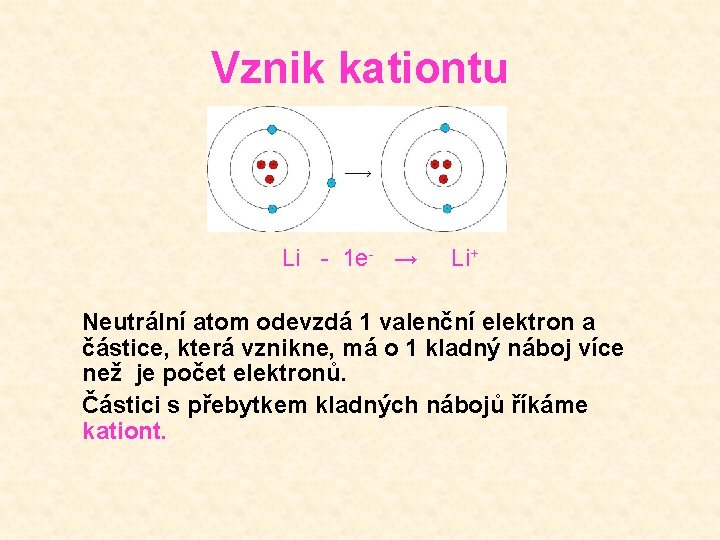
Vznik kationtu Li - 1 e- → Li+ Neutrální atom odevzdá 1 valenční elektron a částice, která vznikne, má o 1 kladný náboj více než je počet elektronů. Částici s přebytkem kladných nábojů říkáme kationt.

Vlastnosti alkalických kovů Jsou stříbrolesklé, měkké, dají se lehce krájet nožem. Na vzduchu se rychle pokrývají vrstvičkou sloučenin, zejména s kyslíkem, proto se chrání před vzduchem uložením v petroleji. Mají malou hustotu (menší než voda) a nízkou teplotu tání. Sloučeniny alkalických kovů charakteristicky zbarvují plamen (viz obr. ). sloučenina lithia červené zbarvení sloučenina draslíku- růžovofialové zbarvení. sloučenina sodíku- žluté zbarvení

Reakce alkalických kovů s vodou Reakce s vodou je (s výjimkou lithia) bouřlivá až explozivní. Vznikají při ní hydroxidy a vodík (H 2). Reakce sodíku s vodou Reakce draslíku s vodou 2 Na + 2 H 2 O → H 2 + 2 Na. OH 2 K + 2 H 2 O → H 2 + 2 KOH

Užití alkalických kovů • Lithium - v jaderné technice – při výrobě vodíkové bomby • Sodík - v osvětlovací technice v sodíkových výbojkách • Sodík a draslík - slitina 75% draslíku a 25% sodíku, jejíž teplota tání je – 10° C se využívá jako „chladící kapalina“ v jaderných reaktorech. Její výhodou je, že nezpůsobuje korozi potrubí, nevýhodou je nebezpečí exploze při vniknutí vody do chladícího systému. Zpět na přehled prvků

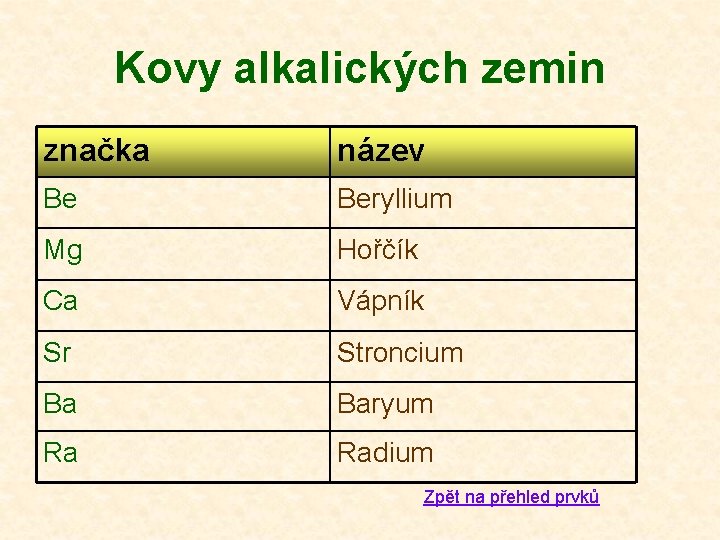
Kovy alkalických zemin značka název Be Beryllium Mg Hořčík Ca Vápník Sr Stroncium Ba Baryum Ra Radium Zpět na přehled prvků

Beryllium (Be)

Vlastnosti • Beryllium a hořčík se velmi liší svými vlastnostmi od kovů alkalických zemin. • Práškovité beryllium vyvolává kožní ekzémy a poškozuje dýchací cesty. • Berylium je tvrdé (rýpe do skla), ale křehké (za normální teploty) a poměrně těžce tavitelné. • Za červeného žáru je tažné. • Špatně vede elektrický proud a teplo. Stavba atomu Be

Použití • Minerály beryllia se využívají ve šperkařství jako drahokamy a polodrahokamy. Nejznámější a největší drahokamy berylu jsou usazeny v anglické koruně. smaragd • Mimořádně důležitou vlastností kovového berylia je jeho velmi vysoká propustnost pro rentgenové záření a nízkoenergetické neutrony. Proto je cenným materiálem především v jaderné energetice. • Speciální slitiny s mědí se používají na výrobu nejiskřivého ručního nářadí; kladiv ap. určených pro používání v provozech, ve kterých hrozí nebezpečí výbuchu. Zpět na přehled prvků

Hořčík Mg -je lehký, stříbrolesklý a středně těžký kov -je těžší než voda -vede hůře el. proud a teplo -je rozpustný ve všech běžných kyselinách -odolný vůči korozi

Využití n n n n -v pyrotechnice -výroba lehkých a pevných slitin -na letadla a automobily -jiskřivý efekt -zesílení intenzity ohně -v minulosti fotografování (místo blesku) dnes se využívá se při fotografování velkých prostor -ve zdravotnictví

Zpět na přehled prvků

VÁPNÍK Značka: Ca Latinský název: Calcium

Vlastnosti • Je to šedobílý, lesklý, měkký kov • Vodu bouřlivě rozkládá, vylučuje z ní vodík. • Není tolik reaktivní jako alkalické kovy, ale je lepší ho uchovávat pod petrolejem. • Bezbarvý plamen se vápníkem barví cihlově červeně. • Vápník má teplotu tání 845 °C, teplotu varu 1482 °C a byl objeven roku 1808. • Je to chemicky velmi aktivní prvek

Výskyt • Nejběžnější horninou na bázi vápníku je vápenec, uhličitan vápenatý Ca. CO 3 tvořený minerálem kalcitem nebo aragonitem stejného chemického složení. • Speciální typ představuje křída, téměř čistý měkký pórovitý vápenec s typicky zářivě bílou barvou, nacházející se například na pobřeží kanálu La Manche nebo na Rujáně. • Nejvíce ceněnou odrůdou vápence je mramor nebo travertin, používaný především k dekorativním účelům - obklady budov, sochy. Je obsažen též v mořské vodě. Vápník je důležitý biogenní prvek. Nejvíce je zastoupený v živočišných organismech. • křídové útesy anglického Doveru Krápníková jeskyně

Použití • Velká reaktivita kovového vápníku slouží v hutnictví k odstraňování malých množství síry a kyslíku z taveniny železa a při výrobě oceli. • Vápník se používá jako přísada při výrobě vápenatých skel nebo jako součást některých slitin - například olověný ložiskový kov, který se vyráběl v Německu. • K výrobě páleného a hašeného vápna. Vápenaté sloučeniny jsou lidstvu známy již od starověku - pálením vápence nebo mramoru se získávalo a dodnes získává pálené vápno neboli oxid vápenatý Ca. O, jeho reakcí s vodou vzniká hašené vápno neboli hydroxid vápenatý, který se používal a dodnes používá k přípravě malty. • Vápno je součástí při výrobě dnes patrně nejběžnějšího stavebního materiálu – cementu. Po smíšení s pískem a vodou vzniká pevná, tvrdá a odolná hmota – beton, s níž se setkáváme denně jako materiálem pro konstrukce moderních staveb a základním materiálem silnic, leteckých přistávacích drah, železničních pražců aj. • Uhličitan vápenatý se kromě stavebnictví používá také k výrobě křídy, jako nátěrová barva (tzv. křídová běloba), do zubních prášků, tmelů, v lékařství atd.

Zajímavosti • V přírodě je ve formě sloučenin značně rozšířen, například ve vápenci, dolomitu, sádrovci; je obsažen též v mořské vodě. Vápník je důležitý biogenní prvek. Nejvíce je zastoupený v živočišných organismech. • Tělo dospělého muže o hmotnosti 70 kg obsahuje okolo 1200 g vápníku, nejvíce v kostech (99 %). • Malé množství ionizovaného vápníku v tělesných tekutinách je důležité pro srážení krve, pro normální dráždivost srdce, svalů a nervů a propustnost membrán. • je nezbytný pro zdravý vývin a růst kostí a zubů. • (Hlavní zdroj vápníku v lidské potravě představuje mléko a mléčné výrobky. Kromě toho je vápník ve zvýšené míře přítomen ve většině listové zeleniny, semenech, ořeších, ovesných vločkách a řadě minerálních vod. Zpět na přehled prvků

Stroncium Sr Strontium Objeveno roku 1790

Vlastnosti • Poměrně měkký, lehký, reaktivní kov, který se svými vlastnostmi více podobá vlastnostem alkalických kovů. • V kapalném amoniaku se rozpouští za vzniku černého roztoku. Stroncium patří k lepším vodičům elektrického proudu a tepla. Není tolik reaktivní jako alkalické kovy, ale přesto je jeho reaktivita natolik vysoká, že může být dlouhodobě uchováváno pouze pod vrstvou petroleje nebo nafty, s nimiž nereaguje. Soli stroncia barví plamen červeně. • Stroncium reaguje za pokojové teploty s vodou i kyslíkem. Na vzduchu se okamžitě pokrývá vrstvou nažloutlého oxidu, práškové stroncium je na vzduchu schopno samovolného vznícení.

Využití • Sloučenin stroncia se využívá při výrobě pyrotechnických produktů pro jejich výraznou barevnou reakci v plameni. • sloučeniny stroncia ve speciálních aplikacích sklářského průmyslu, příkladem mohou být katodové trubice pro výrobu obrazovek barevných televizních přijímačů. • Vysokého indexu odrazivosti titaničitanu strontnatého Sr 2 Ti. O 3 se využívá v různých optických aplikacích, např. měření barevnosti látek nebo analýze spekter odražených paprsků z barevných povrchů. Ze stejného důvodu používá často šperkařský průmysl titaničitan strontnatý jako levnější náhradu diamantu. • Některých strontnatých solí, například dusičnanu strontnatého, se využívá v pyrotechnice k barvení plamene na červeno. Zpět na přehled prvků

Baryum Ba

Vlastnosti • Rozpustné soli barya jsou jedovaté. • Poměrně lehký, měkký, radioaktivní kov, tímto se spíše podobá alkalickým kovům. • Je velmi dobrý jako vodič tepla a elektrického proudu. • Je nejreaktivnější s alkalických zemin. • Baryum reaguje za pokojové teploty s vodou a kyslíkem. • Baryum je stříbrně bílý. • Plamen barví na zeleno.

Použití • Peroxid barnatý se používá k bělení hedvábí rostlinných vláken a slámy. • Další uplatnění sloučeniny barya ve speciálních aplikacích sklářského průmyslu. • Baryum je jako poměrně velký atom schopno značné absorpce rentgenova záření. Při rentgenovém snímkování trávícího traktu vypije pacient suspenzi síranu barnatého ve vodě a po několika desítkách minut je možno získat velmi kvalitní snímek pacientova žaludku a střev. Zpět na přehled prvků

Radium Ra

Vlastnosti • Mimořádně silný radioaktivní zářič. Jednotlivé izotopy radia vyzařují všechny druhy radioaktivního záření – paprsky alfa, beta i gama. • V čistém stavu je radium bílý, těžký, velmi reaktivní kov, který se velmi podobá vlastnostem alkalických kovů. • Je nejreaktivnější z kovů alkalických zemin a reaktivitou se velmi podobá alkalickým kovům. • Radium ve tmě poskytuje modré luminiscenční světlo. • Jeho reaktivita je natolik vysoká, že může být dlouhodobě uchováváno pouze pod vrstvou petroleje nebo nafty, s nimiž nereaguje. • Soli radia barví plamen sytě červeně.

Zajímavosti • Dnes není radium prakticky užíváno. • Radium bylo objeveno roku 1898 Marií Curie. Skłodowskou, jejím manželem Pierem a Gustavem Bémontem v jáchymovském smolinci U 3 O 8, který byl v té době pouze odpad při těžbě galenitu Pb. S. Z této rudy se jim podařilo po mnohaletém úsilí izolovat chlorid radnatý Ra. Cl 2. Na izolaci 1 gramu chloridu radnatého spotřebovali 10 tun (10 000 gramů) smolince. • Maria Curie-Skłodowska díky dlouhodobému styku s radioaktivními prvky (zejména s radiem) zamřela na anemii v roce 1934. Zpět na přehled prvků

Halogeny značka název F Fluor Cl Chlor Br Brom I Jod At Astat Zpět na přehled prvků

FLUOR F

Vlastnosti • extrémně jedovatý a toxický plyn, který leptá dokonce i sklo • v silné vrstvě je zelenožlutý s dráždivým zápachem • kapalný fluor má banánově žlutou barvu • plynný je extrémně reaktivní, ochotně až explozivně se slučuje již za studena s vodíkem, bromem, jodem, sírou, fosforem, arsenem, antimonem, borem, křemíkem a s mnoha kovy

Použití • Kyselina fluorovodíková HF, dodávána na trh často jako 40% roztok, leptá a rozpouští sklo a uplatňuje se proto ve sklářském průmyslu (leptání a matování skla). • Používá se na výrobu plastů např. - teflon, freonů (náplň chladniček, hnací plyn do sprejů). Freony ale poškozují ozonosféru – vznik ozonových děr. Molekuly freonů Výrobky z teflonu

Zajímavost • příjem fluoru je žádoucí především pro vývoj zdravých zubů. Zpět na přehled prvků

Chlor Cl

Vlastnosti • Chlor je velmi reaktivní plyn, má žlutozelenou barvu a štiplavý zápach. • Chlor je jedovatý, silně leptá sliznice. Jeho hustota je asi 2, 5 krát větší než hustota vzduchu. • Tvoří dvouatomové molekuly. • Byl objeven roku 1774 a až za 36 let byl pojmenován tak jak ho známe. • Je rozpustný ve vodě a ničí v ní bakterie. • Vyskytuje se v mořské vodě a ve vnitrozemských jezerech. • Obsažen v kuchyňské soli Na. Cl.

Využití • Pro dezinfekci pitné vody a vody v bazénech. • Chloristan draselný se používá jako palivo v raketových motorů. • Během 1. světové války němečtí vojáci zneužili chlor jako otravnou látku a při použití zemřelo 5000 fran. a britských vojáků. • V papírenském a textilním průmyslu se používá k bělení surovin. Krystaly Na. Cl Zpět na přehled prvků

BROM Značka: Br Latinský název: Bromum

Vlastnosti Brom je hnědočervená kapalina se silným zápachem. n Vypařuje se v těžké plyny. n S ostatními látkami reaguje prudce – tím vznikají bromidy. n Brom lze použít i jako katalyzátor. n

Výskyt Brom se vyskytuje v přírodě v podobě bromidu sodného a hořečnatého. n Vyskytuje se i v mořské vodě a solných pramenech. n

Využití V lékařství n V lázeňství – Jodobromové prameny např. : lázně Darkov. n Ve fotofilmu se nachází bromid stříbra (Ag. Br) n

Zajímavost Brom byl objeven roku 1826. n Objevitelem byl Francouz Palárd. n Látku nazval podle řeckého boha Bromose (bromos – zápach) n Zpět na přehled prvků

Jod I je prvek za skupiny halogenů, tvoří tmavě fialové destičkovité krystalky .

Vlastnosti Jód je velmi vzácný prvek, který se v přírodě vyskytuje pouze ve sloučeninách. Byl objeven roku 1811 francouzským chemikem Barnardem Courtoisem.

Použití Roztok jódu ve směsi alkohol-voda je nazýván jódová tinktura a slouží v medicíně jako dezinfekční činidlo Ve farmacii – součást některých léků Důležitý pro správnou činnost štítné žlázy (jodidovaná sůl)

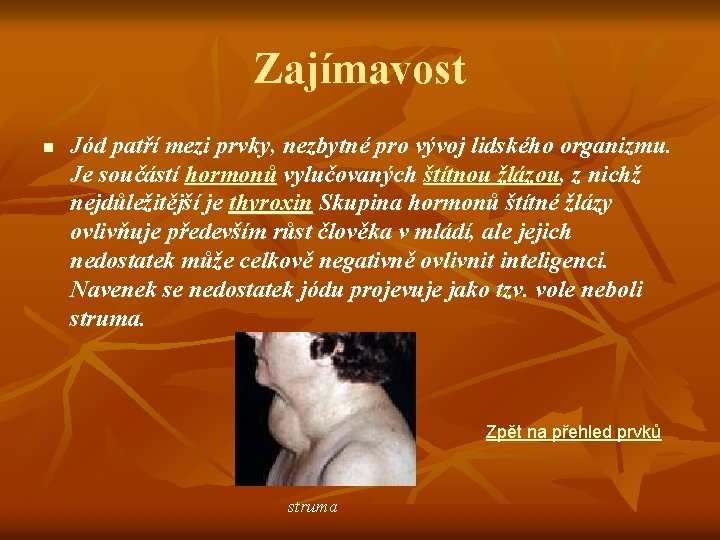
Zajímavost n Jód patří mezi prvky, nezbytné pro vývoj lidského organizmu. Je součástí hormonů vylučovaných štítnou žlázou, z nichž nejdůležitější je thyroxin Skupina hormonů štítné žlázy ovlivňuje především růst člověka v mládí, ale jejich nedostatek může celkově negativně ovlivnit inteligenci. Navenek se nedostatek jódu projevuje jako tzv. vole neboli struma. Zpět na přehled prvků struma

ASTAT At

Vlastnosti a zajímavosti l je nejtěžším známým prvkem ze skupiny halogenů, existuje pouze ve formě nestabilních radioaktivních izotopů. l Astat má 33 známých izotopů, všechny jsou radioaktivní. l Astat byl poprvé připraven v roce 1940 na University of California v Berkeley ostřelováním bismutu alfa částicemi. l Mnoho sloučenin astatu bylo připraveno a studováno v mikroskopickém množství, protože se velmi rychle rozpadají vlivem radioaktivity. Využití těchto sloučenin je hlavně pro teoretické studie, ale předpokládá se i možné využití v nukleární medicíně. Zpět na přehled prvků

Vzácné plyny značka název He Helium Ne Neon Ar Argon Kr Krypton Xe Xenon Rn Radon Zpět na přehled prvků

Helium He • • Druhá nejvíce zastoupená složka vesmírné hmoty. Na Zemi přítomno jen velmi vzácně. Vyskytuje se především ve všech svítících hvězdách. V zemské atmosféře se vyskytuje jen ve vyšších vrstvách a díky své mimořádně nízké hmotnosti postupně z atmosféry vyprchává do meziplanetárního prostoru. • Malý elektrický odpor, dobře vede elektrický proud. (využití při výrobě výbojek). • Helium září intenzivně žlutě.

Použití He • K plnění balónů a vzducholodí (nevýhoda - vysoká cena). • Směsí He, O 2 a N 2 se plní tlakové láhve s dýchací směsí pro potápění do velkých hloubek. Na rozdíl od dusíku totiž ani pod velkým tlakem nezpůsobuje tzv. hloubkové opojení, takže potápěč je schopen pracovat ve velkých hloubkách i přes 300 metrů. Zároveň omezuje vznik otravy kyslíkem a současně zmenšuje riziko kesonové nemoci, která vzniká při rychlém výstupu potápěče na hladinu uvolněním bublinek plynného dusíku v krvi s možností mechanického poškození různých tkání. Zpět na přehled prvků

Neon Ne • • Bezbarvý plyn, bez chuti a zápachu, nereaktivní. V 1 litru vody se při 20°C rozpustí 10, 4 ml neonu. Neon má velmi dobrou elektrickou vodivost. Má velmi malý elektrický odpor. Toho se využívá v osvětlovací technice. Neon má ve výbojkách šarlatovou barvu (modrou). Zpět na přehled prvků

Argon Ar • má malý elektrický odpor a vede velmi dobře elektrický proud. Díky tomu v uzavřených trubicích, kterými prochází elektrický proud, vznikají elektrické výboje. Toho se využívá v osvětlovací technice. • Argon září při větší koncentraci červeně, při nižších přechází přes fialovou a modrou až k bílé barvě. • Argon je hojně zastoupen v zemské atmosféře. Tvoří přibližně její 1 %. • Ve 100 litrech vzduchu je 934 ml argonu. • Získává se frakční destilací zkapalněného vzduchu.

Použití Ar • Inertních vlastností argonu se využívá při svařování kovů, kde tvoří ochrannou atmosféru kolem roztaveného kovu a zabraňuje vzniku sloučenin, které zhoršují mechanické vlastnosti sváru. • Argon se ve směsi s dusíkem používá jako ochranná atmosféra žárovek a jako prostředí pro uchovávání potravin. V této směsi se také používá k plnění sáčků (například brambůrek), které jsou takto ochráněny před zvlhnutím a před rozmačkáním. • Čistého argonu se používá ve výbojkách, elektrických obloucích a doutnavých trubicích, kde podle koncentrace dokáže vytvořit červenou, fialovou, modrou a bílou barvu. Zpět na přehled prvků

Krypton Kr • Tak jako Ar má nízký elektrický odpor a velmi dobrou vodivost elektrického proudu. • Využití v osvětlovací technice. Krypton má zelenavě až světle fialovou barvu, která zřeďováním kryptonu přechází až v bílou barvu. • Krypton nachází uplatnění hlavně v osvětlovací technice, kde se ho využívá k plnění kryptonových žárovek a některých zářivek. Zpět na přehled prvků

Xenon Xe • Má velmi malý elektrický odpor, a proto vede velmi dobře elektrický proud. Toho se využívá v osvětlovací technice. Xenon má fialovou barvu, ale ředěním xenonu ve výbojové trubici barva ztrácí na plnosti a při velkém zředění vydává xenon pouze bílé světlo • Xenon je přítomen v zemské atmosféře v koncentraci přibližně 5. 106 % • Ve 100 litrech vzduchu je obsaženo 0, 0087 ml xenonu. • Záření Xe působí baktericidně a xenonové výbojky nalézají využití pro dezinfekci. • Xenonové výbojky jsou schopné produkovat mimořádně intenzivní světelné záblesky o velmi krátkém trvání výboje. To umožňuje fotografovat a filmovat velmi rychlé děje (průlet vystřelené kulky překážkou, výbuchy apod. ). žárovka výbojka Zpět na přehled prvků

Radon Rn • Radon ve výbojce vydává jasně bílé světlo. • Izotopy Rn se používají někdy pro krátkodobé lokální ozařování vybraných tkání. • Radonová voda (voda obsahující rozpuštěný radon) se používá rovněž v balneologii, například v jáchymovských lázních. • Typická délka pobytu pacienta ve vaně s radonovou vodou je 20 minut. • Může v malých dávkách vyvěrat sám z podloží přímo v plynné podobě. Zpět na přehled prvků

Další kovy: značka název Ti Cr Fe Co Ni Cu Zn Ag Titan Chrom Železo Kobalt Nikl Měď Zinek Stříbro Au W Ir Pt Hg Pb Sn Al Zlato Wolfram Iridium Platina Rtuť Olovo Cín Hliník Zpět na přehled prvků

Titan Ti Vlastnosti: • velmi lehký a tvrdý kov • ocelový vzhled • odolný vnějším vlivům a vysokým teplotám • za běžné teploty nereaguje s kyselinami

Použití: • lehké a pevné slitiny titanu s Al, Mn, Zn na výrobu brýlí, jízdních kol, okapů, golfových holí, konstrukce letadel • k výrobě antikorozních ocelí • k výrově tělních (zubních, kloubních)implantátů, lodních šroubů, luxusních hodinek • k výrobě některých chirurgických nástrojů • v body piercingu


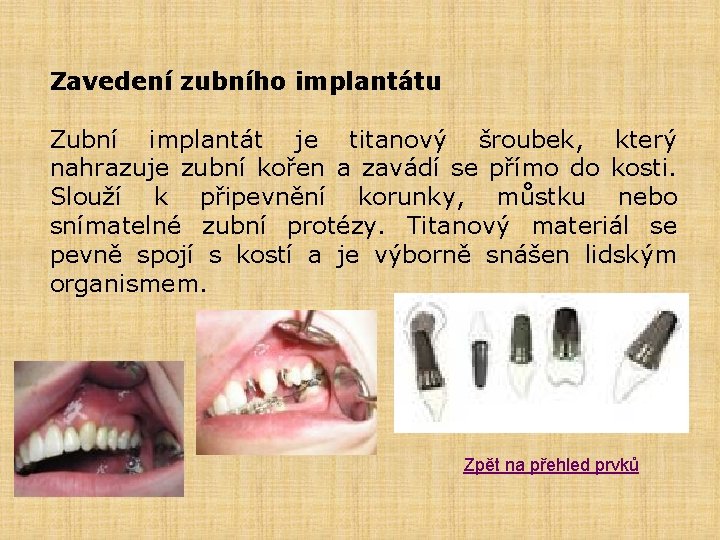
Zavedení zubního implantátu Zubní implantát je titanový šroubek, který nahrazuje zubní kořen a zavádí se přímo do kosti. Slouží k připevnění korunky, můstku nebo snímatelné zubní protézy. Titanový materiál se pevně spojí s kostí a je výborně snášen lidským organismem. Zpět na přehled prvků

CHROM Značka: Cr Latinský název: Chromium

Vlastnosti • Chrom je nejtvrdším elementárním kovem a vyznačuje se mimořádně nízkou reaktivitou a vysokou chemickou odolností. • Přes svoji značnou chemickou stálost se chrom pomalu rozpouští v neoxidujících kyselinách (kyselina chlorovodíková), zatímco kyseliny s oxidačním působením povrch kovu pasivují. Chrom se oxiduje při zahřívání v kyslíkovém plameni nebo s oxidačními činidly, jako jsou dusičnany nebo chlorečnany. Přímo se také slučuje s halogeny, se sírou, dusíkem, uhlíkem, křemíkem, borem a některými kovy, avšak teprve za žáru.

Použití • • • V každodenním životě se s chromem setkáme spíše jako s materiálem, chránícím kovové povrchy před korozí za současné zvýšení jejich estetického vzhledu. Klasickým příkladem je chromování chirurgických nástrojů i jiných zařízení používaných v medicíně (sterilizátory, zubařské nástroje a podobné předměty sloužící k vyšetření pacienta. V civilním životě nalezneme chromované předměty často ve vybavení koupelen, jako součást luxusních automobilových doplňků a v řadě dalších aplikací. Zpět na přehled prvků

Železo Fe (Ferrum) • • • Vlastnosti Výskyt Využití Historie Zajímavosti

Železo • Vlastnosti: • Výskyt • Je to druhý • Železo je poměrně nejrozšířenější kov na měkký, světle šedý až Zemi zastoupen i ve bílý kov s malou vesmíru odolností proti korozi.

Využití • při výrobě slitin a pro výrobu většiny základních technických prostředků používaných člověkem. • chirurgické nástroje, energetický průmysl, nářadí

Historie Zajímavosti • Lidstvu je znám již od • V organismu se podílí na pravěku. přenášení kyslíku k buňkám a tím umožňuje • Objev výroby a využití život mnoha organismů železa byl jedním ze na naší planetě základních momentů vzniku současné civilizace. • Galvanizace-je pokovení železa vrstvou zinku, • přesto však jeho různými ochrannými průmyslová výroba v nátěry laků, olejů a vrstev masovém měřítku začíná sloučenin oxidů. Je to teprve v 18. století našeho ochrana proti korozi. letopočtu

Využití a historie Zpět na přehled prvků

Kobalt (Co) lat. název Cobaltum

Vlastnosti n n n Je to lesklý, namodralý tvrdý feromagnetický kov. Rozpouští se ve zředěné kyselině chlorovodíkové a sírové za vývoje vodíku. Dobře se rozpouští ve zředěné kyselině dusičné.

Použití n Kobalt se používá při výrobě některých druhů ocelí a jako katalyzátor v chemickém průmyslu.

Zajímavosti n Jméno kobalt má základ v německém pojmenování skřítků Koboltů, kteří byly spíše zlomyslní a kazili horníkům práci

Vlastnosti • • Je stříbrobílý, feromagnetický, kujný a tažný kov Silně lesklý kov Je v pevném skupenství Ve zředěných minerálních kyselinách se nikl rozpouští • Má schopnost pohlcovat velké množství vodíku • Výskyt v zemské kůře Zpět na přehled prvků

Nikl Značka: Ni Latinský název: Niccolum

Použití • Antikorozní ochrana • Výroba chemického nádobí • Ocelářský průmysl • Je součástí velmi odolných slitin ( Monelův kov) • Patří mezi mincovní kovy • Slitinám niklu k výrobě šperků • Houbovitý nikl se využívá jako katalyzátor při hydrogenacích.

Zajímavosti • Při velkých nebo pravidelných dávkách niklu se zvyšuje riziko rakoviny. • Kožní alergie na nikl • Surovina pro elektrické články Zpět na přehled prvků

Měď , chemická značka: Cu je ušlechtilý kovový prvek načervenalé barvy, používaný člověkem již od starověku. Vyznačuje se velmi dobrou tepelnou a elektrickou vodivostí, dobře se mechanicky zpracovává a je odolný proti atmosférické korozi. Je základní součást Historického vývoje

• Měď, stejně jako stříbro a zlato, patří ke kovům známým od nejstarších dob. Měď sloužila v podobě bronzu již v prehistorických dobách ke zhotovování zbraní, různých předmětů a ozdob, podle výroby bronzu se nazývá i celé období - doba bronzová. O těchto třech kovech se dovídáme z Homérových spisů. Féničané měli na ostrově Kypr měděné doly, a proto Římané nazývali měď aes cyprium. Z tohoto výrazu se časem vyvinulo označení cuprum, čili česky měď.

• Měď je v zemské kůře přítomna poměrně vzácně. Odhaduje se, že její obsah činí 55 – 70 kg. V mořské vodě se její koncentrace pohybuje pouze na úrovni 0, 003 miligramů v jednom litru. Předpokládá se, že ve vesmíru připadá na jeden atom mědi přibližně 1 miliarda atomů vodíku.

využití slitin • Hlavním zdrojem pro průmyslovou výrobu mědi jsou sulfidické rudy, které jsou poměrně bohaté na železo, ale obsah mědi se v nich pohybuje kolem 1 %. Vytěžená ruda se proto nejprve drtí a koncentruje, čímž obsah mědi stoupne na 15 až 20 %

Čistý kov • 1. Čistá měď nalézá uplatnění pro svoji odolnost proti korozi, protože se na vzduchu působením atmosférické vlhkosti a oxidu uhličitého rychle pokryje tenkou vrstvičkou nazelenalého zásaditého uhličitanu měďnatého (měděnka), který ji účinně chrání proti další korozi. Používá se např. pro: střešní krytiny materiál pro výrobu odolných okapů a střešních doplňků trubic pro rozvody technických plynú

• 2. Vysoká elektrická vodivost elektrických vodičů jak pro průmyslové aplikace (elektromotory, při výrobě elektronických součástek, např. integrovaných obvodů

• 3. Vynikající tepelná vodivost mědi se uplatní při výrobě: • kotlů a zařízení pro rychlý a bezeztrátový přenos tepla chladičů např. v počítačích, automobilech a průmyslových zařízeních kuchyňského nádobí

Slitiny mědi • Bronz (Cu + Sn) • Mosaz (Cu + Zn) Zpět na přehled prvků

Zinek Zn

Vlastnosti a výskyt • Zinek je modrobílý kov, nekoroduje a je křehký • Zinek se nachází v zemské kůře

Využití • Zinek je antikorozní, a proto se využívá zejména do slitin a k pozinkování plechů Zpět na přehled prvků

Ag Argentum Objev: Starověk

Využití • Kovové stříbro: CD, DVD kvalitní zrcadla pamětní mince, medaile řetízky stříbrné kulky proti vlkodlakům • Slitina stříbra: v pájce dentální využití

Biologický význam • • • Ničí houby a plísně Zabíjí parazity Pomáhá regeneraci buněk V malých dávkách posiluje imunit. systém Pomáhá na ekzémy, vyrážky…


Zajímavost • Stříbro je základ rozvoje fotografií. • Ale dnes se používají digitální fotoaparáty Zpět na přehled prvků

Zlato Au

Vlastnosti žlutý, lesklý n drahý kov n kujný n má velkou hustotu n dobře vede elektrický proud a teplo n

Použití v zubním lékařstvím n ve šperkařství n v elektronice n ve sklářském průmyslu k barvení nebo zlacení skla n k pozlacování soch n mince, medaile n Zpět na přehled prvků

Hliník Al Latinsky Aluminium Protonové číslo je 13

Vlastnosti hliníku Neušlechtilý stříbřitě šedý, nestálý, kujný kov, elektricky velmi dobře vodivý a vyskytuje se v pevném skupenství. V přírodě se vyskytuje zejména ve formě sloučenin, nejznámější rudou je bauxit. Hliník je v čistém stavu velmi reaktivní, na vzduchu se však rychle pokryje tenkou vrstvičkou oxidu Al 2 O 3, která chrání kov před další oxidací.

Využití hliníku Kovový hliník nalézá uplatnění především díky své poměrně značné chemické odolnosti a nízké hmotnosti. Tenká hliníková fólie = alobal. Proto se z něj vyrábějí např. některé drobné mince, ale i běžné kuchyňské nádobí a příbory. Vzhledem k dobré elektrické vodivosti se kovového hliníku dříve často využívalo jako materiálu pro elektrické vodiče

Výskyt v přírodě Hliník je třetím nejvíce zastoupeným prvkem v zemské kůře. Díky velké reaktivitě hliníku se v přírodě setkáváme prakticky pouze s jeho sloučeninami.

Zdravotní rizika Poměrně diskutovaným problémem je riziko používání hliníkového nádobí a příborů při přípravě a konzumaci potravy.

Sloučeniny hliníku a jejich význam Nejvýznamnější sloučeninou hliníku je oxid hlinitý, Al 2 O 3. Tato látka se vyskytuje v řadě modifikací se zcela odlišnými fyzikálně chemickými vlastnostmi. Další sloučeniny jsou např. : Chlorid hlinitý, Fluorid hlinitý a Octan hlinitý (využívá se na otoky – podvrtnutý kotník).

Slitiny hliníku Nejdůležitější je však uplatnění hliníku ve formě slitin, z nichž bezesporu nejznámější je slitina s hořčíkem, mědí a manganem, známá jako dural. Tento materiál má oproti samotnému hliníku mnohem větší pevnost a tvrdost při zachování velmi malé měrné hmotnosti. Zároveň jsou i značně odolné vůči korozi. Používá se jako ideální materiál pro letecký a automobilový průmysl, ale setkáme se s ním při výrobě výtahů, jízdních kol, lehkých žebříků a podobných aplikacích.

Zpět na přehled prvků

Wolfram 1)chem. značka W 2) šedý až stříbřitě bílý kov 2) velmi těžký a mimořádně obtížně tavitelný kov 3) přidává se do slitin, v čisté formě vlákna do žárovek

Zajímavosti a využití l l objeven roku 1781 švédským chemikem Wilhelmem Scheelem Wolframové vlákno v žárovkách Do slitin (malé množství v oceli) Za 2. sv války do střeliva do tanků a děl tzv. penetračních projektily (kvůli své velké hustotě a odolnosti) Zpět na přehled prvků

Iridium Ir l l drahý kov šedivě bílé barvy objeveno roku 1804 Ušlechtilý, poměrně tvrdý i když křehký kov elektricky i tepelně středně dobře vodivý

Využití a zajímavosti l l Hlavní naleziště představuje Sibiř a jižní Afrika legováno do slitin s rhodiem a platinou Ve sklářském průmyslu jako materiál do speciálních pecí na tažení optických vláken automobilovém průmyslu se z iridia vyrábějí elektrody zapalovacích svíček s mimořádnou životností pro motory závodních automobilů a používá se i v katalyzátorech. Zpět na přehled prvků

Platina Pt

Vlastnosti • Platina je - nejtvrdší - velmi drahý - odolný kov Platina je odolná proti účinkům kyselin a proti plynům.

Platinové kovy • tvoří s dalšími pěti příbuznými kovy iridiem-Ir, osmiem-Os, paládiem –Pd, rhodiem-Rh a rutheniem-Ru skupinu tzv. platinových kovů. • Dobrou pevností v žáru se vyznačují hlavně některé slitiny platiny (s niklem a rhodiem)

Využití • používá se v elektrotechnickém průmyslu, chemickém průmyslu, ve výrobě skla, klenotnictví, hutnictví a v lékařství • Vzhledem ke svým mechanickým vlastnostem a chemické odolnosti jsou platina a především její slitiny s rhodiem a iridiem používány na výrobu odolného chemického nádobí pro rozklady vzorků tavením nebo spalováním za vysokých teplot. • Ve sklářském průmyslu je základním materiálem speciálních pecí na výrobu optických vláken. • Katalytických vlastností jemně rozptýlené kovové platiny se využívá i v autokatalyzátorech, které slouží k odstranění nežádoucích látek z výfukových plynů. Zpět na přehled prvků

Rtuť Hg Hydrargyrum

Vlastnosti • Rtuť je kapalný kovový prvek stříbrné barvy. Je těžká a dobře vede el. proud. Patří mezi přechodné prvky. • Slouží jako součást slitin (amalgámů) a jako náplň různých přístrojů (teploměr). • Rtuť je jediným kovem, který je za normálních podmínek kapalný.

Výskyt • V přírodě se rtuť vyskytuje poměrně vzácně i jako elementární prvek. • Hlavním minerálem a zdrojem pro výrobu je však sulfid rtuťnatý, Hg. S, česky rumělka neboli cinabarit. • Největší světová ložiska tohoto nerostu nacházejí ve Španělsku, Slovinsku, Itálii, USA a Rusku Rumělka-

Využití • Nejvýznamnější uplatnění v praxi má rtuť ve formě svých slitin s jinými kovy – amalgámy. • Ochotně je vytváří s Au, Ag, Cu, Zn, Cd, Na, naopak s železnými kovy jako jsou Fe, Ni a Co nevznikají vůbec. • V běžném životě se nejčastěji setkáme s amalgámy dentálními, používanými v zubním lékařství jako velmi odolná výplň zubu po odstranění zubního kazu. Zpět na přehled prvků

Olovo Pb Těžký toxický kov, který se vyskytuje v zemské kůře a v rudách zinku a stříbra.

Vlastnosti n n n Pevné skupenství Velmi nízký bod tání Je dobře kujné Odolný vůči korozi Měkký Pohlcuje gama záření a rentgenové záření

Použití n n n n Na el. akumulátory K zalévání skla ve středověku Dříve na vodovodní rozvody Do nádob k udržení kyseliny sírové (nereaguje s ní) K ochraně na rentgen. pracovištích Na výrobu lustrů, těžítek, váz Na výrobu střeliva (diabolky) Vánoční zvyklosti – odlévání olova vitráže Zpět na přehled prvků

Cín Stannum Sn • je kov, který je lidstvu znám již od středověku. • součást slitiny bronzu • jeho teplota tání je -7°C a teplota varu 59°C • vyskytuje se v zemské kůře • nízko tavitelný kov • už v bibli se vyskytuje pojem cín a cínové nádoby

Využití - v potravinářství ideální materiál pro styk s dlouhodobě uchovávanými potravinami. Protože cena samotného cínu je poměrně vysoká, je plech pro výrobu konzerv obvykle ze slitin železa a cínem v tenké vrstvě je pokrýván vnitřní povrch, který je v kontaktu s potravinami. -vysoká odolnost cínu proti korozi a jeho zdravotní nezávadnost. -obal – tenká cínová fólie = staniol Zpět na přehled prvků

Další nekovy: značka název C Uhlík N Dusík O Kyslík P Fosfor H Vodík S Síra Zpět na přehled prvků

Uhlík (C) Patří mezi nekovy a je v pevném skupenství!!!

Výskyt • Vyskytuje se v přírodě jako diamant a grafit (tuha), ve všech druzích uhlí, je obsažen také v ropě, zemním plynu a ve všech organických látkách.

Použití • • Koks se používá jako palivo při výrobě surového železa. Saze se používají jako pigment při výrobě pneumatik. Aktivní uhlí se využívá v cukrovarech nebo jako lék. Průmyslové diamanty se využívají především k osazování různých vrtných a řezných hlavic nástrojů, které pro svou činnost musí vykazovat mimořádnou tvrdost a odolnost. • Broušené diamanty – brilianty se uplatňují ve šperkařství • grafit k výrobě elektrod, používá se jako tuha do tužek a slouží také jako mazadlo ložisek

Zpět na přehled prvků

Dusík N lat. Nitrogenium

Vlastnosti Vlasnosti : plynná, bezbarvá, mírně zapáchající látka, bez chuti, není toxicky ani jinak nebezpečný, je tvořen dvouatomovými molekulami, které jsou spojeny velmi pevnou trojnou vazbou (trojná vazba má za následek nízkou reaktivitu), je to interní plyn, to znamená, že reaguje i s jinými chemickými sloučeninami pouze za vysokých teplot a tlaků. Za laboratorní teploty reaguje pouze s lithiem a plutoniem, ale při vysokých teplotách s většinou prvků ( kyslík okolo t 2500 C )

Použití Plynný dusík : využívá se v prostředí, kde je nebezpečí výbuchu, při výrobě integrovaných obvodů, nerezové oceli a používá se k plnění obalů výrobků, aby nedošlo k jejich zmačkání a zvlhčení – napřiklad sáčky s brambůrky, dále v hasících přístrojích. Kapalný dusík : využívá se k uchovávání tkání nebo spermií a vyjíček v lázni z kapalného dusíku Zpět na přehled prvků

KYSLÍK Lat. Oxygenium O

Vlastnosti • kyslík je velmi reaktivní plyn • nezbytný pro existenci života na naší planetě • slučování kyslíku s ostatními prvky se nazývá hoření. Jde prakticky vždy o exotermní reakci, která vede k uvolnění značného množství tepelné a světelné energie. Produkty hoření se nazývají oxidy

Výskyt • Na Zemi je kyslík velmi rozšířeným prvkem. • V atmosféře tvoří plynný kyslík 21 objemových %. • Voda oceánů, které pokrývají 2/3 zemského povrchu je hmotnostně složena z 90 % kyslíku. • V zemské kůře je kyslík majoritním prvkem, je přítomen téměř ve všech horninách. Jeho obsah je odhadován na 46 – 50 hmotnostních %. V hlubších vrstvách zemského tělesa zastoupení kyslíku klesá a předpokládá se, že v zemském jádře je přítomen pouze ve stopách. • Ve vesmíru je zastoupení kyslíku podstatně nižší. Na 1 000 atomů vodíku zde připadá pouze jeden atom kyslíku.

Použití kyslíku • • • Kyslík se praktiky výlučně vyrábí destilací zkapalněného vzduchu. Vyrobený kyslík se uchovává buď ve zkapalněném stavu ve speciálních Dewarových nádobách (viz obrázek) nebo plynný v ocelových tlakových lahvích (modrý pruh) V medicíně se čistý kyslík používá při operacích a traumatických stavech pro podporu pacientova dýchání. Směsi kyslíku nebo vzduchu s inertními plyny slouží potápěčům k potlačení kesonové nemoci při ponorech do velkých hloubek. Také vysokohorští horolezci a letci se v nutných případech uchylují k dýchání čistého kyslíku. I piloti stíhacích letadel jsou vybaveni směsmi stlačených plynů, jejichž základní složkou je kyslík. Američtí astronauti programu Apollo dýchali také atmosféru čistého kyslíku, což umožnilo snížit tlak v kabině zhruba na třetinu běžné hodnoty a tak odlehčit její hermetickou konstrukci. To se ale stalo osudným posádce Apolla 1, která ve vysoce hořlavé atmosféře uhořela. Při hoření směsi kyslíku s vodíkem lze dosáhnout teploty přes 3 000 °C. Proto se kyslíko-vodíkový plamen využívá k řezání oceli a tavení kovů s vysokým bodem tání, např. platinových kovů. Je potřebný při výrobě oceli. Kapalný kyslík většinou slouží jako okysličovadlo raketových motorů při letech kosmických lodí. Kyslík se používá jako jedna ze složek pro náplň některých typů palivových článků

OZON O 3 • Za normálních podmínek je to vysoce reaktivní plyn modré barvy a charakteristického zápachu s mimořádně silnými oxidačními účinky. • Při teplotě -112 °C kondenzuje na kapalný tmavě modrý ozon a při -193 °C se tvoří červenofialový pevný ozon.

Využití ozonu • V medicíně slouží ke sterilizaci nástrojů. • Baktericidní účinky ozonu slouží k desinfekci pitné vody namísto dříve hojně využívané dezinfekce vody plynným chlorem nebo chlornanem. • Silné oxidační účinky ozonu se velmi často využívají v papírenském průmyslu k bělení celulózy pro výrobu papíru.


Ozonová vrstva • Mimořádně významnou roli pro pozemský život hraje tzv. ozonová vrstva atmosféry, která chrání planetu před ultrafialovým slunečním zářením. Je to část stratosféry ve výšce 25 – 35 km nad zemským povrchem, v níž se nachází značně zvýšený poměr ozonu vůči běžnému dvouatomovému kyslíku. Ozonová díra nad Antarktidou Vznik ozonu z kyslíku při elektrickém výboji – blesku.

Přízemní ozon • Tento plyn je lidskému zdraví nebezpečný, působí dráždění a nemoci dýchacích cest, zvyšuje riziko astmatických záchvatů, podráždění očí a bolesti hlavy. Zpět na přehled prvků

VODÍK H Hydrogenium

VLASTNOSTI • bezbarvý, lehký plyn • bez chuti a zápachu • hořlavý, hoří namodralým plamenem, ale hoření nepodporuje • je 14, 38 krát lehčí než vzduch • vytváří sloučeniny se všemi prvky periodické tabulky s výjimkou vzácných plynů, zejména pak s uhlíkem, kyslíkem, sírou a dusíkem, které tvoří základní stavební jednotky života na Zemi.

POUŽITÍ • V poslední době se vodíku stále více využívá při výrobě amoniaku z prvků - dusíku a vodíku. • Hoření, neboli reakce kyslíku s vodíkem, je silně exotermní a lze při ní dosáhnout teplot přes 3 000 °C. Toho se běžně využívá při svařování nebo řezání kyslíkovodíkovým plamenem. • Vodík jako zdroj energie přestavuje pravděpodobně budoucnost energetiky i dopravy. Při spalování vodíku vzniká vedle značného energetického zisku pouze ekologicky naprosto nezávadná voda. • Automobilové motory na bázi spalování plynného vodíku jsou v současné době předmětem intenzivního výzkumu předních světových výrobců motorů. • Dříve se vodík využíval v letectví k plnění vzducholodí a balónů. Katastrofa vzducholodi Hindenburg v roce 1937, která shořela přistání s několika desítkami obětí, éru vodíkem plněných dopravních prostředků lehčích než vzduch definitivně ukončila.

IZOTOPY VODÍKU • Klasický atom vodíku H (někdy nazývaný protium), tvořený jedním protonem a jedním elektronem. Tento izotop je nejjednodušší atom ve vesmíru a tvoří jeho převažující část. • Atom s jádrem 2 H, který obsahuje v jádře jeden proton a jeden neutron se označuje jako deuterium. Někdy mu bývá přiřazována i chemická značka D, přestože se nejedná o jiný prvek. • Ve spojení s kyslíkem tvoří deuterium tzv. těžkou vodu, D 2 O. Tato sloučenina má významné využití v jaderném průmyslu. Je velmi účinným moderátorem, tedy látkou zpomalující rychlost neutronů. • Jako tritium (čti trícium) se označuje vodík 3 H, který má jádro složeno z jednoho protonu a 2 neutronů a bývá někdy označován chemickou značkou T. Tritium se též v některých případech používá pro výrobu svítících ručiček a indexů hodinek, které pak září celou noc bez ohledu na to, zda byly před tím vystaveny světlu.

Laboratorní příprava • V Kippově přístroji • Elektrolýzou vody • Reakcí kovu (Al) s kyselinou (HCl) Zpět na přehled prvků

Fosfor-P Nekovový prvek

Výskyt n n V přírodě pouze ve formě vázaných sloučenin. Elementální fosfor se vyskytuje ve třech alotropních modifikacích: bílý červený černý

Bílý n n n Vysoká reaktivita hoření. Je to měkká látka nažloutlé barvy. Lze krájet nožem. Je jedovatý a na vzduchu samovznětlivý. Ve tmě jeho páry fosforeskují. Je dobrý na výrobu leteckých pum.

Červený n n Vzniká zahříváním bílého na 250°C pod tlakem. Za působení normálního světla vznikne také ale daleko pomaleji. Je potřebný pro výrobu zápalek.

Černý n n Je velmi stálý. Ve slitinách značně zvyšuje tvrdost výsledku. Přidává se pro výrobu polovodičů Zpět na přehled prvků

SÍRA (S) Vlastnosti 1) 2) 3) 4) křehká pevné skupenství krystalická žlutá jednoklonná bezbarvá

SÍRA n n n VYUŽITÍ Výroba zápalek Dezinfekce Proti plísni a růstu hub Chemický průmysl

SÍRA n n n VÝSKYT Síra se vyskytuje ve volném stavu nebo vázaná (např. v sulfidech). Ložiska síry jsou v Povolží, Kazachstánu, USA, Polsku.

SÍRA n n ZAJÍMAVOSTI Síra se vyskytovala již v dávnověku. Ve starověké Číně ji používali jako jednu ze složek střelného prachu. Jako součást výbušnin a zábavní pyrotechniky se používá i dodnes, i když po vynálezu dynamitu její význam poklesl.

SÍRA Zpět na přehled prvků

Polokov: značka název Si Křemík Zpět na přehled prvků

Křemík Značka: Si Latinský název: Silicium Je polokovový prvek

Vlastnosti • • • Má vlastnosti polovodiče Je ve skupenství pevném Hnědá až černá barva Je odolný vůči většině minerálních látek Elementární křemík je ve vzduchu neomezeně stálý • V přírodě se s ním setkáváme pouze ve formě sloučenin

Výskyt • V čisté podobě se křemík v přírodě nevykytuje, setkáváme se pouze s jeho sloučeninami ( např. v oxidu křemičitém a v křemičitanech). • Je po kyslíku druhým nejvíce zastoupeným prvkem v zemské kůře, 26 -28% zemské kůry

Využití • • Hutnictví- k výrobě slitin K výrobě polovodičů K výrobě slunečních baterií Elektrické součástky

Zajímavosti • Surový křemík se vyrábí v elektrických pecích z přečištěného křemenného písku a koksu vysoce čistý křemík Zpět na přehled prvků

KONEC Zpět na úvodní stranu Zpět na přehled prvků