PERATURAN MENTERI KESEHATAN RI NOMOR 168MENKESPERII2005 TENTANG PREKURSOR












- Slides: 14

PERATURAN MENTERI KESEHATAN RI. NOMOR 168/MENKES/PER/II/2005 TENTANG PREKURSOR FARMASI

• Prekursor adalah zat atau bahan pemula atau bahan kimia tertentu yang dapat digunakan sebagai bahan baku/penolong untuk keperluan proses produksi industri farmasi • (Permenkes No. 168/Menkes/Per/II/2005) • tetapi bisa juga yang membantu proses pembentukan narkoba. perkusor ini bisa sebagai perantara terbentuknya zat lain, atau dapat bekerja sebagai zat asam dalam pementukan garam narkoba.

Pada Peraturan Menteri Kesehatan Nomor 168/Menkes/Per/II/2005 , Prekursor Farmasi terdapat 25 jenis , yaitu 1. 2. 3. 4. 5. 6. 7. 8. Anhidrida Asetat Asam Klorida Asam Sulfat Aseton Etil Eter Kalium Permanganat Metil Etil Keton Toluen Asam N-asetil antranilat dan garamnya 9. Efedrin dan garamnya 10. Ergometrin (INN) dan garamnya 11. Ergotamin (INN) dan garamnya 12. Isosafrol 13. Asam lisergat dan garamnya 14. 3, 4 - Metilen dioksi fenil -2 propanon 15. 1 -Fenil - 2 – propanon 16. Piperonal 17. Pseudo efedrina (INN) dan garamnya 18. Safrol 19. Norefedrin (lain-lain) 20. Asam antranilat 21. Dietil eter -Mutu Farmasi - Lain-lain 22. Asam fenil asetat dan garamnya 23. Piperidina dan gramnya 24. Asam sulfat; oleum -Asam sulfat dari Copper Smelter - Lain – lain

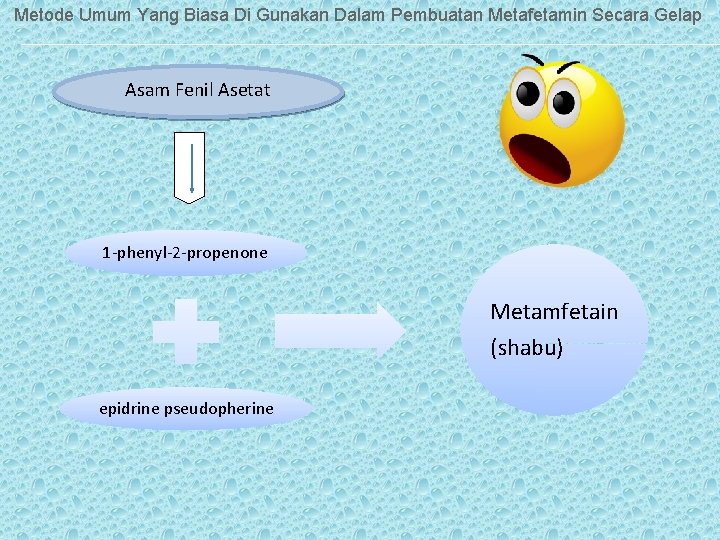
Metode Umum Yang Biasa Di Gunakan Dalam Pembuatan Metafetamin Secara Gelap Asam Fenil Asetat 1 -phenyl-2 -propenone Metamfetain (shabu) epidrine pseudopherine

Untuk Keamanan dan Menjaga dari Penyalahgunaan Prekursor, Pemerintah mengatur alur pendistribusian, tatacara penyimpanan, dan laporan segala kegiatan yang berhubungan dengan Prekursor Farmasi, dalam Permenkes RI. nomor 168/Menkes/Per/II/2005

• Penunjukan IP prekursor maupun IT Prekursor, di tetapkan oleh Direktur Jendral Pelayanan Kefarmasian dan Alat Kesehatan

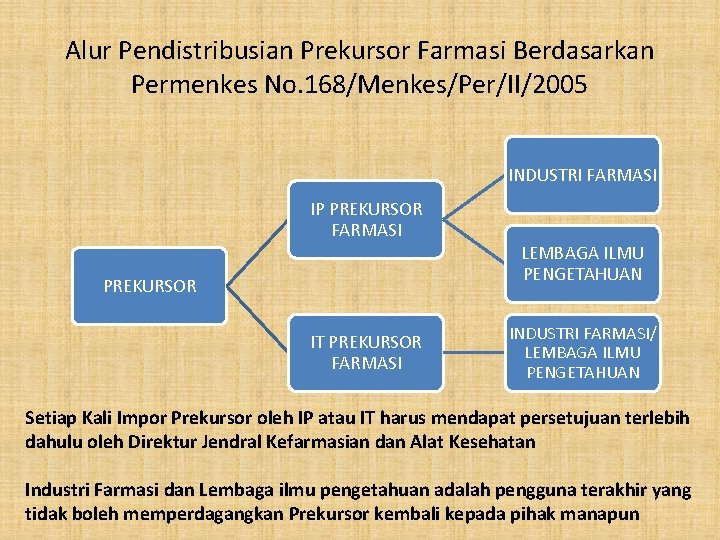
Alur Pendistribusian Prekursor Farmasi Berdasarkan Permenkes No. 168/Menkes/Per/II/2005 INDUSTRI FARMASI IP PREKURSOR FARMASI LEMBAGA ILMU PENGETAHUAN PREKURSOR IT PREKURSOR FARMASI INDUSTRI FARMASI/ LEMBAGA ILMU PENGETAHUAN Setiap Kali Impor Prekursor oleh IP atau IT harus mendapat persetujuan terlebih dahulu oleh Direktur Jendral Kefarmasian dan Alat Kesehatan Industri Farmasi dan Lembaga ilmu pengetahuan adalah pengguna terakhir yang tidak boleh memperdagangkan Prekursor kembali kepada pihak manapun

Persyaratan IP Prekursor a. b. c. d. e. f. Fotokopi Izin Usaha Industri Farmasi; Fotokopi Angka Pengenal Importir Produsen (API P); Fotokopi Tanda Daftar Perusahaan (TDP); Fotokopi Nomor Pokok Wajib Pajak (NPWP); Rencana produksi selama 1 (satu) tahun; Surat pernyataan dari penanggung jawab produksi yang menyatakan kebutuhan prekursor selama 1 (satu) tahun; dan g. Fotokopi SIK/SP Apoteker penanggung jawab produksi.

Persyaratan IT Prekursor a) b) c) d) e) f) Surat Izin Usaha Pedagang Besar Bahan Baku Farmasi; Fotokopi Surat Izin Usaha Perdagangan (SIUP); Fotokopi Angka Pengenal Importir Umum (API U); Fotokopi Tanda Daftar Perusahaan (TDP); Fotokopi Nomor Pokok Wajib Pajak (NPWP); Fotokopi Pemberitahuan Impor Barang (PIB) yang menunjukan pengalaman bidang impor prekursor dalam 3 (tiga) tahun; g) Surat pernyataan tidak keberatan impor prekursor dari apoteker penanggung jawab pedagang besar bahan baku farmasi; h) Rencana pendistribusian ke industri farmasi pengguna akhir; dan i. SIK atau SP Apoteker penanggung jawab pedagang besar bahan baku farmasi.

INGAT ! • Industri Farmasi yang menggunakan prekursor untuk memproduksi Narkotika dan Psikotoprika harus mendapat izin dari Menteri Kesehatan (pasal 20) • IP Prekursor dan IT Prekursor yang sudah di tunjuk WAJIB melaksanakan Pencatatan dan Pelaporan. Paling lambat tanggal 15 setiap bulannya (Pasal 23 dan 24)

Setiap Prekursor yang di edarkan harus diberi wadah atau kemasan diberi penandaan berupa tulisan “PREKURSOR”

Pelanggaran terhadap ketentuan dalam Permenkes ini akan dikenakan sanksi administratif yaitu a. Pencabutan penunjukan sebagai IP Prekursor Farmasi apabila: 1. Mengimpor prekursor yang jenis atau jumlahnya tidak sesuai dengan yang tercantum dalam dokumen penunjukan IP Prekursor Farmasi. 2. Memperdagangkan atau memindahtangankan prekursor yang diimpornya. 3. Tidak melaporkan realisasi impor dan penggunaannya sebanyak 2 (dua) kali dalam waktu 3 (tiga) bulan. 4. Terdapat cukup bukti melakukan pelanggaran atau dugaan tindak pidana yang berkaitan dengan penyalahgunaan penunjukan IP Prekursor Farmasi atau dinyatakan bersalah oleh pengadilan atas pelanggaran dan tindak pidana yang berkaitan dengan penyalahgunaan narkotika dan atau psikotropika yang memanfaatkan prekursor yang diimpornya.

LANJUTAN b. Pencabutan penunjukan sebagai IT Prekursor Farmasi, apabila: 1. 2. 3. Mengimpor prekursor yang jenis atau jumlahnya tidak sesuai dengan yang tercantum dalam dokumen persetujuan impor. Tidak melaporkan realisasi impor dan pendistribusiannya sebanyak 2 (dua) kali dalam waktu 3 (tiga) bulan. Terdapat cukup bukti melakukan pelanggaran atau dugaan tindak pidana yang berkaitan dengan penyalahgunaan penunjukan IT Prekursor Farmasi atau dinyatakan bersalah oleh pengadilan atas pelanggaran dan tindak pidana yang berkaitan dengan penyalahgunaan narkotika dan atau psikotropika yang memanfaatkan prekursor yang diimpornya.
