PENGOLAHAN LIMBAH INDUSTRI Oleh Abdul Rohim Tualeka LIMBAH

PENGOLAHAN LIMBAH INDUSTRI Oleh : Abdul Rohim Tualeka

LIMBAH INDUSTRI TERDIRI DARI : - LIMBAH CAIR (v) - LIMBAH GAS/PARTIKEL(v) - LIMBAH PADAT (x)

LIMBAH DI INDUSTRI A. LIMBAH CAIR a. LIMBAH KIMIA 1. LIMBAH KIMIA ANORGANIK Logam 2 Berat : Fe, Mn, Cr, Ca, dll. ) ( Non Logam : H 2 SO 4 ) 2. LIMBAH KIMIA ORGANIK Mengandung Lemak, protein, karbohidrat b. LIMBAH BIOLOGI B. Limbah partikel dan gas (SO 2, H 2 S, CH 4, NH 3, dll. )

A. PENGOLAHAN LIMBAH CAIR a. LIMBAH KIMIA 1. PENGOLAHAN LIMBAH CAIR KIMIA ANORGANIK DENGAN CARA : 1) OKSIDASI : Dengan AERASE, KLORIN, KMn. O 4) 2) PERTUKARAN ION

1) OKSIDASI Oksidasi Dengan aerase = Mengontakkan udara dg air limbah agar kandungan logam, misal Fe dan Mn yang ada dlm air limbah bereaksi dg O 2 yg ada di udara membentuk endapan senyawa besi dan Mangan. Untuk Limbah mengandung Fe : 4 Fe 2++ O 2 +10 H 2 O ==4 Fe(OH)3 (s)+8 H+ Untuk Limbah mengandung Mn : Mn 2+ + O 2 + H 2 O == Mn. O 2(s) + 2 H+

Ket : Aerasi efektif pd p. H 6, 5 – 8, 5. Pertanyaan : Setelah diteliti di Lab, ditemukan dalam IPAL PT. Y terdapat 5 kg Fe. Tentukan : Dengan menggunakan aerase, berapa volume O 2 dan volume udara yang dibutuhkan untuk mengendapkan 1 gr Fe, 5 kg Fe ( Dalam kondisi normal ( Vol 1 mol gas = 22, 4 L); Ar. Fe=56, Ar. O = 16 )

Jawaban : Untuk 1 gr Fe : 4 Fe 2++ O 2 +10 H 2 O== 4 Fe(OH)3 (s)+ 8 H+ Fe = 1/56 ( n = mol = gr/Ar ) n. O 2 = ¼ x 1/56 Vol. O 2 = ¼ x 1/56 x 22, 4 L = 0, 1 L Vol udara=100/20 x¼ x 1/56 x 22, 4 =0, 5 L Untuk 5 kg Fe ? Berapa biaya yang dibutuhkan untuk mengolah limbah 5 kg Fe ? ( diskusikan) n

OKSIDASI DG KLORIN (klorinasi) Fe 2++ Cl 2 +6 H 2 O== 2 Fe(OH)3 (s)+ 8 H+ +2 Cl. Ket : Klorin berupa gas. Disimpan dalam bentuk cair dalam tabung silinder dg P = 5 -10 atm. Untuk klorinasi dilarutkan dalam air dan dimasukkan dalam air limbah.

Oksidasi dg KMn. O 4 3 Fe 2++ KMn. O 4 +7 H 2 O== 3 Fe(OH)3 (s)+ Mn. O 2 + K+ + 5 H+ Pada prakteknya kebutuhan KMn. O 4 ternyata lebih sedikit dari kebutuhan yang dihitung berdasarkan stoikiometri karena terbentuk Mn. O 2 berlebih yang dapat berfungsi sebagai oksidator.

2)Pertukaran ion menggunakan ion zeolit (Z) = senyawa kompleks Natrium, Alumino, Silikat dan pasir hijau Contoh : Na 2 Z + Fe(HCO 3)2 == Fe. Z (s) + 2 Na(HCO 3) Na 2 Z + Mn(HCO 3)2 == Mn. Z(s) + 2 Na(HCO 3)

2. PENGOLAHAN LIMBAH CAIR KIMIA ORGANIK 1) KOAGULASI 2)DENGAN PROSES ADSORPSI 3) DENGAN PROSES BIOLOGI

1) KOAGULASI = Proses pembubuhan bahan kimia ke dalam air agar kotoran dalam air yang berupa bahan kimia padatan tersuspensi dapat menggumpal dan cepat mengendap. Biasa digunakan tawas : Al 2(SO 4)318 H 2 O Al 2(SO 4)3. 18 H 2 O+3 Ca(HCO 3)2==2 Al(OH)3(s)+3 Ca. SO 4+6 CO 2 (g)+ 18 H 2 O Al 2(SO 4)3. 18 H 2 O+3 Ca(OH)2 == 2 Al(OH)3 (s)+3 Ca. SO 4 +6 CO 2 Ket : Ca(HCO 3)2 dan Ca(OH)2 terkandung dalam air (g) + 18 H 2 O

Pengendapan kotoran terjadi karena pembentukan Al(OH)3 yang berupa partikel padat yg akan menarik partikel-partikel kotoran sehingga menggumpal bersama-sama, menjadi besar dan berat membentuk flok dan segera dapat mengendap.

Ion Al(OH)3 juga diperoleh dari hidrolisis Al 2(SO 4)3. Reaksinya sbb : Al 2(SO 4)318 H 2 O + H 2 O == [Al(OH)3]6. Al 3+ + 3 SO 42 - + 18 H+=
![Limbah cair organik mengandung koloid seperti lumpur, [S 2 O 2]n. x. OH- , Limbah cair organik mengandung koloid seperti lumpur, [S 2 O 2]n. x. OH- ,](http://slidetodoc.com/presentation_image_h/be0f7be8978e39f23180bb8a110e2527/image-15.jpg)
Limbah cair organik mengandung koloid seperti lumpur, [S 2 O 2]n. x. OH- , senyawa logam organik seperti Fe dan Mn dalam zat warna organik dan asam humus. Limbah-limbah tsb bermuatan negatif. Untuk mengendapkan limbah 2 tsb dibubuhkan koagulan yaitu Al 2(SO 4)3. n. H 2 O yang dalam air menjadi koloid [Al(OH)3]n. x. Al 3+ yang bermuatan positif. Koloid bermuatan positif ini akan menarik koloid bermuatan negatif dan menggumpal menjadi gumpalan yang besar membentuk flok sehingga dapat mengendapkan dapat dipisahkan lewat saringan.

Cara pembubuhan tawas : Sejumlah tawas dilarutkan dalam air kemudian dimasukkan ke dalam air limbah lalu diaduk dengan cepat hingga merata selama kurang lebih 2 menit. Setelah itu kecepatan pengadukan dikurangi sedemikian rupa sehingga terbentuk gumpalan-gumpalan kotoran yang disebut flok.

2) PROSES ADSORPSI : KEMAMPUAN MENEMPEL SUATU ZAT PD PERMUKAAN. SORBAT : BAGIAN YG MENEMPEL ADSORBEN : BAGIAN TEMPAT MENEMPEL CONTOH ADSORBEN : ARANG AKTIF

ADSORPSI DIPENGARUHI OLEH : PERMUKAA SUATU ZAT SERTA LUAS AREANYA. KARBON AKTIF MEMILIKI LUAS PERMUKAANH 200 m 2/g SHG AKTIF MENYERAP ADSORBAT DLM JUMLAH BESAR

PROSES ADSORPSI : 1. MOLEKUL 2 ADSORBAT DIPINDAHKAN DARI BAGIAN TERBESAR LARUTAN KE PERMUKAAN ANTARA 2. MOLEKUL 2 ADSORBAT DIPINDAHKAN DR PERMUKAAN ANTARA KE PERMUKAAN LUAR ADSORBEN 3. MOLEKUL 2 ADSORBAT DIPINDAHKAN KE PERMUKAAN LUAR DARIO ADSORBEN MENYEBAR MENUJU PORI-PORI ADSORBEN 4. MOLEKUL 2 ADSORBEN MENEMPEL PADAPERMUKAAN MOLEKUL PORI-PORI ADSORBEN.

HUBUNGAN MATEMATIS YG MENGGAMBARKAN PROSES DIATAS DIGAMBARKAN OLEH FRUENDLICH DIKENAL De. ENGAN (ISOTERM FREUNDLICH, 1916 ): ISOTERM INI DIKEMBANGKAN DG ASUMSI : 1) ENERGI YG TERLIBAT DLM PROSES ADSORPSI TDK SELALU SAMA 2)TDK SELURUH PERMKUKAAN MEDIA TERLIBAT DLM PROSES ADSORPSI 3) ENERGI DLM PERMUKAANH MEDIA ADALAH HETEROGEN

PERSAMAAN ISOTERM FREUNDLICH x/m = kf. C 1/n Ket : x = massa zat terlarut yang diadsorpsi (mg) m= massa adsorben ( mg) C = konsentrasi zat terlarut yg tertinggal pd titik kesetimbangan (mg/L) kf dan n = konstanta

PERTANYAAN : Hasil tes lab dengan menggunakan karbon aktif serbuk : Perc. Ke : Dosis (K(mg/L) [C]o mg/L [C]1 mg/L (m) (kons. awal) (kons. akhir) I II III 12 7 ? 20 12 15 5 2 3 a. Tentukan persamaan Isoterm Freundlich b. Tentukan dosis KA yang diperlukan untuk mereduksi [C]o 15 mg/L menjadi 3 mg/L

Jawaban : x/m=k. c 1/n Perc (1) : 15/12 = kf. 51/n (2) : 10/7 = kf. 21/n Perc (1) : 15/12 k. 51/n ---- = ----10/7 k. 21/n n = -7, 25 Substitusi ke perc (1): k = 1, 5625 Substitusi ke perc (3): m = 8, 9 a. Pers. Isoterm Freundlich: x/m = 1, 5625 C -1/7, 25 b. m = 8, 9 mg/L

3) PROSES BIOLOGI a) PENGOLAHAN CARA AEROB Bakteri Aerob Bahan Organik + MO + O 2 H 2 O + CO 2 Pada proses ini : terdapat pd sebuah kolam berbentuk segi empat, agak dangkal agar sinar matahari sampai di dasar kolam. i) PROSES KOLAM OKSIDASI Faktor 2 yg berpengaruh : a. Dalam kolam : 1 – 1, 5 m b. Kondisi limbah : hrs disaring terlebih dahulu, p. H 6, 5 – 8, 5. c. Ikilim : saat kemarau baik, saat hujan tidak baik krn terjadi kondisi anaerob.

ii) PROSES LUMPUR AKTIF Baik karena mengandung zat pengurai shg sangat baik untuk mengolah bahan organik Untuk proses pengolahan perlu dipertimbangkan : a. Setiap meter kubik limbah air dibutuhkan udara 8 m 3 b. Air limbah dlm tangki aerasi tidak lebih 8 jam Keuntungan lumpur aktif : tidak menimbulkan bau dan air olahan cukup baik
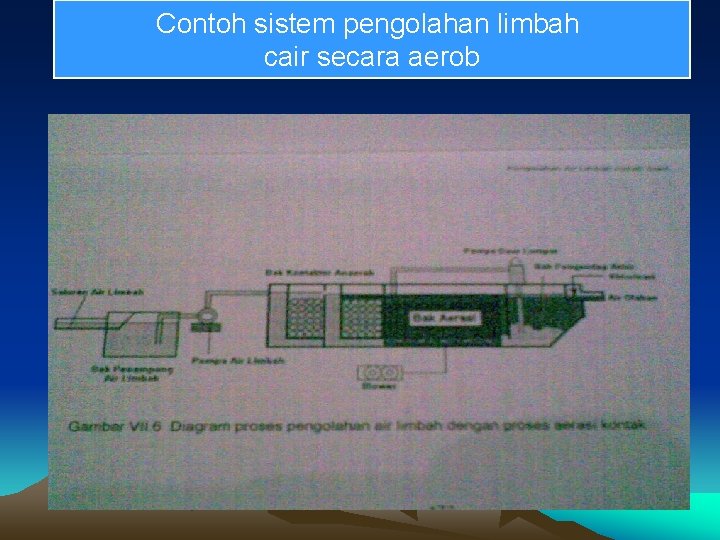
Contoh sistem pengolahan limbah cair secara aerob .

b) PENGOLAHAN CARA ANAEROB Bakteri anaerob Bahan organik CH 4 + CO 2 Bekerja efisien pd suhu rendah 10 -30 o. C, biaya operasi rendah, cocok untuk proses industri dg BOD tinggi dan padatan organik berjumlah besar. Keuntungan : Penggunaan energi sedikit, memproduksi gas yg dapat dimanfaatkan, lumpur yg dihasilkan sedikit, bau tidak timbul.

Contoh Sistem Pengolahan Limbah cair secara anaerob .

b. LIMBAH BIOLOGIS ( MIKROORGANISME) CONTOH LIMBAH BIOLOGI ( BAKTERI E. COLI, VIRUS, DLL. ) BAHAN-BAHAN YANG DIGUNAKAN : KLORIN (Cl 2, KAPORIT ATAU Ca(OCl)2, OZON, SINAR UV, Na. OCl. BEBERAPA HAL YG PERLU DIPERHATIKAN DALAM MEMILIH BAHAN KIMIA ADALAH : a. daya racun bahan kimia b. waktu kontak yg diperlukan c. efektifitasnya d. rendahnya dosis e. tidak toksik terhadap hewan dan manusia f. Tetap tahan terhadap air g. biaya yang murah untuk pemakaian yang massal

DALAM PERTIMBANGAN TSB DIGUNAKAN : Klorin, O 3, UV. a) klorin berupa gas : Cl 2 + H 2 O ----- HOCl + H+ + Clb) Klorin oksida ( kaporit ) Ca(OCl)2 ----- Ca 2+ + 2 OCl. OCl- + H+ ----- HOCl Ket : HOCl, OCl- : Free Available Chlorin Klor Bebas ) Dengan daya bunuh HOCl 40 – 80 X > OCl-

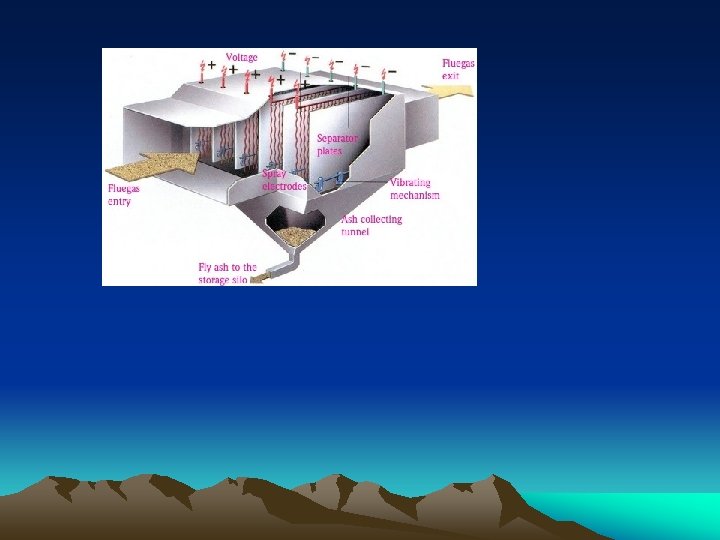
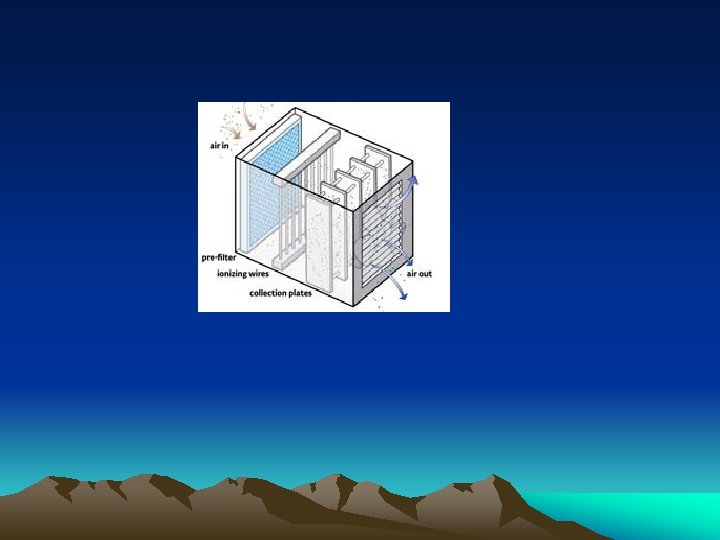
B. PENGOLAHAN LIMBAH PARTIKEL DAN GAS 1. Limbah Partikel Alat : presipitator elektrostatik Cara Kerja : partikel dilewatkan pada bagian yg mempunyai potensial elektrostatik tinggi shg bermuatan. Partikel tsb kemudian akan tertarik ke bagian lain yg muatannya berlawanan.
PRESIPITATOR .
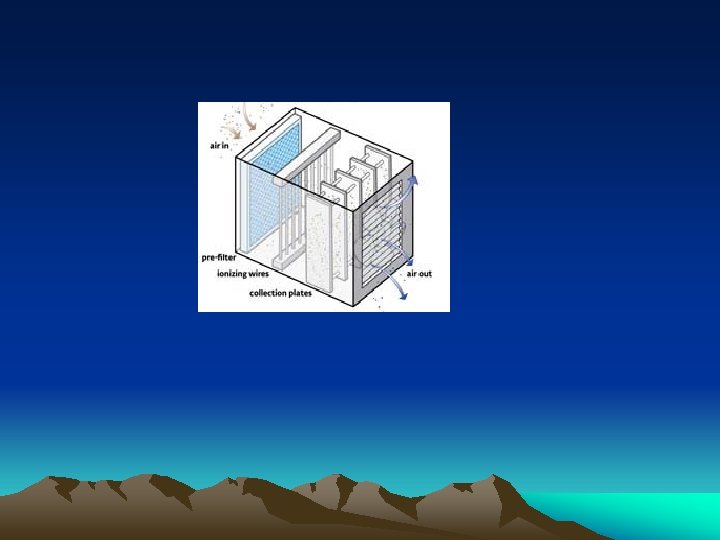

Bagaimana mereka bekerja Muatan listrik diterapkan pada partikel tertarik ke perangkat. Kemudian partikel ditangkap di piring malah dibebankan. Kelebihan: Mereka memiliki biaya operasi yang relatif rendah. Beberapa melakukan tugasnya dengan baik untuk menghilangkan debu, serbuk sari, dan asap. Cons: Sebagian besar ozon membuat beberapa. Model dengan fans kecil atau tidak ada penggemar tidak efektif untuk menghilangkan debu dan asap. Mereka yang memiliki kipas angin dapat berisik pada kecepatan tinggi. Pelat koleksi perlu dibersihkan sering, jadi ada perawatan lebih diperlukan daripada dengan filter berbasis unit.





2. limbah Gas a. Scrubber (alat untuk membersihkan gas yg mudah bereaksi dg air ) Prinsif kerja alat : Mencampurkan air dg uap/gas dalam satu kolam. Pada umumnya arah aliran berlawanan agar kontak uap/ gas dg air dapat sempurna.
SCRUBBER .
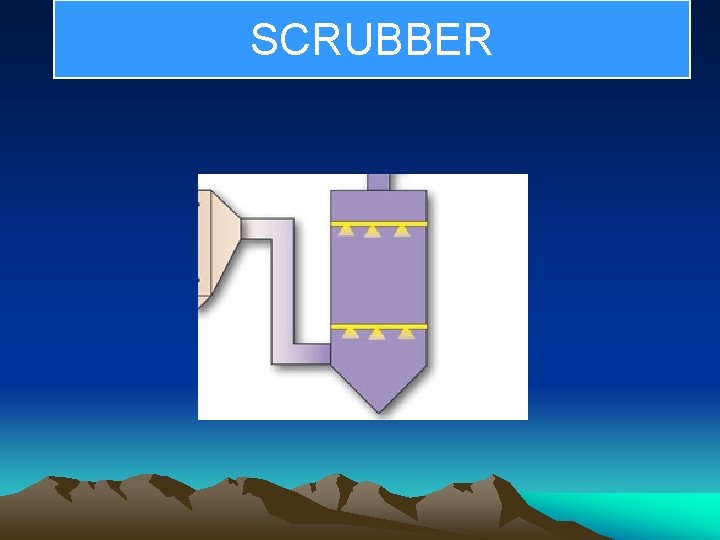
SCRUBBER .

SCRUBBER .

SCRUBBER Setelah dedusting biasanya scrubber digunakan untuk menghilangkan gas asam seperti HCl dan SO 2. Dua proses scrubbing digunakan, basah scrubber dan (kuasi-) scrubber kering. Dalam scrubber basah gas buang disemprot dengan campuran cair dari air dan kapur. Polutan gas asam bereaksi dengan cairan untuk membentuk gipsum yang dapat dihapus dari air limbah untuk menghasilkan drywalls. Menggunakan proses scrubbing kering solusi air diganti dengan bubuk kapur atau campuran bubur air dan kapur. Untuk kontrol operasi yang tepat dari pemantauan proses kering terus menerus HCl, SO 2 dan konsentrasi H 2 O sangat penting. Solusi kami: .

Cara kerja Scrubber dg menara penyemprot Gas kotor masuk dari bagian dasar akibat tekanan. Gas membumbung ke atas sementara dari atas dimasukkan pipa air yg dilengkapi dg sprayer ( penyemprot ) shg air keluar merupakan titik 2 air memenuhi menara. Karena gaya berat, titik air turun sementara gas naik bersama udara. Gas yang terkandung dlm udara bereaksi dg air dan turun kebawah lalu ditampung dan dialirkan ke tempat tertentu.

b. Adsorpsi ( menyerap gas dengan menempelkan gas pada permukaan ), ada 2 macam : (1) Adsorpsi fisik atau Van der Waals - Panas adsorpsi rendah ( sekitar 10. 000 kal/mole ) - Kesetimbangan adsorpsi reversibel dan cepat Misal : adsorpsi gas pada arang aktif (2) Adsorpsi kimia atau adsorpsi aktivasi -Panas adsorpsi tinggi (20. 000 -100. 000 kal/mole) -Adsorpsi terjadi dengan pembentukan senyawa kimia, hingga ikatannya lebih kuat. Contoh : adsorpsi CO pada W, O 2 pada Ag, Au, Pt, C H 2 pada Ni
- Slides: 47