PENGOLAHAN LIMBAH CAIR SECARA FISIK dan KIMIA PENGENDAPAN

PENGOLAHAN LIMBAH CAIR SECARA FISIK dan KIMIA,
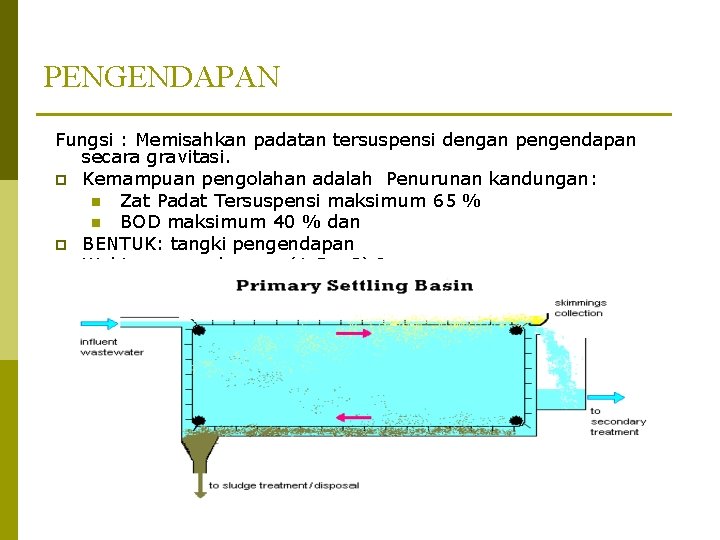
PENGENDAPAN Fungsi : Memisahkan padatan tersuspensi dengan pengendapan secara gravitasi. p Kemampuan pengolahan adalah Penurunan kandungan: n Zat Padat Tersuspensi maksimum 65 % n BOD maksimum 40 % dan p BENTUK: tangki pengendapan p Waktu pengendapan : (1, 5 – 3) Jam.
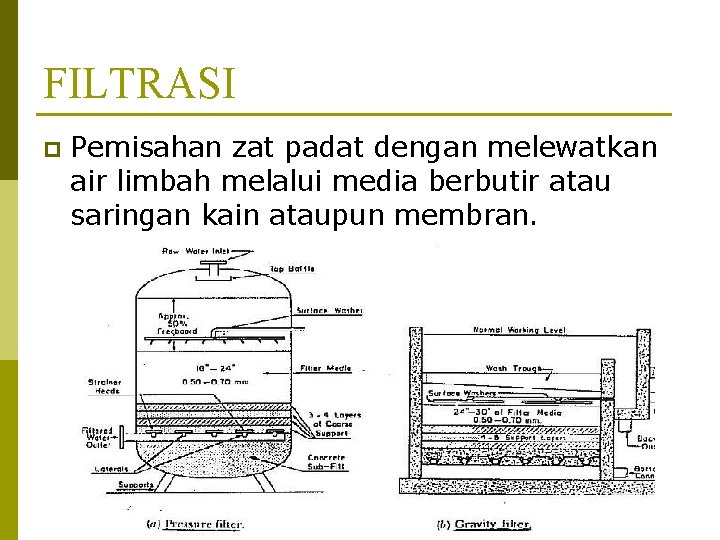
FILTRASI p Pemisahan zat padat dengan melewatkan air limbah melalui media berbutir atau saringan kain ataupun membran.
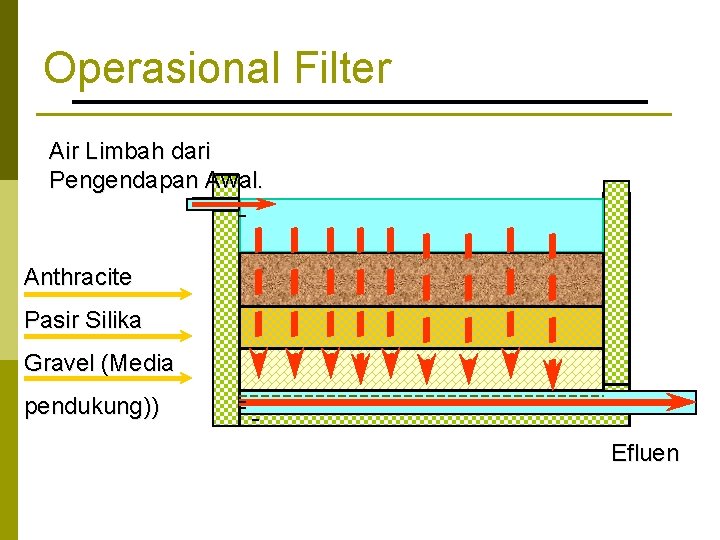
Operasional Filter Air Limbah dari Pengendapan Awal. Anthracite Pasir Silika Gravel (Media pendukung)) Efluen
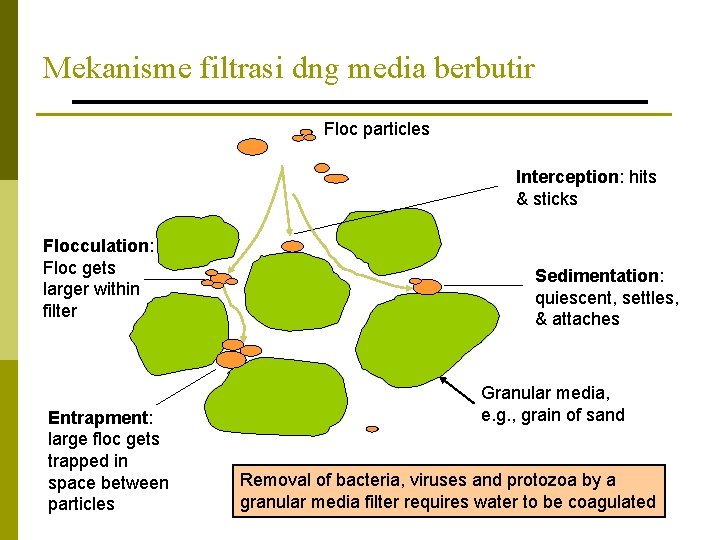
Mekanisme filtrasi dng media berbutir Floc particles Interception: hits & sticks Flocculation: Floc gets larger within filter Entrapment: large floc gets trapped in space between particles Sedimentation: quiescent, settles, & attaches Granular media, e. g. , grain of sand Removal of bacteria, viruses and protozoa by a granular media filter requires water to be coagulated

PENGOLAHAN SECARA KIMIA Netralisasi : penambahan kimia berupa zat asam ataupun basa terhadap air limbah yang bersifat asam maupun basa, sampai p. H berkisar 7, 0 p Bahan Kimia yang diperlukan : p n n Asam : H 2 SO 4, HCl, HNO 3 Basa : Ca(OH)2, Na. OH

Koagulasi Kimiawi p Tujuan n n p Mengikat dan menyisihkan senyawa organik dan anorganik serta partikel – partikel koloid berukuran halus. Penambahan koagulan : Kapur, Tawas. Garam Besi, dan polimer untuk merubah muatan ion. Aplikasi n n n Penambahan koagulan dng disertai pengadukan cepat Dilanjutkan dengan mekanisme pengadukan lambat (flokulasi) agar terbentuk gumpalan yang besar, Hasil koagulasi – flokulasi dipisahkan dengan proses pengendapan dan atau filtrasi

Continued … Chemical Coagulation Lime+ Heavy metals SS removal Polymer +- SS control Alum+ Aluminum sulfate Iron+ Ferric chloride Ferric sulfate Ferrous sulfate SS removal P removal Mekanisme: – Destabilisasi dengan netralisasi muatan ion – Reduksi muatan yang mengikat bagian pertikel – partikel halus. + + + _ _ _ + + + +++ + _ _ + + + + + _ _ _ + + +_ _ ++ _ _ _ _ _
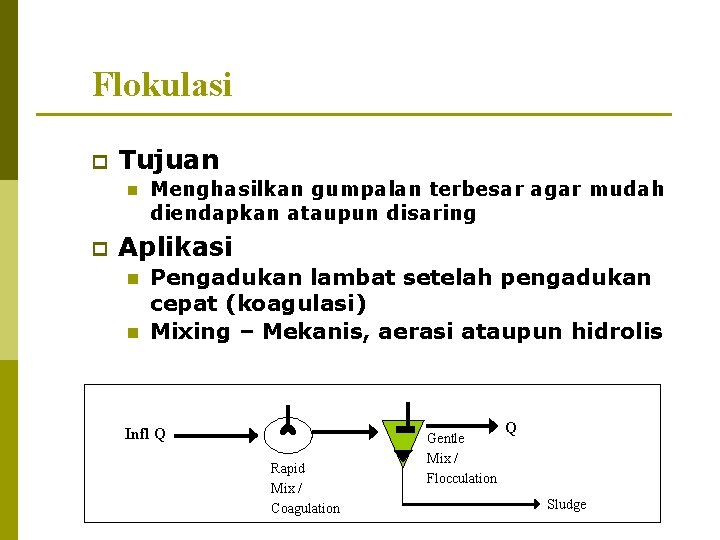
Flokulasi p Tujuan n p Menghasilkan gumpalan terbesar agar mudah diendapkan ataupun disaring Aplikasi n n Pengadukan lambat setelah pengadukan cepat (koagulasi) Mixing – Mekanis, aerasi ataupun hidrolis Infl Q Rapid Mix / Coagulation Gentle Mix / Flocculation Q Sludge
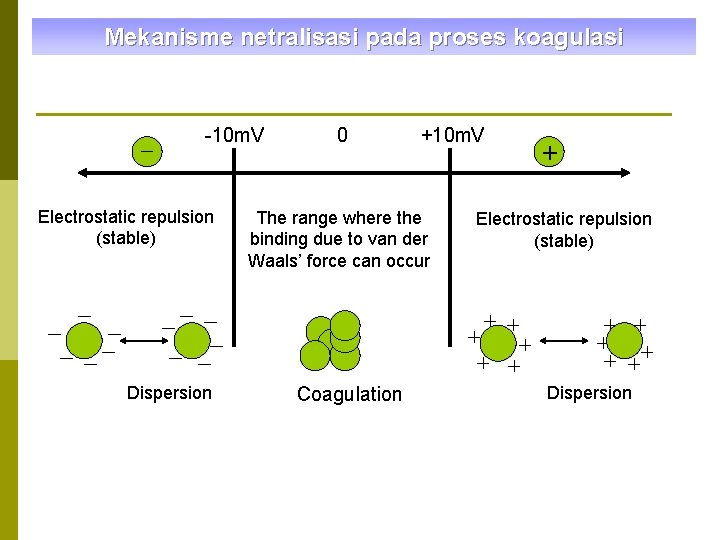
Mekanisme netralisasi pada proses koagulasi -10 m. V Electrostatic repulsion (stable) 0 +10 m. V The range where the binding due to van der Waals’ force can occur Electrostatic repulsion (stable) + + + Dispersion Coagulation + + + + Dispersion
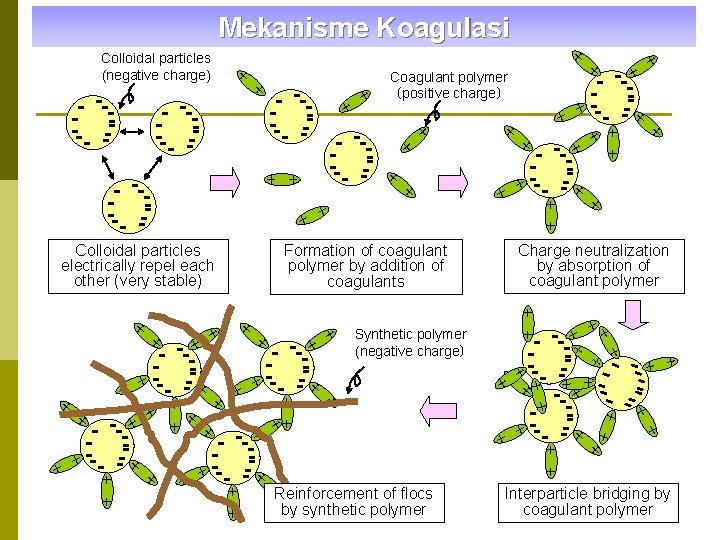
Mekanisme Koagulasi + + Coagulant polymer (positive charge) + + + + + Reinforcement of flocs by synthetic polymer + + + + ++ + + + + Synthetic polymer (negative charge) + + + + Charge neutralization by absorption of coagulant polymer + + + + Formation of coagulant polymer by addition of coagulants + + + + + + Colloidal particles electrically repel each other (very stable) + + + Colloidal particles (negative charge) + Interparticle bridging by coagulant polymer
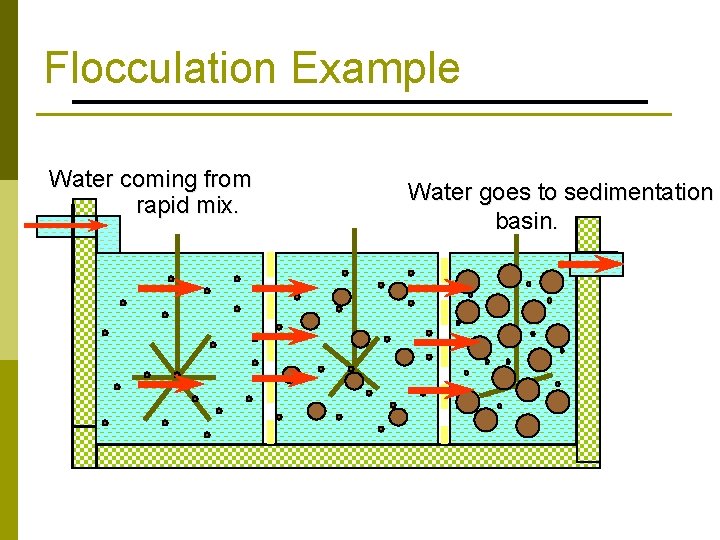
Flocculation Example Water coming from rapid mix. Water goes to sedimentation basin.

PENGOLAHAN AIR LIMBAH MENGANDUNG LOGAM BERAT

Kandungan logam berat dalam air limbah Cadmium (Cd), p Chrom (Cr), p Timbal (Pb), p Seng (Zn), p Nikel (Ni), p Tembaga (Cu), p Cyanida (CN). p dll p

BAHAN PENCEMAR INI UMUMNYA BERSIFAT RACUN BAGI MIKROORGANISME DAN MAKHLUK HIDUP. ” p Kriteria kualitas air buangan industri yang dibuang ke badan air permukaan tidak boleh memberikan gangguan pada ekosistim biota air yang ada didalamnya p

p Menurut (U. S. EPA 1986) batasan maksimum konsentrasi logam berat BERDAMPAK akut dan kronis pada ekosistim : n n badan sungai-danau sebesar 0, 012 – 1, 00 g/l air laut sebesar 0, 025 – 560 g/l.
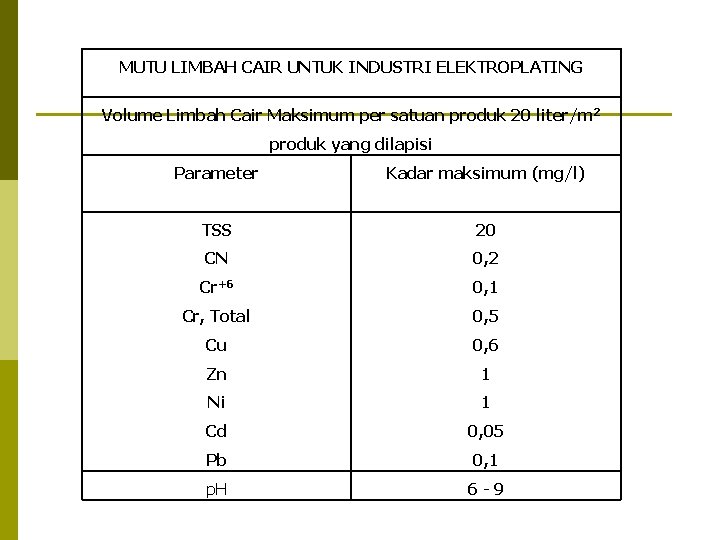
MUTU LIMBAH CAIR UNTUK INDUSTRI ELEKTROPLATING Volume Limbah Cair Maksimum per satuan produk 20 liter/m 2 produk yang dilapisi Parameter Kadar maksimum (mg/l) TSS 20 CN 0, 2 Cr+6 0, 1 Cr, Total 0, 5 Cu 0, 6 Zn 1 Ni 1 Cd 0, 05 Pb 0, 1 p. H 6 -9

PRINSIP PENURUNAN LOGAM BERAT DALAM AIR LIMBAH 1. 2. p PRESIPITASI – PENGENDAPAN – PENYARINGAN PRESIPITAS I– PENGENDAPAN – PENYERAPAN/ PERTUKARAN ION. PRESIPITASI KIMIA n n “PRESIPITASI KIMIA ADALAH SUATU PROSEDUR STANDAR UNTUK MENYISIHKAN/MENURUNKAN LOGAM BERAT DARI AIR DAN AIR LIMBAH. ” PRESIPITAT ADALAH BUTIRAN HALUS HASIL PROSES PENGIKATAN SECARA KIMIA ATAU KOAGULASI AKIBAT REAKSI KIMIA.

� EFISIENSI PENGOLAHAN DENGAN PRESIPITASI TERGANTUNG PADA DUA FAKTOR: �KELARUTAN TEORITIS �PEMISAHAN PADATAN DARI LARUTAN YANG MEMBAWANYA. � EFISIENSI PRESIPITASI DAPAT DIBANTU DENGAN BAHAN KOPRESIPITASI. � “BAHAN KIMIA KOPRESIPITASI BERFUNGSI MENYERAP, MENGGUMPALKAN. ” � BAHAN KIMIA BERSIFAT KOPRESIPITASI ADALAH ALUMINIUM HIDROKSIDA (AL(OH)3 DAN FERI HIDROKSIDA FE(OH)3. � BAHAN KIMIA PEMBENTUK PRESIPITAT : KAPUR (Ca. O) ATAU SODA API (Na. OH).
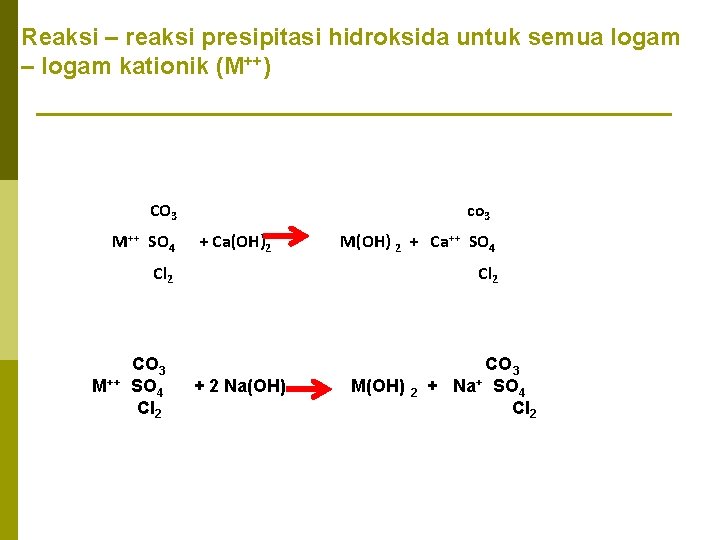
Reaksi – reaksi presipitasi hidroksida untuk semua logam – logam kationik (M++) CO 3 M++ SO 4 co 3 + Ca(OH)2 M(OH) 2 + Ca++ SO 4 Cl 2 M++ CO 3 SO 4 Cl 2 + 2 Na(OH) M(OH) 2 CO 3 + Na+ SO 4 Cl 2

p Kelebihan Kapur dari Sodium : n n garam – garam kapur bersifat mengendap dan dapat bertindak sebagai Ko-presipitat. mudah didapatkan dipasaran Kerugian pemakaian kapur : Jumlah lumpur lebih besar. p Logam berat dapat pula dipresipitasi sebagai Sulfida dan karbonat. p
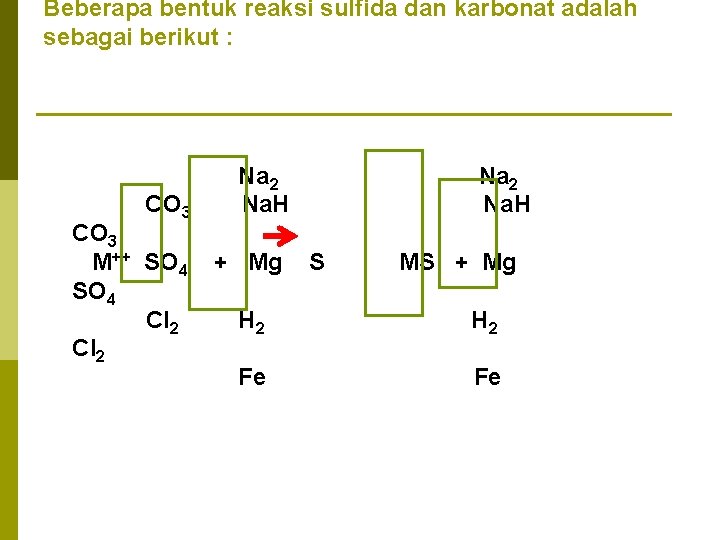
Beberapa bentuk reaksi sulfida dan karbonat adalah sebagai berikut : CO 3 M++ SO 4 Cl 2 Na. H + Mg Na 2 Na. H S MS + Mg H 2 Fe Fe

p p PENGENDAPAN LOGAM Pb dan Ni LEBIH BAIK DENGAN PRESIPITASI KARBONAT ION - ION PENGGANGGU PRESIPITASI : ION CIANIDA DAN AMMONIA. Cyanida dihilangkan dengan khlorinasi alkali n Ammonia dihilangkan dengan aerasi dan khlorinasi titik retak. “Pengolahan limbah Krom (Cr 6+) harus direduksi terlebih dahulu menjadi krom trivalen (Cr 3+) kemudian di presipitas. I dengan Kapur”. n

Penyerapan (adsorpsi) Penyerapan Anion dan kation dapat dilakukan dengan menggunakan media penyerap seperti Karbon Aktif, Aluminium Oksida, Besi Oksida, Silika, Lempung dan bahan sintetis (Zoelit, resin). p Proses Adsorpsi merupakan fungsi , p. H tinggi untuk penyerapan Kation sedang p. H rendah untuk penyerapan Anion p

Pertukaran Ion (Ion Exchange) Media penukar yang umum digunakan adalah ion Na+ dan H+. Reaksi yang umum terjadi adalah : 2 R-Na+ + M 2+ R 2 -M 2+ + 2 Na+ 2 R-H+ + M 2+ R 2 -M 2+ + 2 H+

PERFORMANSI (KINERJA) PROSES PENYISIHAN LOGAM Cadmium (Cd) Teknologi Konsentrasi Effluen g Cd/l - Presipitasi hidroksida , p. H 8 – 8, 5 - Kopresipitasi dengan Fe(OH)3, p. H 6 – 10 40 – 50 - Presipitasi hidroksida dengan penyaringan, p. H 10 0, 7 – 80 100 – 1000 – 11, 5 - Presipitasi Sulfida dan Kapur, p. H 8, 5 – 10 - Presipitasi Sulfida - Ion Exchange 2 – 29 5 – 10 1 – 50

. Krom (Chromium , Cr). Metode : reduksi valensi dan presipitasi p Proses reduksi : p n n Asidifikasi, menjadi p. H 2 – 3 Penambahan kimia reduktor : Sulfur dioksida, Sodium Bisulfite, Ferrous Sulfate.
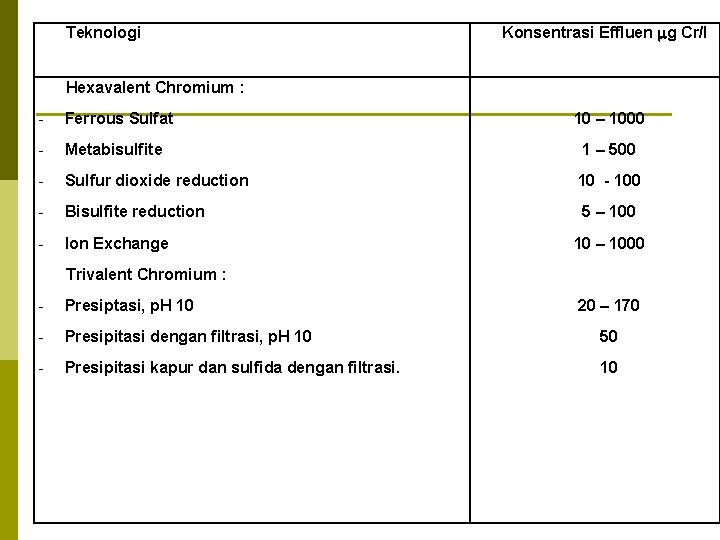
Teknologi Konsentrasi Effluen g Cr/l Hexavalent Chromium : - Ferrous Sulfat - Metabisulfite - Sulfur dioxide reduction - Bisulfite reduction - Ion Exchange 10 – 1000 1 – 500 10 - 100 5 – 100 10 – 1000 Trivalent Chromium : - Presiptasi, p. H 10 - Presipitasi dengan filtrasi, p. H 10 50 - Presipitasi kapur dan sulfida dengan filtrasi. 10 20 – 170

Tembaga (Cu) Metode pengolahan standar adalah presipitasi. p. H optimum presipitasi Cu adalah p. H 9 dan p. H 10. Ion Pengganggu CN dan Ammonia Teknologi Konsentrasi Effluen g Cu/l -Presipitasi hidroksida dengan filtrasi, 10 – 400 p. H 8, 5 Presipitasi hidroksida plus sulfida dengan filtrasi, p. H 8, 5 10 – 200 Pertukaran Ion Presipitasi Sulfida dan Kapur dengan filtrasi 10 – 50 10 5

Timbal (Pb) p p p Metode standard : Presipitasi timbal Penggangu proses : Timbal Organik Pretreatmen : Khlorinasi pemecah senyawa organik. Teknologi Konsentrasi Effluen g Pb/l -Presipitasi hidroksida, p. H 11, 5 10 – 500 Presipitasi karbonat p. H 9 - 9, 5 10 – 30 Presipitasi Sulfida dengan filtrasi Pertukaran Ion 10 dan Kapur 5 50

Nikel (Ni) Teknologi Konsentrasi Effluen g Ni/l -Presipitasi kapur, p. H 9 - 12 Presipitasi kapur dengan filtrasi , 500 50 – 150 p. H 9 - 12 Presipitasi Sulfida dengan filtrasi dan Kapur 40
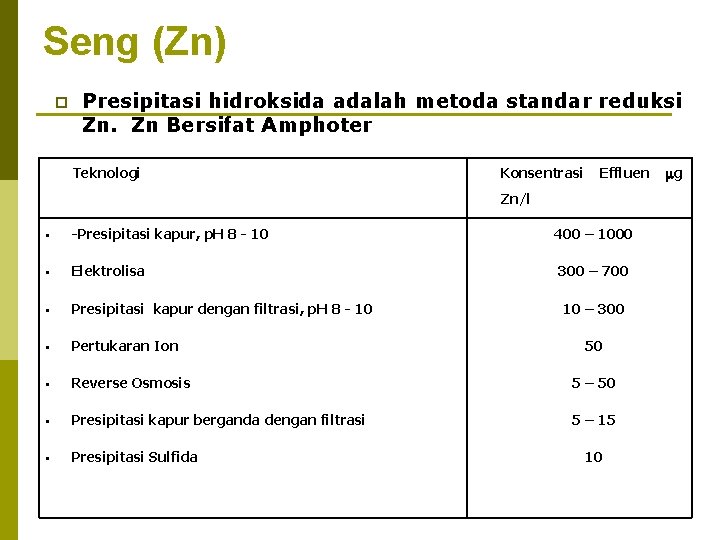
Seng (Zn) p Presipitasi hidroksida adalah metoda standar reduksi Zn. Zn Bersifat Amphoter Teknologi Konsentrasi Effluen Zn/l -Presipitasi kapur, p. H 8 - 10 400 – 1000 Elektrolisa Presipitasi kapur dengan filtrasi, p. H 8 - 10 Pertukaran Ion Reverse Osmosis 5 – 50 Presipitasi kapur berganda dengan filtrasi 5 – 15 Presipitasi Sulfida 300 – 700 10 – 300 50 10 g

Sianida (CN) p Proses pengolahan : n Oksidasi dengan Khlor n Dekomposisi elektorlitik, bila konsentrasi sianida sangat tinggi, n Ozonisasi, n Penyerapan dengan karbon aktif.
- Slides: 33