Pendahuluan Titrasi AsamBasa penetapan kadar suatu zat asam


Pendahuluan Titrasi Asam-Basa penetapan kadar suatu zat (asam atau basa) berdasarkan atas reaksi Asam-Basa). Pada analisis volumetri : § Asidimetri : suatu zat dititrasi dengan suatu asam § Alkalimetri : suatu zat dititrasi dengan suatu basa § Titik akhir titrasi didasarkan pada perubahan p. H pada Titik Ekivalen (TE). Daerah dimana terjadi perubahan p. H bergantung pd sifat dan konsentrasi zat penitrasi / zat yang dititrasi. Pada titrasi asam basa perlu diperhatikan: § Faktor-faktor yg menentukan kesempurnaan reaksi asam basa § Pemilihan indikator yang digunakan

Teori Asam Basa § Teori Arrhenius (1884) Asam dlm larutan air Basa dlm larutan air ion hidrogen (H+) ion hidroksida (OH-) Secara umum : Asam : HA H+ + A Basa : BOH B+ + OHpenetralan : H+ + OHH 2 O Beberapa tanggapan : § Hanya terbatas dlm larutan air § Dlm larutan ion tdk terdapatkan ion H+ yg bebas § Ada beberapa asam dan basa tidak mengandung ion H+ dan OH§ Beberapa zat spt amonia & natrium karbonat dpt menetralkan asam tanpa lebih dahulu menghasilkan OH-

§ Teori Bronsted- Lowry (1923) Asam : donor proton Basa : akseptor proton Asam dan basa saling berkaitan dalam pertukaran proton disebut pasangan asam-basa konjugasi Asam 1 H+ + basa konjugasi 1 Basa 2 OH- +Asam konjugasi 2 Reaksi asam basa : Asam 1 + Basa 2 basa konjugasi 1 + asam konjugasi 2 Menurut Teori ini, asam dpt berupa : - Molekul netral : HCl, H 2 SO 4, HNO 3, CH 3 COOH, H 2 O dsb - Anion : HSO 4 -, H 2 PO 4 - dll - Kation : NH 4+ - Ion Kompleks : Al(H 2 O)63+ Sedangkan basa dpt berupa : - Molekul netral : NH 3, RNH 2, R 1 R 2 NH, H 2 O - Ion hidroksida : OH- Anion : CH 3 COO-, CO 32 -, HS- dsb

Contoh-contoh reaksi asam-basa : HCl + H 2 O H 3 O+ + Cl. HAc + H 2 O H 3 O+ + Ac. H 3 PO 4 + H 2 O H 3 O+ + H 2 PO 4 NH 4+ + H 2 O H 3 O+ + NH 3 H 2 O + NH 3 NH 4+ + OHHAc + NH 3 NH 4+ + Ac. Air dpt bertindak sebagai asam (donor proton) maupun sebagai basa (akseptor proton). Pelarut demikian disebut amfiprotik

Teori Ionisasi Elektrolit Kuat dan Lemah Elektrolit dibagi 2 golongan : § Elektrolit kuat § Elektrolit lemah Dalam larutan asam : HA + H 2 O H 3 O+ +A-

Dalam larutan, air besar sekali : Nilai Ka menentukan kekuatan asam, makin besar Ka, makin kuat asam tersebut.

Kesetimbangan Ionisasi Air H 2 O + H 2 O Disingkat : H 2 O H 3 O+ + OHH+ + OH- Pada 250 C, bj air = 997, 044 gram/L

karena H 2 O elektrolit sangat lemah, H 2 O dianggap konstan

Pengertian p. H § Menurut Sorense (1909) Fungsi log ini blh dipakai secara lebih luas : p. OH = - log p. Kb = - log Kb p. Ka = - log Ka p. Kw = - log Kw Untuk larutan netral (250 C) : p. H = p. OH = 7

Perhitungan p. H asam dan basa 1. p. H asam kuat dan basa kuat dihitung dari konsentrasi molarnya HCl 0, 1 M, H+ = 10 -1 p. H = 1 H+ = 10 -1 p. OH = 1 Na. OH 0, 1 M p. H =14 – 1 = 13 2. p. H asam lemah dan basa lemah, dihitung dari konsentrasi asam basa dan Ka/Kb untuk asam lemah HA

HA H+ + A - Bila HA awal = c mol/L, maka yang tidak berdissosiasi : c - H+ karena H+ kecil maka c - H+ c HA

Dengan cara yang sama untuk basa lemah NH 4 OH :

Larutan Buffer : zat-zat yang dapat menahan perubahan p. H, dalam praktek sistem buffer dibuat dengan jalan mencampurkan asam lemah atau basa lemah dengan garamnya. contoh : § Campuran asam lemah + garamnya CH 3 COOH + CH 3 COONa H 3 PO 4 + Na 2 HPO 4
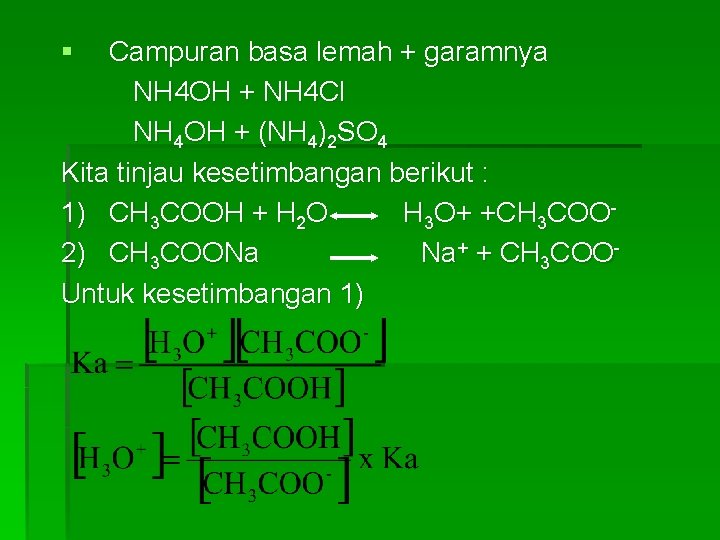
§ Campuran basa lemah + garamnya NH 4 OH + NH 4 Cl NH 4 OH + (NH 4)2 SO 4 Kita tinjau kesetimbangan berikut : 1) CH 3 COOH + H 2 O H 3 O+ +CH 3 COO 2) CH 3 COONa Na+ + CH 3 COOUntuk kesetimbangan 1)

§ Penambahan CH 3 COONa menyebabkan kesetimbangan 1) bergeser ke kiri maka bertambah kecil. misal awal = Ca dan = Cg yang tak berdisosiasi = ; sedangkan

Karena kesetimbangan 1) begeser ke kiri, maka menjadi kecil, sehingga dpt diabaikan thd Ca dan Cg


Sifat larutan Buffer § Pada pengenceran p. Hnya tetap § Penambahan sedikit asam atau basa kuat p. H tidak berubah

§ Kapasitas Buffer utk mengabsorsi asam atau basa tgt pd konsentrasi zat pembuffer. makin tinggi konsentrasi makin besar kapasitasnya Pada pembuatan buffer dgn p. H ttt, hrs dipilih camp. asam-garam atau basa-garam yg p. Ka atau p. Kbnya sedekat mungkin dgn p. H yg diinginkan. § Salah satu contoh buffer di alam adalah plasma darah. Buffer ini bekerja krn adanya H 2 CO 3 dan HCO 3 - jika kelebihan ion H+ maka :

§ Dengan mekanisme ini konsentrasi ion H+ dlm darah konstan. Contoh lain adalah buffer H 2 PO 4 - - HPO 42 - dan hemoglobin

Hidrolisis § Hidrolisis adalah reaksi antara ion-ion garam dgn air. Menurut Bronsted reaksi ini merupakan reaksi asam-basa. § Garam-garam dibagi dlm 4 golongan : - Garam-garam yg ion-ionnya aprotik (tdk mempunyai kecenderungan untuk mengikat atau melepaskan proton, misalnya Na. Cl, KNO 3 dsb). Larutannya bereaksi netral - Garam-garam yg anionnya adalah proton akseptor, misalnya Na. Ac, KCN, Na 2 CO 3 dan Na 2 S. Larutannya bereaksi basa - Garam-garam yg kationnya adalah proton donor, misalnya Al. Cl 3, Fe. Cl 3, (NH 4)2 SO 4. Larutannya bereaksi asam - Garam-garam yg kation-kationnya adalah asam dan anionnya adalah basa, misalnya NH 4 Ac, NH 4 CN. Larutannya bereaksi asam, basa atau netral bergantung kekuatan asam dan basanya

TETAPAN HIDROLISIS DAN DERAJAT HIDROLISIS § Hidrolisis dari anion yg proton akseptor CH 3 COOH- + H 2 O CH 3 COOH + OH- Kh = tetapan hidrolisis

INDIKATOR ASAM-BASA § Indikator asam-basa adalah senyawa organik yg berupa asam lemah atau basa lemah dimana warna molekul yang tdk berdisosiasi berbeda dng warna ionnya. Warna indikator dpt terlihat ditentukan oleh pembentukan konsentrasi bentuk asam & konsentrasi bentuk basa :

Warna bentuk asam akan terlihat bila : Warna bentuk basa akan terlihat bila : Trayek perubahan warna indikator antara p. H = p. Kin 1. Bila [HIn. A] = [HIn. B-], akan terlihat warna antara bentuk asam dan bentuk basa

Tabel Perubahan bentuk warna indikator pada bermacam-macam p. H Larutan HIn. A / In. B- Warna 1 2 3 4 5 6 7 8 10. 000 : 1 100 : 1 1: 1 1 : 100 1 : 1. 000 Merah Jingga Kuning Merah : Kuning : p. H = 2 Daerah perubahan p. H : 4 – 6, diantara kedua harga p. H ini : warna jingga
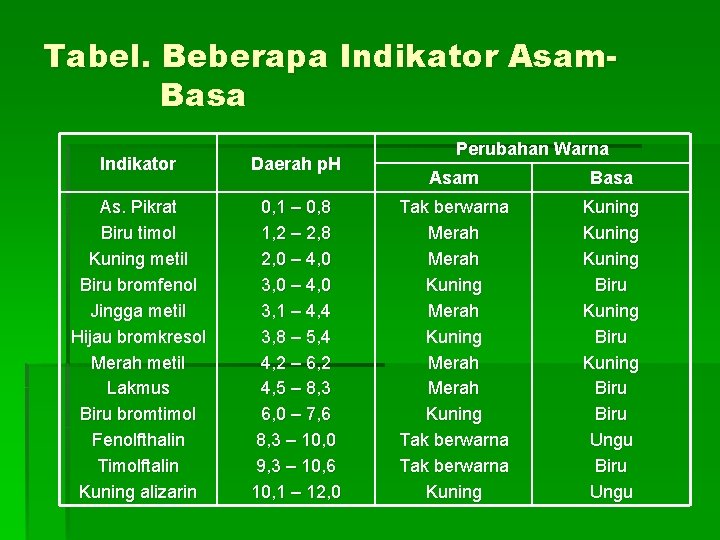
Tabel. Beberapa Indikator Asam. Basa Indikator Daerah p. H As. Pikrat Biru timol Kuning metil Biru bromfenol Jingga metil Hijau bromkresol Merah metil Lakmus Biru bromtimol Fenolfthalin Timolftalin Kuning alizarin 0, 1 – 0, 8 1, 2 – 2, 8 2, 0 – 4, 0 3, 1 – 4, 4 3, 8 – 5, 4 4, 2 – 6, 2 4, 5 – 8, 3 6, 0 – 7, 6 8, 3 – 10, 0 9, 3 – 10, 6 10, 1 – 12, 0 Perubahan Warna Asam Basa Tak berwarna Merah Kuning Merah Kuning Tak berwarna Kuning Biru Kuning Biru Ungu

§ Untuk beberapa titrasi yg titik akhir titrasi dlm trayek p. H sangat kecil digunakan indikator campuran contoh : - jingga metil + brom kresol hijau berubah warna dari jingga menjadi biru hijau pd p. H 4, 3 § Tipe lain dari indikator campuran : indikator universal. Indikator ini menunjukkan bermacam-macam warna utk trayek p. H yg sangat besar. Misal : Indikator nomor 1 : p. H 3 4 5 6 7 8 Warna merah jingga kuning biru jingga hijau 9 biru 10 ungu

TITRASI ASAM BERBASA BANYAK §TITRASI ASAM POLIPROTIK §PENENTUAN NITROGEN METODE KJELDAHL

Titrasi Asam Poliprotik Asam-asam yang mengandung lebih dari satu atom hidrogen disebut asam poliprotik (asam berbasa banyak) Misalnya : H 2 SO 4, H 2 C 2 O 4, H 2 CO 3, H 3 PO 4, As. Tartrat, Asam suksinat, As. Sitrat, As. Malonat. Jika Ka 1/Ka 2 dari asam berbasa dua sangat besar (Ka 1: Ka 2 = 104) maka asam tersebut dapat dtitrasi sebagai asam berbasa satu dan sebagai asam berbasa dua secara terpisah

Titrasi Asam karbonat H 2 CO 3 mengion dua tingkat : H 2 CO 3 H+ + HCO 3 - ; Ka 1 = 3 x 10 -7 HCO 3 H+ + CO 33 - ; Ka 2 = 6 x 10 -11 Jika H 2 CO 3 Dititrasi dengan Na. OH, maka p. H pada T. E Pertama adalah p. H larutan Na. HCO 3, dan dapat dihitung sebagai berikut : HCO 3 H+ + CO 32 Dalam hal ini [H+] [CO 32 -], karena sebagian H+ bersenyawa dengan HCO 3 - membentuk H 2 CO 3


Indikator yg digunakan untuk TE adalah : PPT ( p. H 8, 2 – 10 )

Ka 2 sangat kecil sehingga H 2 CO 3 tidak dapat dititrasi sebagai asam berbasa dua dengan cara langsung. Secara tidak langsung dapat dilakukan sebagai berikut : Kelebihan Ba(OH)2 dapat dititrasi dengan larutan standar HCl dengan PPT sebagai indikator

Titrasi Asam Fospat H 3 PO 4 mempunyai konstan ionisasi terpisah baik sekali karena Ka 1/Ka 2 = 1, 0. 105 dan Ka 2/Ka 3 = 1, 4. 105 jadi H 3 PO 4 dapat dititrasi sebagai asam berbasa satu atau asam berbasa dua, tetapi tidak dapat dititrasi sebagai asam berbasa tiga.

H 3 PO 4 H+ + H 2 PO 4 - : Ka 1 = 7. 10 -3 H 2 PO 4 H+ + HPO 42 - : Ka 2 = 7. 10 -8 HPO 4 H+ + PO 43 - : Ka 3 = 5. 10 -13 Bila dalam larutan terdapat campuran H 2 PO 4 maka p. H larutan dihitung sebagai campuran buffer
- Slides: 36