PENDAHULUAN Pengertian termodinamika Beberapa thermo panas dynamis gerakanperubahan


PENDAHULUAN � Pengertian termodinamika � Beberapa thermo (panas) dynamis (gerakan/perubahan) istilah penting : a. Sistem -> bagian alam semesta yg menjadi perhatian kita b. Lingkungan -> bagian lainnya diluar sistem

� Antara sistem dan lingkungan dpt terjadi pertukaran energi dan massa. Berdasarkan hal itu ada 3 jenis sistem : a. Sistem terbuka -> sistem yg dpt mempertukarkan energi & massa dg lingkungan b. Sistem tertutup -> sistem yg hanya dpt mempertukarkan energi dg lingkungan c. Sistem terisolasi -> sistem yg tdk dpt mempertukarkan energi & massa dg lingkungan

HUKUM TERMODINAMIKA I � Setiap sistem kimia mempunyai sejumlah energi yg besarnya bergantung pd keadaan sistem. Energi ini disebut energi dalam. � Energi dalam -> energi yg tersimpan dlm sistem -> U � Energi dalam merupakan fungsi keadaan. � Perubahan energi dalam dinyatakan dg : ∆U = U 2 – U 1

� Perubahan energi dalam ini dpt berupa : 1) kalor yg tmbul / diserap (q) 2) kerja yg dilakukan oleh sistem (w) � Jika suatu sistem tdk melakukan kerja dan pd sistem tersebut ditambahkan sejumlah kalor, maka ∆U=q � Jika pd sistem dilakukan suatu kerja tetapi tanpa diikuti perpindahan kalor dari / ke lingkungan, mka ∆U = w � Jika sistem menerima kalor dan pd sistem dilakukan kerja, maka ∆U = q+w

� Keterangan : w (+) : kerja dilakukan pd sistem (w>0) w (-) : sistem melakukan kerja (w<0) q (+) : sistem menerima kalor (q>0) q (-) : sistem mengeluarkan kalor (q<0) � Kerja yg dilakukan oleh sistem menyangkut ekspansi dan kompresi volum, maka w = ∆(PV), oleh karena PV = n. RT, maka ∆(PV) = ∆n RT, jika P dan T konstan, maka : ∆(PV) = ∆n RT = w

� Untuk ekspansi (sistem melakukan kerja) maka : ∆U = q - ∆n RT -> ∆U = q – w � Untuk kompresi (sistem dilakukan kerja), maka : ∆U = q + ∆n RT -> ∆U = q+w KALOR REAKSI TERMODINAMIKA � HK. I Termodinamika ∆U = q+w � Jika reaksi berlangsung pd wadah tertutup, shg volum tetap, maka ∆U = qv � Reaksi kimia kebanyakan tdk dilakukan pd volum tetap, tapi dilakukan pada wadah terbuka pd tekanan tetap. � Perubahan kalor pd keadaan semacam ini disebut perubahan entalpi (∆H)

� � Perubahan entalpi dinyatakan : ∆H = ∆U + ∆(PV) ∆H = q + w + ∆(PV) Perubahan berlangsung pd tekanan tetap w = - ∆(PV), karena itu ∆H = q - ∆(PV) + ∆(PV), shg ∆H = qp ∆H (-) : utk proses eksoterm, dan ∆H (+) : utk proses endoterm Scr eksperimen, penentuan ∆H pd kondisi tetap menggunakan kalorimeter larutan. Untuk penentuan ∆U dilakukan pd volum tetap menggunakan kalorimeter bomb.

� Perbedaan ∆H dan ∆U Pada beberapa hal, perbedaan keduanya sangat kecil, khususnya pd reaksi kimia dimana reaktan & produk semuanya berupa cairan atau padatan. Pada kondisi ini ∆V sangat kecil, demikian pula ∆(PV) , sehingga ∆H=∆U. Bagi reaksi yg menyangkut gas, ∆(PV) tidak dpt diabaikan. Apabila gas dianggap ideal, sehingga memenuhi pers. Keadaan PV = n. RT, maka pada suhu yg sama : ∆(PV) = [∆n(gas)]RT ∆H = ∆U + [∆n(gas)]RT

� HUKUM HESS ENTALPI ∆H tidak bergantung pd bagaimana reaksi tersebut berlangsung tetapi hanya bergantung pada keadaan awal & akhir. Contoh: Hitung ∆H utk reaksi : 2 Al(s) + Fe 2 O 3(s) -> 2 Fe(s) + Al 2 O 3(s) , dari Perubahan entalpi pembakaran Al dan Fe : 2 Al(s) + 3/2 O 2(g) -> Al 2 O 3(s) ∆H = -1669, 8 k. J 2 Fe(s) + 3/2 O 2(g) -> Fe 2 O 3(s) ∆H = -824, 2 k. J

Panas/Kalor Pembentukan Standar � Semua zat berada pada keadaan standar (25°C, 1 atm), dinyataan dengan ∆Hf° �∆Hf° penting utk menghitung panas reaksi standar. ∆Hreaksi° = Ʃ ∆Hf° produk - Ʃ ∆Hf° reaktan Contoh : hitung ∆Hreaksi° untuk reaksi : C 2 H 4(g) + H 2(g) -> C 2 H 6(g)
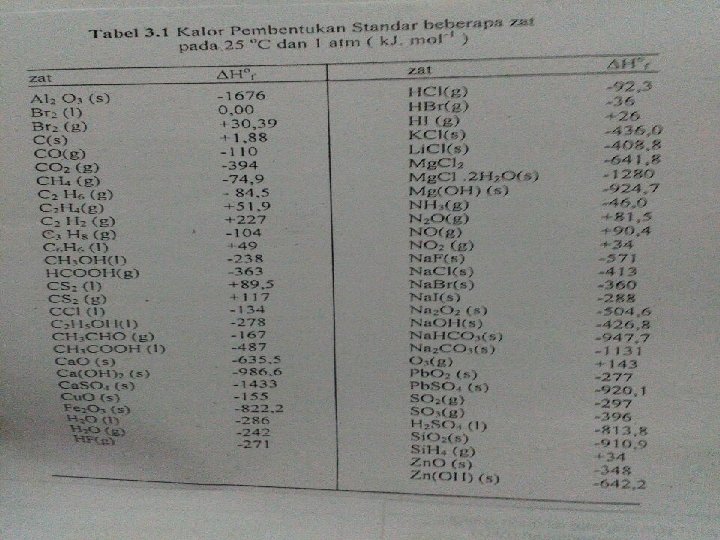

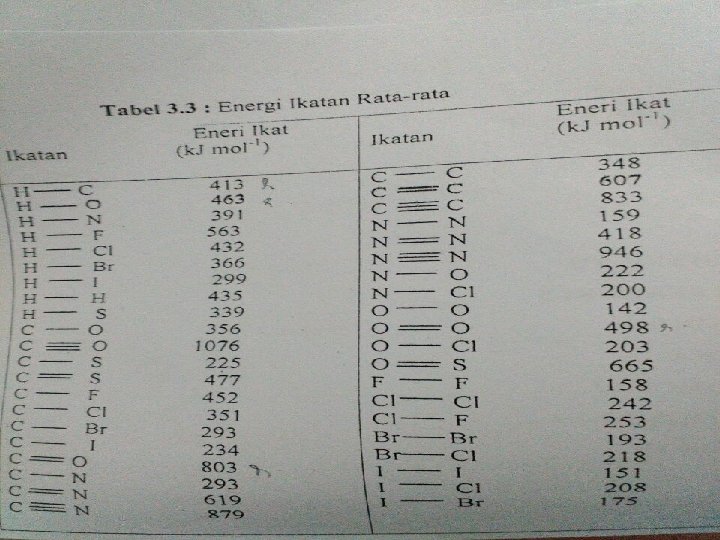
ENERGI IKATAN &ENERGI IKATAN RATA � Energi ikatan -> energi yg diperlukan utk memutuskan 1 ikatan utk menghasilkan pecahan-pecahan yg netral. � Energi ikatan rata-rata -> dapat digunakan utk menghitung panas pembentukan dg ketepaatan yang dapat diandaikan. ∆H = Ʃ ∆HD (ikatan putus) - Ʃ ∆HD (ikatan terbentuk)

� Contoh : Perkirakan harga ∆H pembakaran metana CH 4(g) + 2 O 2(g) -> CO 2(g) + 2 H 2 O(g) Diket : H-C : 413 k. J/mol H-O : 463 k. J/mol O=O : 498 k. J/mol C=O : 803 k. J/mol
- Slides: 15