PEMBAHASAN SOAL KIMIA PAKET 3 SOAL NOMOR 1

PEMBAHASAN SOAL KIMIA PAKET 3

SOAL NOMOR 1 Dalam kaidah yang dikemukakan oleh Friedrich Hund (1894 – 1968) pada tahun 1930, disebutkan bahwa elektron-elektron dalam orbital-orbital suatu subkulit cenderung untuk tidak berpasangan. Elektron-elektron akan berpasangan apabila pada subkulit itu sudah tidak ada lagi orbital kosong. Jawaban : B
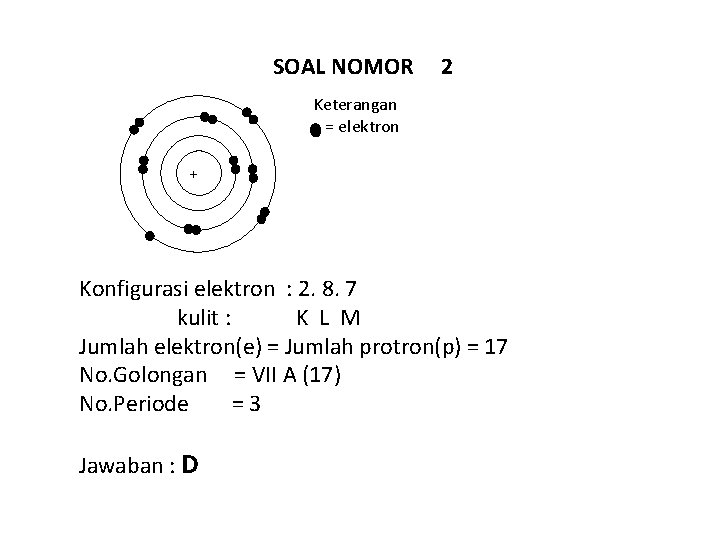
SOAL NOMOR 2 Keterangan = elektron + Konfigurasi elektron : 2. 8. 7 kulit : K L M Jumlah elektron(e) = Jumlah protron(p) = 17 No. Golongan = VII A (17) No. Periode =3 Jawaban : D

SOAL NOMOR 3 Ikatan ion : terjadi antar atom yang mempunyai keelektronegatifan kecil (cenderung melepas elektron) dengan atom yang mempunyai keelektronegatifan besar (cenderung menangkap elektron) konfigur Unsur asi Keelektronegatifan ion Na 2. 8. 1 kecil Na+ Ca 2. 8. 8. 2 kecil Ca 2+ S 2. 8. 6 besar S 2 - Cl 2. 8. 7 Besar Cl- Jawaban : C kation anion Na+ Ca 2+ S 2 - Cl- Jenis ikatan Na 2 S Ca. S Na. Cl Ca. Cl 2 ion

SOAL NOMOR 4 Ciri-ciri senyawa yang berikatan logam : 1. pada suhu kamar berwujud padat, kecuali Hg; 2. keras tapi lentur/dapat ditempa; 3. mempunyai titik didih dan titik leleh yang tinggi; 4. penghantar listrik dan panas yang baik; 5. mengilap. Jawaban : A
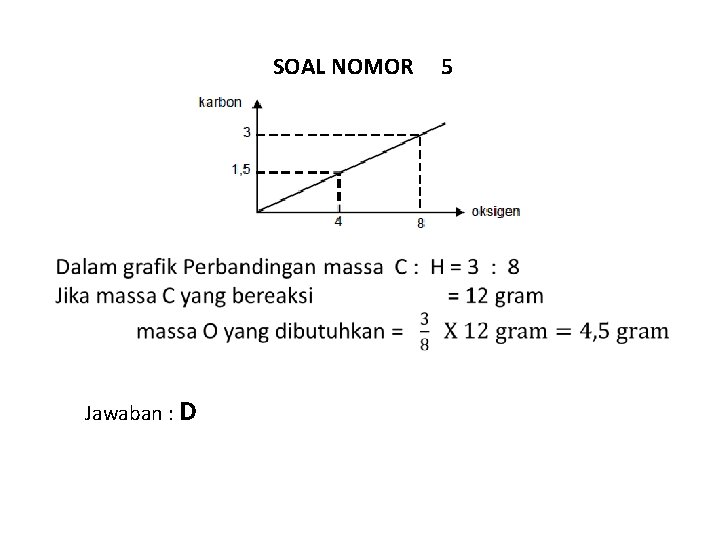
SOAL NOMOR Jawaban : D 5

SOAL NOMOR 6 Persamaan reaksi setara harus memenuhi : Jumlah unsur-unsur sesudah reaksi = sebelum reaksi Persamaan reaksi yang memenuhi N 2 O 5(g) + 2 KOH(aq) → 2 KNO 3(aq) + H 2 O(l) Jawaban : B

SOAL NOMOR 7 Berdasarkan uji alat elektrolit kekuatan larutan elektrolit: 1. Elektrolit kuat bila nyala lampu terang dan banyak gelembung gas 2. Elektrolit sedang-lemah bila nyala lampu redup-tidak menyala dan ada gelembung gas 3. Non elektrolit bila lampu tidak menyala dan tidak ada gelembung gas Kesimpulan : larutan I, III merupakan larutan elektrolit Dari uji lakmus disimpulkan : Larutan I bersifat netral (garam) Larutan I bersifat asam Larutan I bersifat basa Jawaban : E

SOAL NOMOR 8 Indikator I : memberi warna biru jika p. H larutan > 3 (dari asam hingga basa) Indikator II : memberi warna biru jika p. H larutan 8 – 9, 5 (basa) Indikator III : memberi warna biru jika p. H larutan > 7 (basa) Indikator IV : memberi warna biru jika p. H larutan > 10 (basa) Indikator V : memberi warna biru jika p. H larutan > 8 Jawaban : A
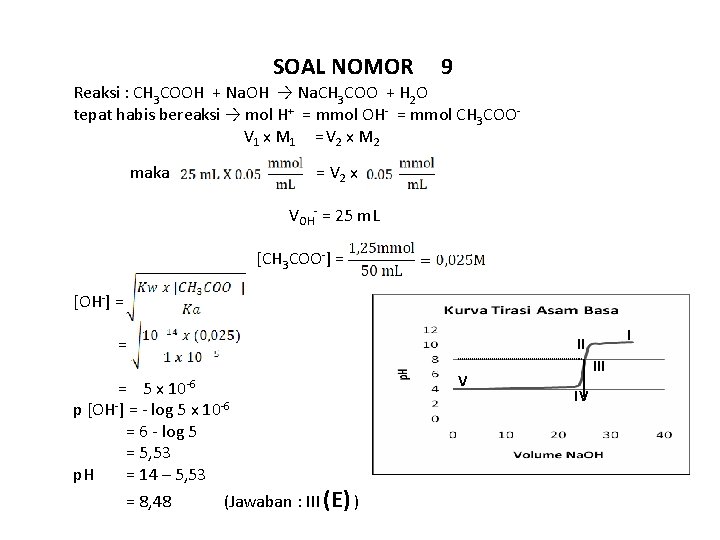
SOAL NOMOR 9 Reaksi : CH 3 COOH + Na. OH → Na. CH 3 COO + H 2 O tepat habis bereaksi → mol H+ = mmol OH- = mmol CH 3 COOV 1 x M 1 = V 2 x M 2 maka = V 2 x VOH- = 25 m. L [CH 3 COO-] = [OH-] = = = 5 x 10 -6 p [OH-] = - log 5 x 10 -6 = 6 - log 5 = 5, 53 p. H = 14 – 5, 53 = 8, 48 I II (Jawaban : III (E) ) V III IV
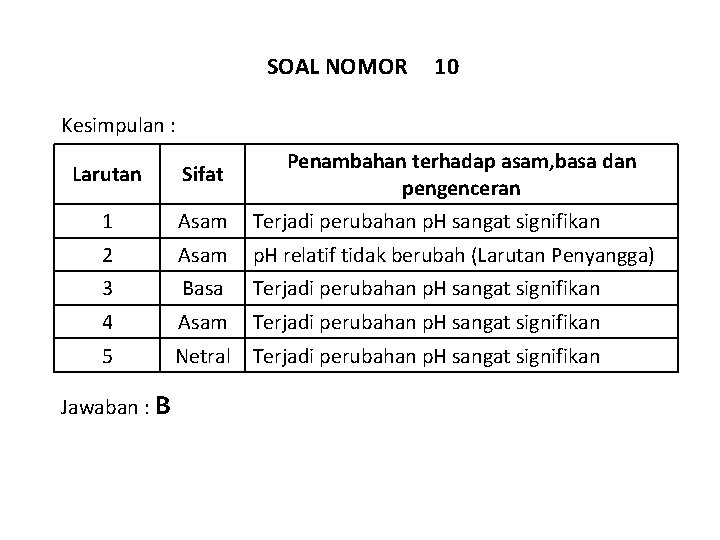
SOAL NOMOR 10 Kesimpulan : Penambahan terhadap asam, basa dan pengenceran Larutan Sifat 1 Asam Terjadi perubahan p. H sangat signifikan 2 Asam p. H relatif tidak berubah (Larutan Penyangga) 3 Basa Terjadi perubahan p. H sangat signifikan 4 Asam Terjadi perubahan p. H sangat signifikan 5 Netral Terjadi perubahan p. H sangat signifikan Jawaban : B
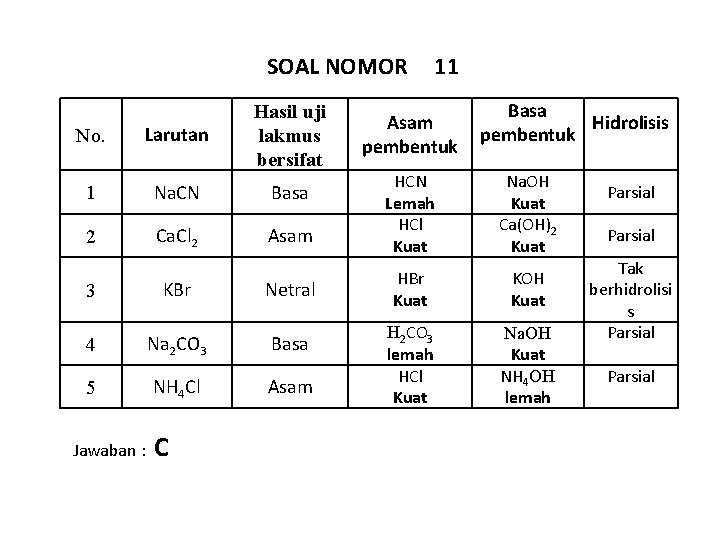
SOAL NOMOR No. Larutan Hasil uji lakmus bersifat 1 Na. CN Basa 2 Ca. Cl 2 Asam 3 KBr Netral 4 Na 2 CO 3 Basa 5 NH 4 Cl Asam Jawaban : C 11 Asam pembentuk Basa Hidrolisis pembentuk HCN Lemah HCl Kuat Na. OH Kuat Ca(OH)2 Kuat HBr Kuat KOH Kuat H 2 CO 3 lemah HCl Kuat Na. OH Kuat NH 4 OH lemah Parsial Tak berhidrolisi s Parsial
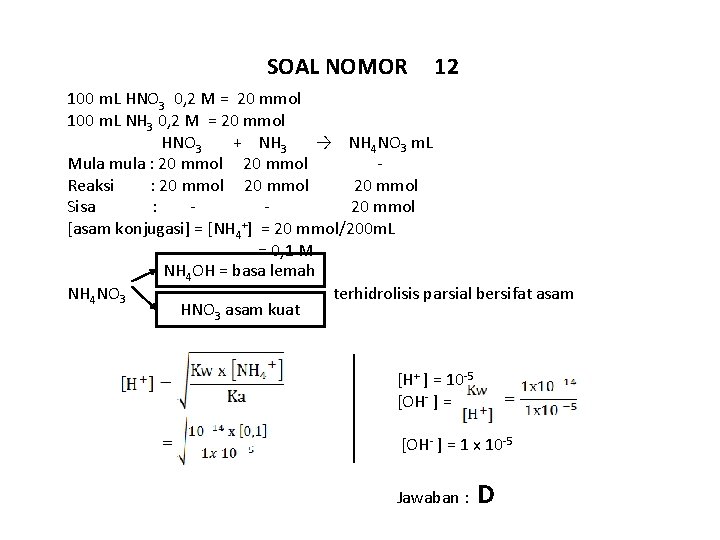
SOAL NOMOR 12 100 m. L HNO 3 0, 2 M = 20 mmol 100 m. L NH 3 0, 2 M = 20 mmol HNO 3 + NH 3 → NH 4 NO 3 m. L Mula mula : 20 mmol Reaksi : 20 mmol Sisa : 20 mmol [asam konjugasi] = [NH 4+] = 20 mmol/200 m. L = 0, 1 M NH 4 OH = basa lemah NH 4 NO 3 terhidrolisis parsial bersifat asam HNO 3 asam kuat [H+ ] = 10 -5 [OH- ] = 1 x 10 -5 Jawaban : D

SOAL NOMOR 13 Kemolaran Ca. SO 4 = 0, 68 gram : 136 gram/mol = 0, 005 mol /L = 0, 005 M Ca. SO 4 (s) Ca 2+ (aq) + SO 42 - (aq) Kelarutan : s s s 0, 005 M Hasil kali kelarutan Ksp = s 2 (aq) = (0, 005)2 = 2, 5 x 10 -5 Jawaban : A

SOAL NOMOR 14 Pada volum dan konsentrasi yang sama jumlah partikel (ion) terbanyak Ba. Cl 2 = 3 ion No. Larutan 1 2 3 4 5 Mg. SO 4 urea Ba. Cl 2 Na. Cl glukosa Jenis elektrolit Non elektrolit Jumlah partikel 2 1 3 2 1 Tekanan Uap Jenuh pada 25°C (mm. Hg) 224 35 20 56 112 Perbedaan penurunan tekanan uap antara larutan Non elektrolit dan elektrolit sebesar faktor Van’t Hoff = i = (1+(n-1)α) Jumlah ion semakin banyak akan diperoleh penurunan tekanan uap besar → tekanan uap jenuh larutan semakin kecil Jawaban : C

SOAL NOMOR 15 Pada konsentrasi dan volum sama : Perbedaan besarnya ΔTf dan ΔTb larutan non elektrolit dan elektrolit Menurut Van’t Hoff, sebesar i = 1 + (n – 1) α) Larutan urea 0. 1 M merupakan larutan non elektrolit Larutan Na. Cl 0. 1 M merupakan larutan elektrolit C – D merupakan kurva P – T pelarut murni B – E merupakan kurva P – T terlarut non elektrolit A – F merupakan kurva P – T terlarut elektrolit A B C P a d a t A ’ B ’ C’ D E F gas cair D’ E’ F ’ C’ adalah titik beku air D’ adalah titik didih air B’ adalah titik beku Larutan urea E’ adalah titik didih Larutan urea A’ adalah titik beku Larutan Na. Cl F’ adalah titik didih Larutan Na. Cl Perubahan titik beku(ΔTf)dan titik didih(ΔTb) larutan Na. Cl A’- B’ dan E’ – F’ Jawaban : B

SOAL NOMOR 16 Campuran : 1) Na. Cl + air → larutan Na. Cl 2) Tepung terigu + air dipanaskan → dispersi koloid (sol) 3) Sabun + air → dispersi koloid (sol) 4) Gula + air → larutan gula yang menghasilkan sistem koloid adalah 2 dan 3 Jawaban : E

SOAL NOMOR 17 Pembuatan koloid cara dispersi adalah merubah partikel kasar(berukuran > 10 -5 cm) menjadi partikel koloid : cara dispersi terdapat pada pembuatan koloid -Gas H 2 S dialirkan ke dalam endapan Ni. S. - Sol logam dibuat dengan cara busur Bredig. -Agar-agar dipeptisasi dalam air. Jawaban : A
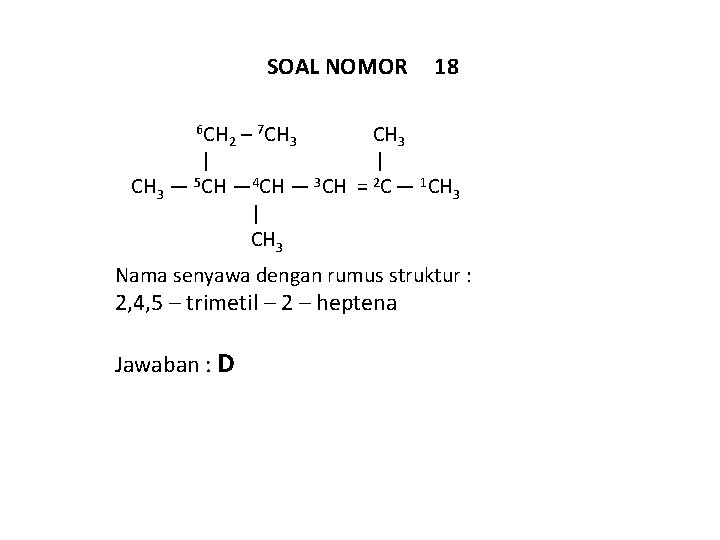
SOAL NOMOR 6 CH 18 CH 3 | | CH 3 ― 5 CH ― 4 CH ― 3 CH = 2 C ― 1 CH 3 | CH 3 2 – 7 CH 3 Nama senyawa dengan rumus struktur : 2, 4, 5 – trimetil – 2 – heptena Jawaban : D
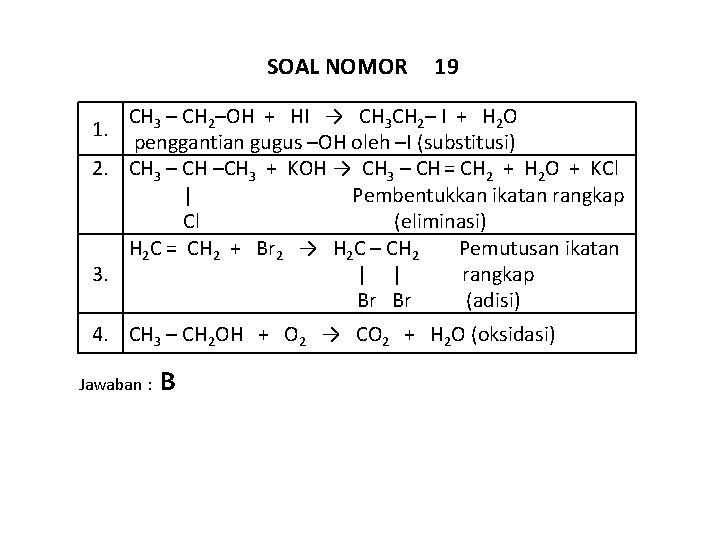
SOAL NOMOR 19 CH 3 – CH 2–OH + HI → CH 3 CH 2– I + H 2 O penggantian gugus –OH oleh –I (substitusi) 2. CH 3 – CH –CH 3 + KOH → CH 3 – CH = CH 2 + H 2 O + KCl | Pembentukkan ikatan rangkap Cl (eliminasi) H 2 C = CH 2 + Br 2 → H 2 C – CH 2 Pemutusan ikatan 3. | | rangkap Br Br (adisi) 1. 4. CH 3 – CH 2 OH + O 2 → CO 2 + H 2 O (oksidasi) Jawaban : B
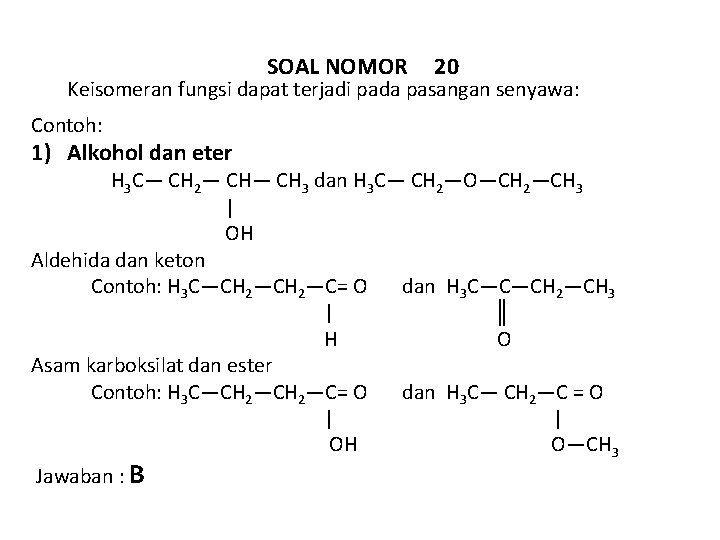
SOAL NOMOR 20 Keisomeran fungsi dapat terjadi pada pasangan senyawa: Contoh: 1) Alkohol dan eter H 3 C― CH 2― CH 3 dan H 3 C― CH 2―O―CH 2―CH 3 | OH Aldehida dan keton Contoh: H 3 C―CH 2―C= O dan H 3 C―C―CH 2―CH 3 | ║ H O Asam karboksilat dan ester Contoh: H 3 C―CH 2―C= O dan H 3 C― CH 2―C = O | | OH O―CH 3 Jawaban : B

SOAL NOMOR 21 Senyawa X adalah propanon, memenuhi sifat-sifat yang tertulis yakni: 1) Bertitik didih rendah karena tak terjadi ikatan hidrogen antarmolekulnya. 2) Mengandung tiga atom karbon karena mempunyai rumus H 3 C―C― CH 3 ║ O 3) Tidak mengubah warna lakmus biru. 4) Tidak dapat dioksidasi karena tak mempunyai atom H yang terikat langsung pada C karbonil. 5) Adisi dengan gas H 2 dihasilkan alkohol sekunder. H 3 C―C― CH 3 + H 2 → H 3 C―C― CH 3 (alkohol sekunder) ║ | O OH Jawaban : C
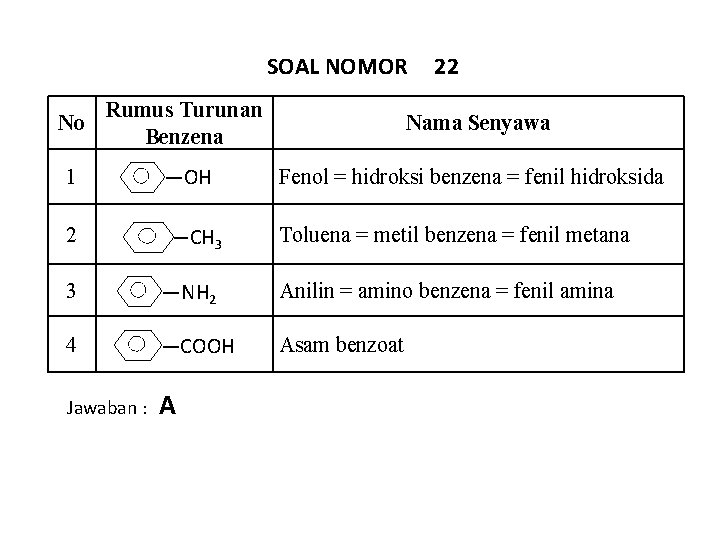
SOAL NOMOR 22 No Rumus Turunan Benzena 1 ―OH Fenol = hidroksi benzena = fenil hidroksida 2 ―CH 3 Toluena = metil benzena = fenil metana 3 ―NH 2 Anilin = amino benzena = fenil amina 4 ―COOH Asam benzoat Jawaban : A Nama Senyawa

SOAL NOMOR 23 Senyawa turunan benzena dan kegunaannya yang tepat adalah sebagai berikut. No Rumus Struktur 1 2 3 4 5 O ǁ Kegunaan Antiseptik, desinfektan, bahan plastik Sebagai pelarut, bahan bakuzat peledak (TNT) Bahan zat warna, obat sulfa (antibakteri) Pengawet makanan Bahan dasar membuat fenol Kegunaan natrium benzoat sebagai pengawet makanan Jawaban : D

SOAL NOMOR 24 Identifikasi protein yang mengandung tertentu sebagai berikut Pengamatan Warna terhadap Biuret Xantoproteat Timbal(II) nitrat Belerang hitam (Pb. S) Polipeptida ungu Gugus fenil jingga Bahan-bahan yang mengandung belerang dan gugus fenil adalah putih telur dan susu. Spesi Jawaban: A
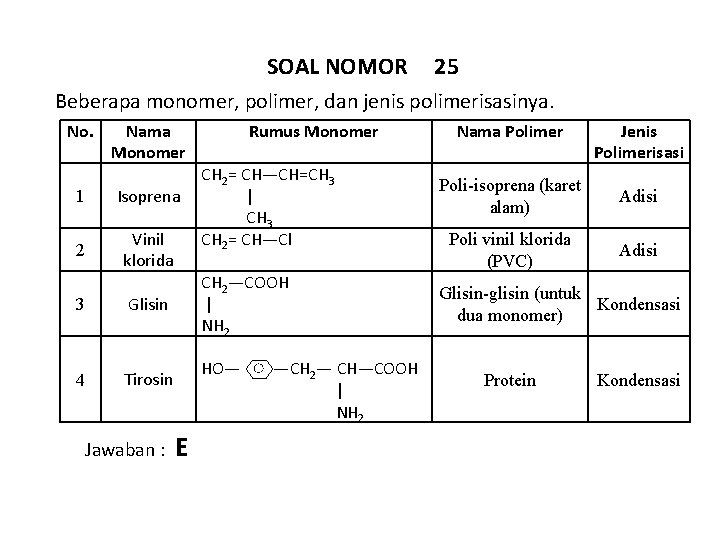
SOAL NOMOR 25 Beberapa monomer, polimer, dan jenis polimerisasinya. No. Nama Monomer 1 Isoprena 2 Vinil klorida 3 Glisin 4 Tirosin Jawaban : Rumus Monomer CH 2= CH―CH=CH 3 | CH 3 CH 2= CH―Cl CH 2―COOH | NH 2 HO― E ―CH 2― CH―COOH | NH 2 Nama Polimer Jenis Polimerisasi Poli-isoprena (karet alam) Adisi Poli vinil klorida (PVC) Adisi Glisin-glisin (untuk Kondensasi dua monomer) Protein Kondensasi

SOAL NOMOR 26 Perbedaan reaksi eksoterm dan endoterm No Pembeda 1 Perpindahan kalor 2 3 4 Reaksi ΔH Entalpi sistem Eksoterm dari sistem ke lingkungan negatif berkurang Endoterm dari lingkungan ke sistem positif bertambah Suhu lingkungan naik turun Reaksi endoterm akan terjadi perpindahan kalor dari lingkungan ke sistem (reaksi yang memerlukan panas). Reaksi endoterm mengakibatkan suhu lingkungan menjadi turun. Percobaan yang memenuhi reaksi endoterm tersebut adalah nomor 1, 3, dan 4. Jawaban : B

SOAL NOMOR 27 Menurut hukum Hess kalor reaksi tidak ditentukan oleh jalannya reaksi melainkan keadaan awal dan keadaan akhir. - ∆H 1 adalah proses penguraian 2 mol SO 3 = -(- 790. 4 k. J) proses penguraian 1 mol SO 3 = 790. 4 k. J : 2 = 395, 2 k. J Jawaban : D

Reaksi: 2 H 2 O(l) 2 H–O | H SOAL NOMOR 28 → 2 H 2(g) → 2 H–H + Pemutusan ikatan 2 x (2 O – H ) = 4 x 464 k. J = 1856 k. J + O 2(g) O=O Pembentukan ikatan 2 x (H – H) = 2 x 436 k. J = 872 k. J O = 500 k. J + = 1372 k. J ∆H reaksi = Energi ikat (Pemutusan – Pembentukan) ∆H reaksi = 1856 k. J - 1372 k. J ∆H reaksi = 484 k. J Jawaban : E
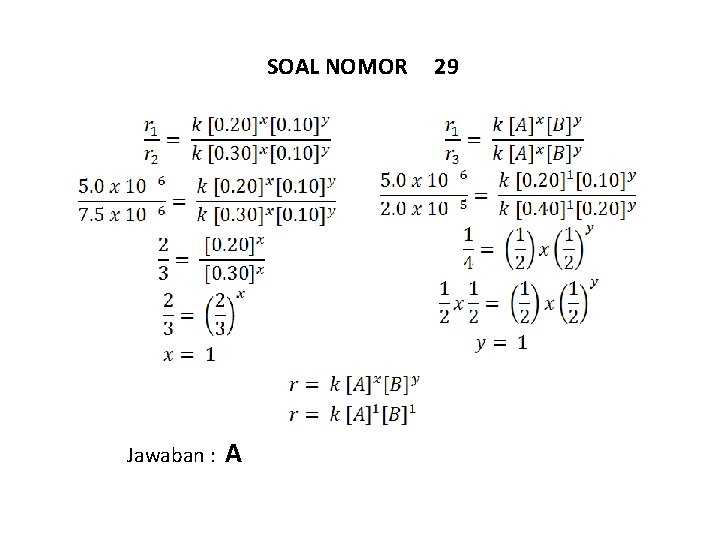
SOAL NOMOR Jawaban : A 29

SOAL NOMOR 30 Katalis adalah zat yang terlibat dalam mekanisme reaksi tetapi pada akhir reaksi diperoleh kembali dalam jumlah yang tetap Katalis mempercepat reaksi dengan jalan menurunkan energi pengaktifan agar reaksi dapat berlangsung. Pada mekanisme tahap reaksi P + Q → PQ. Tahap I : P + Q → PQ (lambat) Tahap II : P + R → PR (cepat) Tahap III : PR + Q → PQR (cepat) Tahap IV : PQR → PQ + R (cepat) Spesi R ikut dalam mekanisme reaksi dan diperoleh kembali pada akhir reaksi dalam jumlah yang tetap adalah R Jawaban : C

SOAL NOMOR 31 Pada reaksi setimbang : 2 HI(g) H 2(g) + I 2(g) ΔH = + 53 k. J Jika pada suhu tetap tekanan diperbesar / volum diperkecil maka kesetimbangan akan bergeser ke arah reaksi dengan jumlah molekul terkecil keset imbangan homogen gas di atas produk dan reaktan mempunyai jumlah molekul sama maka kesetimbangan tidak bergeser / tetap (jumlah masing-m 2 sing spesi tetap) Jawaban : gambar C

SOAL NOMOR 32 Pada reaksi setimbang : A(g) + 2 B(g) tekanan total 4 atm tekanan parsial gas A 1, 6 atm tekanan parsial gas B 0, 8 atm tekanan parsial gas C =(4 – 1, 6 – 0, 8)atm = = 2, 5 Jawaban : D 2 C(g)
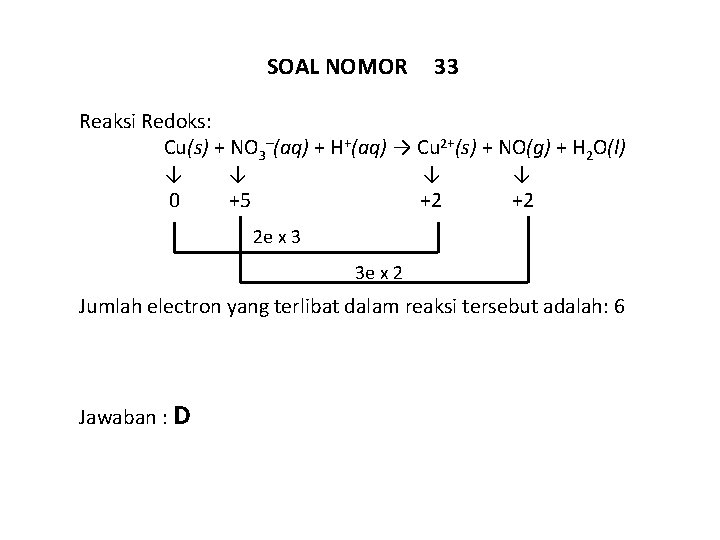
SOAL NOMOR 33 Reaksi Redoks: Cu(s) + NO 3–(aq) + H+(aq) → Cu 2+(s) + NO(g) + H 2 O(l) ↓ ↓ 0 +5 +2 +2 2 e x 3 3 e x 2 Jumlah electron yang terlibat dalam reaksi tersebut adalah: 6 Jawaban : D

SOAL NOMOR 34 Berdasarkan gambar sel, (Ag) sebagai kutub negatif atau anode akan melepas elektron dan mengalami oksidasi. (Pb) sebagai kutub positif sel atau katode akan menerima elektron dan mengalami reduksi. Anode: Pb(s) → Pb 2+(aq) + 2 e Eo = +0. 13 V Katode: 2 e + 2 Ag+(aq) → 2 Ag(s) Eo = +0. 80 V + Pb(s) + 2 Ag+(aq) → Pb 2+ (aq) + 2 Ag(s) Eo sel= +0, 93 V Penulisan notasi sel yang paling sesuai adalah: Pb |Pb 2+║ Ag+|Ag. Eo sel= +0, 93 V Atau Eo sel = Eo reduksi – Eo oksidasi = (+ 0, 80 ) – (- 0, 13) = +0, 93 V Jawaban : E

SOAL NOMOR 35 Berdasarkan gambar sel, larutan Zn. SO 4 dielektrolisis. Reaksi yang terjadi adalah: Anode: 2 H 2 O(l) → O 2(g) + 4 H+(aq) + 4 e. Katode: 2 e- + Zn 2+(aq) → Zn(s) Jawaban : A

SOAL NOMOR 36 Berdasarkan gambar sel, larutan Zn. SO 4 dielektrolisis. Reaksi yang terjadi adalah: Katode: 2 e- + Zn 2+(aq) → Zn(s) 1 mol Zn = 2 mol elektron = 2 F 2 F =1 mol Zn 0. 2 F = 0. 2 F/2 F x 1 mol Zn 0. 2 F = 0. 1 mol Zn = 0. 1 x Ar Zn 0. 2 F = (0. 1 x 65) = 6. 5 gram Jawaban : E

SOAL NOMOR 37 Satu dari beberapa faktor penyebab korosi logam adalah kontak langsung dengan O 2 dan dipercepat oleh kelembaban H 2 O. Proses korosi tersebut akan terhambat jika logam dihindarkan dari kontak langsung dengan O 2 dan H 2 O. Jawaban : D

SOAL NOMOR 38 Pada tabel berikut ini dicantumkan bahan kimia dan manfaatnya. No. 1 2 3 4 5 Bahan Kimia KIO 3 Ca. SO 4 Mg(OH)2 Na. OCl Jawaban : B Manfaat iodisasi garam gibs obat pencahar obat maag pengelantang

SOAL NOMOR 39 Untuk memperoleh logam aluminium dapat dilakukan dengan cara elektrolisis leburan bauksit (Al 2 O 3. 2 H 2 O) dalam kriolit Na 3 Al. F 6. Fungsi kriolit Na 3 Al. F 6 pada proses tersebut adalah untuk merendahkan titik leleh Al 2 O 3 dari 2000 o. C menjadi 1000 o. C. Jawaban: A

SOAL NOMOR 40 Sumber utama logam aluminium adalah bauksit (Al 2 O 3). Untuk memperoleh logam itu dapat dilakukan dengan cara leburan bauksit dielektrolisis dengan menggunakan elektrode grafit melalui reaksi berikut. Katode : Al 3+(ℓ) + 3 e → Al(ℓ) Anode : 2 O 2− (ℓ) → O 2(g) + 4 e Pengolahan logam itu dikenal dengan nama proses Hall - Haroult. Jawaban : C
- Slides: 41