Patologia 8 Diabete mellito di tipo 1 Diabete

Patologia 8. Diabete mellito di tipo 1

Diabete Mellito: definizione (1) ØIl Diabete mellito e’ un gruppo di patologie caratterizzate da una alterata omeostasi del glucosio, con una persistente instabilità del livello glicemico del sangue, dovuta ad una insufficienza assoluta o relativa di insulina (o della capacita’ di rispondere ad essa). ØPuo’ essere di tipo primario o secondario ad altre patologie (pancreatite cronica, emocromatosi, acromegalia, sindrome di Cushing).

Diabete Mellito: definizione (2) Si riconoscono due tipi di diabete mellito primario ØDiabete mellito di tipo 1 (DM-1): immunomediato, caratterizzato dalla distruzione delle cellule B pancreatiche, che comprende circa il 10% di tutte le forme. Precedentemente noto come “insulin dependend diabetes mellitus (IDDM)”. ØDiabete mellito di tipo 2 (DM-2): A patogenesi non immunitaria, per lo piu’ dovuto ad alterata risposta all’insulina. Detto anche non chetosico. Comprende circa il 90% di tutte le forme di diabete mellito.
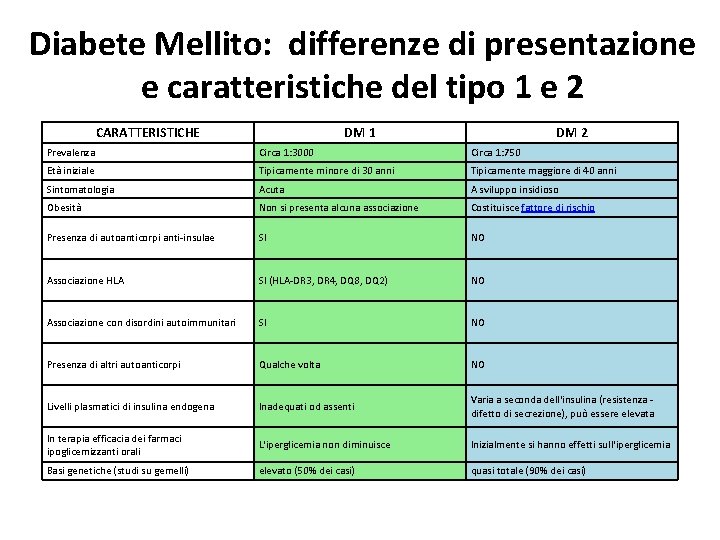
Diabete Mellito: differenze di presentazione e caratteristiche del tipo 1 e 2 CARATTERISTICHE DM 1 DM 2 Prevalenza Circa 1: 3000 Circa 1: 750 Età iniziale Tipicamente minore di 30 anni Tipicamente maggiore di 40 anni Sintomatologia Acuta A sviluppo insidioso Obesità Non si presenta alcuna associazione Costituisce fattore di rischio Presenza di autoanticorpi anti-insulae SI NO Associazione HLA SI (HLA-DR 3, DR 4, DQ 8, DQ 2) NO Associazione con disordini autoimmunitari SI NO Presenza di altri autoanticorpi Qualche volta NO Livelli plasmatici di insulina endogena Inadequati od assenti Varia a seconda dell'insulina (resistenza - difetto di secrezione), può essere elevata In terapia efficacia dei farmaci ipoglicemizzanti orali L'iperglicemia non diminuisce Inizialmente si hanno effetti sull'iperglicemia Basi genetiche (studi su gemelli) elevato (50% dei casi) quasi totale (90% dei casi)

Diabete mellito di tipo 1 (1) ØA base autoimmune ØInfiltrazione di linfociti T CD 4+ e CD 8+ e macrofagi nelle isole pancreatiche ØPresenza di autoanticorpi verso le cellule dell’isole di Langherans ØDistruzione delle cellule-b pancreatiche comportando la insulino deficienza ØEziopatologia multifattoriale: §Basi Genetiche: -50% di presenza in gemelli, §Fattori ambientali: -associazione HLA, -associazione con ed altri geni della risposta immune e del metabolismo dell’insulina -infezioni (virus coxackie, rubella etc), -reattivita’ a proteine di origine alimentare

Diabete mellito di tipo 1 (2) Le caratteristiche epidemiologiche permettono di distinguere due tipi principali DM 1 a: -rapporto F: M circa 1: 1. 2, DM 1 b: -eta’ di esordio <15 -20 anni, -occasionale associazione con altre patologie autoimmuni, -presenza di pochi altri autoanticorpi organo specifici -rapporto F: M 5: 1, -eta’ di esordio qualsiasi, -presenza di altri disordini, -autoimmunitari (tiroide, anemia perniciosa), -presenza di molti altri autoanticorpi organo specifici

Eziopatologia del Diabete mellito di tipo 1

Evidenze delle associazioni genetiche nella eziopatogenesi del diabete mellito di tipo 1 ØIl rischio di sviluppare DM 1 nella popolazione generale e’ di circa 0. 3%-0. 5%. Al contrario il rischio tra familiari e’: § 30 -50% nei gemelli omozigoti § 5 -10% nei gemelli dizigotici §similmente tra fratelli il rischio e’ approsimativamente del 6% ØUna forte associazione (Rischio Relativo >6) e’ stata trovata con alcune varianti alleliche del HLA di classe II §Inizialmente trovati associati HLA-DR 3 e –DR 4 ed eterozigosi per DR 3/DR 4, §Associazione principale con HLA-DQ 2 e -DQ 8 che sono in linkage disequilibrium con DR 3 e DR 4 §Rischio relativo alleli associati HLA-DQ>DR>DP>classe I
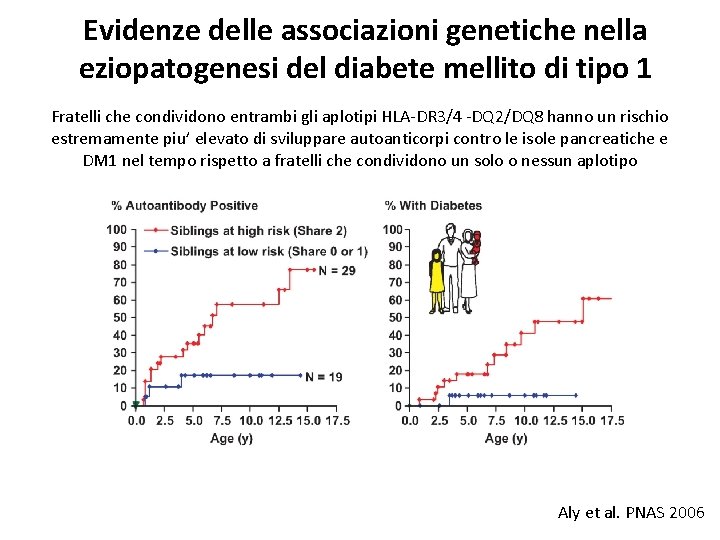
Evidenze delle associazioni genetiche nella eziopatogenesi del diabete mellito di tipo 1 Fratelli che condividono entrambi gli aplotipi HLA-DR 3/4 -DQ 2/DQ 8 hanno un rischio estremamente piu’ elevato di sviluppare autoanticorpi contro le isole pancreatiche e DM 1 nel tempo rispetto a fratelli che condividono un solo o nessun aplotipo Aly et al. PNAS 2006
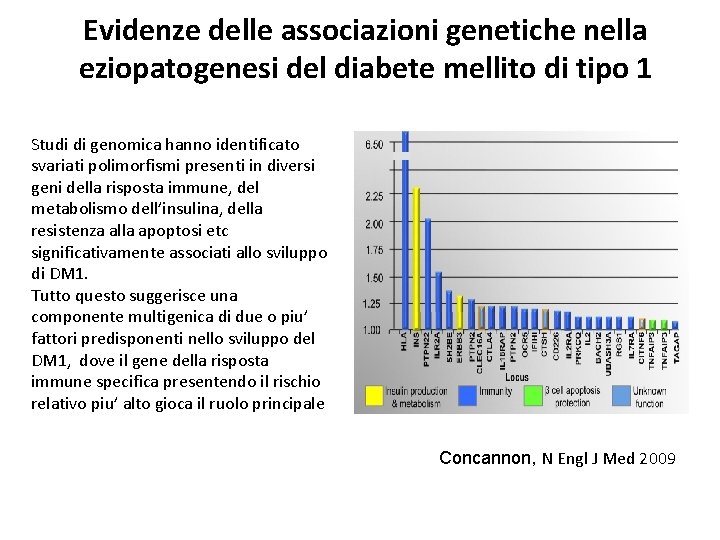
Evidenze delle associazioni genetiche nella eziopatogenesi del diabete mellito di tipo 1 Studi di genomica hanno identificato svariati polimorfismi presenti in diversi geni della risposta immune, del metabolismo dell’insulina, della resistenza alla apoptosi etc significativamente associati allo sviluppo di DM 1. Tutto questo suggerisce una componente multigenica di due o piu’ fattori predisponenti nello sviluppo del DM 1, dove il gene della risposta immune specifica presentendo il rischio relativo piu’ alto gioca il ruolo principale Concannon, N Engl J Med 2009

Evidenze della presenza di fattori ambientali nella eziopatogenesi del diabete mellito di tipo 1 ØUna componente ambientale nello sviluppo del DM 1 e’ evidente dagli studi di genetica classica dove i gemelli omozigoti sviluppano entrambi DM 1 solo in circa il 50% dei casi ØStudi di popolazione evidenziano che soggetti provenienti da aree a bassa frequenza di DM 1, quando vivono in aree a maggior frequenza presentano lo stesso rischio e la stessa proporzione di incidenza
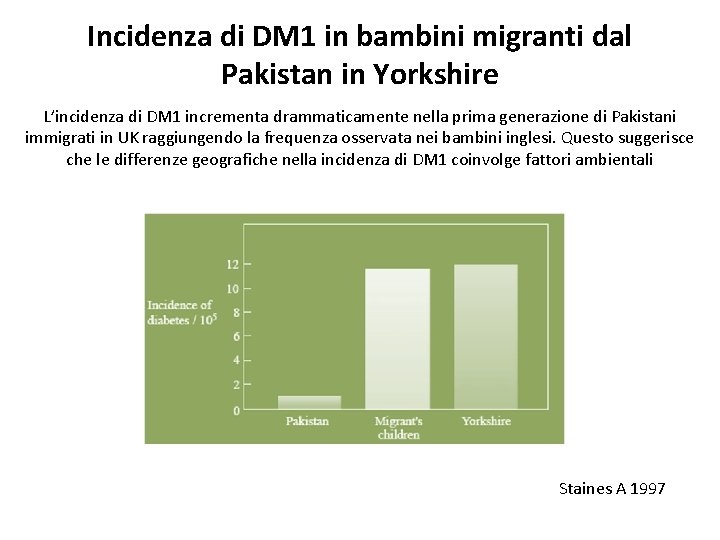
Incidenza di DM 1 in bambini migranti dal Pakistan in Yorkshire L’incidenza di DM 1 incrementa drammaticamente nella prima generazione di Pakistani immigrati in UK raggiungendo la frequenza osservata nei bambini inglesi. Questo suggerisce che le differenze geografiche nella incidenza di DM 1 coinvolge fattori ambientali Staines A 1997

Evidenze della presenza di fattori ambientali nella eziopatogenesi del diabete mellito di tipo 1 ØUna componente ambientale nello sviluppo del DM 1 e’ evidente dagli studi di genetica classica dove i gemelli omozigoti sviluppano entrambi DM 1 solo in circa il 50% dei casi ØStudi di popolazione evidenziano che soggetti provenienti da aree a bassa frequenza di DM 1, quando vivono in aree a maggior frequenza presentano lo stesso rischio e la stessa proporzione di incidenza, suggerendo che le differenze geografiche nella incidenza di DM 1 coinvolge fattori ambientali ØCome per altre patologie autoimmuni, anche per il DM 1 e’ stata formulata “l’ipotesi dell’igiene”. Alla riduzione dell’incidenza di diverse patologie infettive e verosimilmente alla ridotta circolazione di batteri patogeni per il miglioramento della condizioni igieniche si e’ osservato un aumento delle patologie autoimmunitarie
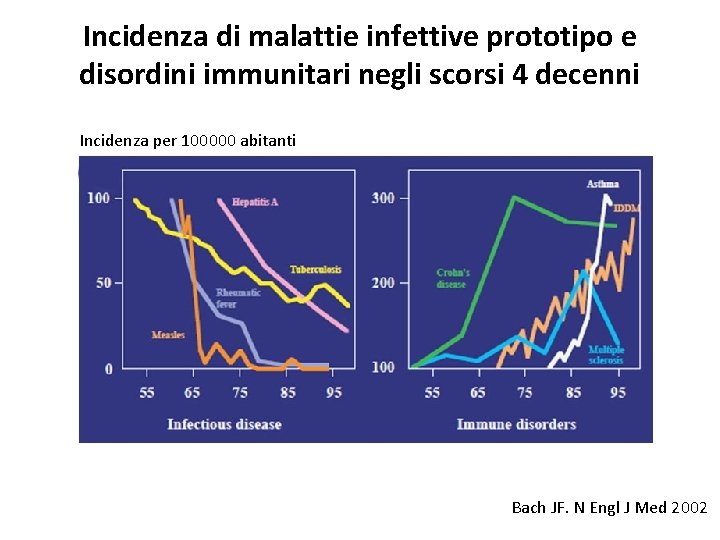
Incidenza di malattie infettive prototipo e disordini immunitari negli scorsi 4 decenni Incidenza per 100000 abitanti Bach JF. N Engl J Med 2002

Evidenze della presenza di fattori ambientali nella eziopatogenesi del diabete mellito di tipo 1 ØUna componente ambientale nello sviluppo del DM 1 e’ evidente dagli studi di genetica classica dove i gemelli omozigoti sviluppano entrambi DM 1 solo in circa il 50% dei casi ØStudi di popolazione evidenziano che soggetti provenienti da aree a bassa frequenza di DM 1, quando vivono in aree a maggior frequenza presentano lo stesso rischio e la stessa proporzione di incidenza, suggerendo che le differenze geografiche nella incidenza di DM 1 coinvolge fattori ambientali ØCome per altre patologie autoimmuni, anche per il DM 1 e’ stata formulata “l’ipotesi dell’igiene”. Alla riduzione dell’incidenza di diverse patologie infettive e verosimilmente alla ridotta circolazione di batteri patogeni per il miglioramento della condizioni igieniche si e’ osservato un aumento delle patologie autoimmunitarie ØDiverse infezioni virali sono state chiamate in causa quali fattore scatenante DM 1 (virus coxackie, rubella etc). Ad esempio nel modello del ratto, l’infezione da Kilham rat virus (KRV) induce diabete in ceppi di ratto resistenti. ØE’ ora anche noto che diversi ceppi di ratto, tutti con lo stesso MHC di classe II, sviluppano diabete quando infettati con diversi virus o quando stimolati con agonisti dei Toll Like Receptors (TLR). ØLa reazione avversa a diversi alimenti (es: latte di mucca) oppure l’introduzione precoce di cereali nella dieta, sono stati indicati come fattori predisponenti DM 1

Immunopatogenesi del diabete mellito di tipo 1

Immunopatogenesi del DM 1 Sommario eventi Il diabete mellito di tipo 1 e’ un malattia autoimmune organo-specifica. Quindi I meccanismi di sviluppo sono comuni a quella di altre patologie autoimmunitarie: ØIn un background di predisposizione genetica vi e’ un evento scatenante che abbatte la tollerenza periferica contro le cellule b del pancreas; ØVi e’ una risposta immunitaria specifica diretta contro le cellule b del pancreas; ØSi osserva un infiltrato di linfociti T (CD 4+ e CD 8+) e macrofagi nelle insule pancreatiche; ØSi ha produzione di autoanticorpi contro le isole pancreatiche ØNe consegue la distruzione progressiva delle cellule b ed il crollo la produzione di insulina; ØLe manifestazioni cliniche diventano evidenti quando la distruzione delle cellule b e’ quasi totale, in quanto inizialmente una ipertrofia compensatoria delle cellule b ancora attive permette la secrezione di una quantita’ sufficiente di insulina ed il controllo dei livelli ematici di glucosio.
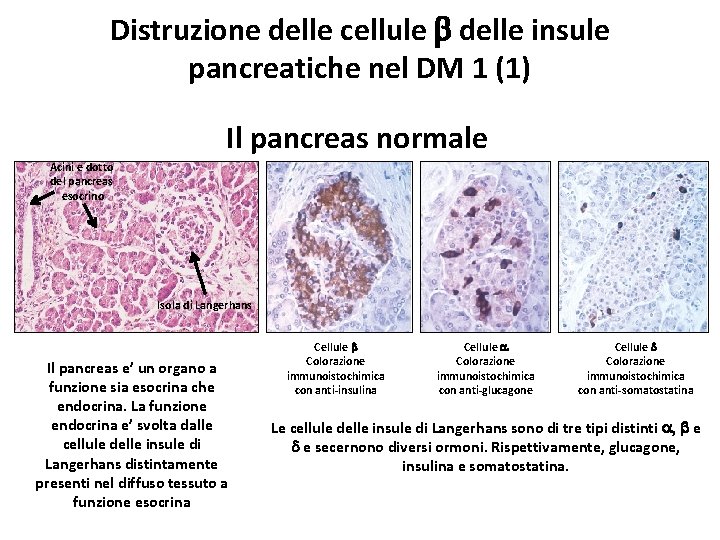
Distruzione delle cellule b delle insule pancreatiche nel DM 1 (1) Il pancreas normale Acini e dotto del pancreas esocrino Isola di Langerhans Il pancreas e’ un organo a funzione sia esocrina che endocrina. La funzione endocrina e’ svolta dalle cellule delle insule di Langerhans distintamente presenti nel diffuso tessuto a funzione esocrina Cellule b Colorazione immunoistochimica con anti-insulina Cellule a Colorazione immunoistochimica con anti-glucagone Cellule d Colorazione immunoistochimica con anti-somatostatina Le cellule delle insule di Langerhans sono di tre tipi distinti a, b e d e secernono diversi ormoni. Rispettivamente, glucagone, insulina e somatostatina.
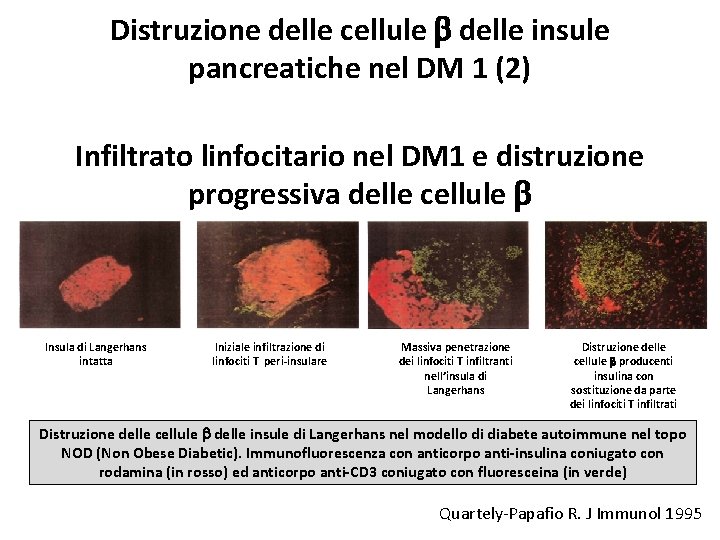
Distruzione delle cellule b delle insule pancreatiche nel DM 1 (2) Infiltrato linfocitario nel DM 1 e distruzione progressiva delle cellule b Insula di Langerhans intatta Iniziale infiltrazione di linfociti T peri-insulare Massiva penetrazione dei linfociti T infiltranti nell’insula di Langerhans Distruzione delle cellule b producenti insulina con sostituzione da parte dei linfociti T infiltrati Distruzione delle cellule b delle insule di Langerhans nel modello di diabete autoimmune nel topo NOD (Non Obese Diabetic). Immunofluorescenza con anticorpo anti-insulina coniugato con rodamina (in rosso) ed anticorpo anti-CD 3 coniugato con fluoresceina (in verde) Quartely-Papafio R. J Immunol 1995
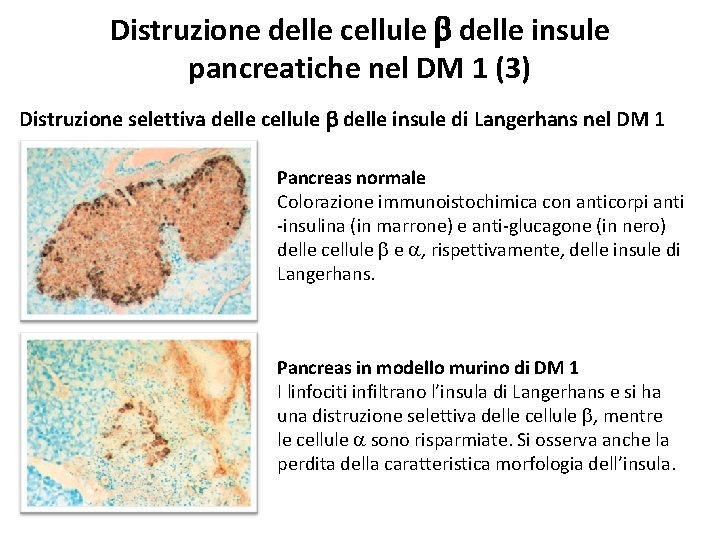
Distruzione delle cellule b delle insule pancreatiche nel DM 1 (3) Distruzione selettiva delle cellule b delle insule di Langerhans nel DM 1 Pancreas normale Colorazione immunoistochimica con anticorpi anti -insulina (in marrone) e anti-glucagone (in nero) delle cellule b e a, rispettivamente, delle insule di Langerhans. Pancreas in modello murino di DM 1 I linfociti infiltrano l’insula di Langerhans e si ha una distruzione selettiva delle cellule b, mentre le cellule a sono risparmiate. Si osserva anche la perdita della caratteristica morfologia dell’insula.
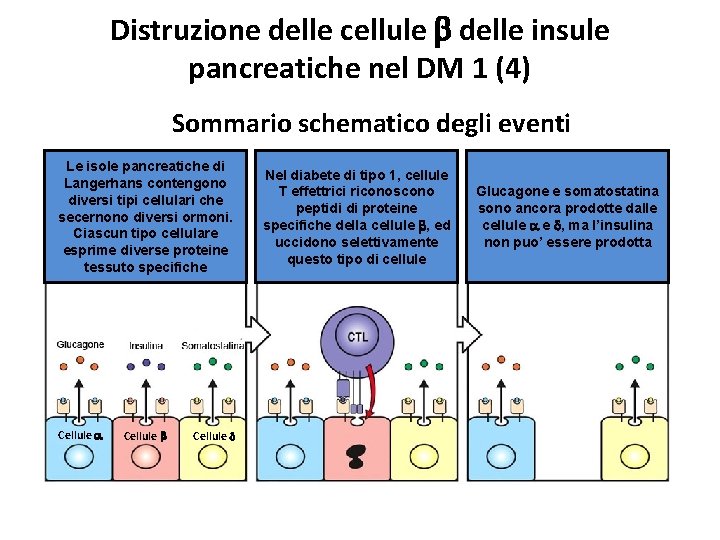
Distruzione delle cellule b delle insule pancreatiche nel DM 1 (4) Sommario schematico degli eventi Le isole pancreatiche di Langerhans contengono diversi tipi cellulari che secernono diversi ormoni. Ciascun tipo cellulare esprime diverse proteine tessuto specifiche Cellule a Cellule b Cellule d Nel diabete di tipo 1, cellule T effettrici riconoscono peptidi di proteine specifiche della cellule b, ed uccidono selettivamente questo tipo di cellule Glucagone e somatostatina sono ancora prodotte dalle cellule a e d, ma l’insulina non puo’ essere prodotta
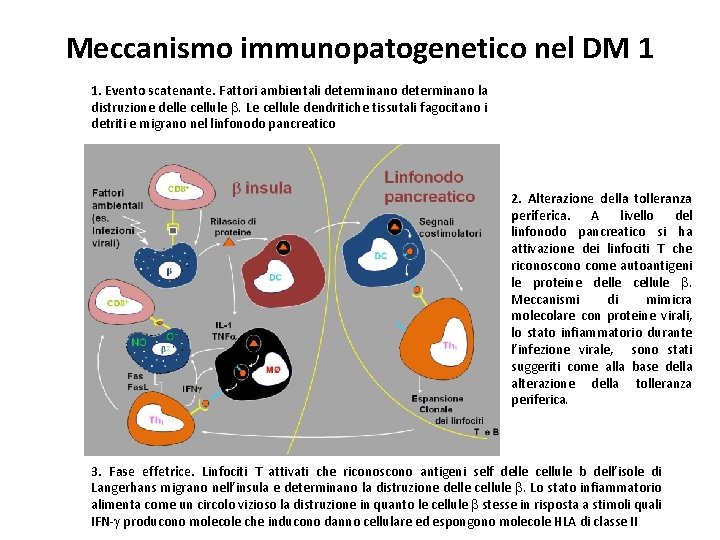
Meccanismo immunopatogenetico nel DM 1 1. Evento scatenante. Fattori ambientali determinano la distruzione delle cellule b. Le cellule dendritiche tissutali fagocitano i detriti e migrano nel linfonodo pancreatico 2. Alterazione della tolleranza periferica. A livello del linfonodo pancreatico si ha attivazione dei linfociti T che riconoscono come autoantigeni le proteine delle cellule b. Meccanismi di mimicra molecolare con proteine virali, lo stato infiammatorio durante l’infezione virale, sono stati suggeriti come alla base della alterazione della tolleranza periferica. 3. Fase effetrice. Linfociti T attivati che riconoscono antigeni self delle cellule b dell’isole di Langerhans migrano nell’insula e determinano la distruzione delle cellule b. Lo stato infiammatorio alimenta come un circolo vizioso la distruzione in quanto le cellule b stesse in risposta a stimoli quali IFN-g producono molecole che inducono danno cellulare ed espongono molecole HLA di classe II
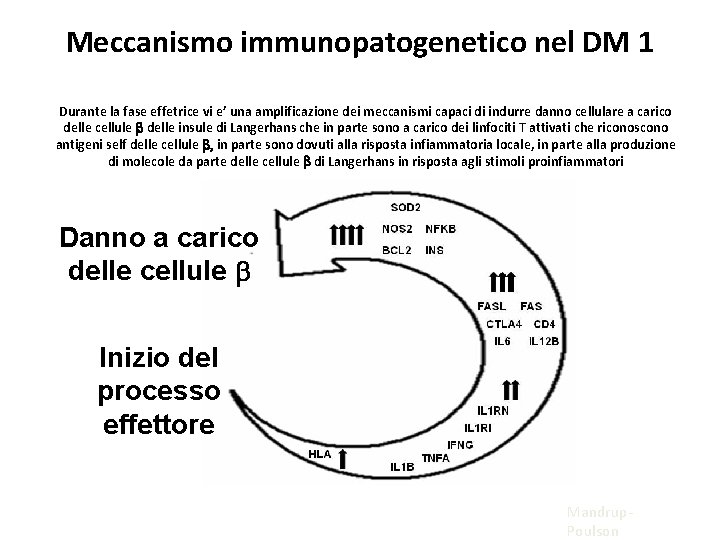
Meccanismo immunopatogenetico nel DM 1 Durante la fase effetrice vi e’ una amplificazione dei meccanismi capaci di indurre danno cellulare a carico delle cellule b delle insule di Langerhans che in parte sono a carico dei linfociti T attivati che riconoscono antigeni self delle cellule b, in parte sono dovuti alla risposta infiammatoria locale, in parte alla produzione di molecole da parte delle cellule b di Langerhans in risposta agli stimoli proinfiammatori Danno a carico delle cellule b Inizio del processo effettore Mandrup. Poulson
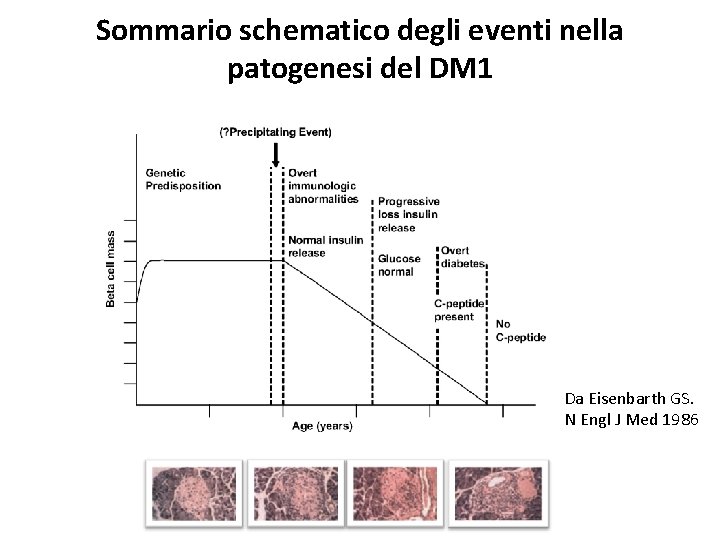
Sommario schematico degli eventi nella patogenesi del DM 1 Da Eisenbarth GS. N Engl J Med 1986

Autoanticorpi nel DM 1 ØDiversi autoantigeni specifici per il DM 1 sono stati identificati. ØGli autoanticorpi “classicamente denominati” anti isole pancreatiche sono un mix di autoanticorpi di cui 4 antigeni principali sono stati definiti e validati in workshop internazionali: §Insulina, §La Acido Glutammico Decarbossilasi [Glutamic Acid Decarboxylase (GAD o GAD 65)], §Una Tirosin Fosfatasi denominata Islet antigen 2 (IA-2), §Trasportatore di zinco specifico delle cellule b [islet-specific zinc transporter (Znt 8)] recentemente identificato. ØSono disponibili test immunochimici specifici per determinare il livello di ciascun di questi anticorpi di cui e’ possibile farne un uso prognostico.

Autoantigeni per linfociti T nel DM 1 ØGli stessi antigeni target degli anticorpi sono il maggior target del riconoscimento dei linfociti T insieme alla “islet-specific glucose-6 -phosphatase catalytic subunitrelated protein” (IGRP) ed al precursore dell’insulina [Pre. Pro-Insuline (PPI)] ØNei modelli murini l’insulina funziona da antigene principale per i linfociti T CD 4 con oltre il 90% delle cellule infiltranti diretti contro il peptide 9 -23 dell’insulina. Da questo riconoscimento vi e’ una attivazione “downstream” sia dei CD 4 che dei CD 8 specifici sia per l’insulina ed altri antigeni delle cellule b (GAD, IA-2 e IGRP) ØNell’uomo sono stati riscontrati sia linfociti T CD 4 -specifici per l’insulina e GAD che linfociti T CD 8 -specifici per PPI, IA-2, Insulina e IGRP ØIl presenza di linfociti T CD 8 circolanti diretti contro PPI, IA-2, Insulina e IGRP e’ stato osservato in soggetti con recente esordio di DM 1
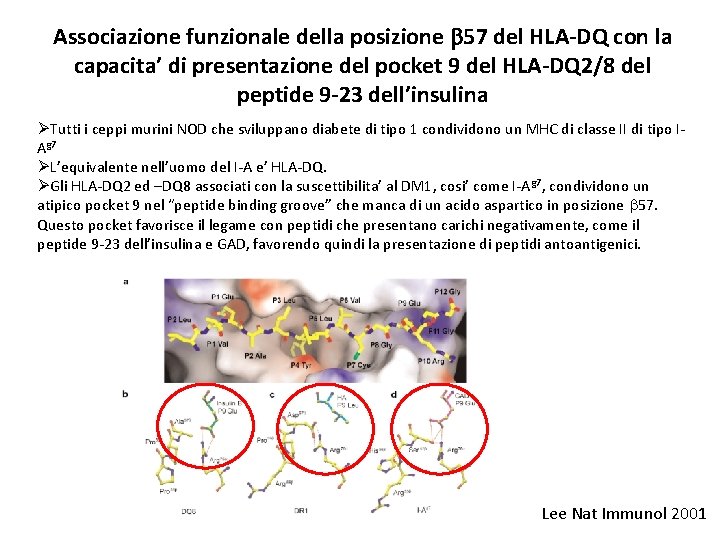
Associazione funzionale della posizione b 57 del HLA-DQ con la capacita’ di presentazione del pocket 9 del HLA-DQ 2/8 del peptide 9 -23 dell’insulina ØTutti i ceppi murini NOD che sviluppano diabete di tipo 1 condividono un MHC di classe II di tipo IAg 7 ØL’equivalente nell’uomo del I-A e’ HLA-DQ. ØGli HLA-DQ 2 ed –DQ 8 associati con la suscettibilita’ al DM 1, cosi’ come I-A g 7, condividono un atipico pocket 9 nel “peptide binding groove” che manca di un acido aspartico in posizione b 57. Questo pocket favorisce il legame con peptidi che presentano carichi negativamente, come il peptide 9 -23 dell’insulina e GAD, favorendo quindi la presentazione di peptidi antoantigenici. Lee Nat Immunol 2001

Complicazioni del Diabete mellito di tipo 1
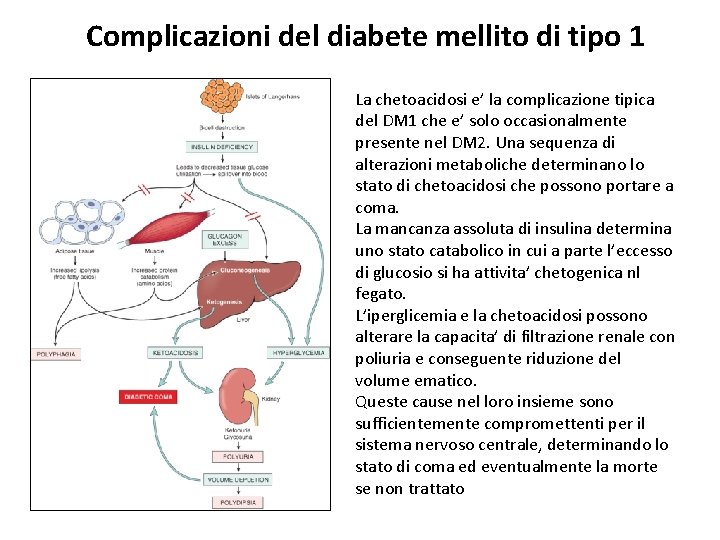
Complicazioni del diabete mellito di tipo 1 La chetoacidosi e’ la complicazione tipica del DM 1 che e’ solo occasionalmente presente nel DM 2. Una sequenza di alterazioni metaboliche determinano lo stato di chetoacidosi che possono portare a coma. La mancanza assoluta di insulina determina uno stato catabolico in cui a parte l’eccesso di glucosio si ha attivita’ chetogenica nl fegato. L’iperglicemia e la chetoacidosi possono alterare la capacita’ di filtrazione renale con poliuria e conseguente riduzione del volume ematico. Queste cause nel loro insieme sono sufficientemente compromettenti per il sistema nervoso centrale, determinando lo stato di coma ed eventualmente la morte se non trattato
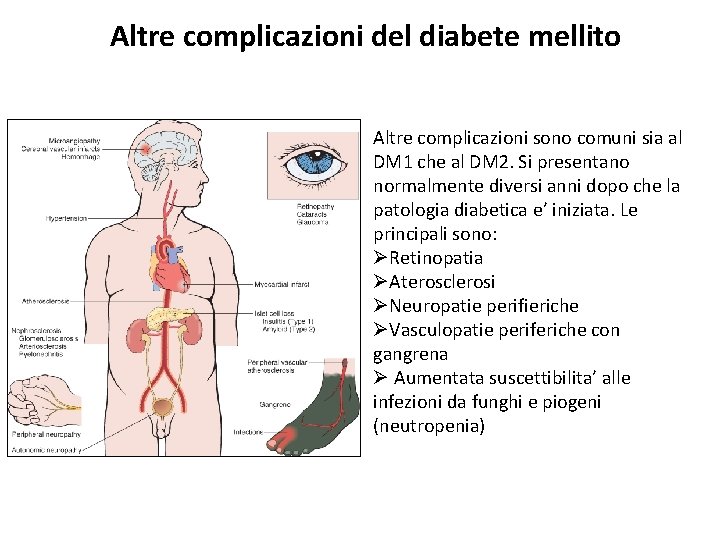
Altre complicazioni del diabete mellito Altre complicazioni sono comuni sia al DM 1 che al DM 2. Si presentano normalmente diversi anni dopo che la patologia diabetica e’ iniziata. Le principali sono: ØRetinopatia ØAterosclerosi ØNeuropatie perifieriche ØVasculopatie periferiche con gangrena Ø Aumentata suscettibilita’ alle infezioni da funghi e piogeni (neutropenia)

Prevenzione del Diabete mellito di tipo 1
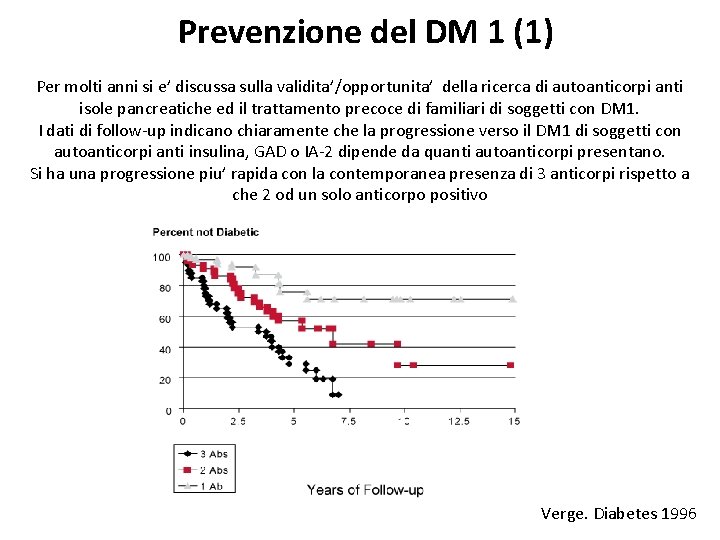
Prevenzione del DM 1 (1) Per molti anni si e’ discussa sulla validita’/opportunita’ della ricerca di autoanticorpi anti isole pancreatiche ed il trattamento precoce di familiari di soggetti con DM 1. I dati di follow-up indicano chiaramente che la progressione verso il DM 1 di soggetti con autoanticorpi anti insulina, GAD o IA-2 dipende da quanti autoanticorpi presentano. Si ha una progressione piu’ rapida con la contemporanea presenza di 3 anticorpi rispetto a che 2 od un solo anticorpo positivo Verge. Diabetes 1996
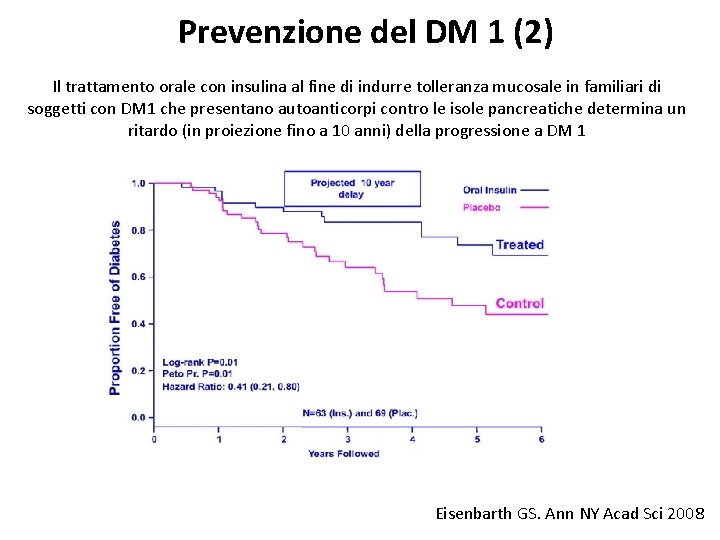
Prevenzione del DM 1 (2) Il trattamento orale con insulina al fine di indurre tolleranza mucosale in familiari di soggetti con DM 1 che presentano autoanticorpi contro le isole pancreatiche determina un ritardo (in proiezione fino a 10 anni) della progressione a DM 1 Eisenbarth GS. Ann NY Acad Sci 2008
- Slides: 33