Pathogenese des Typ2 Diabetes Erhhte hepatische Glukoseproduktion Periphere
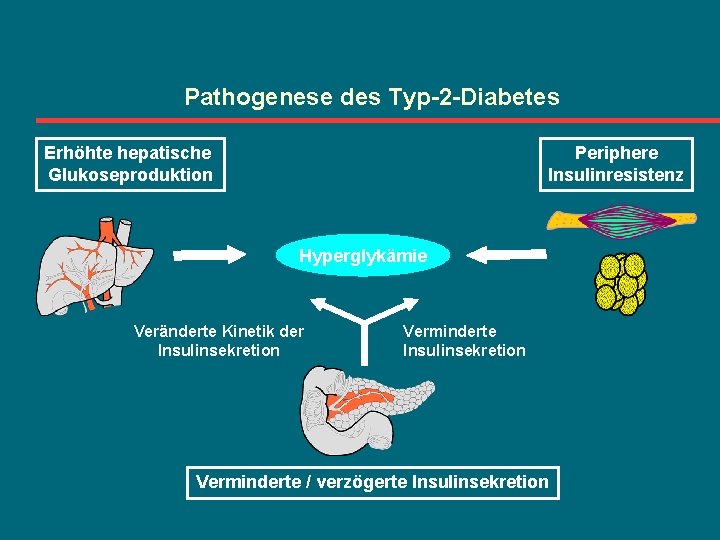
Pathogenese des Typ-2 -Diabetes Erhöhte hepatische Glukoseproduktion Periphere Insulinresistenz Hyperglykämie Veränderte Kinetik der Insulinsekretion Verminderte / verzögerte Insulinsekretion
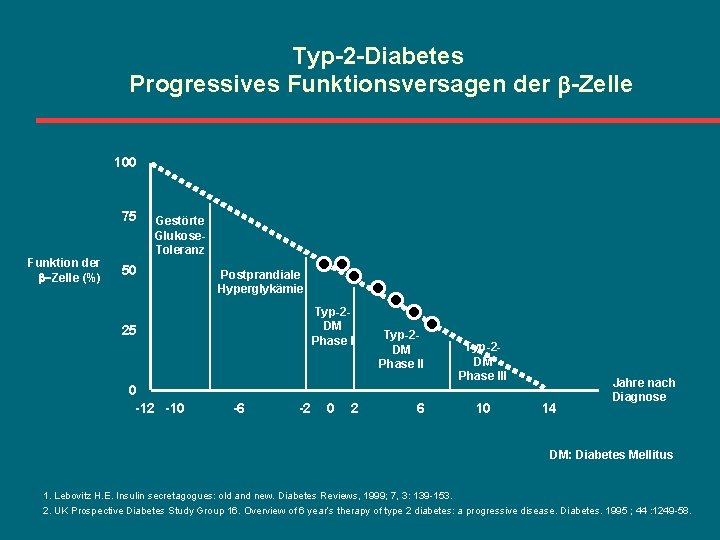
Typ-2 -Diabetes Progressives Funktionsversagen der -Zelle 100 75 Funktion der -Zelle (%) Gestörte Glukose. Toleranz 50 Postprandiale Hyperglykämie Typ-2 DM Phase I 25 0 -12 -10 -6 -2 0 2 Typ-2 DM Phase II 6 Typ-2 DM Phase III 10 14 Jahre nach Diagnose DM: Diabetes Mellitus 1. Lebovitz H. E. Insulin secretagogues: old and new. Diabetes Reviews, 1999; 7, 3: 139 -153. 2. UK Prospective Diabetes Study Group 16. Overview of 6 year’s therapy of type 2 diabetes: a progressive disease. Diabetes. 1995 ; 44 : 1249 -58.
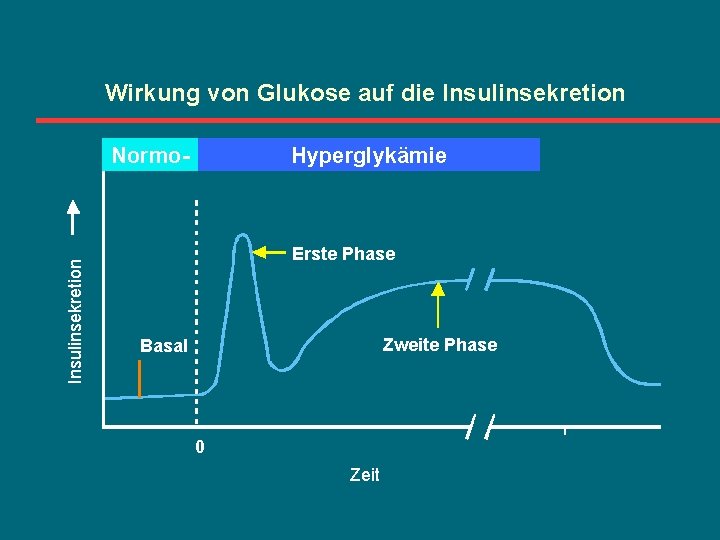
Wirkung von Glukose auf die Insulinsekretion Normo- Hyperglykämie Erste Phase Zweite Phase Basal 0 Zeit

Biphasische Insulinsekretion zur Kontrolle des Glukosemetabolismus bei Nicht-Diabetikern l Erste Phase der Insulinsekretion – Innerhalb der ersten 5 -10 Minuten nach Beginn der Mahlzeit – Unterdrückung der endogenen Glukoseproduktion in der Leber – Sensibilisierung der Körperzellen für die Aufnahme der exogenen Glukose aus der Nahrung l Zweite Phase der Insulinsekretion – Bedarfsgerechte Freisetzung von Insulin aus der ß-Zelle – Periphere Glukoseaufnahme aus der Blutbahn Davies, Diabetes Med 1994; Swinburn, Metabolism 1995; Butler, Diabetes 1991; Kahn SE et al. , Internationnal Textbook of DM, 1997
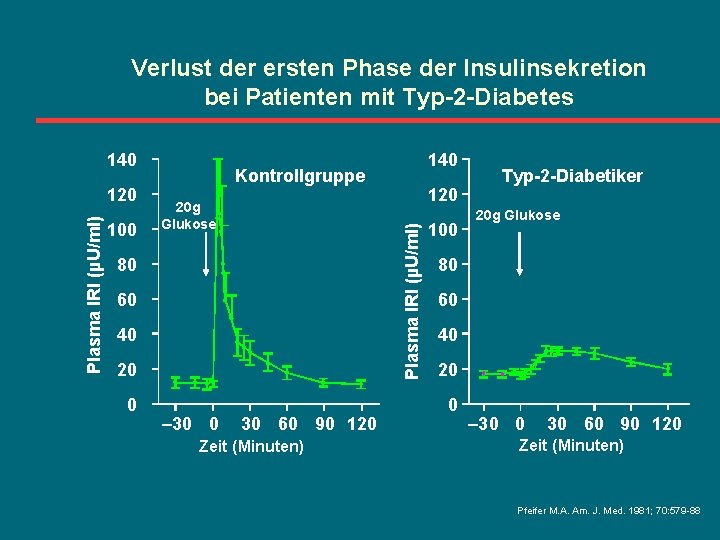
Verlust der ersten Phase der Insulinsekretion bei Patienten mit Typ-2 -Diabetes 140 100 Kontrollgruppe 20 g Glukose 80 60 40 20 0 – 30 0 120 Plasma IRI (µU/ml) 120 140 30 60 90 120 Zeit (Minuten) 100 Typ-2 -Diabetiker 20 g Glukose 80 60 40 20 0 – 30 0 30 60 90 120 Zeit (Minuten) Pfeifer M. A. Am. J. Med. 1981; 70: 579 -88
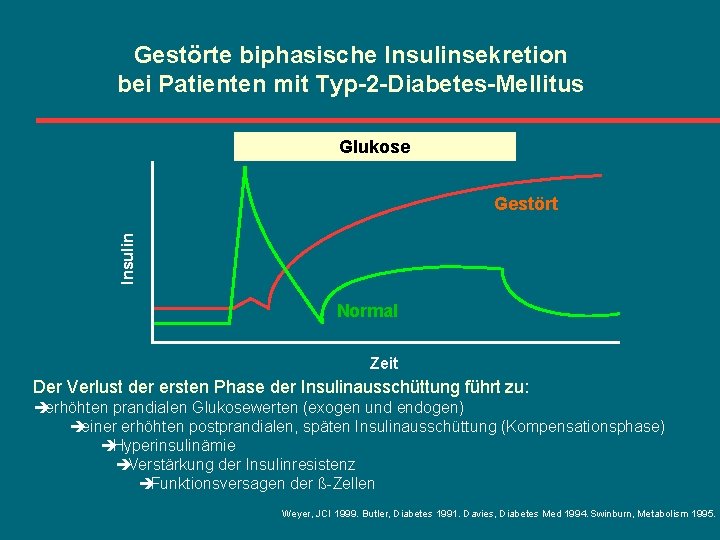
Gestörte biphasische Insulinsekretion bei Patienten mit Typ-2 -Diabetes-Mellitus Glukose Insulin Gestört Normal Zeit Der Verlust der ersten Phase der Insulinausschüttung führt zu: èerhöhten prandialen Glukosewerten (exogen und endogen) èeiner erhöhten postprandialen, späten Insulinausschüttung (Kompensationsphase) èHyperinsulinämie èVerstärkung der Insulinresistenz èFunktionsversagen der ß-Zellen Weyer, JCI 1999. Butler, Diabetes 1991. Davies, Diabetes Med 1994. Swinburn, Metabolism 1995.
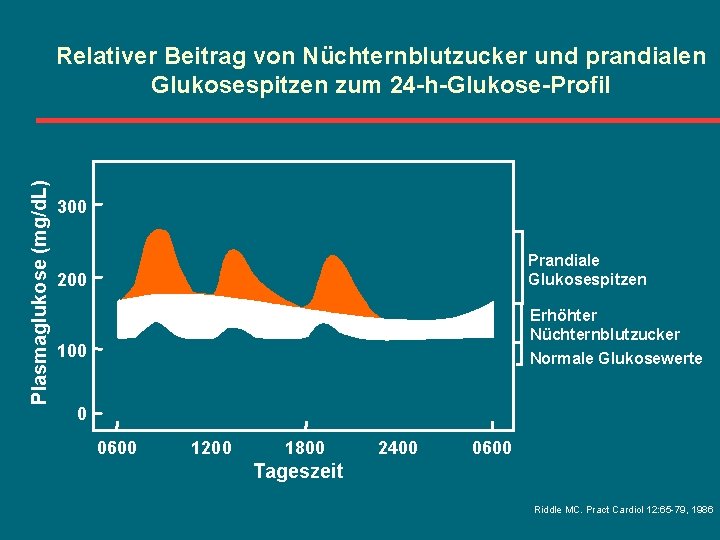
Plasmaglukose (mg/d. L) Relativer Beitrag von Nüchternblutzucker und prandialen Glukosespitzen zum 24 -h-Glukose-Profil 300 Prandiale Glukosespitzen 200 Erhöhter Nüchternblutzucker 100 Normale Glukosewerte 0 0600 1200 1800 2400 0600 Tageszeit Riddle MC. Pract Cardiol 12: 65 -79, 1986
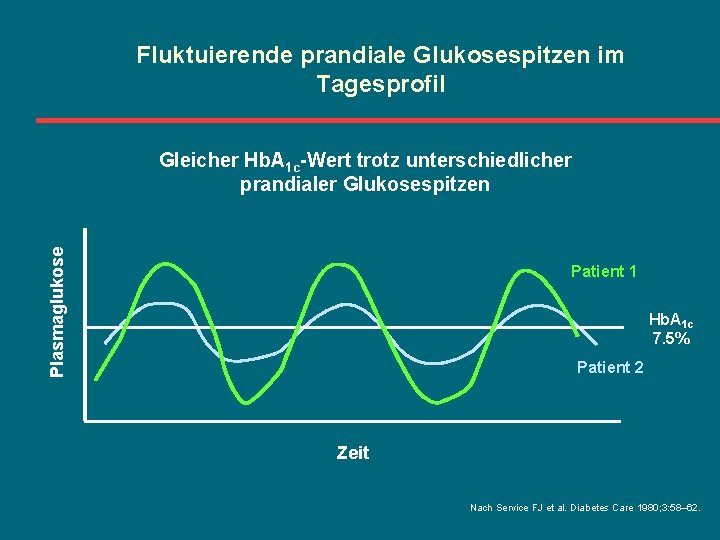
Fluktuierende prandiale Glukosespitzen im Tagesprofil Plasmaglukose Gleicher Hb. A 1 c-Wert trotz unterschiedlicher prandialer Glukosespitzen Patient 1 Hb. A 1 c 7. 5% Patient 2 Zeit Nach Service FJ et al. Diabetes Care 1980; 3: 58– 62.

Kardiovaskuläre Mortalität beim Typ-2 -Diabetes Epidemiologische Daten Prandiale Glukosespitzen sind ein unabhängiger Risikofaktor für kardiovaskuläre Mortalität • Diabetes Interventions Study, Diabetologia 1996 • Honolulu Heart Study, Diabetes Care 1997 • Rancho Bernardo Study, Diabetes Care 1998 • Whitehall, Paris, Helsinki Study, Diabetes Care 1998 • Paris Prospective Study, Diabetes Care 1999 • Hoorn Study, Diabetologia 1999 • Pacific and Indian Ocean Study, Diabetologia 1999 • Funagata Diabetes Study, Diabetes Care 1999 • DECODE-Study-Group, The Lancet 1999

DECODE: Diagnose von Diabetes nach ADA und / oder WHO Kriterien ADA n = 654 ADA und WHO n = 489 WHO n = 522 Diagnostiziert als Typ-2 -Diabetiker: • nur 65% durch alleinige Messung der Nüchternplasmaglukosewerte • 100% durch zusätzliche Messung der postprandialen Plasmaglukosewerte Nach DECODE Study Group. Br Med J 1998; 317: 371– 375.
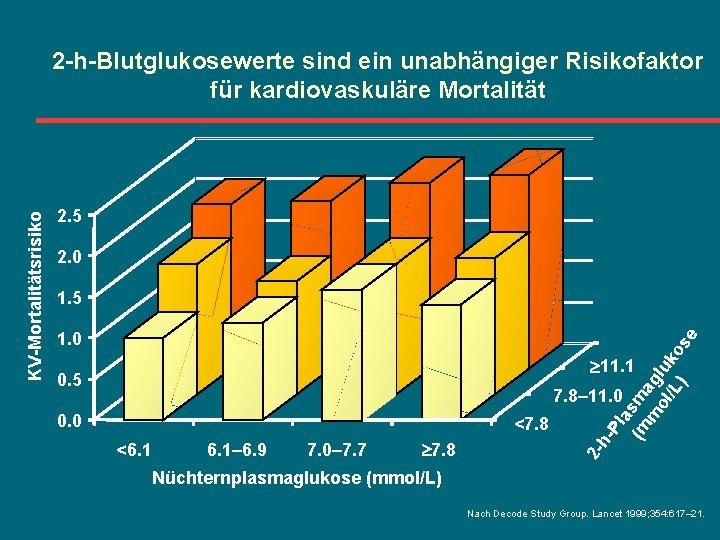
2. 5 2. 0 1. 5 a (m sm m agl ol uk /L ) ose 1. 0 ³ 11. 1 0. 5 0. 0 <6. 1– 6. 9 7. 0– 7. 7 ³ 7. 8 h- <7. 8 Pl 7. 8– 11. 0 2 - KV-Mortalitätsrisiko 2 -h-Blutglukosewerte sind ein unabhängiger Risikofaktor für kardiovaskuläre Mortalität Nüchternplasmaglukose (mmol/L) Nach Decode Study Group. Lancet 1999; 354: 617– 21.
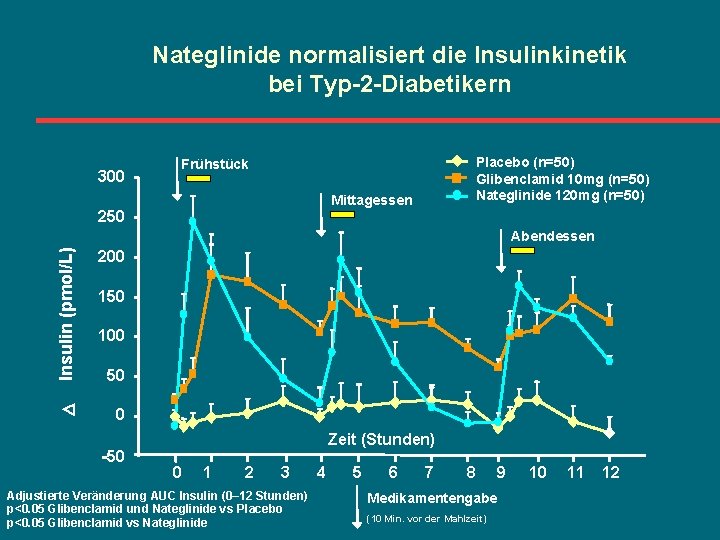
Nateglinide normalisiert die Insulinkinetik bei Typ-2 -Diabetikern 300 Placebo (n=50) Glibenclamid 10 mg (n=50) Nateglinide 120 mg (n=50) Frühstück Mittagessen 250 Insulin (pmol/L) Abendessen 200 150 100 50 0 -50 Zeit (Stunden) 0 1 2 3 Adjustierte Veränderung AUC Insulin (0– 12 Stunden) p<0. 05 Glibenclamid und Nateglinide vs Placebo p<0. 05 Glibenclamid vs Nateglinide 4 5 6 7 8 Medikamentengabe (10 Min. vor der Mahlzeit) 9 10 11 12
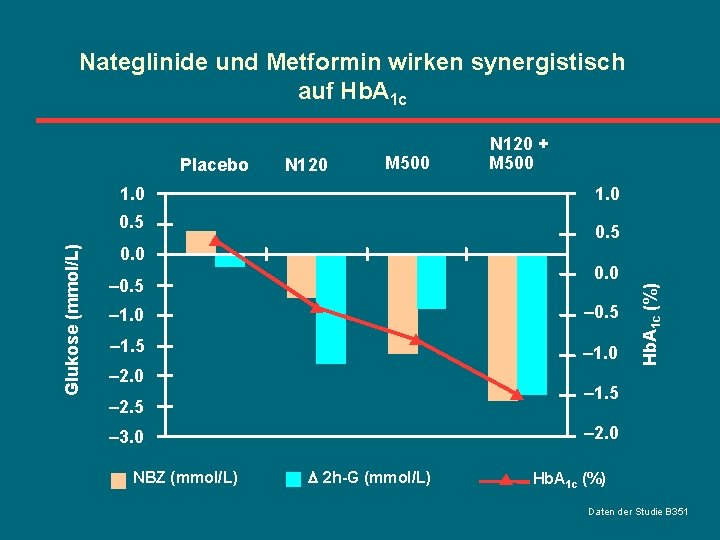
Nateglinide und Metformin wirken synergistisch auf Hb. A 1 c N 120 M 500 1. 0 Glukose (mmol/L) 0. 5 0. 0 – 0. 5 – 1. 0 – 2. 0 – 1. 5 – 2. 0 – 3. 0 NBZ (mmol/L) Hb. A 1 c (%) Placebo N 120 + M 500 2 h-G (mmol/L) Hb. A 1 c (%) Daten der Studie B 351
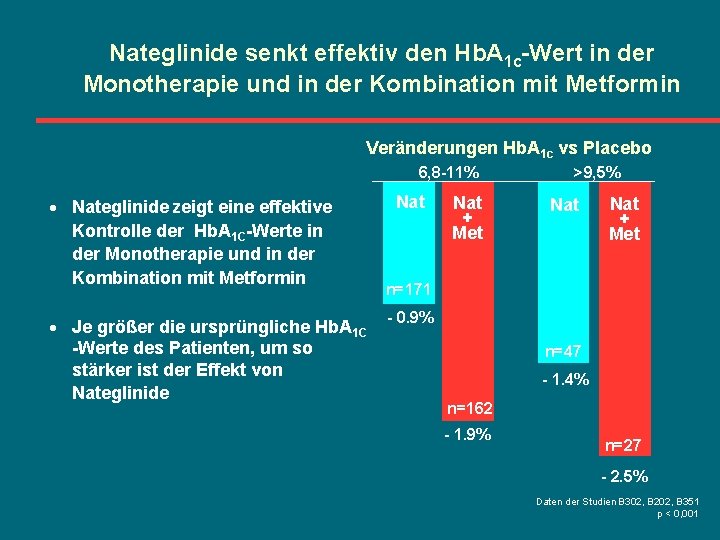
Nateglinide senkt effektiv den Hb. A 1 c-Wert in der Monotherapie und in der Kombination mit Metformin Veränderungen Hb. A 1 c vs Placebo 6, 8 -11% · Nateglinide zeigt eine effektive Kontrolle der Hb. A 1 C-Werte in der Monotherapie und in der Kombination mit Metformin · Je größer die ursprüngliche Hb. A 1 C -Werte des Patienten, um so stärker ist der Effekt von Nateglinide Nat + Met >9, 5% Nat + Met n=171 - 0. 9% n=47 - 1. 4% n=162 - 1. 9% n=27 - 2. 5% Daten der Studien B 302, B 202, B 351 p < 0, 001

Take home messages • Typ-2 -Diabetes mellitus ist die Kombination von zwei Pathologien - Periphere Insulinresistenz und - Verlust der frühen Phase der Insulinsekretion. • Postprandiale Glukosespitzen sind ein unabhängiger Risikofaktor für die kardiovaskuläre Mortalität. • Die Messung der postprandialen Glukosewerte nach 1 – 2 Stunden zusammen mit den Nüchtern Plasmaglukosewerten (FPG) durch den Patienten ist wichtig für die Therapieoptimierung. • Neue Wirkstoffe wie z. B. Nateglinide erlauben es, das physiologische Insulin-Sekretionsprofil wieder herzustellen, ohne den Insulinspiegel über längere Zeit zu erhöhen.
- Slides: 15