Paed Dr Jozef Beuka jbenuskanextra sk Fzov diagram

Paed. Dr. Jozef Beňuška jbenuska@nextra. sk

Fázový diagram: - je grafické znázornenie závislosti teploty a tlaku, - je graf, v ktorom každý bod roviny znázorňuje istý stav látky pri zvolenej termodynamickej teplote T a tlaku p. - graf, v ktorom sú znázornené krivka topenia, krivka nasýtenej pary a sublimačná krivka.
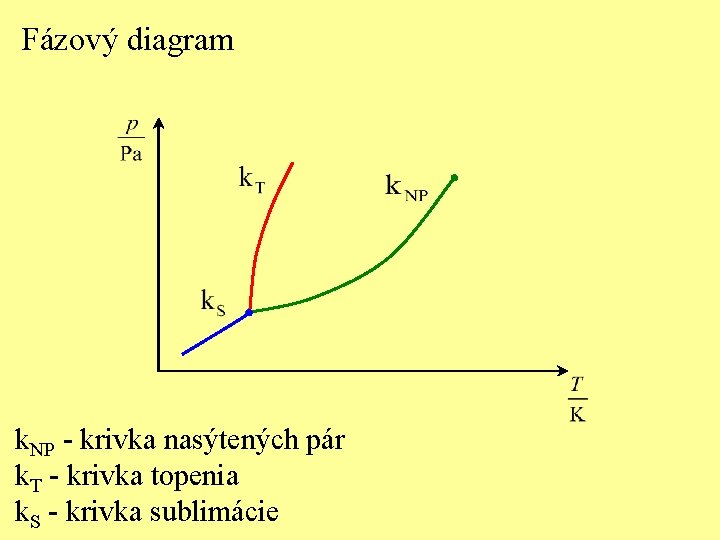
Fázový diagram k. NP - krivka nasýtených pár k. T - krivka topenia k. S - krivka sublimácie
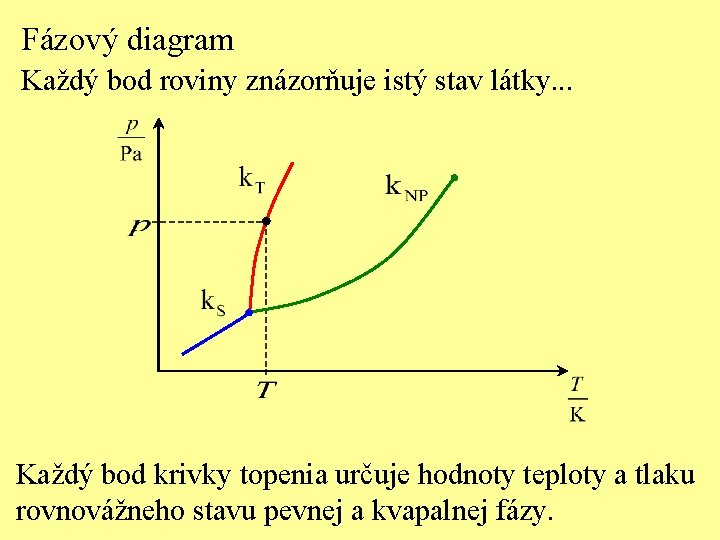
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . Každý bod krivky topenia určuje hodnoty teploty a tlaku rovnovážneho stavu pevnej a kvapalnej fázy.
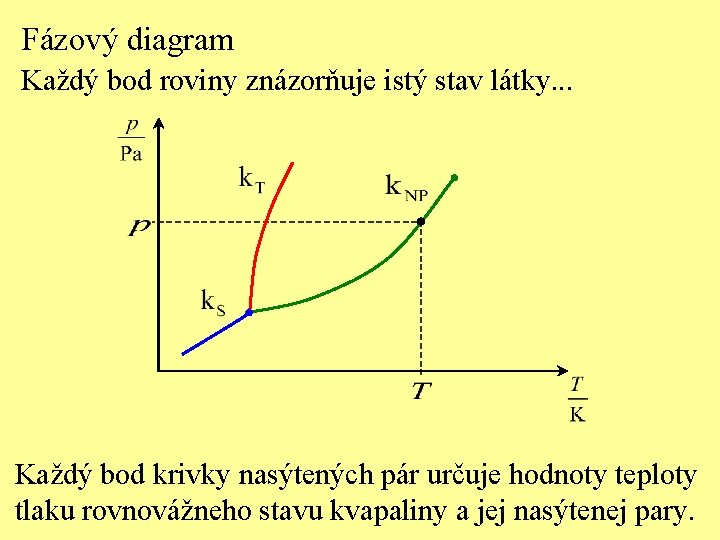
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . Každý bod krivky nasýtených pár určuje hodnoty teploty tlaku rovnovážneho stavu kvapaliny a jej nasýtenej pary.
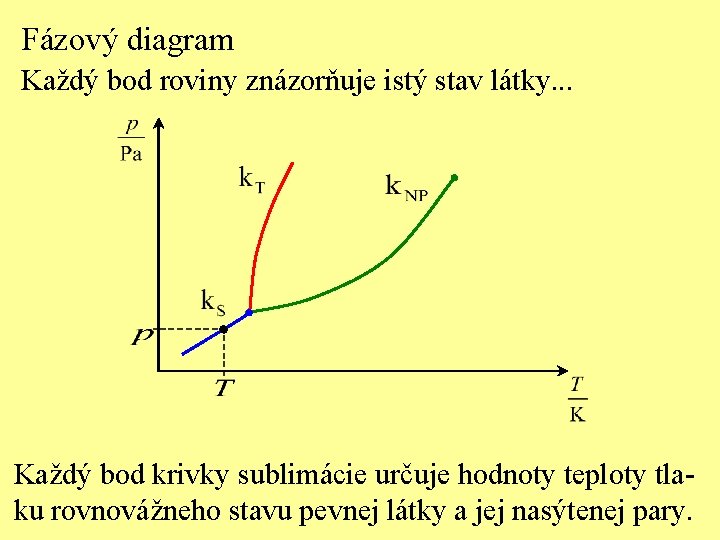
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . Každý bod krivky sublimácie určuje hodnoty teploty tlaku rovnovážneho stavu pevnej látky a jej nasýtenej pary.
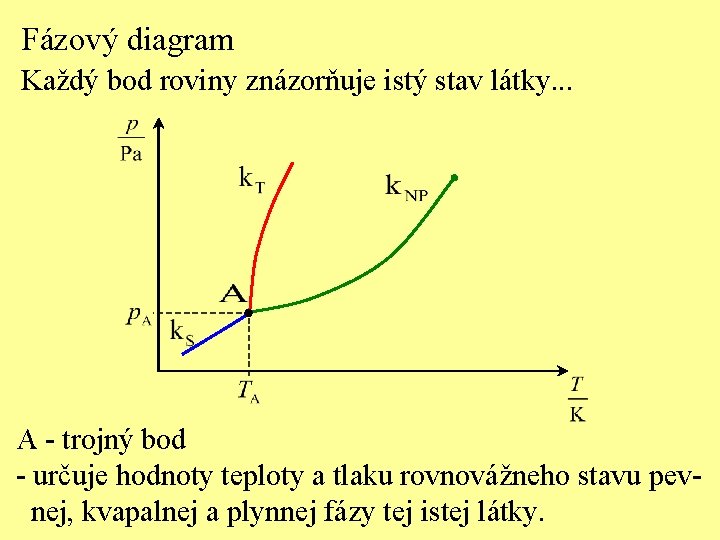
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . A - trojný bod - určuje hodnoty teploty a tlaku rovnovážneho stavu pevnej, kvapalnej a plynnej fázy tej istej látky.
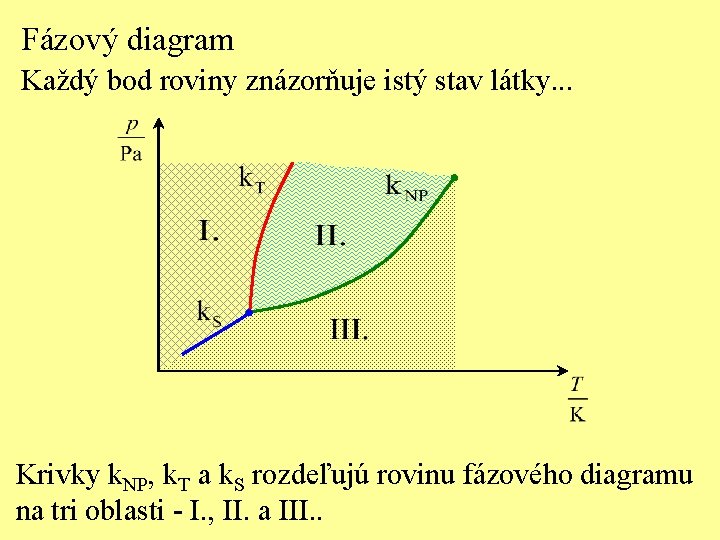
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . Krivky k. NP, k. T a k. S rozdeľujú rovinu fázového diagramu na tri oblasti - I. , II. a III. .
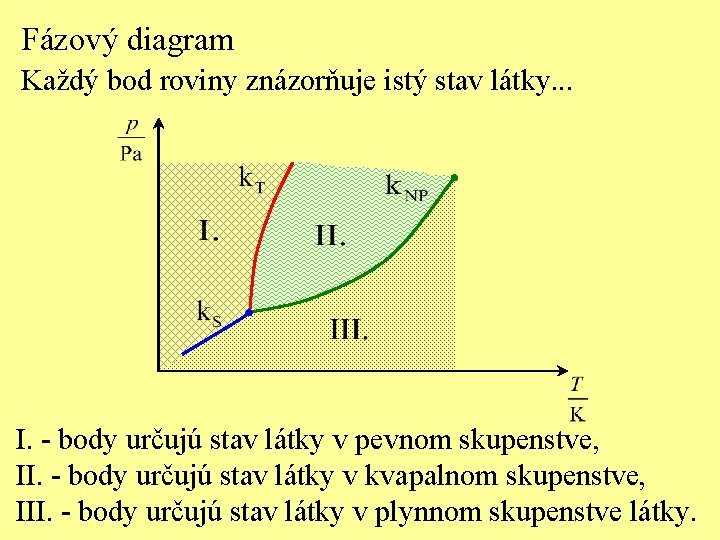
Fázový diagram Každý bod roviny znázorňuje istý stav látky. . . I. - body určujú stav látky v pevnom skupenstve, II. - body určujú stav látky v kvapalnom skupenstve, III. - body určujú stav látky v plynnom skupenstve látky.
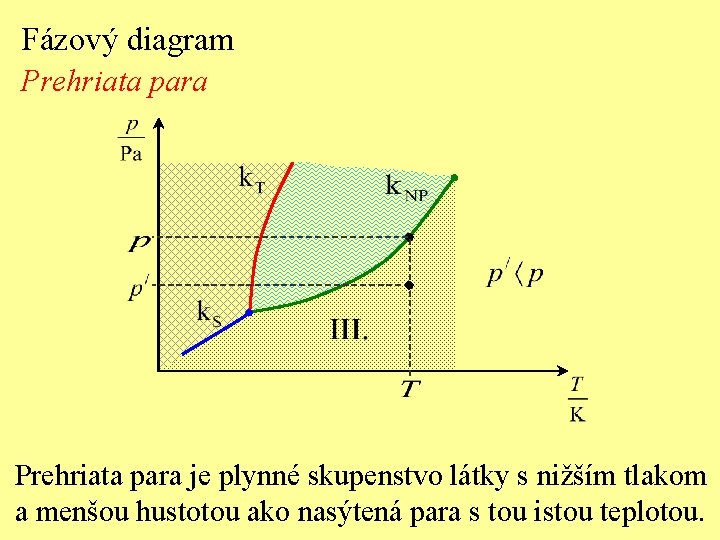
Fázový diagram Prehriata para je plynné skupenstvo látky s nižším tlakom a menšou hustotou ako nasýtená para s tou istou teplotou.
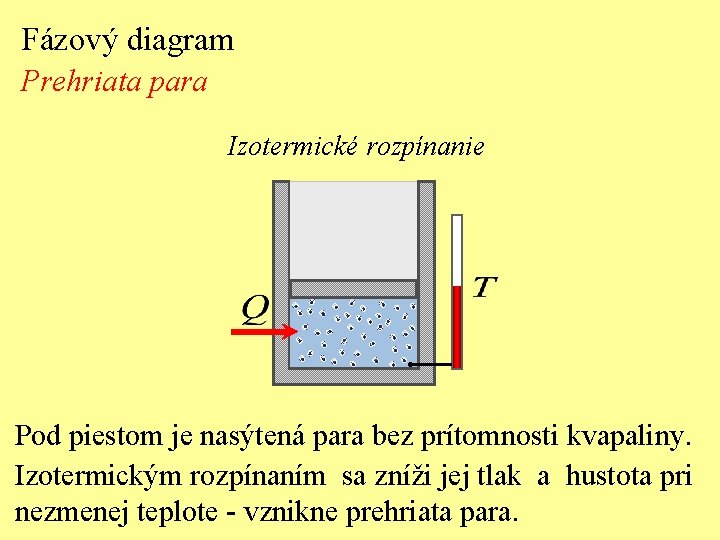
Fázový diagram Prehriata para Izotermické rozpínanie Pod piestom je nasýtená para bez prítomnosti kvapaliny. Izotermickým rozpínaním sa zníži jej tlak a hustota pri nezmenej teplote - vznikne prehriata para.
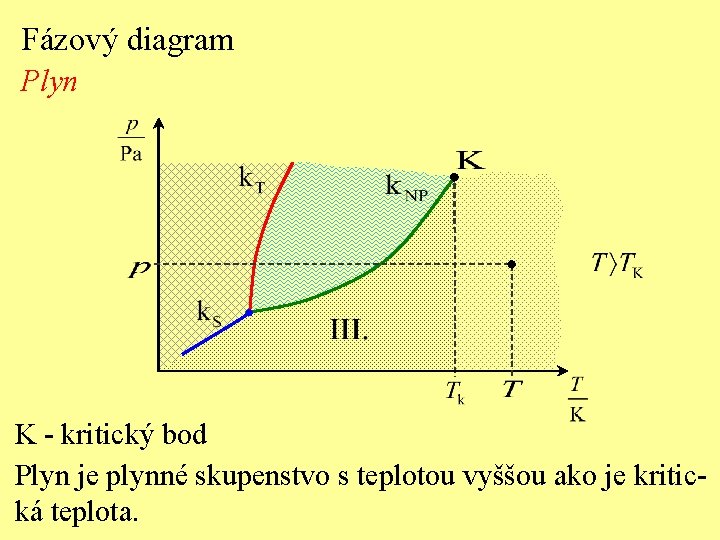
Fázový diagram Plyn K - kritický bod Plyn je plynné skupenstvo s teplotou vyššou ako je kritická teplota.
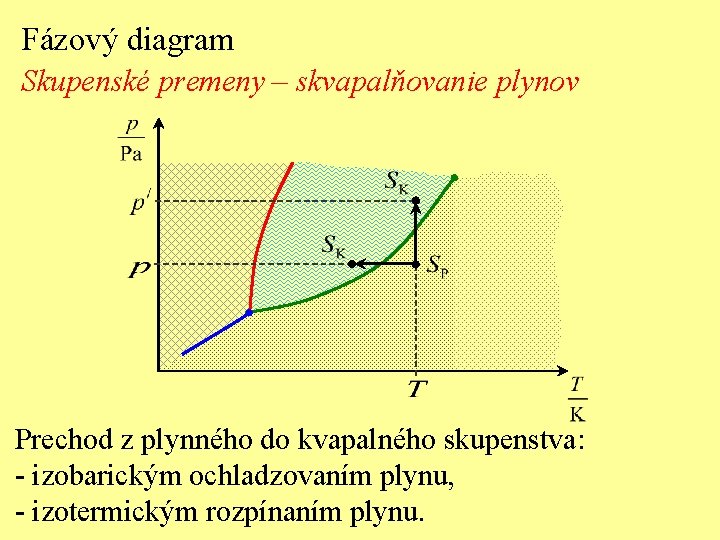
Fázový diagram Skupenské premeny – skvapalňovanie plynov Prechod z plynného do kvapalného skupenstva: - izobarickým ochladzovaním plynu, - izotermickým rozpínaním plynu.

Test Každý bod roviny fázového diagramu znázorňuje: a) istý stav látky pri zvolenej termodynamickej teplote a tlaku, b) stav rovnováhy medzi rôznymi stavmi istej látky, c) prechod medzi rôznymi stavmi istej látky, d) fázu určitého skupenstva látky. 1

Test Trojný bod vo fázovom diagrame znázorňuje: a) hodnoty termodynamickej teploty a tlaku rovnovážneho stavu pevnej a kvapalnej fázy, b) hodnoty termodynamickej teploty a tlaku rovnovážneho stavu pevnej, kvapalnej a plynnej fázy, c) hodnoty termodynamickej teploty a tlaku rovnovážneho stavu pevnej a plynnej fázy, d) hodnoty termodynamickej teploty a tlaku rovnovážneho stavu kvapalnej a plynnej fázy. 2

Test Prehriata para je: a) plynné skupenstvo látky s vyššou teplotou ako nasýtená para s tým istým tlakom, b) plynné skupenstvo látky s nižšou teplotou ako nasýtená para s tým istým tlakom, c) plynné skupenstvo látky s vyšším tlakom ako nasýtená para s tou istou teplotou, d) plynné skupenstvo látky s nižším tlakom ako nasýtená para s tou istou teplotou. 3

Test Prechod z plynného do kvapalného skupenstva je možné realizovať: a) izobarickým ochladzovaním, b) izotermické rozpínanie, c) izotermické stláčaním, d) izobarickým zohrievaním. 4
- Slides: 17