p ENGERTIAN Stoikiometri berasal dari katakata Yunani stoicheion

p. ENGERTIAN Stoikiometri berasal dari kata-kata Yunani stoicheion (=unsur) dan metrein (= mengukur) berarti mengukur unsur-unsur Ilmu yang mmempelajari tentang pengukuran materi yang berdsarkan pada rumus kimia dan persamaan kimia yang berimbang. Hubungan kuantitatif antara zat-zat yang terkait dalam reaksi kimia

Konsep Mol 1 mol adalah satuan bilangan kimia yang jumlah atom-atomnya atau molekulnya sebesar bilangan Avogadro dan massanya = Mr senyawa itu Jika bilangan Avogadro = L Maka L = 6. 023 x 10 1 mol atom = L buah atom massanya Ar 1 molekul = L buah molekul, massanya = Mr 23

Contoh berapa molekul yang terdapat dalam 20 gr Na. OH Jawab : Mr Na. OH : 23 + 16 +1 = 40 Mol Na. OH = massa/Mr = 20/40 = 0, 5 mol Banyaknya molekul Na. OH 0, 5 L = 0, 5 x 6, 023 x 10 23 Massa molekul relatif (Mr) suatu senyawa merupakan penjumlahan dari massa atom unsur-unsur penyusunnya Contoh : Jika Ar X = 10 Y = 50 berapakah molekul relatif senyawa X 2 Y 4 Jawab : Mr X 2 Y 4 = 2 x Ar X + 4 x Ar Y = 2. 10 + 4 x 50 = 220

1 mol tidak hanya menunjukkan atom sejumlah bilangan Avogadro tetapi juga 1 mol unsur memiliki massa = massa atom tersebut dalam satuan gram n Mol zat = massa zat (gram)/ massa atom zat (gram/mol) = gram/ Ar/Mr 1 mol senyawa mempunyai massa = massa molekul senyawa tsb dalam satuan gram Contoh : 1 mol H 2 SO 4 ----- 2 mol H 1 mol S dan 4 mol O Mr H 2 SO 4 = (2 x Ar H)+(1 x. Ar S)+(4 x. Ar O) = (2 x 1) + (1 x 32) + ( 4 x 16) = 98 Jadi massa 1 mol H 2 SO 4 = 98 Berarti sebanyak 6, 02 x 10 23 buah molekul H 2 SO 4 (1 mol H 2 SO 4) memilki massa 98 gr

Contoh 2 Hitung % berat unsur yang terdapat dalam senyawa natrium klorida (Mr = 58, 5 gr/mol) Jawab : 1 buah molekul Na. Cl------ 1 buah aton Na 1 buah atom Cl Jadi 1 mol Na. Cl (58, 5)---- 1 mol Na (23 g) 1 mol Cl (35, 5) % berat Na = 1 x Ar Na/ Mr Na. Cl x 100 % berat Cl = 1 x Ar Cl/Mr Na. Cl x 100

RUMUS MOLEKUL DAN RUMUS EMPIRIS Rumus kimia : menunjukkan jumlah relatif atom unsur-unsur dalam suatu zat Contoh : H 2 SO 4, HCl Rumus Empiris : rumus yang menyatakan perbandingan terkecil atom-atom dari unsur yang menyusun senyawa Rumus Molekul : rumus yang menyatakan jumlah atom-atom dari unsur-unsur yang menyusun suatu molekul senyawa ----- memberikan jumlah mol
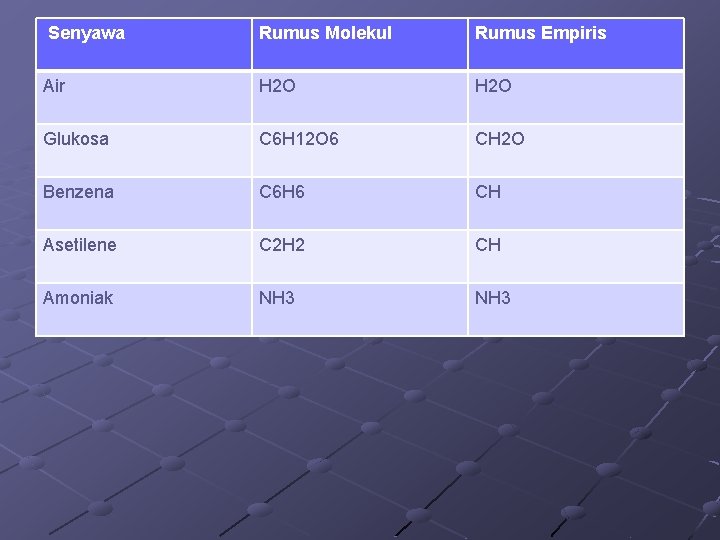
Senyawa Rumus Molekul Rumus Empiris Air H 2 O Glukosa C 6 H 12 O 6 CH 2 O Benzena C 6 H 6 CH Asetilene C 2 H 2 CH Amoniak NH 3

Cara menentukan Rumus Empiris a. Tentukan massa atau persen setiap unsur dalam senyawa b. membagi massa setiap unsur dengan massa atom relatif (Ar) ---- diperoleh perbandingan mol setiap unsur 1 atom c. Mengubah perbandingan yang diperoleh menjadi bil. Sederhana dengan cara membagi dengan bil bulat terkecil

Cara menentukan rumus Molekul a. Menentukan Rumus Empiris b. Massa Molekul Relatif Contoh soal 1. Rumus empiris suatu cairan adalah C 2 H 4 O. Tentukan rumus molekul jika massa molekul relatifnya = 88 Mr C 2 H 4 O = 2 x 12 + 1 x 4 +1 x 16 = 44 44)n = 88 n= 2 RM= C 4 H 8 O 2

2. Suatu senyawa organik dgn Mr=80 mengandung 60 % karbon, 5 % hidrogen dan sisanya adalah nitrogen. Tentukan rumus molekulnya Jawab : Perbandingan 60: 5: 35 3. Suatu senyawa mengandung 28, 6% magnesium, 14, 3% karbon dan 57, 1% oksigen, Tentukan rumus empirisnya Macam Unsur Magnesium Karbon Oksigen Lambang unsur Mg C O Massa/persen tase 28, 6 14, 3 57, 1 Ar


STOIKHIOMETRI Stoikhiometri adalah hubungan kuantitatif antara zat-zat yang terkait dalam suatu reaksi kimia. Misalnya, apabila 1 g Ca. CO 3 dipanaskan sampai terurai seluruhnya, berapa gram Ca. O dan CO 2 akan dihasilkan ? Ca. CO 3 Ca. O + CO 2 Atau sebaliknya 0, 56 g Ca. O yang direaksikan dengan CO 2 berapa gram Ca. CO 3 paling banyak dihasilkan ? Dan berapa g CO 2 diperlukan ? Ca. O + CO 2 Ca. CO 3

PEREAKSI PEMBATAS Cara penentuan reaksi pembatas adalah dengan membagi jumlah mol zat yang tersedia dengan koefisien masing-masing. Hasil yang paling rendah menyatakan bahwa zat itulah pereaksi pembatasnya. Contoh : 0, 9 g HCl direaksikan dengan 1, 01 g Na 2 B 4 O 7 dan 0, 9 g H 2 O Reaksi : HCl + Na 2 B 4 O 7 + H 2 O Na. Cl + H 3 BO 3 Setarakan : 2 HCl + Na 2 B 4 O 7 + 5 H 2 O Uraian a. Tersedia (mmol) b. Koefisien c. Hasil bagi (a/b) 2 Na. Cl + 4 H 3 BO 3 2 HCl + Na 2 B 4 O 7 + 5 H 2 O 24, 7 5 50 2 1 5 12, 35 5 10 Nilai terkecil 5 dihasilkan oleh Na 2 B 4 O 7. Jadi Na 2 B 4 O 7 adalah pereaksi pembatas.

HUBUNGAN STOIKHIOMETRIS DI DALAM SENYAWA Persen Berat Unsur dalam Senyawa Rumus ferri sulfat, Fe 2(SO 4)3 , menyatakan bahwa 1 molekul garam itu terbentuk dari 2 atom Fe , 3 atom S dan 12 atom O. 1 mol Fe 2(SO 4)3 , berisi 2 mol Fe, 3 mol S dan 12 mol O 400 g Fe 2(SO 4)3 berisi 112 g Fe, 96 g S dan 192 g O atau 28 % Fe, 24 % S dan 48 % O n x Ar. Unsur %-berat unsur dalam senyawa = x 100 Mr. Senyawa n = jumlah atom unsur dalam molekul atau senyawa

Tugas 1. Lengkapi tabel berikut ; Senyawa Jumlah atom Jumlah mol H 3 PO 4 . . atom H, . . atom P dan. . atom O . . mol H, . . g mol P P dan. . g dan. . O= …g mol O Jumlah g % -berat Bila senyawa tersebut sebanyak 50 g 3, 06% H, 1, 5 g H, 15, 5 g P 31, 6 % P dan 32, 5 g O dan 65, 3 %O (NH 4)3 As. O 3 K 3 Fe(CN)6 C 2 H 5 OH Cari Ar. unsur dalam sistem berkala unsur 2. Manakah pupuk yang mengandung N lebih banyak per gram pupuk : Amonium Nitrat, Urea atau ZA? Cari rumus molekul Urea dan ZA

HUBUNGAN STOIKHIOMETRIS ANTARA ZAT DALAM REAKSI Perbandingan koefien reaksi = perbandingan jumlah mol zat-zat dalam reaksi tersebut. Langkah-langkah Pemecahan soal Stoikhiometri : 1. Menulis persamaan reaksi dengan rumus kimia 2. Melengkapi persamaan reaksi dengan koefien reaksi 3. Mencari zat yang diketahui jumlahnya dan bila masih perlu mengubah jumlah itu menjadi jumlah dalam satuan mol 4. Berdasar perbandingan koefien, menentukan jumlah mol zat yang ditanyakan banyaknya 5. Jumlah mol zat yang dicari selanjutnya diubah menjadi jumlah dalam gram atau dalam satuan lain sesuai dengan soalnya. 6. Memeriksa kebenaran.


- Slides: 18