OXIDAO E REDUO Oxidao a PERDA de ELTRONS





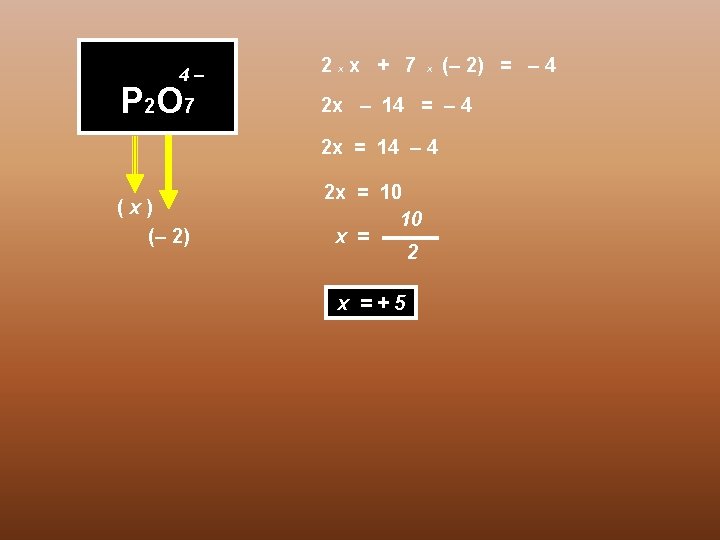















- Slides: 37


OXIDAÇÃO E REDUÇÃO Oxidação é a PERDA de ELÉTRONS Redução é o GANHO de ELÉTRONS + Na Cl –

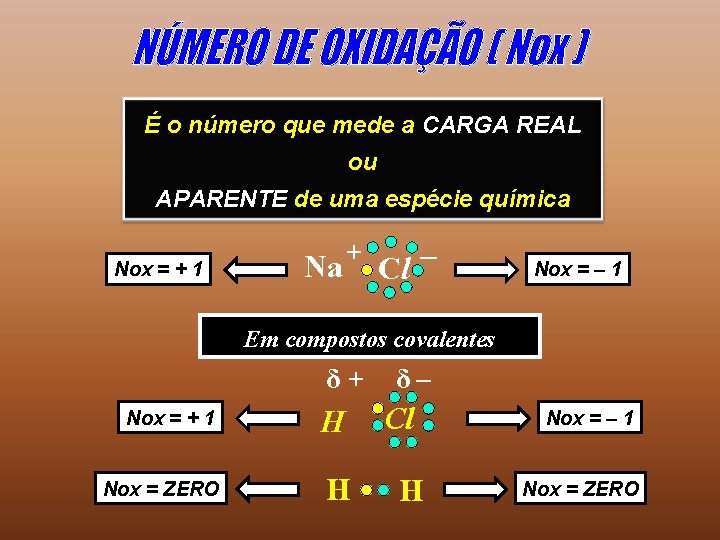
É o número que mede a CARGA REAL ou APARENTE de uma espécie química Nox = + 1 Na + Cl – Nox = – 1 Em compostos covalentes δ+ Nox = + 1 H Nox = ZERO H δ– Cl H Nox = – 1 Nox = ZERO

É a perda de elétrons ou aumento do Nox É o ganho de elétrons ou diminuição do Nox

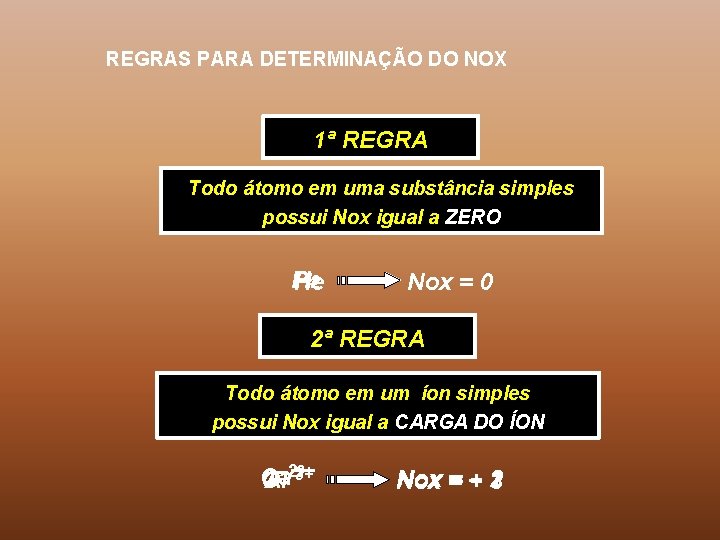
REGRAS PARA DETERMINAÇÃO DO NOX 1ª REGRA Todo átomo em uma substância simples possui Nox igual a ZERO H P 42 He Nox = 0 2ª REGRA Todo átomo em um íon simples possui Nox igual a CARGA DO ÍON – 3+ Ca O Al F 2– 2+ Nox = + – 2 1 3

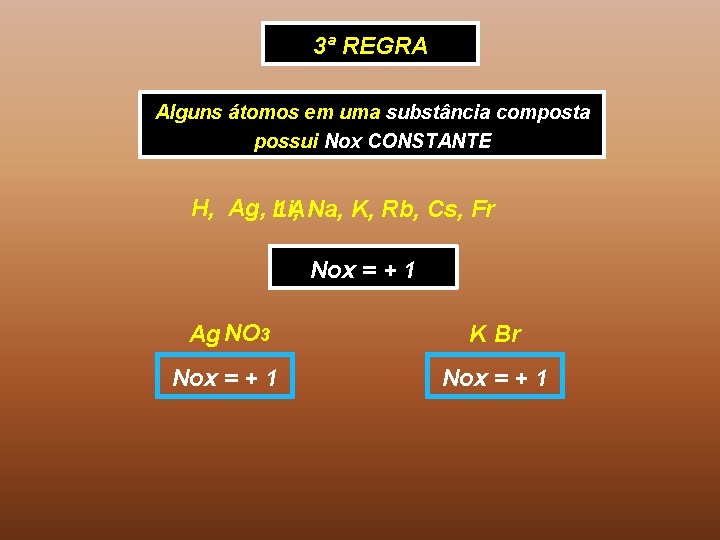
3ª REGRA Alguns átomos em uma substância composta possui Nox CONSTANTE H, Ag, Li, 1 A Na, K, Rb, Cs, Fr Nox = + 1 Ag NO 3 K Br Nox = + 1

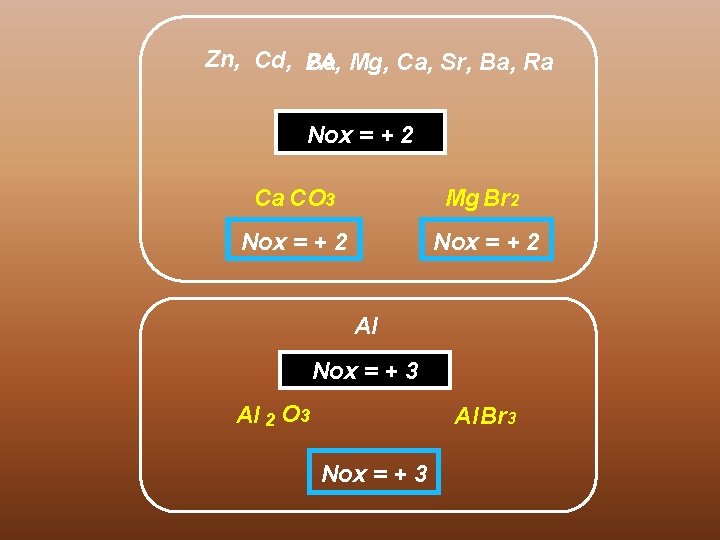
Zn, Cd, Be, 2 A Mg, Ca, Sr, Ba, Ra Nox = + 2 Ca CO 3 Mg Br 2 Nox = + 2 Al Nox = + 3 Al 2 O 3 Al Br 3 Nox = + 3

calcogênios (O, S, Se, Te, Po) quando for o mais eletronegativo (no final da fórmula) Al 2 O 3 Nox = – 2 H 2 S Nox = – 2 halogênios (F, Cl, Br, I, At) quando for o mais eletronegativo (no final da fórmula) Al Cl 3 Nox = – 1 HF Nox = – 1

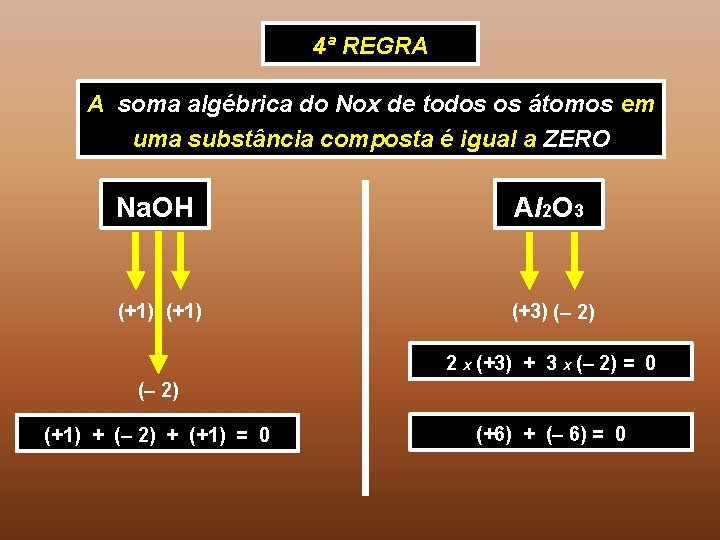
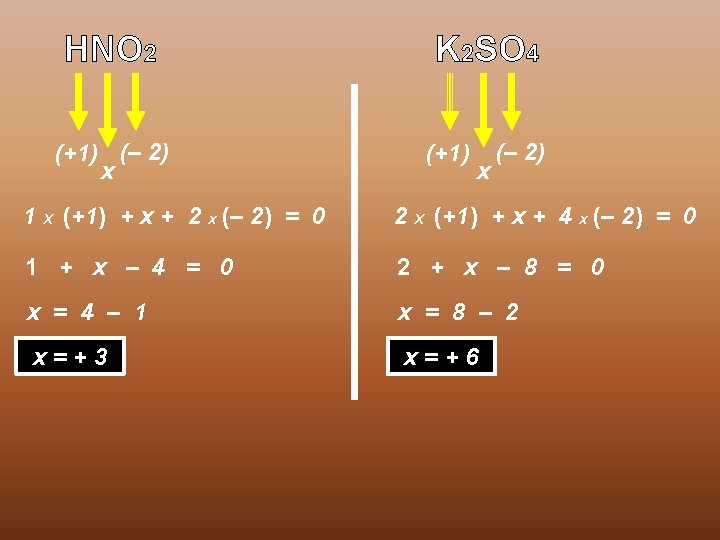
4ª REGRA A soma algébrica do Nox de todos os átomos em uma substância composta é igual a ZERO Na. OH Al 2 O 3 (+1) (+3) (– 2) 2 x (+3) + 3 x (– 2) = 0 (– 2) (+1) + (– 2) + (+1) = 0 (+6) + (– 6) = 0

exemplo Ba 2 As 2 O 7 (+2) 2 X (+2) + 2 x x (– 2) x + 7 x (– 2) = 0 4 + 2 x – 14 = 0 2 x = 14 – 4 2 x = 10 x= 10 2 x=+5


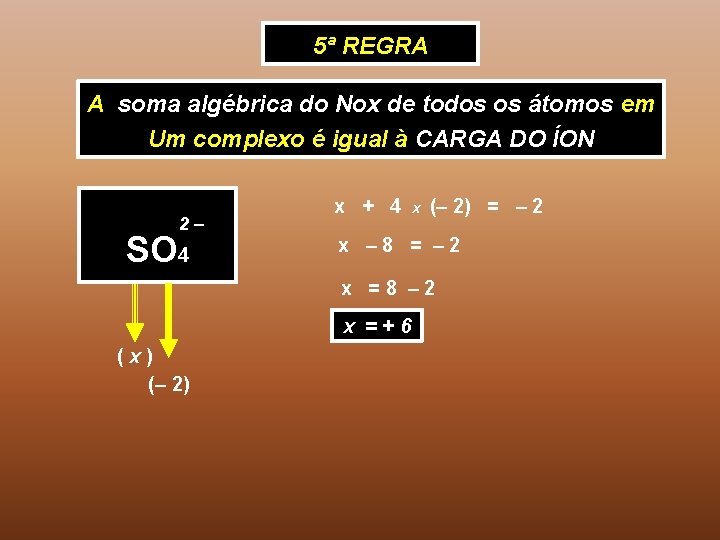
5ª REGRA A soma algébrica do Nox de todos os átomos em Um complexo é igual à CARGA DO ÍON 2– SO 4 x + 4 x (– 2) = – 2 x – 8 = – 2 x =8 – 2 x =+6 (x) (– 2)
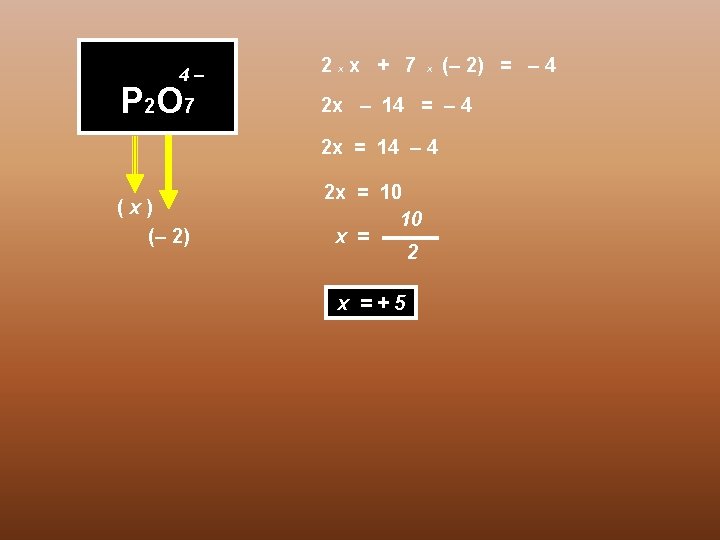
4– P 2 O 7 2 xx + 7 x 2 x – 14 = – 4 2 x = 14 – 4 (x) (– 2) = – 4 2 x = 10 10 x = 2 x =+5

01) (Vunesp) No mineral perovskita, de Ca. Ti. O 3, o número de oxidação do titânio é: a) + 4. +2 b) + 2. Ca Ti O 3 c) + 1. d) – 1. e) – 2. x – 2 2 + x – 6 = 0 x = 6– 2 x = +4

02) Nas espécies químicas Br. O 3 1– , Cl 2 e Hl, os halogênios têm números de oxidação, respectivamente, iguais a: a) – 5, zero e – 1. b) – 5, – 5 e – 1. c) – 1, – 5 e + 1. d) zero, zero e + 1. e) + 5, zero e – 1. x – 2 Br O 31 – x– 6=– 1 x=6– 1 x=+5 Cl 2 Nox = zero HI Nox = – 1

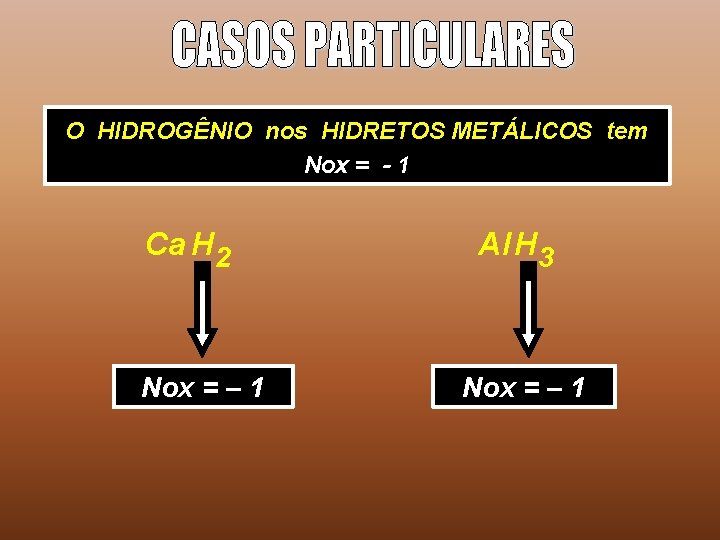
O HIDROGÊNIO nos HIDRETOS METÁLICOS tem Nox = - 1 Ca H 2 Nox = – 1 Al H 3 Nox = – 1

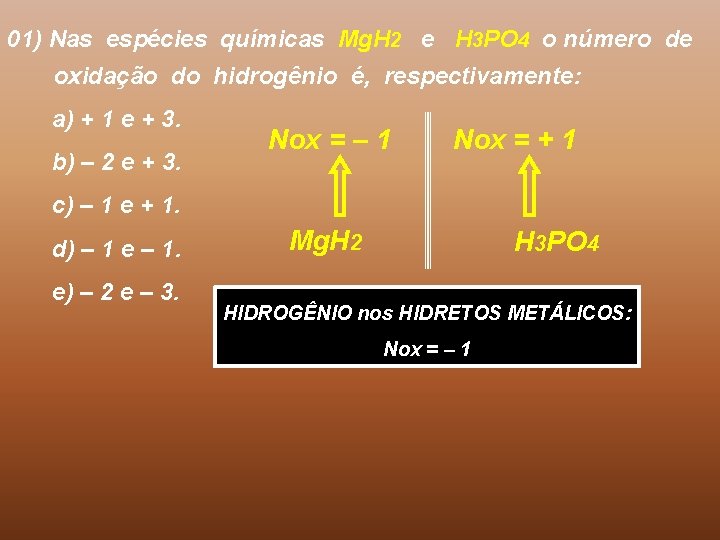
01) Nas espécies químicas Mg. H 2 e H 3 PO 4 o número de oxidação do hidrogênio é, respectivamente: a) + 1 e + 3. b) – 2 e + 3. Nox = – 1 Nox = + 1 c) – 1 e + 1. d) – 1 e – 1. e) – 2 e – 3. Mg. H 2 H 3 PO 4 HIDROGÊNIO nos HIDRETOS METÁLICOS: Nox = – 1

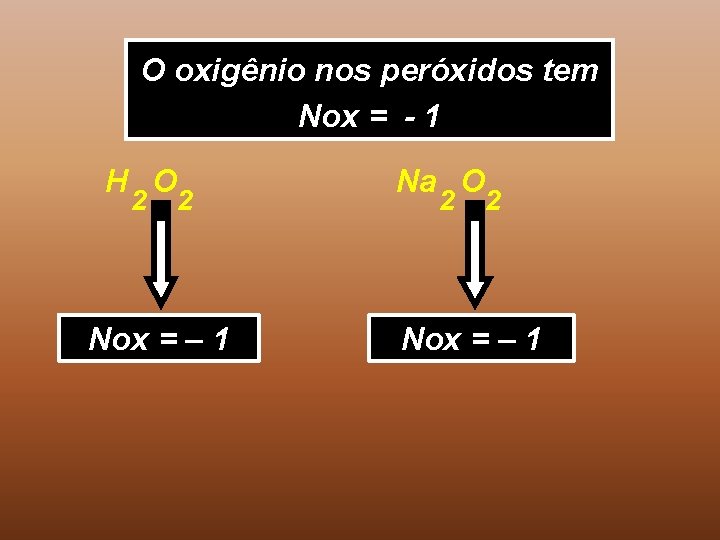
O oxigênio nos peróxidos tem Nox = - 1 H O 2 2 Nox = – 1 Na O 2 2 Nox = – 1

01) Nos compostos Ca. O e Na 2 O 2 o oxigênio tem número de oxidação, respectivamente, igual a: a) – 2 e – 2. b) – 2 e – 1. Ca. O Na 2 O 2 c) – 1 e – 1. d) – 2 e – 4. e) – 2 e + 1. Nox = – 2 Nox = – 1 OXIGÊNIO nos PERÓXIDOS Nox = – 1

As reações que apresentam os fenômenos de OXIDAÇÃO e REDUÇÃO são denominadas de reações de óxido-redução (oxi-redução ou redox). 0 +1 0 Fe + 2 HCl +2 H 2 + Fe. Cl 2 OXIDAÇÃO REDUÇÃO Esta é uma reação de OXI-REDUÇÃO

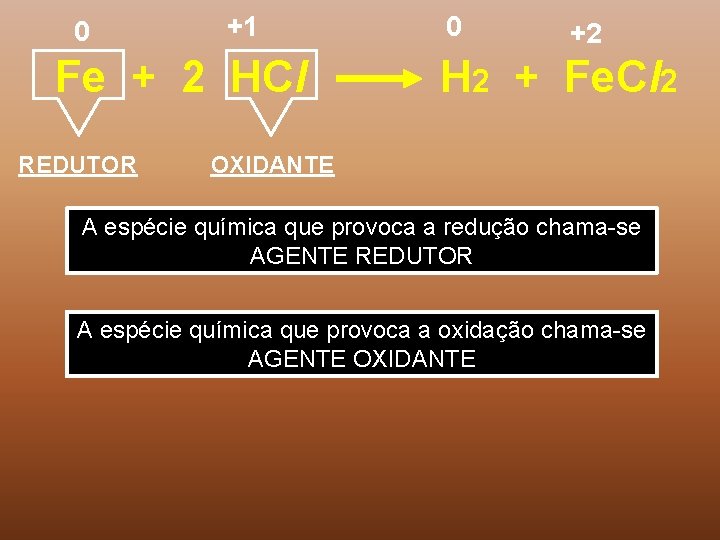
0 +1 Fe + 2 HCl REDUTOR 0 +2 H 2 + Fe. Cl 2 OXIDANTE A espécie química que provoca a redução chama-se AGENTE REDUTOR A espécie química que provoca a oxidação chama-se AGENTE OXIDANTE

01) Na equação representativa de uma reação de oxi-redução: Ni + Cu 2+ Ni 2+ + Cu a) O íon Cu b) O íon Cu 2+ 2+ é o oxidante porque ele é oxidado. é o redutor porque ele é reduzido. c) O Ni é redutor porque ele é oxidado. d) O Ni é o oxidante porque ele é oxidado e) O Ni é o oxidante e o íon Cu 2+ é o redutor.

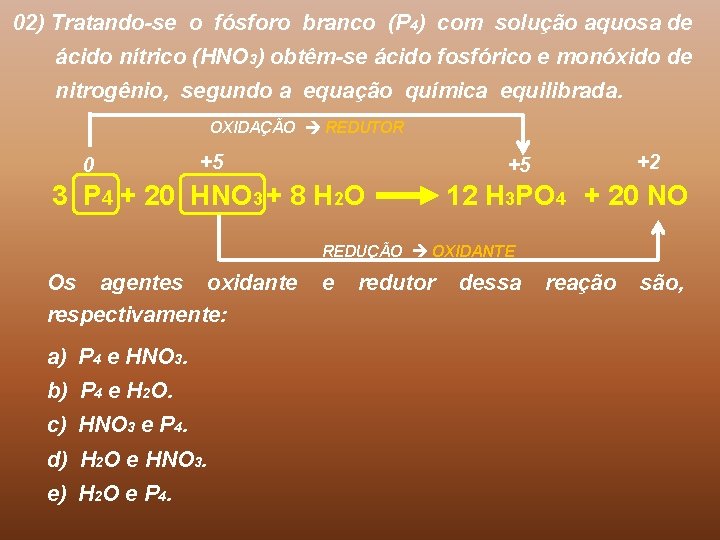
02) Tratando-se o fósforo branco (P 4) com solução aquosa de ácido nítrico (HNO 3) obtêm-se ácido fosfórico e monóxido de nitrogênio, segundo a equação química equilibrada. OXIDAÇÃO REDUTOR 0 +5 +2 +5 3 P 4 + 20 HNO 3 + 8 H 2 O 12 H 3 PO 4 + 20 NO REDUÇÃO OXIDANTE Os agentes oxidante respectivamente: a) P 4 e HNO 3. b) P 4 e H 2 O. c) HNO 3 e P 4. d) H 2 O e HNO 3. e) H 2 O e P 4. e redutor dessa reação são,

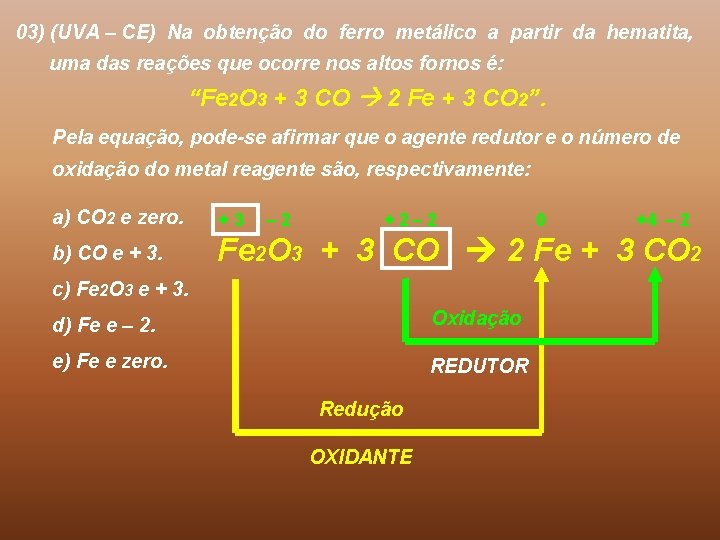
03) (UVA – CE) Na obtenção do ferro metálico a partir da hematita, uma das reações que ocorre nos altos fornos é: “Fe 2 O 3 + 3 CO 2 Fe + 3 CO 2”. Pela equação, pode-se afirmar que o agente redutor e o número de oxidação do metal reagente são, respectivamente: a) CO 2 e zero. +3 b) CO e + 3. Fe 2 O 3 + 3 CO 2 Fe + 3 CO 2 – 2 + 2– 2 c) Fe 2 O 3 e + 3. d) Fe e – 2. Oxidação e) Fe e zero. REDUTOR Redução OXIDANTE 0 +4 – 2

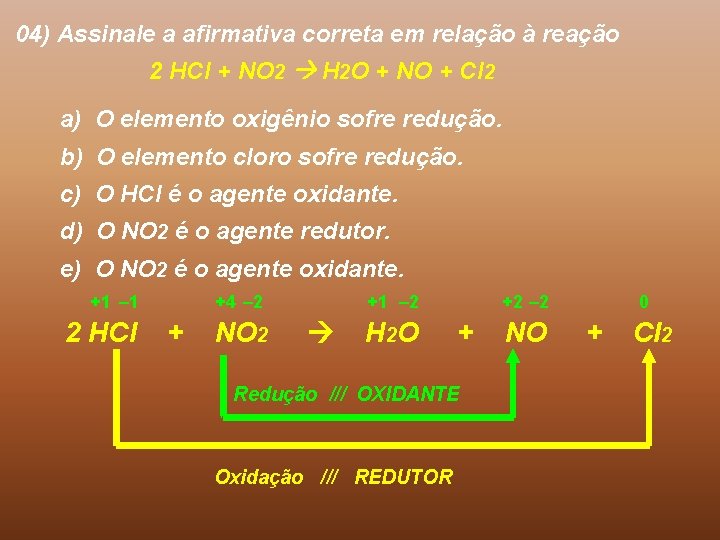
04) Assinale a afirmativa correta em relação à reação 2 HCl + NO 2 H 2 O + NO + Cl 2 a) O elemento oxigênio sofre redução. b) O elemento cloro sofre redução. c) O HCl é o agente oxidante. d) O NO 2 é o agente redutor. e) O NO 2 é o agente oxidante. +1 – 1 2 HCl +4 – 2 + NO 2 +1 – 2 H 2 O +2 – 2 + Redução /// OXIDANTE Oxidação /// REDUTOR NO 0 + Cl 2

Balanceamento de Reações de Oxido-Redução Regras para o balanceamento: 1º) Determinar, na equação química, qual espécie se oxida e qual se reduz. 2º) Escolher os produtos ou reagentes para iniciar o balanceamento.

3º) Encontrar os Δoxid e Δred : Δoxid = número de elétrons perdidos x atomicidade do elemento Δred = número de elétrons recebidos x atomicidade do elemento As atomicidades são definidas no membro de partida (reagentes ou produtos). Atomicidade – Representa o maior número de átomos daquele elemento. 4º) Se possível, os Δoxid e Δred podem ser simplificados. Exemplificando. . . Δoxid = 4 Δred = 2 simplificando. . . Δoxid = 2 Δred = 1

5º) Para igualar os elétrons nos processos de oxidação e redução: O Δoxid se torna o coeficiente da substância que contém o átomo que se reduz. O Δred se torna o coeficiente da substância que contém o átomo que se oxida. 6º) Os coeficientes das demais substâncias são determinados por tentativas, baseando-se na conservação dos átomos. Os exemplos a seguir ajudarão à compreensão

Balanceamento de Reações de Oxido-Redução S + HNO 3 NO 2 + H 2 O + H 2 SO 4 O S oxida; vai de nox = 0 para nox = +6. Esta oxidação envolve 6 elétrons e a atomicidade do S é 1: Δoxid = 6 x 1 = 6 O N reduz; vai de nox = +5 para nox = +4. Esta redução envolve 1 elétron e a atomicidade do N é 1: Δred = 1 x 1 = 1 Invertendo os coeficientes obtidos, como manda o método, temos:

Balanceamento de Reações de Oxido-Redução 1 S + 6 HNO 3 => NO 2 + H 2 O + H 2 SO 4 Para os outros coeficientes deve ser usado o método de tentativa: 1 S + 6 HNO 3 => 6 NO 2 + 2 H 2 O + 1 H 2 SO 4 Mais Exemplos?

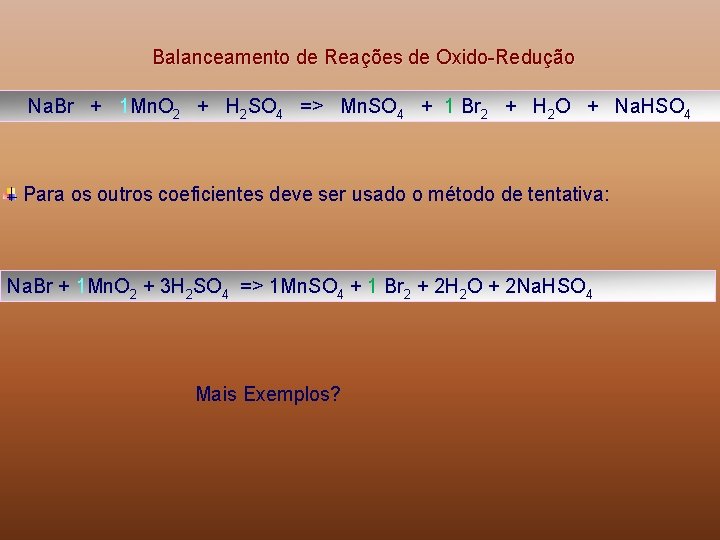
Balanceamento de Reações de Oxido-Redução Na. Br + Mn. O 2 + H 2 SO 4 => Mn. SO 4 + Br 2 + H 2 O + Na. HSO 4 O Br oxida; vai de nox = -1 para nox = 0. Esta oxidação envolve 1 elétron e a atomicidade do Br no Br 2 é 2: Δoxid = 1 x 2 = 2 O Mn reduz; vai de nox = +4 para nox = +2. Esta redução envolve 2 elétrons e a atomicidade do Mn no Mn. O 2 é 1: Δred = 2 x 1 = 2 Invertendo os coeficientes obtidos, como manda o método, temos:

Balanceamento de Reações de Oxido-Redução Na. Br + 1 Mn. O 2 + H 2 SO 4 => Mn. SO 4 + 1 Br 2 + H 2 O + Na. HSO 4 Para os outros coeficientes deve ser usado o método de tentativa: Na. Br + 1 Mn. O 2 + 3 H 2 SO 4 => 1 Mn. SO 4 + 1 Br 2 + 2 H 2 O + 2 Na. HSO 4 Mais Exemplos?

Balanceamento de Reações de Oxido-Redução Uma mesma substância contém os átomos que se oxidam e também os que se reduzem Na. OH + Cl 2 => Na. Cl. O + Na. Cl + H 2 O Os átomos de Cl no Cl 2 tem nox igual a zero. No segundo membro temos: Cl com nox = +1 no Na. Cl. O Cl com nox = -1 no Na. Cl. Como a única fonte de Cl na reação é o Cl 2, a reação pode ser reescrita: Na. OH + Cl 2 => Na. Cl. O + Na. Cl + H 2 O Como o Cl 2 vai ser o elemento de partida tanto para a oxidação quanto para a redução, a atomicidade nos dois processos será igual a 2. A oxidação envolve mudança do nox do Cl no Cl 2 de zero para +1, ou seja, um elétron: Δoxid = 1 x 2 = 2

Balanceamento de Reações de Oxido-Redução Na redução o nox do Cl no Cl 2 vai de zero para -1, ou seja, um elétron. Δred = 1 x 2 = 2 Neste caso podemos simplificar: Δoxid = Δred = 1 Na. OH + 1 Cl 2 => Na. Cl. O + Na. Cl + H 2 O Para os outros coeficientes deve ser usado o: método de tentativa: 4 Na. OH + 1 Cl 2 => 2 Na. Cl. O + 2 Na. Cl + 2 H 2 O 4 Na. OH + 2 Cl 2 => 2 Na. Cl. O + 2 Na. Cl + 2 H 2 O

Balanceamento de Reações de Oxido-Redução A água oxigenada atuando como oxidante Fe. Cl 2 + H 2 O 2 + HCl => Fe. Cl 3 + H 2 O O oxigênio da água oxigenada tem nox = -1, no H 2 O, tem nox = -2. Reduziu envolvendo 1 elétron. A atomicidade do oxigênio na substância de partida (H 2 O 2) é igual a 2: Δred = 2 x 1 = 2 O ferro do Fe. Cl 2 tem nox = 2+, já no segundo membro, no Fe. Cl 3, tem nox = 3+. Oxidou envolvendo 1 elétron. A atomicidade do ferro na substância de partida (Fe. Cl 2) é igual a 1: Δoxid = 1 x 1 = 1 Invertendo os coeficientes: 2 Fe. Cl 2 + 1 H 2 O 2 + HCl => Fe. Cl 3 + H 2 O 2 Para os outros coeficientes deve ser usado o método de tentativa: 2 Fe. Cl 2 + 1 H 2 O 2 + HCl => Fe. Cl 3 + H 2 O 2

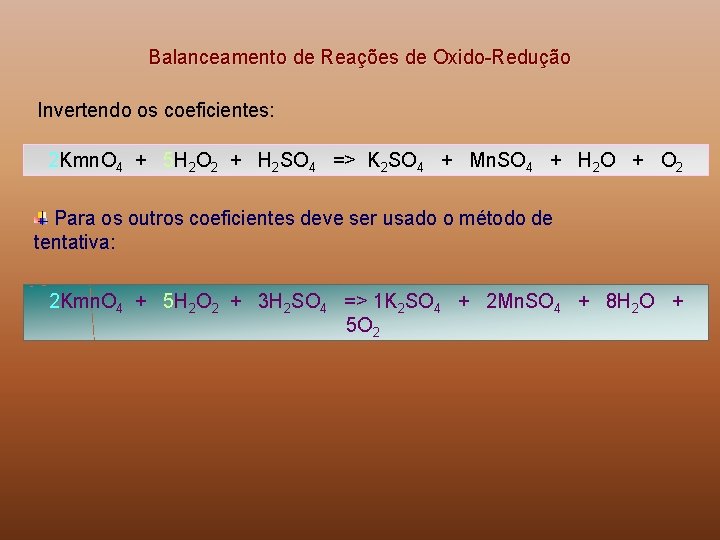
Balanceamento de Reações de Oxido-Redução A água oxigenada atuando como redutor Kmn. O 4 + H 2 O 2 + H 2 SO 4 => K 2 SO 4 + Mn. SO 4 + H 2 O + O 2 O Mn no Mn. O 4, possui nox = 7+. No Mn. SO 4, o Mn tem nox = a 2+. Reduziu envolvendo 5 elétrons. A atomicidade do Mn na substância de partida (KMn. O 4) é igual a 1: Δred = 5 x 1 = 5 No primeiro membro temos o oxigênio com dois nox diferentes: nox = 1 - na água oxigenada e nox = 2 - no H 2 SO 4 e KMn. O 4 Como o O 2 é gerado a partir da água oxigenada, ela será a substância de partida. O oxigênio, na água oxigenada tem nox = 1 -. No O 2 tem nox igual a zero. Oxidou com variação de um elétron. A atomicidade do oxigênio na substância de partida (H 2 O 2) é igual a 2: Δoxid = 1 x 2 = 2

Balanceamento de Reações de Oxido-Redução Invertendo os coeficientes: 2 Kmn. O 4 + 5 H 2 O 2 + H 2 SO 4 => K 2 SO 4 + Mn. SO 4 + H 2 O + O 2 Para os outros coeficientes deve ser usado o método de tentativa: 2 Kmn. O 4 + 5 H 2 O 2 + 3 H 2 SO 4 => 1 K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O + 5 O 2