Overin SeksKord Stromal Tmrleri Do Dr Canan Kabaca

Overin Seks-Kord Stromal Tümörleri Doç. Dr. Canan Kabaca Kocakuşak Zeynep Kamil Kadın ve Çocuk Hastalıkları EAH Jinekolojik Onkoloji Cerrahisi

Seks-Kord Stromal Tümörler • Seks-kord veya over stromasından orijin alırlar. • Hem benign hem de malign tümörlerden oluşan heterojen neoplasm grubudur. - Bu nedenle farklı biolojik davranış, klinik prezentasyon ve prognoz

Seks-Kord Stromal Tümörler • Over Stromal hücreler; Teka hücreleri, Fibroblastlar ve Leydig hücreleri , • Gonadal primitif seks-kord hücreleri ise Granulosa hücreleri Sertoli hücreleri • SKST’lerde bu hücre tipleri ayrı ya da karışık bir şekilde bulunur • Morfoloji hücre tipine göre değişkenlik gösterir.

Seks-Kord Stromal Tümörler • Overin nadir tümörlerinden • Over tümörlerinin %5 -8’i • Yıllık insidansı 2. 1/1, 000 kadın • Tüm yaş grubunda görülür ama sıklık 4. ve 5. dekadda artmakta • Genellikle sessiz, yavaş büyüyen tümörlerdir ama daha agresiv tümörler de olabilirler.

2003 WHO sınıflaması 2014’de revize oldu

Saf stromal tümörler • Eski sınıflamadaki; * Luteinize Tekoma * Stromal luteoma *Minör seks-kord elemanlı Stromal tümör tanıları artık kullanılmamakta. Mikrokistik stromal tümör, yeni adlandırılan, nadir tm. lerden Çoğu benign --- Fibrom (en sık SCST) --- Tekoma --- Sklerozan stromal tümörler --- Leydig tümörler Sellüler fibrom -- Düşük malign potansiyel (hafif atipi ve > 4 mitoz /10 BB) Steroid cell tümörler-- 1/3’ü klinik olarak malign - Çoğu androjenik

Saf seks kord tümörler

Miks Seks-Kord Stromal Tümörler Sertoli hücre komponentinin tubuler differensiasyon derecesine göre alt gruplara ayrılır. • 2014 WHO sınıflamasında - Stromal-Leydig hücreli tümör ve - Gynandroblastoma artık yok.

Seks-Kord Stromal Tümörler • Diğer over tümörleri gibi, * Genellikle abdominal kitle semptomları (ağrı, distansiyon , torsiyon) • Diğer over tümörlerinden farklı olarak, * Hormonal aktifdir ör; - hirsutism ve virilizasyon, - menstruel değişiklikler, primer/sekonder amenore - prekoks puberte • Ovarian hücrelerden (ör, granulosa ve teka hücreleri) oluşan tm. ler sıklıkla hiperestrojenik, • Testiküler hücrelerden (ör, Sertoli ve Leydig hücreler) oluşan tm. ler genellikle hiperandrojenik

Seks-Kord Stromal Tümörler- Patoloji • • Tipik olarak tek taraflı, 10 -15 cm, solid, sert, sıklıkla kanamalı ve /veya nekrotiktir. Morfolojisi diğer over tümörlerine benzer bu nedenle immünhistokimya teşhiste yararlıdır. Ayırıcı tanıda ; karsinom, sarkom, germ hücreli tümörler ve melanom vardır SKST’lerin geleneksel İHK markerı: İnhibin ve Calretinin’dir. - Her 2 marker da bazı endometrioid adenokanserlerde de zayıf pozitiftir - Pozitiflik epitelyal over tümörlerini ekarte etmez (Rabban ve Zaluedek. , 2003) • Steroidogenic factör 1(SF 1) - gonadal gelişim ile ilişkilidir ve SKST teşhisinde kullanışlıdır - bu marker epitelyal tümörlerde negatiftir. • Diğer (WT 1, FOXL 2, CD 56, melan A, CD 10 ve CD 99) - spesifite ve sensitivitesi düşüktür

Granüloza Hücreli Tümörler • Tüm over kanserlerinin %2 -5’i • Yıllık insidansı 0. 61 vaka /100. 000 kadın • 1. Juvenil tip Gr. HT * tüm Gr. HT’lerin %5’i * tipik olarak çocuk ve genç yetişkinlerde - puberte öncesi Gr. HT’lerin %85’i • 2. Erişkin tip Gr. HT * genellikle perimenaposal ve erken postmenaposal dönemde • Ayırım yaş ile değil morfoloji ile olur.

Erişkin tip Gr. HT / Klinik Prezentasyon • • Genellikle büyük palpable overyen kitle ile presente olur. Vaskülarize ve hemorajiktir (tümör rüptürü hematoperitona neden olabilir) Hiper-estrojenizme bağlı semptomlar tüm yaş gruplarında olabilir. %25 -50 vakada endometrial hiperplazi, %5 -13 vakada endometrial kanser histolojik olarak bulunur. (Kottarathil et al. , 2013) • Gr. HT’ler İnhibin A ve/veya İnhibin B salgılar * Serum İnhibin seviyelerindeki artış tipik olarak radyolojik progresyondan 11 ay önce oluşabilir (Pectasides et al. , 2009) • Estrojen seviyeleri hastalık aktivitesini göstermede kullanılmaz. * %30 vakada Estrojen salgılanmaz • AMH özellikle granulosa hücrelerinden salgılanır. * özellikle postmenapozal ve BSO’lu Gr. HT’de hastalık takibinde kullanılabilir. * inhibin ve estrojene kıyasla diğer gonadal ve ekstragonadal tümörlerce salgılanmaz

Erişkin tip Gr. HT - FOXL 2 mutasyonu • DNA Dizileme Teknolojilerinde ki gelişmeler bu nadir over tm. lerinde yaygın mutasyon olan genlerin keşfine olanak vermiştir. • FOXL 2; normal granulosa hücrelerinin gelişimi için transkripsiyon faktörü kodlar. • FOXL 2 mutasyonu; - oldukça spesifik ve sensitif moleküler markerdir. - tipik olarak erişkin tip Gr. HT de bulunur • Erişkin tip Gr. HT - yaklaşık %97’sinde FOXL 2 geninde missence point mutasyonu (402 C →G) saptanmış (Shah et al. , 2009) • Juvenil tipte saptanmamış (nadir ? ? ). • Özellikle hasta beklenen yaşta değilse tanıya yardımcı olarak kullanılır. • Erişkin tip Gr. HT’i , juvenil tip ve diğer SKST’den ayırımda kullanılır.
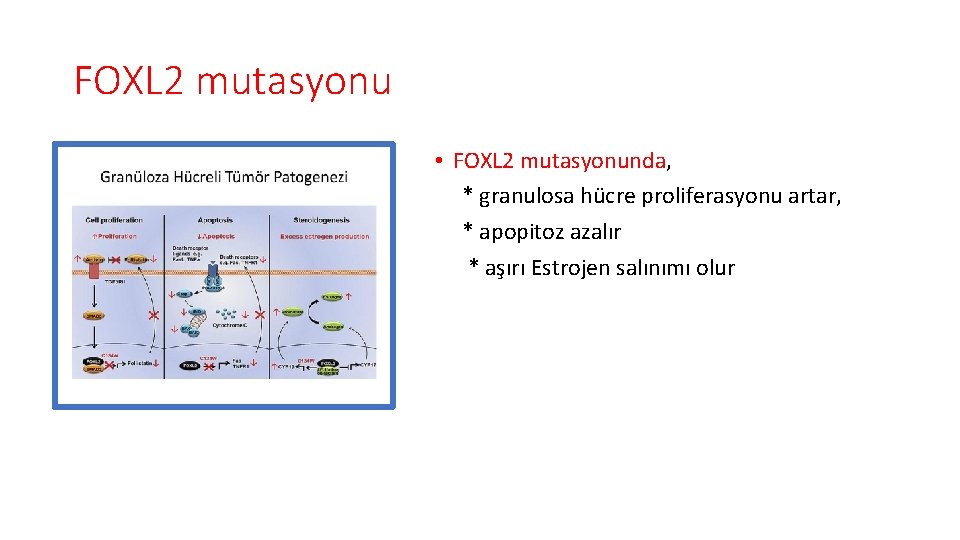
FOXL 2 mutasyonu • FOXL 2 mutasyonunda, * granulosa hücre proliferasyonu artar, * apopitoz azalır * aşırı Estrojen salınımı olur

Erişkin tip Gr. HT • Öngörülemeyen klinik gidişatı vardır • Çoğu erken evredir - kısa ve orta süreli prognozu mükemmeldir – hayat boyu TAKİP - geç nüks ve metastazlar yapar –nüks %6 -48 - ortalama =7. 2 yıl sonra - nüks olan vakada ölüm %50 -80 • Evre I hastalıkta - 5 yıllık sürvi > %90 dır. - 10 yıllık hastalıksız ve genel survi yaklaşık %90 dır. (Mc. Conechy MK et al. , 2016) • Evre III ve IV hastalıkta survi %57 -67’lere düşer. (Kottarathil et al. , 2013)

Erişkin tip Gr. HT - Prognostik faktörler • Tanı anındaki Evre; Gr. HT’lü hastaların sürvisindeki tek prognostik faktördür. • Kötü differansiye, sarkomatoid tip Gr. HT’lerin prognozu kötüdür. • Tümör rüptürü - Nüks ile ilişkili • Nuklear atipi ve artmış mitoz nüks prediktörü olarak kullanılabilir? (Ranganath et al, 2008) • Tümör boyutu (>5 cm)? • Hasta yaşı (>40) ? • P 53 ve Ki-67 prognostik değeri tartışmalı

Juvenil tip Gr. HT • En sık ilk 3 dekadda görülür. • Pre-pubertal kızlarda, %80 prekoks puberte vardır. • Artmış serum progesteron ve testesteron, baskılanmış LH ve FSH genellikle vardır. • Normal overe göre azalmış FOXL 2 ekspresyonu vardır; agresif ilerleme ile korele bulunmuş. (D’Angelo et al. , 2011) • Erken evrede, Erişkin tip Gr. HT’e göre Juvenil Gr. HT’in prognozu daha iyidir. * 3 yıldan sonra geç nüksler nadirdir. • İleri evrede, erken nüks ve agresif klinik gidişat yaygındır. (Kim et al. , 2010)

Juvenil tip Gr. HT – Genetik Duyarlılık ve Moleküler Olaylar • FOXL 2 mutasyonu nadirdir ( hatta bu vakaların yanlış sınıflandırılmış erişkin tip Gr. HT oduğu düşünülmektedir. ) (Boussios S et al. , 2017) • GNAS geninde mutasyon - %30 vakada, - özellikle ileri evre, nüks ve kötü prognoz ile ilişkili (Kalfa et al. , 2006) • PIK 3 CA/AKT sinyal yolağında disregulasyon, AKT 1 mutasyonu (%63) bildirilmiş (Bessiere et al. , 2015) * AKT inhibitörleri ile hedefe yönelik tedaviler denenebilir. • IDH 1 ve IDH 2 mutasyonları gözlenebilir. - Olier hastalığı (enkonromatosis), Maffucci sendromu (enkondromatosis ve hemangiomlar ) - Her iki sendromda da juvenil Gr. HT için artmış risk vardır

Gr. HT’de Tedavi • Bilateralite %3 • Evre IA premenaposal hastalar - USO yaparak fertilite koruyucu cerrahi için uygun. - Endometrial biopsi önerilir (senkronize endometrial kanser %5 ve endometrial hiperplazi %25) • Peri ve postmenaposal kadınlarda TAH-BSO ve full evreleme önerilir. (Kottarathil et al. , 2013) -sistematik lenfadenektomi tartışmalıdır. Rutin lenfadenektomi gereksiz. - SCST de nodal anormallik varsa reseksiyon yapılmalıdır. • KT’e cevap değişken olduğundan tam debulking cerrahi çok önemli (Boussiost et al. , 2017) • Evre I tümörler postop adjuvan tedavisiz çok iyi prognoza sahip - %5 nüks riski var. - Bazı otörler evre IC kötü prognostik faktörler varlığında adjuvan tedavi önermişler (Ray-Couqard et al. , 2014) - Nükler atipi, yüksek mitotik indeks, anöploidi, >40 yaş gibi kötü diagnostik faktörlerin yeri tartışmalı - Evre IC Gr. HT adjuvan tedavi kararında rutin kullanılmamakta bu faktörler varlığında da adjuvan KT verilmeyebilir (Foulkes WD et al. , 2016)

Gr. HT’de Adjuvan Tedavi • Platin tek başına veya kombine (CAP, PVB, BEP) kullanılabilir. • BEP en sık tercih edilen protokol - Cevap oranları (%60 -100) ve cevap süresi 5 -58 ay (Boussiost et al. , 2017) • BEP vs Taksan ve Platini karşılaştıran serilerde cevap oranları aynı %82. (Brown et al. 2005) • Adjuvan KT ile ilgili randomize çalışma yok.

Gr. HT – Nüks Hastalıkta Tedavi • Debulking cerrahi en iyi tedavidir. • BEP; Nüks hastalıkta da iyi bir seçenek gibi durmakta ama randomize çalışma yok. • Hormonal tedavi; İleri evre ve nüks erişkin tip Gr. HT’de potansiyel terapötik seçenek. -Genel olarak tedavi cevap oranı %71, - GNRH agonist, tamoxifen, progestinler ve aromataz inhibitörleri vaka serileri * Yüksek doz MPA ile uzun süreli remisyonlar (14 -42 ay ) bildirilmiş. * Anastrazol ve Letrazol ile remisyon (12 -54 ay) bildirilmiş. (Boussiost et al. , 2017) • Anastrazolün rolü uluslararası multicenter faz II PARAGON ( ANZGOG grup 0903) değerlendiriliyor. • Metastatik ve tam rezeke edilemeyen Gr. HT lerde Orteronel’in Faz II çalışması –Greko II çalışması sonuçları beklenmekte

Gr. HT – Nüks Hastalıkta Tedavi • Anti-VEGF, Bevacizumab, nüks vakalarda kullanılmış. - Gr. HT’lerde VEGF ekspresyonu oldukça yaygın (%93). - %16. 7 cevap oranı ve PFS 9. 3 ay (Broen et al. , 2014) - ALIENOR çalışması (nüks SKST’de)- haftalık paklitaksel X 6 vs haftalık paklitaksel +bevacizumab sonrasında bevacizumab 1 yıl devam ediyor. • Tirozin kinaz inhibitörleri (sorafenib) ile preklinik çalışma yapılmakta • RT - ileri evre ve metastatik Gr. HT’de yeri tartışmalı

Sertoli-Leydig Hücreli Tümörler • Primer over neoplasmlarının < %0. 5 oluşturur. • Sıklıkla 3. ve 4. dekadlarda - %75’i 40 yaş altındadır • Hormonal aktif tümörlerdir. * %30 -40’ı Androjen üretir ve >1/3’ü virilizasyon yapar. * Küçük bir grup estrojeniktir. * Çok nadir (30 vaka) AFP artışı görülmüş (germ hücre dışı AFP salgılayan tm). (El-Bahrewy et al, 2010) • Genellikle tek taraflıdır (Evre I) (%98 ) - SLST prognozu iyidir.

SLHT– Genetik Duyarlılık ve Moleküler Olaylar • SLHT’lerin %60’ında somatik DICER 1 mutasyonu bildirilmiştir. (Heravi-Moussavi et al. , 2012) - DICER 1 geni, matür micro. RNA üretimi ile ilgili endoribonukleazı kodlar. - DICER 1 mutasyonu mi. RNA işlemini etkileyen onkojenik mekanizmadır. • DICER 1 mutasyonları ile ilişkili durumlar. * Plöropulmoner blastoma , * uterin serviksin embryonal rabdomyosarkomu, * renal tümörler, * tiroid nodül ve karsinomları, * nasal kondromezenkimal hamartoma, * ciler body medulloepitelioma, pineoblastoma ve pitüiter blastoma. • DICER 1 mutasyonlarını araştırmak kişisel ya da ailevi tm risklerini belirlemek için önemlidir. - Mutasyonu olan kişilere, karşı overde de nüks riski olableceğinden uzun süreli takip önerilir.

Sertoli-Leydig Hücreli Tümörlerde Tedavi • Fertilite koruyucu cerrahi - USO yeterli. • Postmenapozal ve ileri evre hastalıkta TAH-BSO ve sitoredüktif cerrahi önerilir. • Lenf metastazı beklenmez bu nedenle evrelemede lenfadenektomi yapılmayabilir (Boussios et al. , 2017) • Evre IA-IB iyi differensiye SLHT adjuvan tedavi gerekmez.

Sertoli-Leydig Hücreli Tümörler • En önemli prognostik faktör evre ve histolojik differansiasyondur. - Evre I de 5 yıllık survi %92. 3 - ≥ Evre 2 5 yıllık survi %33 * İyi differensiye formda survi %100 * Orta ve kötü differensiye formda survi %77. 8. • Nüksler erken ama çok sık değil. * nükslerin 2/3’ü ilk 1 yılda olur. * sadece %7’si 5 yıldan sonra

Sertoli-Leydig Hücreli Tümörlerde Adjuvan Tedavi • Adjuvan tedavi ; - Grade 2 -3 hastalık ve - İleri evre varlığında düşünülebilir. • Standart adjuvan tedavi yok. • BEP, nüks vakalarda ve inkomplet rezeksiyonlarda da kullanılır. • BEP’ten daha az toksik Platin+ Taksan kombinasyonu etkili bir alternatif olabilir. Prospektif çalışma gerektirmekte.

Gelecek ve Sonuçlar • Yeni gen analizler SKST’lerin bazı alt tiplerinin patofizyolojilerini yeniden şekillendirdi. • DICER 1, STK 11, FOXL 2, GNAS, AKT 1, IDH 2 gibi gen mutasyonları bu neoplasmların gelişimini etkiler. • Bu gen mutasyonlarına yönelik ajanlar henüz yok; çalışmalar yapılabilir - Moleküler çalışmalar için büyük doku toplama çalışmaları devam etmekte. • Bu tümörler oldukça nadir olduğundan, farklı tedavi modaliteleri ile ilgili randomize çalışmalar zor bu nedenle ulusal ideal olarak uluslararası çalışmalar daha iyi olur. • Tedavi şu an için germ hücreli ya da epitelyal tümörler gibi yapılmakta ama gelişmeler devam ettikçe gelecekte tedavi genetik aberasyonlara yönelik daha kapsamlı olacak gibi gözükmekte

İLGİNİZ İÇİN TEŞEKKÜRLER
- Slides: 29