Over behandelen Wetenschappelijk onderzoek kansen voor de patint

(Over) behandelen Wetenschappelijk onderzoek: kansen voor de patiënt ? Els Witteveen Internist oncoloog UMC Utrecht Cancer Center

Inhoud Algemene begrippen Ontwikkeling van nieuwe medicamenten De feiten over wetenschappelijk onderzoek Deelname aan fase 1 Besluitvorming in de spreekkamer

Curatie versus palliatie en Intentie versus resultaat Begrippen Opzet is curatief (doel genezing) of palliatief (doel is langer behoud kwaliteit van leven) Uitkomst is respons en overleving • respons – – • complete remissie (CR) Partiele respons (PR) Stabiele ziekte (SD) Progressie (PD) overleving – – Ziekte- of progressie vrije overleving (DFS en PFS) Totale overleving (OS) CR + PR= RR CR + PR + SD = CB
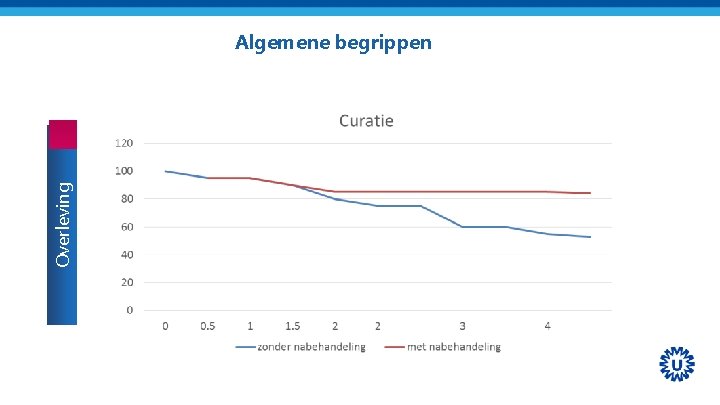
Overleving Algemene begrippen
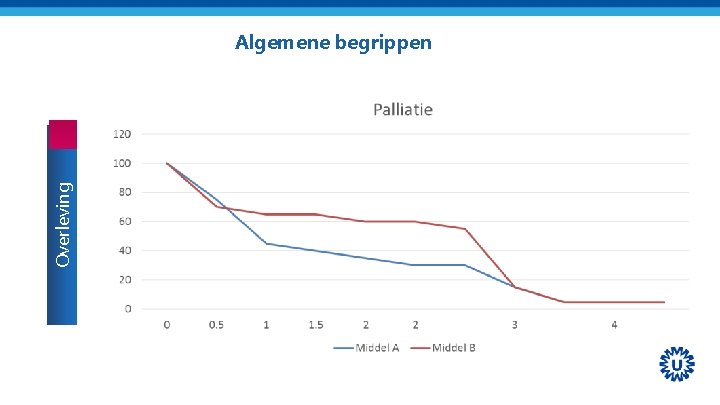
Overleving Algemene begrippen
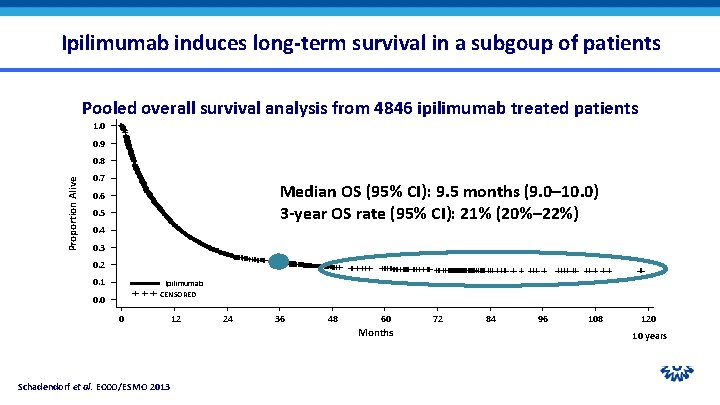
Ipilimumab induces long-term survival in a subgoup of patients Pooled overall survival analysis from 4846 ipilimumab treated patients 1. 0 0. 9 Proportion Alive 0. 8 0. 7 Median OS (95% CI): 9. 5 months (9. 0– 10. 0) 3 -year OS rate (95% CI): 21% (20%– 22%) 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 Ipilimumab CENSORED 0. 0 0 12 24 36 48 60 Months Schadendorf et al. ECCO/ESMO 2013 72 84 96 108 120 10 years
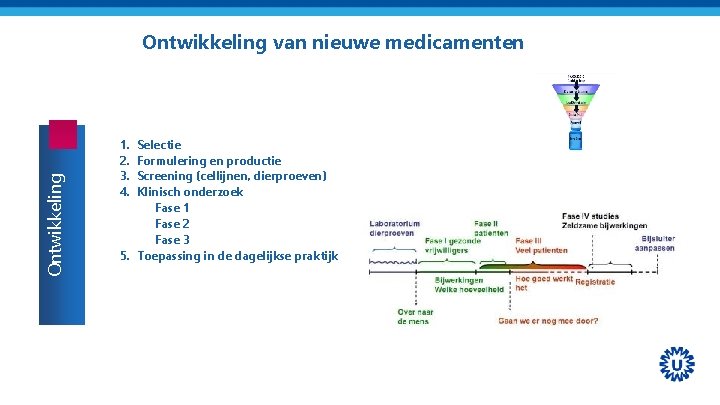
Ontwikkeling van nieuwe medicamenten 1. 2. 3. 4. Selectie Formulering en productie Screening (cellijnen, dierproeven) Klinisch onderzoek Fase 1 Fase 2 Fase 3 5. Toepassing in de dagelijkse praktijk

Ontwikkeling van nieuwe medicamenten voordat we kunnen beginnen… Ontwikkeling Medisch-wetenschappelijk onderzoek en de WMO Onderzoek dat onder de Wet medisch-wetenschappelijk onderzoek met mensen valt, moet vooraf ter goedkeuring worden voorgelegd aan een erkende METC of de CCMO.
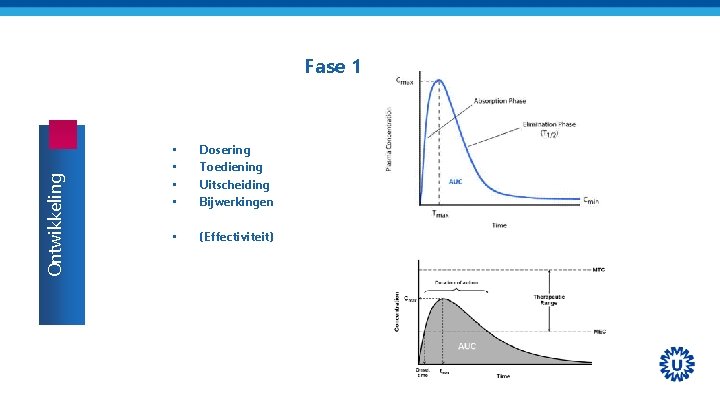
Ontwikkeling Fase 1 • • Dosering Toediening Uitscheiding Bijwerkingen • (Effectiviteit)
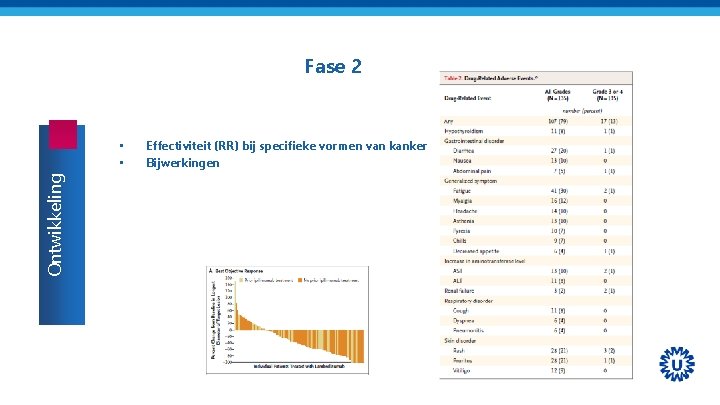
Fase 2 Ontwikkeling • • Effectiviteit (RR) bij specifieke vormen van kanker Bijwerkingen
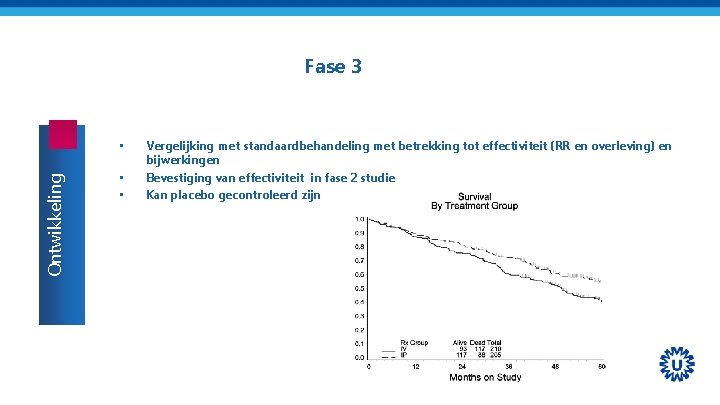
Fase 3 Ontwikkeling • • • Vergelijking met standaardbehandeling met betrekking tot effectiviteit (RR en overleving) en bijwerkingen Bevestiging van effectiviteit in fase 2 studie Kan placebo gecontroleerd zijn

Ontwikkeling van nieuwe medicamenten na het onderzoek , en dan? • Registratie Ontwikkeling – • Vergoeding (Add-on) aanvraag CFH – • Indiening dossier FDA, EMA Indiening dossier door Pharma en zorgverlener Indicatie beroepsgroep – Cie. BOM (Nv. MO) voorschrijven door artsen

Ontwikkeling Fase 4 • • Bijhouden van bijwerkingen op de lange termijn en in de algemene populatie Altijd na registratie • • LAREB Vervangen doelmatigheidsonderzoek

Waarom? Waarom nemen patienten deel aan wetenschappelijk onderzoek? • • • Om de kans op een mogelijk betere behandeling niet te missen (fase 2 en 3) Om de kans op een nieuw medicijn te krijgen (fase 2) Om nog een kans te krijgen (fase 1) • • Om een bijdrage aan het wetenschappelijk onderzoek te geven (fase 2 en 3, soms fase 1) Om voor een iemand anders iets te beteken (fase 1) • “je weet het maar nooit” ‘de laatste strohalm” “voor mijn kinderen” “niets doen is geen optie” (fase 1)

Casus Mevrouw is 52 jaar als zij een operatie ondergaat ivm een adenocarcinoom uitgaande van de urethra Echter binnen 6 maanden blijken er metastasen te zijn ontstaan in klieren (liezen en para-aortaal) en longen Voor deze zeldzame diagnose is geen standaard chemotherapie beschikbaar, een mening die gedeeld wordt door andere centra (en een zoektocht in de literatuur) Zij voelt zich te goed om niets te doen en vraagt haar internist-oncoloog of er echt niets anders is. Zij komt bij ons praten over experimentele studies.

Casus Ik was nog niet van plan om dood te gaan Beloop Niets doen past niet bij mij Ik voel mij fit genoeg om iets te proberen
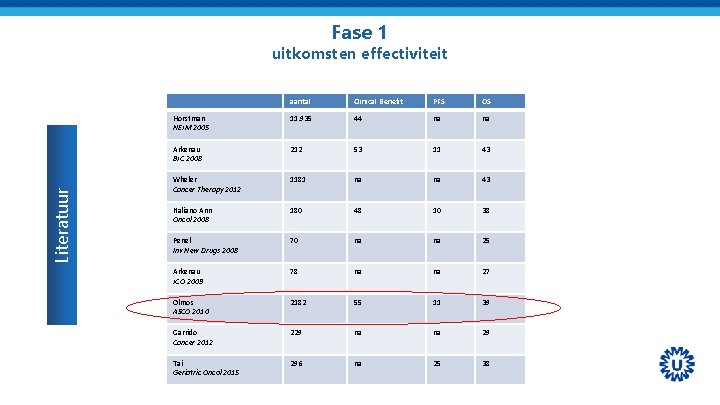
Fase 1 Literatuur uitkomsten effectiviteit aantal Clinical Benefit PFS OS Horstman NEJM 2005 11. 935 44 na na Arkenau BJC 2008 212 53 11 43 Wheler Cancer Therapy 2012 1181 na na 43 Italiano Ann Oncol 2008 180 48 10 38 Penel Inv New Drugs 2008 70 na na 25 Arkenau JCO 2009 78 na na 27 Olmos ASCO 2010 2182 55 11 39 Garrido Cancer 2012 229 na na 29 Tai Geriatric Oncol 2015 296 na 25 38
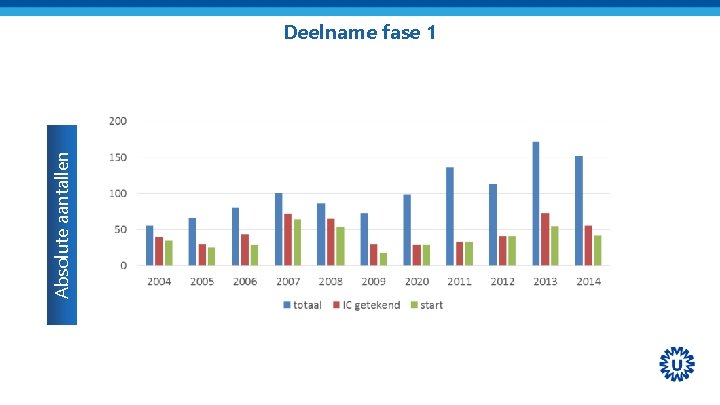
Absolute aantallen Deelname fase 1
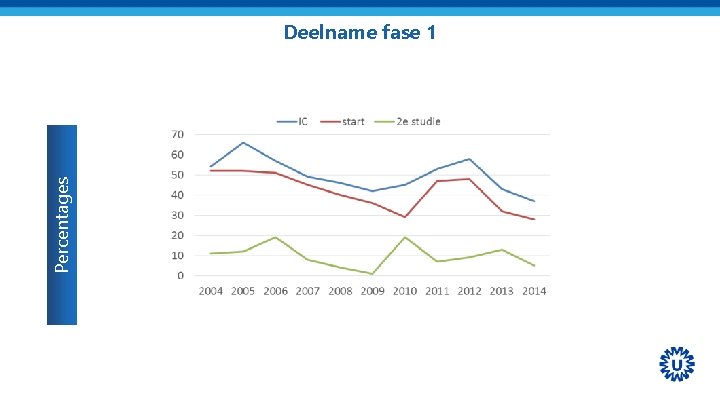
Percentages Deelname fase 1

Voorlichting 1. Wat is het doel van het onderzoek? Het belangrijkste doel is om te onderzoeken wat de hoogste dosis A is die veilig aan kankerpatiënten gegeven kan worden en wat de bijwerkingen zijn die door een behandeling met A kunnen ontstaan. Ook kunnen we door het onderzoek meer te weten komen over hoe A werkt bij kanker. Andere doelen zijn om te onderzoeken wat het middel met het lichaam doet en hoe het lichaam A afbreekt. Verdere mogelijke bijwerkingen van B B is getest in het laboratorium en bij dieren. Niemand kan zeggen welke bijwerkingen u zult krijgen en hoe ernstig deze zullen zijn. Het kan zijn dat u bijwerkingen krijgt die nog niet bekend zijn. Het zou kunnen dat er bijwerkingen ontstaan die levensbedreigend kunnen zijn of zelfs fataal. De bijwerkingen van B die tot nu toe gezien zijn bij dieren en mogelijk ook bij mensen kunnen voorkomen zijn: 1. Wat is het doel van de studie? In deze studie willen we nagaan of het nieuwe middel C veilig is en goed verdragen wordt voor patiënten met gevorderde solide tumoren. Daarnaast wordt er naar de farmacokinetiek (wat het lichaam doet met het geneesmiddel) en farmacodynamiek (wat het geneesmiddel doet met het lichaam) van C gekeken. D is nog een experimenteel middel en is door geen enkele regelgevende gezondheidsinstantie (zoals de Amerikaanse Food and Drug Administration [FDA] of het Europees Geneesmiddelenbureau [EMA]) goedgekeurd om bij mensen met gevorderde solide tumoren te worden gebruikt. Het is niet waarschijnlijk dat u persoonlijk baat heeft bij uw deelname aan dit onderzoek, aangezien niet gegarandeerd kan worden dat de H in combinatie met I is nog niet eerder bij mensen toegediend. combinatie van F en G de verdere ontwikkeling van uw kanker kan Niemand weet welke bijwerkingen u zult krijgen en zo ja, hoe hevig die voorkomen. Bovendien kan niet gegarandeerd worden dat u de kunnen zijn. Soms kunnen bijwerkingen ernstig, langdurig, blijvend of optimale dosering van de onderzoeksmedicatie toegediend, omdat zelfs levensbedreigend zijn. nog niet bepaald is wat de optimale dosering is.
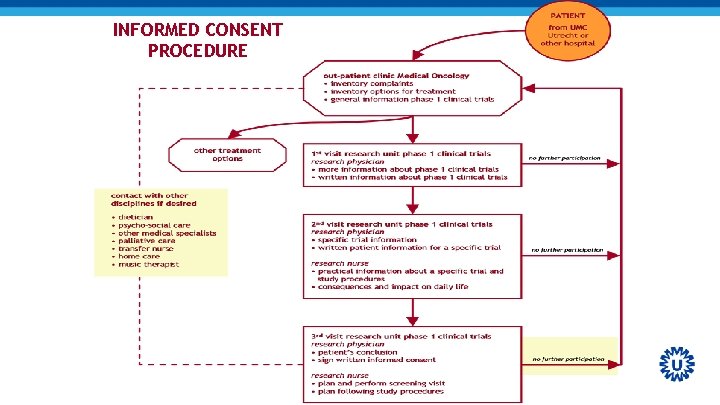
INFORMED CONSENT PROCEDURE

Informed Consent • Na informatie toestemming geven voor deelname • Samen tekenen om te laten zien dat er voorlichting heeft plaatsgevonden en patiënt weet dat hij of zij aan een studie deelneemt en alle vragen heeft kunnen stellen • Geen overname verantwoordelijkheid • Uit dossier moet duidelijk worden dat er tijd tussen informatie en tekenen heeft gezeten

Beloop Casus Zij heeft een gesprek met de internist-oncoloog, en krijgt algemene informatie over deelname aan fase 1 Zij krijg informatie op papier mee Zij praat met haar omgeving en haar huisarts Er volgt een tweede gesprek met de internist-oncoloog en zij besluit tot deelname aan fase 1 Er wordt gezocht naar een passende studie voor haar Zij wordt voorgelicht door de internist-oncoloog i. o. over de specifieke studie en krijgt de patienteninformatie op papier. Aansluitend heeft zij een gesprek met de research-verpleegkundige Twee dagen later komt zij opnieuw en tekent samen met de internist-oncoloog i. o. het toestemmingsformulier Tien dagen later begint zij met de inname van het nieuwe middel, eenmaal daags 2 tabletten.

Beloop Casus Mw V verdraagt de medicatie goed benevens huidklachten die zij met zalven goed onder controle krijgt. Een CT na 6 weken laat afname van de bekende plekken zien Een CT na 3 maanden laat alleen nog kleine plekjes in haar longen zien. Ze begon de medicatie in maart 2011 En slikt ze nog steeds….

Besluitvorming In de spreekkamer standaard of studie, de afweging blijft

Besluitvorming In de spreekkamer standaard of studie, de afweging blijft • De kans op effect is klein • geeft veel bijwerkingen • Patient heeft bijkomende ziektes • Patient twijfelt • Familie twijfelt • Studie vraagt veel extra onderzoek • De kans op effect is groot • geeft weinig bijwerkingen • Patient wil graag • Patient is fit • Veel sociale steun • Studie vraagt weinig extra onderzoek
Shared decision #samenbeslissen
Instilling empathy among doctors pays off for patient care
- Slides: 28