Ostoncrose Dfinition Infarctus osseux irrversible ncrose ischmique par

Ostéonécrose : Définition Infarctus osseux irréversible : nécrose ischémique par interruption du flux sanguin volume et topographie fixés dès le départ Fracture sous-chondrale : os supportant un cartilage articulaire fracture os mort ou os fragilisé par processus de revascularisation Arthrose secondaire : perte congruence articulaire Localisation ; diffusion tête fémorale > condyles fémoraux > tête humérale Bilatérale Multiple ou multifocale Maladie dégénérative dévastatrice adultes jeunes : 2 > 1 — 24 à 45 ans progression implacable en dépit du traitement Mécanisme inconnu Traitement non codifié

Ostéonécrose : Classification imagerie Rx standard ostéonécrose de la tête fémorale Arlet et Ficat Stade 1 : hanche symptomatique avec Rx normales Stade 2 : trame de tête a mais contour tête intact condensation, clarté ou mixte Stade 3 : perte contour ou sphéricité tête : enfoncement, collapsus signe coquille d’œuf : liseré clair sous-chondral : fracture Stade 4 : stade 3 et coxarthrose secondaire pincement interligne, ostéophytose, géodes , condensation Pronostic : perte de la sphéricité de tête fémorale tournant irréversible : évolution vers arthrose secondaire

Ostéonécrose : imagerie IRM : diagnostic précoce Liseré de démarcation : interface réactive entre os vivant et séquestre permanent et irréversible lors suivi délai survenue : 3 à 4 mois après exposition au risque signe caractéristique d’ostéonécrose Séquestre antéro-supérieur : nécrose

Ostéonécrose : Histoire naturelle (1) Ischémie Nécrose constituée, définitive, irréversible, volume immuable Interface réactionnelle : zone fragilité osseuse définitive Contraintes mécaniques nécrose réduite et/ou zone de faible contrainte : bon pronostic nécrose étendue et/ou surface portante : mauvais pronostic Délai entre Dic IRM et collapsus < 2 ans Remplacement prothétique PTH : 50% dans délai 3 ans après Dic Bilatéralisation > 50% à 3 ans

Ostéonécrose : Histoire naturelle (2) Suivi prospectif : survenue < 6 mois après exposition au risque Maladies systémiques + corticothérapie long cours et forte dose hanche normale ostéonécrose IRM 30% à 6 mois ; délai survenue IRM a : 4 mois évolution ostéonécrose Rx a : 20% ; symptomatiques + collapsus : 10% régression : 45 % Transplantés rénaux ostéonécrose : 20% à 6 mois ; délai survenue : 4 mois ostéonécrose bilatérale : 80% douleur retardée de 3 mois vs aspect IRM Lupus évolutif nouvellement diagnostiqué + introduction corticothérapie forte dose ostéonécrose hanche et genoux : 40% ; délai survenue : 3 mois multifocale : 60% (genou et hanche) ; bilatérale : 90%

Ostéonécrose : Facteurs de Risque (1) Corticothérapie : dose > durée CT forte dose et durée courte infections ORL, pulmonaire ; radiculalgie Alcoolisme consommation 150 ml/jour ou 400 ml/semaine Syndrome X : syndrome dysmétabolique DNID - intolérance aux hydrates de carbone HTA obésité abdominale Hypertriglycéridémie hyperinsulinisme - insulinorésistance Thrombophilies thrombo-embolie veineuse personnelle ou familiale dysgravidies, vasculopathie placentaire

Ostéonécrose : Facteurs de Risque (2) Drépanocytose Infection VIH Fracture déplacée ou luxation tête fémorale accident de décompression
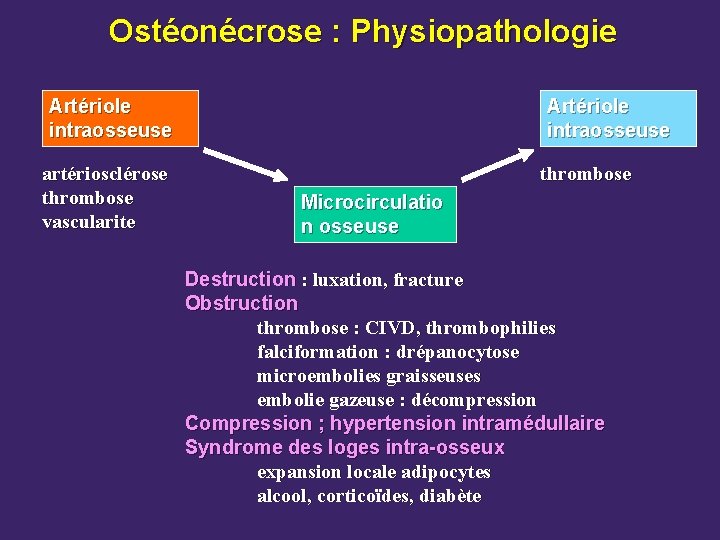
Ostéonécrose : Physiopathologie Artériole intraosseuse artériosclérose thrombose vascularite Artériole intraosseuse thrombose Microcirculatio n osseuse Destruction : luxation, fracture Obstruction thrombose : CIVD, thrombophilies falciformation : drépanocytose microembolies graisseuses embolie gazeuse : décompression Compression ; hypertension intramédullaire Syndrome des loges intra-osseux expansion locale adipocytes alcool, corticoïdes, diabète

Ostéonécrose : Traitement ? Traitement préventif chez sujets à risque : aucun éviter conjonction de facteurs de risque utilisation économe de corticothérapie Traitement médical : aucun Décompression par forage au stade précoce réduction hypertension intramédullaire : antalgie autogreffe de moelle osseuse : apport de progéniteurs osseux : potentiel ostéogénique réparateur

Titre de l'étude : Ostéonécroses de la tête fémorale et facteurs de risque acquis ou génétiques de thrombose : Rôle de l'homocystéine Première enquête épidémiologique multicentrique cas-témoin et de suivi des patients en cohorte active. Investigateur principal et coordinateur de l'étude : Bruno Tribout

Introduction, analyse de la littérature (1) Ostéonécrose de la tête fémorale infarctus osseux compliqué de fracture sous-chondrale puis d’arthrose adultes âge moyen : 25 - 45 ans ; 2 hommes/1 femme impliquée chez 10 % des prothèses de hanche implantées maladie bilatérale et/ou multifocale progression implacable en dépit du traitement : délai de 3 ans pathogénie incertaine recommandations thérapeutiques controversées

Introduction, analyse de la littérature (2) Anomalies fréquentes de l'hémostase acquises ou héréditaires ostéonécrose hypofibrinolyse (diminution de la capacité à lyser les thrombi) et/ou thrombophilie (augmentation de la capacité à former des thrombi) Hypofibrinolyses et ostéonécrose - TPA : activateur tissulaire du plasminogène - PAI-1 : inhibiteur de l'activateur tissulaire du plasminogène - lipoprotéine (a) : inhibiteur compétitif du plasminogène Facteurs de variation du taux de PAI-1 : homozygotie 4 G du polymorphisme 4 G/5 G sur le promoteur du gène du PAI-1 taux de triglycérides, insulinémie et index de masse corporelle

Introduction, analyse de la littérature (3) Thrombophilies et ostéonécrose - déficits protéine C ou protéine S, - résistance à la protéine C activée liée facteur V Leiden - mutation G 20210 A de la prothrombine - anticorps antiphospholipides - hyperhomocystéinémie Facteurs de variation du taux d'homocystéine fonctions rénale, hépatique, thyroidienne alcoolisme statut en vitamines B 2, B 6, B 12 et en folates mutation C 677 T de la méthylène tétrahydrofolate réductase Anomalies de l'hémostase acquises ou héréditaires ostéonécrose Maladie multifactorielle : interactions génétiques environnement

Objectifs (1) Fréquence accrue anomalies de l ’hémostase ostéonécrose facteurs de risque indépendants ? quantifier le risque lié à ces facteurs ? Du fait de biais méthodologiques dans le choix des témoins Première enquête épidémiologique explicative cas-témoin assortie d'un suivi prospectif en cohorte active des patients visant à évaluer l'association thrombophilies, en particuler homocystéine et ostéonécroses tant sur la survenue que sur la récidive Implications théoriques : compréhension physiopathologique des formes idiopathiques Implications pratiques : débouché potentiel vers traitement médical antithrombotiques et/ou vitamines du groupe B

Objectifs : hiérarchisation (2) Objectif primaire : rôle de l'homocystéine comme facteur de risque d'ostéonécrose Objectifs secondaires : * rôle de la sécrétion de PAI-1 et du taux de facteur VIII * rôle des polymorphismes génétiques fréquents facteur V Leiden, mutation G 20210 A de la prothombine * rôle des antiphospholipides * rôle des déficits en inhibiteurs : antithrombine, protéine C, protéine S

Méthodologie (1) 1) enquête épidémiologique étiologique d'observation avec approche explicative de type cas-témoin avec recherche rétrospective de l'exposition aux différents facteurs de risque puis 2) enquête prospective de suivi de la cohorte active de patients évaluant la récidive d'ostéonécrose et la mortalité de hanche (recours à la prothèse totale de hanche) et permettant un suivi longitudinal de l'exposition Justification d'une enquête cas-témoin : 1) hypothèse nouvelle, 2) expositions liées à l'environnement relativement faciles à reconstituer par l'interrogatoire (alcoolisme, corticothérapie), 3) l ’exposition n'est pas un facteur de recrutement, 4) maladie relativement rare, 5) maladie grave entraînant obligatoirement une hospitalisation, 6) enregistrement dans l'étude de nouveaux cas ou cas-incidents consécutifs, 7) nécessité de résultats rapides.

Méthodologie (2) Population de l'étude : Patients consécutifs adultes présentant une ostéonécrose symptomatique de la tête fémorale, uni ou bilatérale nouvellement diagnostiquée en IRM, sans contexte de maladie auto-immune ou de transplantation, susceptibles d'être suivis prospectivement et relevant d'un traitement chirurgical (forage avec autogreffe de moelle osseuse, prothèse totale de hanche). Témoins hospitaliers choisis parmi les patients hospitalisés pour des pathologies rhumatologiques non malignes non inflammatoires (arthrose, lombalgies, fibromyalgie …) et appariés en âge (± 5 ans), sexe, origine géographique et durée d'hospitalisation. Deux témoins hospitaliers seront recrutés pour un patient atteint d'ostéonécrose. Nombre de sujets prévus et nécessaires pour l'étude statistique : 150 patients – 300 témoins hospitaliers

Méthodologie (3) Préétude : homocystéinémie 40 patients ostéonécroses versus 39 témoins hospitaliers 11, 5 ± 7, 5 µmol/l p < 0, 0001 8 ± 2 µmol/l Etude multicentrique : 2 centres : Institut Calot (Berck), CHU Amiens Durée période prospective de suivi : 3 ans Dates prévisionnelles de début d'étude : 01/01/2003 de fin d'étude : 31/12/2005
- Slides: 18