Organische moleculen Organische moleculen 4 basiskarakteristieken 1 Meeste

Organische moleculen

Organische moleculen 4 basiskarakteristieken 1. Meeste moleculen hebben koolstofskelet 2. Slecht uit enkele elementen opgebouwd H 2, O 2, C, N 99, 4 % 3. Modulair opgebouwd 4. Vorm bepaalt het gedrag
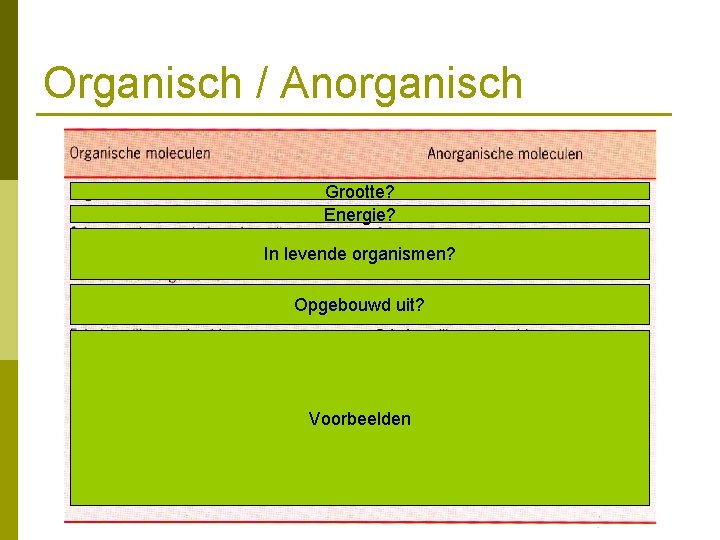
Organisch / Anorganisch Grootte? Energie? In levende organismen? Opgebouwd uit? Voorbeelden

Organische moleculen Koolydraten polymeer p Vetten p Eiwitten polymeer p Nucleïnezuren polymeer p
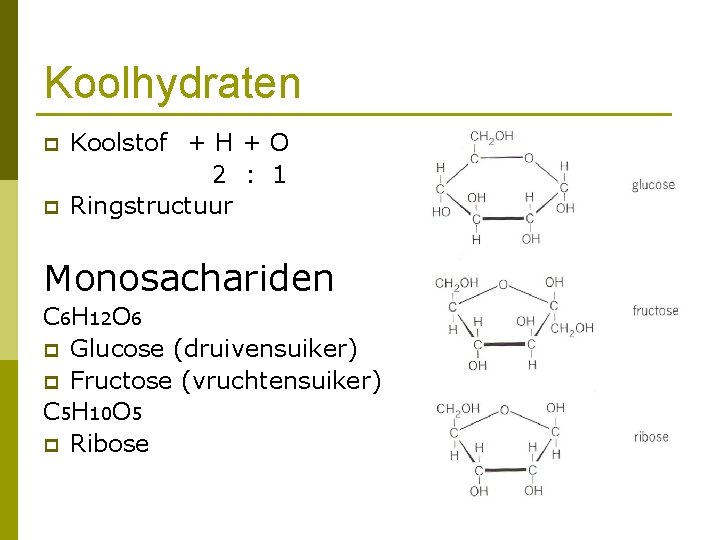
Koolhydraten p p Koolstof + H + O 2 : 1 Ringstructuur Monosachariden C 6 H 12 O 6 p Glucose (druivensuiker) p Fructose (vruchtensuiker) C 5 H 10 O 5 p Ribose
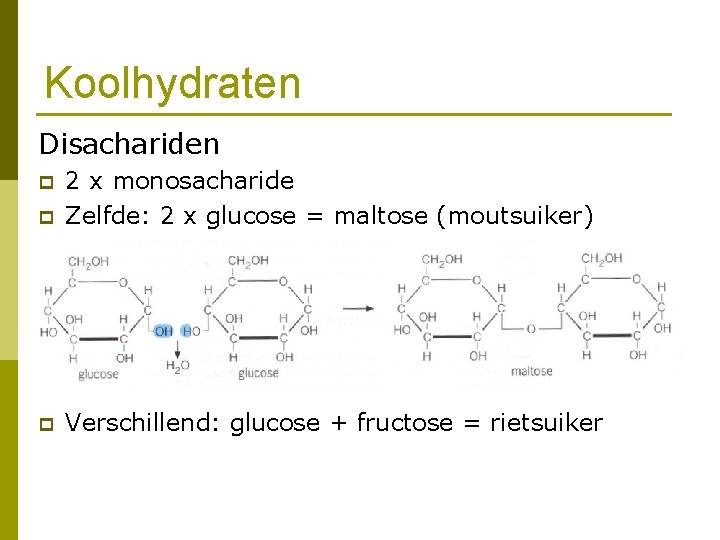
Koolhydraten Disachariden p 2 x monosacharide Zelfde: 2 x glucose = maltose (moutsuiker) p Verschillend: glucose + fructose = rietsuiker p
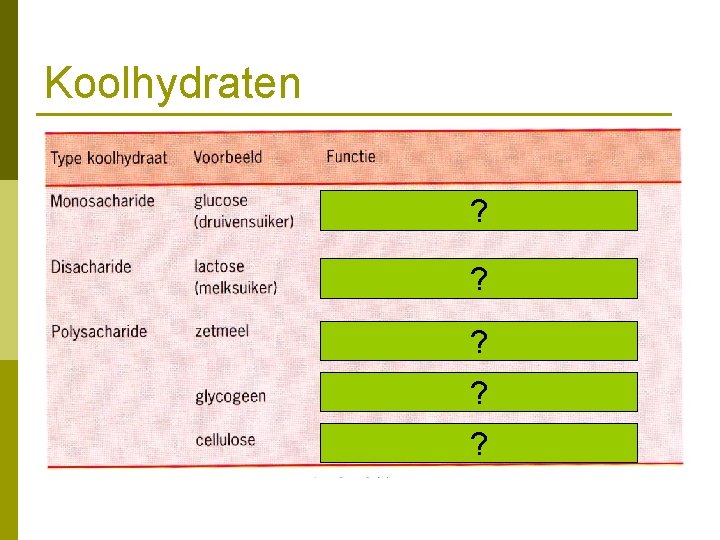
Koolhydraten ? ? ?

Lipiden =? p vetten en vetachtige stoffen p Eigenschappen: n n Apolair (niet oplosbaar in water) Reservestof, brandstof, bouwstof
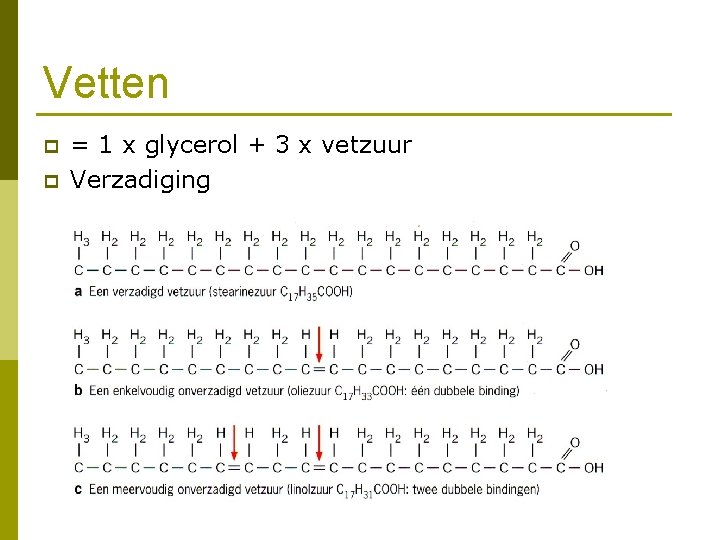
Vetten p p = 1 x glycerol + 3 x vetzuur Verzadiging
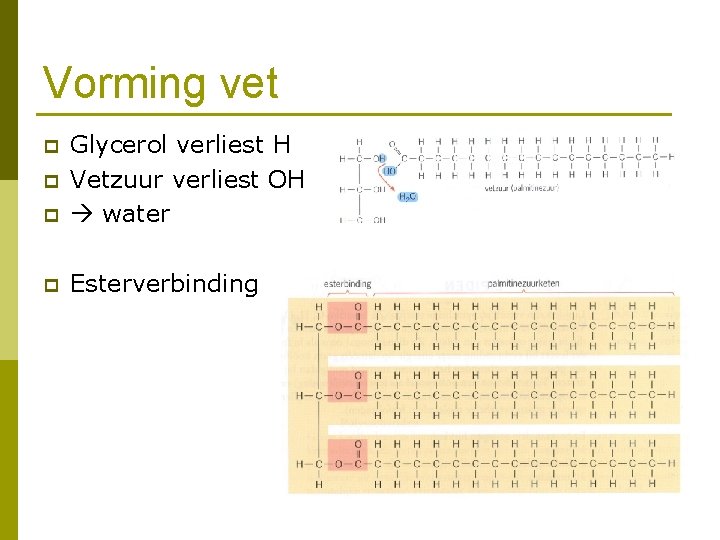
Vorming vet p Glycerol verliest H Vetzuur verliest OH water p Esterverbinding p p
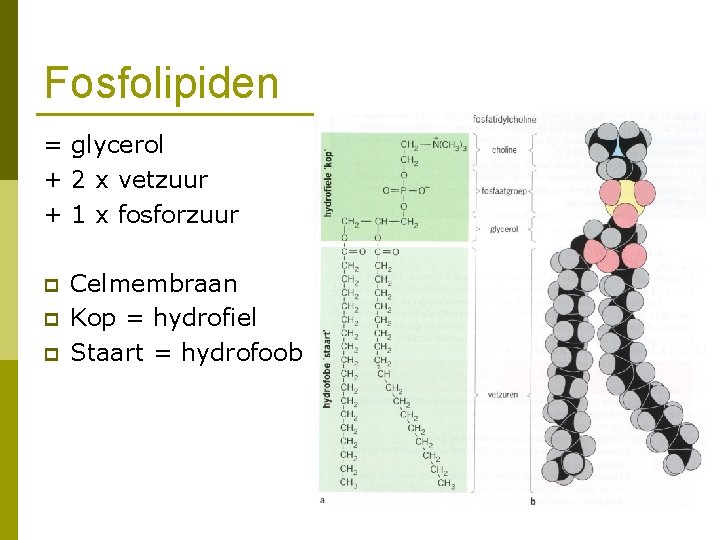
Fosfolipiden = glycerol + 2 x vetzuur + 1 x fosforzuur p p p Celmembraan Kop = hydrofiel Staart = hydrofoob
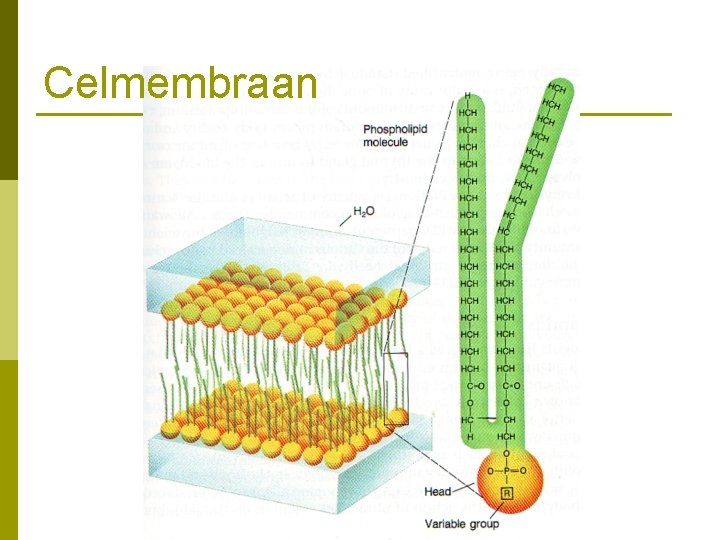
Celmembraan

Eiwitten C, H, O, N, (S) p Proteïnen p Heel veel functies: p n n n n Zenuwstel (neurotransmitters) Spierwerking (actine / myosine) Stoffentransport (hemoglobine – O 2) Afweer (antistoffen) Enzymwerking (katalysator) Homonale werking Bloedstolling (plasma eiwitten)
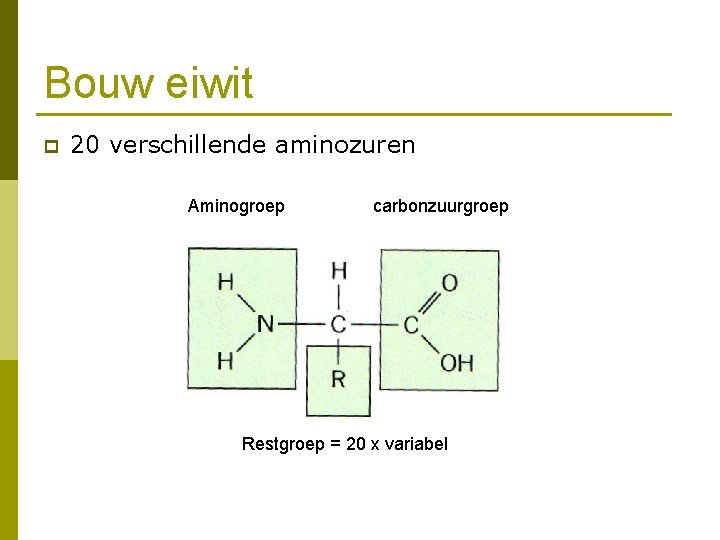
Bouw eiwit p 20 verschillende aminozuren Aminogroep carbonzuurgroep Restgroep = 20 x variabel
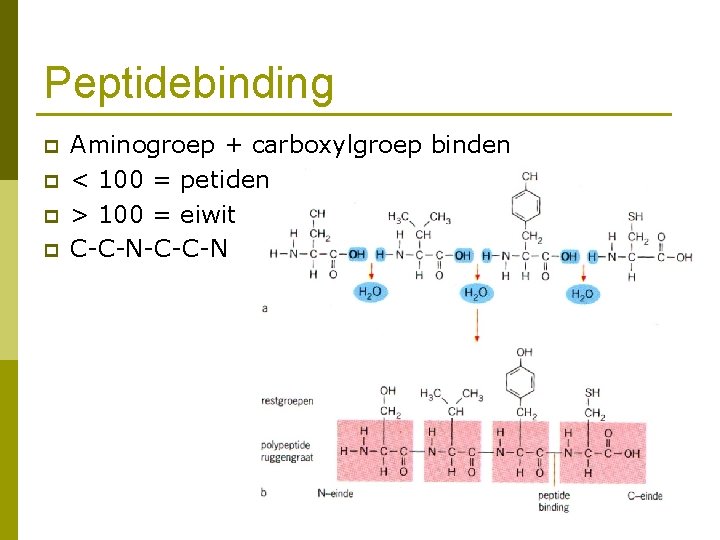
Peptidebinding p p Aminogroep + carboxylgroep binden < 100 = petiden > 100 = eiwit C-C-N-C-C-N

Vorm van eiwitten Primair Volgorde aminozuren
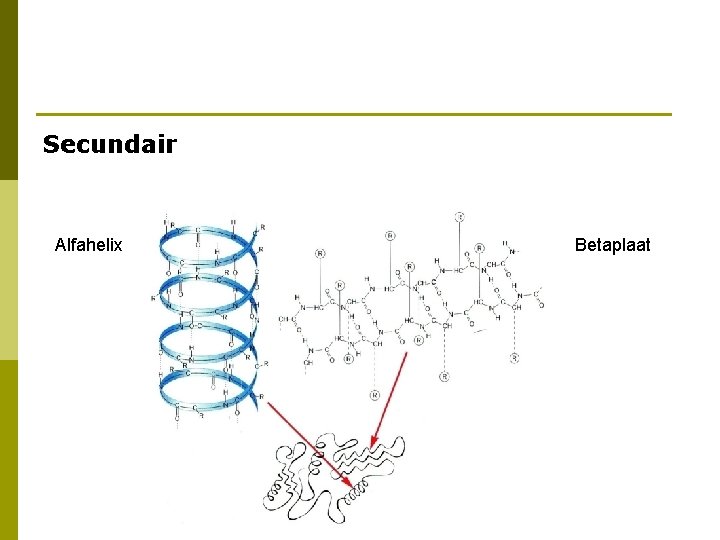
Secundair Alfahelix Betaplaat
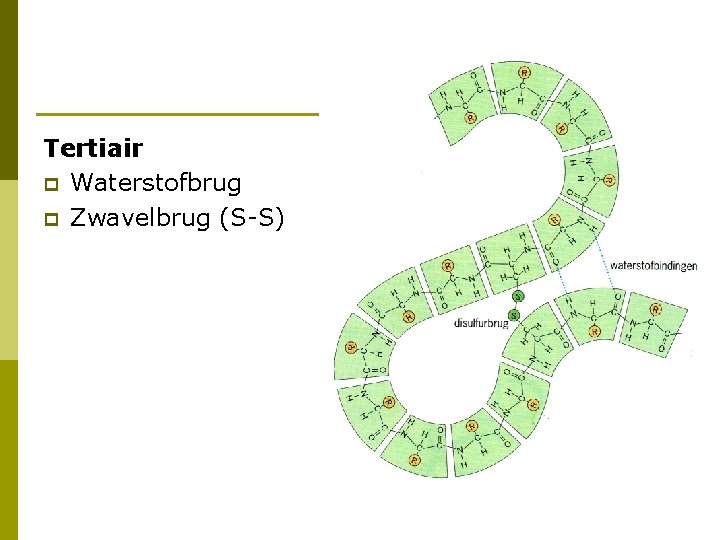
Tertiair p Waterstofbrug p Zwavelbrug (S-S)
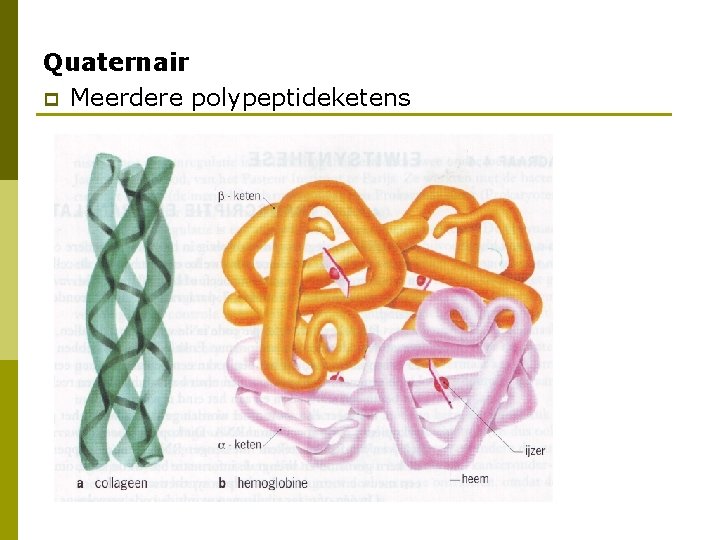
Quaternair p Meerdere polypeptideketens
- Slides: 19