Organick sloueniny obsahujc kyslk dusk a sru Biologicky

Organické sloučeniny obsahující kyslík, dusík a síru Biologicky významné heterocykly Martina Srbová

Organické sloučeniny obsahující kyslík

Elektronová konfigurace atomu kyslíku 1 s 2 2 p 4 Z elektronové konfigurace kyslíku vyplývá, že v molekule organické sloučeniny může být kovalentně vázán jako dvojvazný. O O
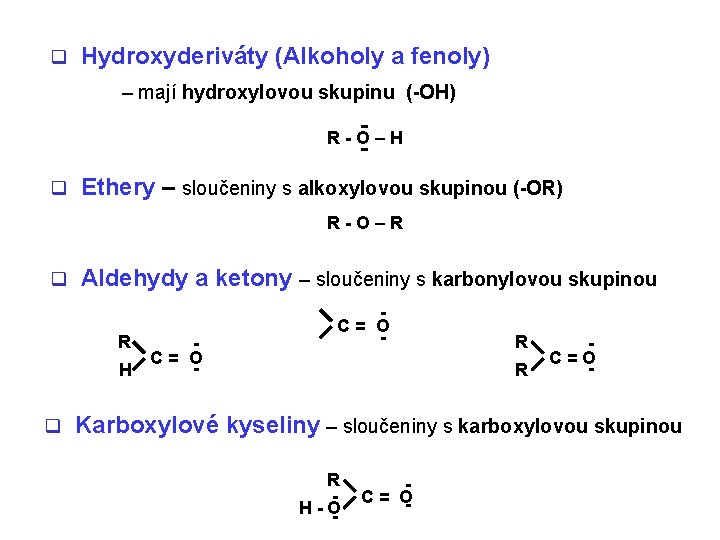
q Hydroxyderiváty (Alkoholy a fenoly) – mají hydroxylovou skupinu (-OH) R-O–H q Ethery – sloučeniny s alkoxylovou skupinou (-OR) R-O–R q Aldehydy a ketony – sloučeniny s karbonylovou skupinou R C= O H q C= O - R R C=O - Karboxylové kyseliny – sloučeniny s karboxylovou skupinou R H -O - - C = O-
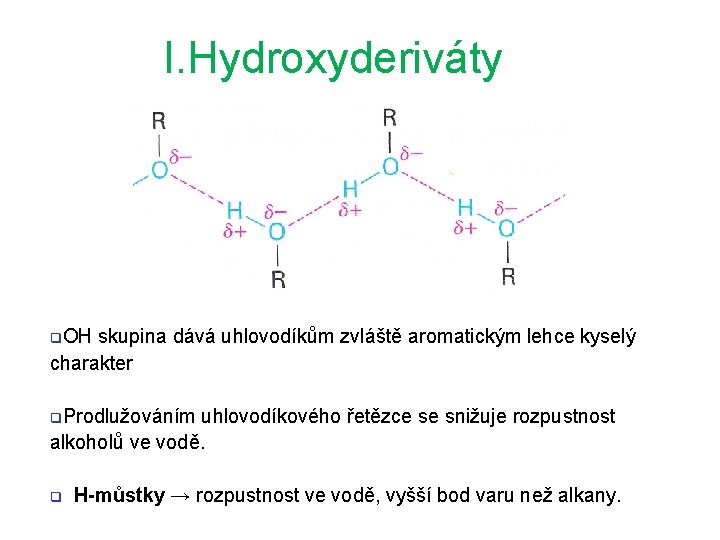
I. Hydroxyderiváty q. OH skupina dává uhlovodíkům zvláště aromatickým lehce kyselý charakter q. Prodlužováním uhlovodíkového řetězce se snižuje rozpustnost alkoholů ve vodě. q H-můstky → rozpustnost ve vodě, vyšší bod varu než alkany.
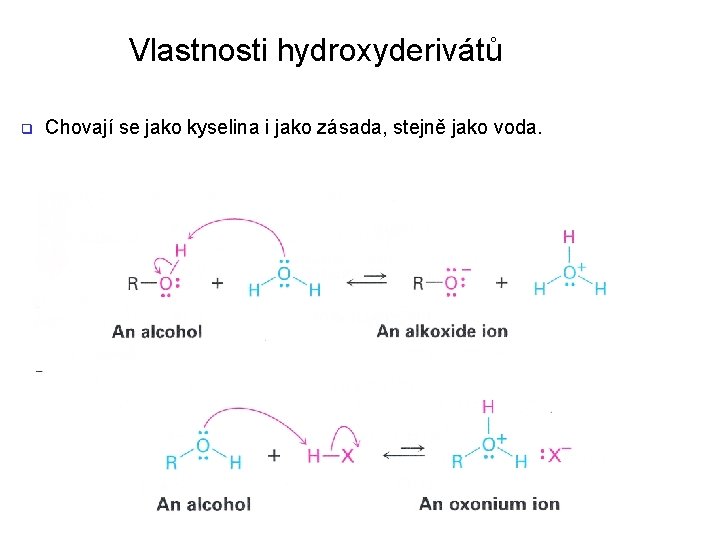
Vlastnosti hydroxyderivátů q Chovají se jako kyselina i jako zásada, stejně jako voda.

Hydroxyderiváty Podle počtu –OH skupin v molekule: • Monohydroxyderiváty • Polyhydroxyderiváty (polyoly) Dioly (dihydroxyderiváty) Trioly (trihydroxyderiváty) Tetroly (tetrahydroxyderiváty) • Fenoly: -OH se přímo váže na aromatické jádro
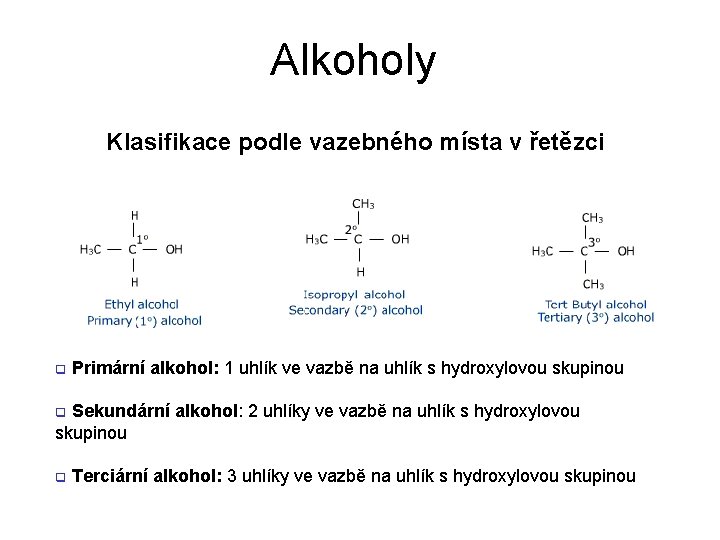
Alkoholy Klasifikace podle vazebného místa v řetězci q Primární alkohol: 1 uhlík ve vazbě na uhlík s hydroxylovou skupinou Sekundární alkohol: 2 uhlíky ve vazbě na uhlík s hydroxylovou skupinou q q Terciární alkohol: 3 uhlíky ve vazbě na uhlík s hydroxylovou skupinou
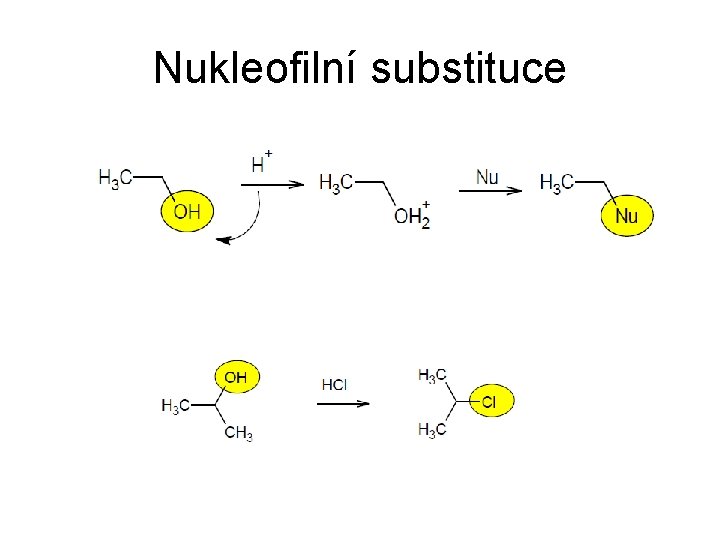
Nukleofilní substituce
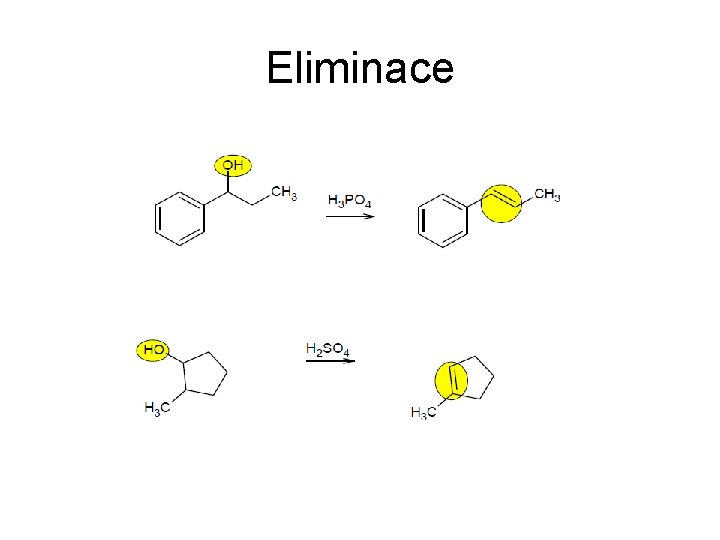
Eliminace
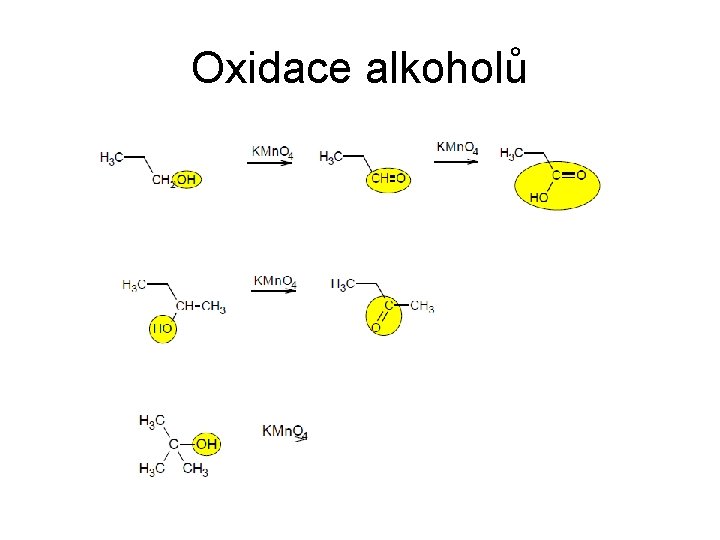
Oxidace alkoholů

Metanol: silně jedovatý, oslepnutí, smrt Etanol (spiritus, líh) Kvasné procesy cukerných šťáv rostlin za přítomnosti kvasinek při teplotě nižší než 37°C. q Nejprve excitační účinky, posléze narkotické účinky, působí jako sedativum. Návyková droga. q q Letální dávka je 6 -8 g/kg ( 1 l vodky).
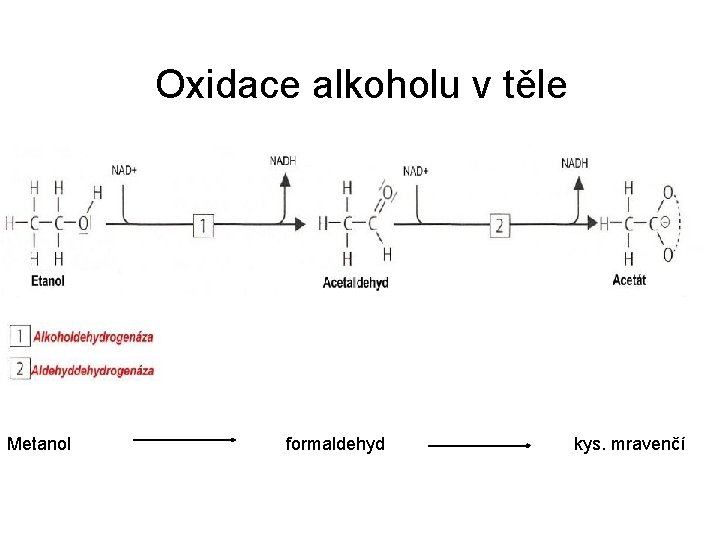
Oxidace alkoholu v těle q Methanol se v játrech oxiduje na formaldehyd Metanol formaldehyd kys. mravenčí

Ethylenglykol - ethan-1, 2 -diol HO–CH 2–OH q Používá se do nemrznoucích směsí Fridex Toxický: 50 ml, letální: 100 ml Nasládlá chut‘, rozpustný ve vodě Glycerol - propan-1, 2, 3 -triol (glycerin) CH 2 - OH Uhlíková kostra glycerolu je součástí biologicky významných látek v organismu q CH - OH CH 2 - OH
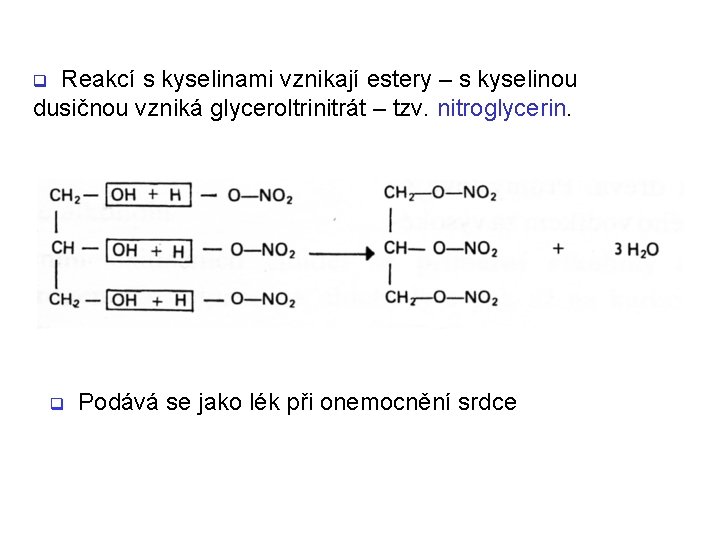
Reakcí s kyselinami vznikají estery – s kyselinou dusičnou vzniká glyceroltrinitrát – tzv. nitroglycerin. q q Podává se jako lék při onemocnění srdce
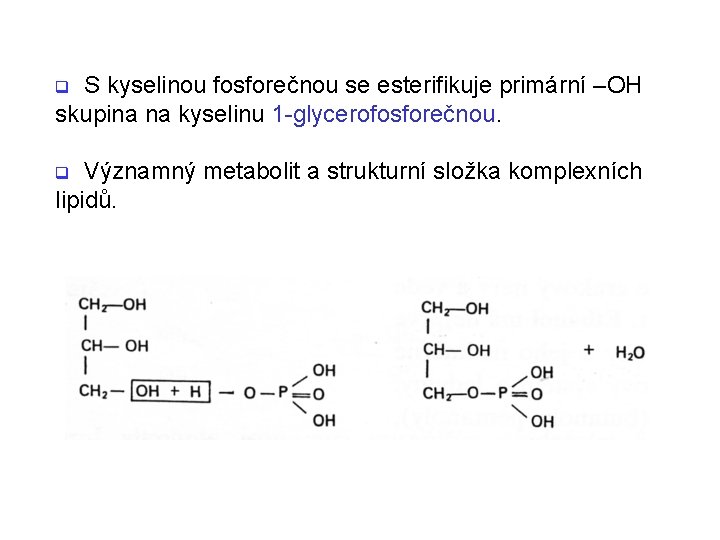
S kyselinou fosforečnou se esterifikuje primární –OH skupina na kyselinu 1 -glycerofosforečnou. q Významný metabolit a strukturní složka komplexních lipidů. q
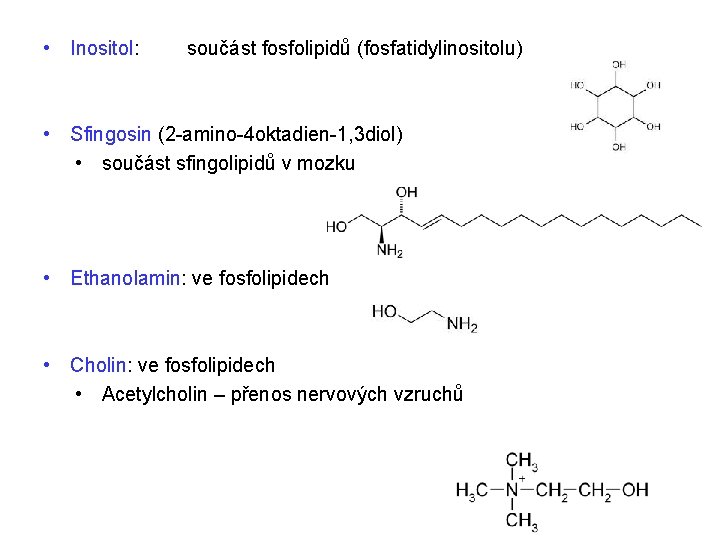
• Inositol: součást fosfolipidů (fosfatidylinositolu) • Sfingosin (2 -amino-4 oktadien-1, 3 diol) • součást sfingolipidů v mozku • Ethanolamin: ve fosfolipidech • Cholin: ve fosfolipidech • Acetylcholin – přenos nervových vzruchů
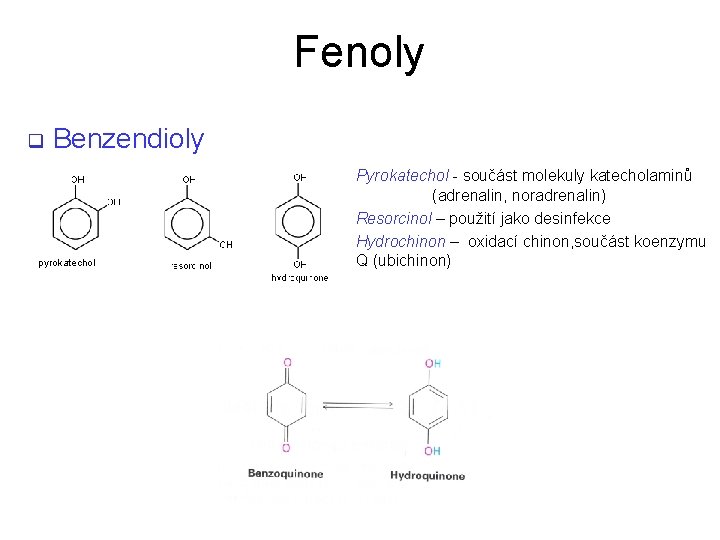
Fenoly q Benzendioly pyrokatechol Pyrokatechol - součást molekuly katecholaminů (adrenalin, noradrenalin) Resorcinol – použití jako desinfekce Hydrochinon – oxidací chinon, součást koenzymu Q (ubichinon)
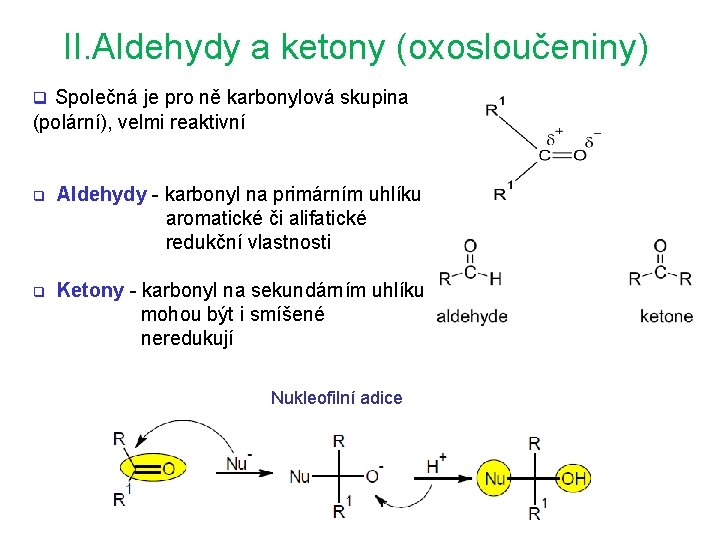
II. Aldehydy a ketony (oxosloučeniny) q Společná je pro ně karbonylová skupina (polární), velmi reaktivní q Aldehydy - karbonyl na primárním uhlíku aromatické či alifatické redukční vlastnosti q Ketony - karbonyl na sekundárním uhlíku mohou být i smíšené neredukují Nukleofilní adice
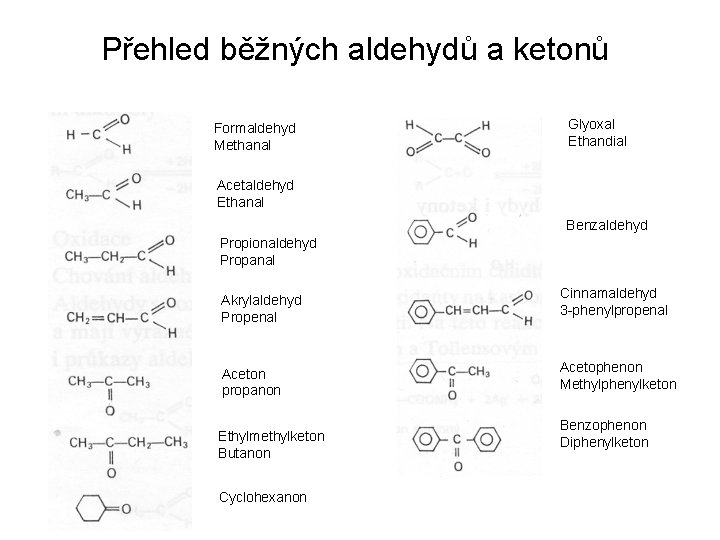
Přehled běžných aldehydů a ketonů Formaldehyd Methanal Glyoxal Ethandial Acetaldehyd Ethanal Benzaldehyd Propionaldehyd Propanal Akrylaldehyd Propenal Cinnamaldehyd 3 -phenylpropenal Aceton propanon Acetophenon Methylphenylketon Ethylmethylketon Butanon Cyclohexanon Benzophenon Diphenylketon
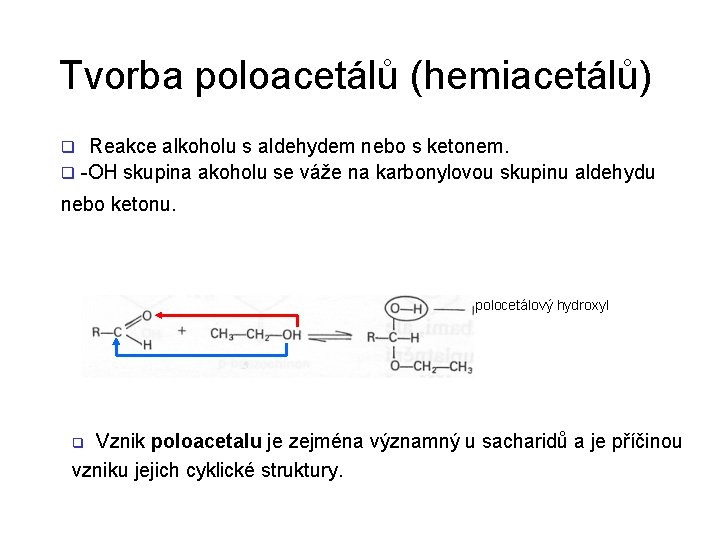
Tvorba poloacetálů (hemiacetálů) Reakce alkoholu s aldehydem nebo s ketonem. q -OH skupina akoholu se váže na karbonylovou skupinu aldehydu q nebo ketonu. polocetálový hydroxyl Vznik poloacetalu je zejména významný u sacharidů a je příčinou vzniku jejich cyklické struktury. q
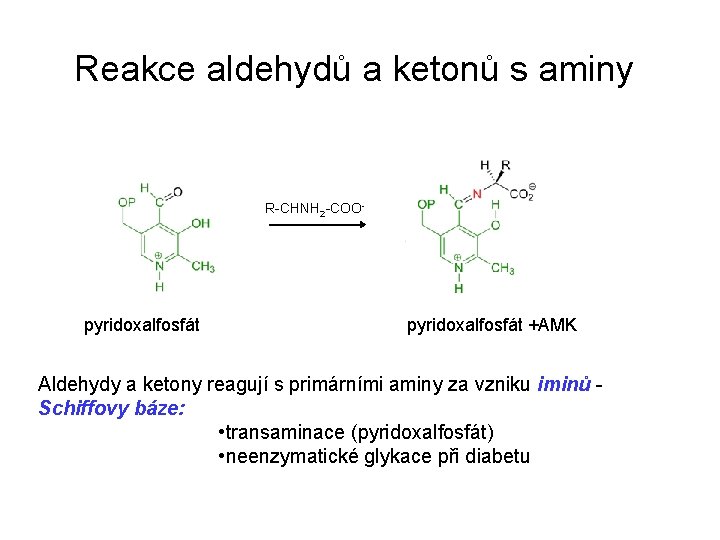
Reakce aldehydů a ketonů s aminy R-CHNH 2 -COO- pyridoxalfosfát +AMK Aldehydy a ketony reagují s primárními aminy za vzniku iminů Schiffovy báze: • transaminace (pyridoxalfosfát) • neenzymatické glykace při diabetu
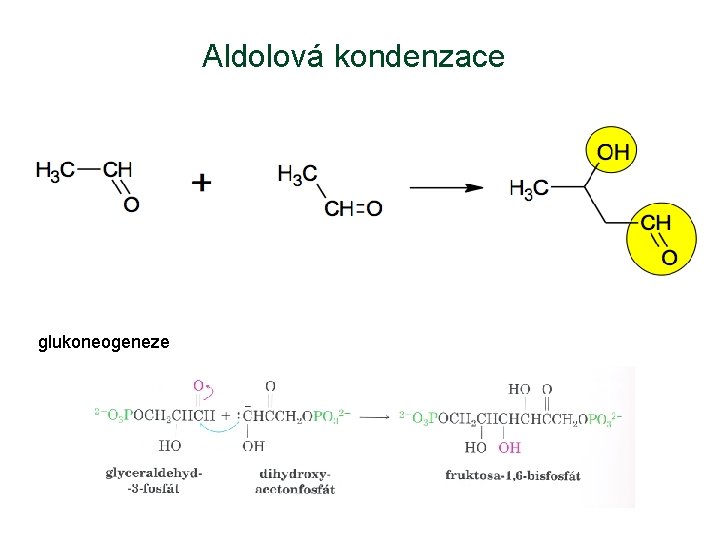
Aldolová kondenzace glukoneogeneze
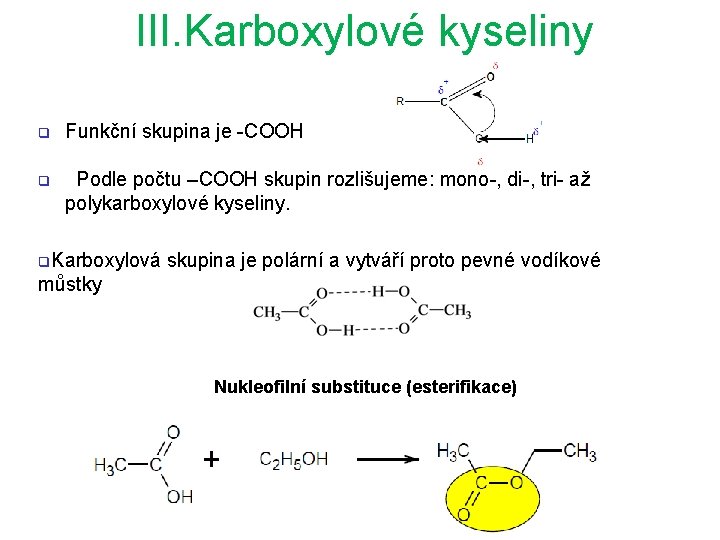
III. Karboxylové kyseliny q Funkční skupina je -COOH q Podle počtu –COOH skupin rozlišujeme: mono-, di-, tri- až polykarboxylové kyseliny. q. Karboxylová skupina je polární a vytváří proto pevné vodíkové můstky Nukleofilní substituce (esterifikace)
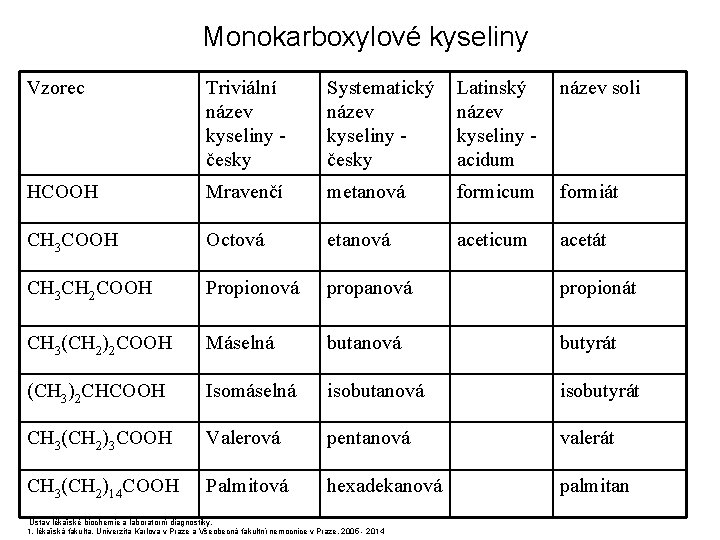
Monokarboxylové kyseliny Vzorec Triviální název kyseliny - česky Systematický název kyseliny - česky Latinský název soli název kyseliny - acidum HCOOH Mravenčí metanová formicum formiát CH 3 COOH Octová etanová aceticum acetát CH 3 CH 2 COOH Propionová propanová propionát CH 3(CH 2)2 COOH Máselná butanová butyrát (CH 3)2 CHCOOH Isomáselná isobutanová isobutyrát CH 3(CH 2)3 COOH Valerová pentanová valerát CH 3(CH 2)14 COOH Palmitová hexadekanová palmitan Ústav lékařské biochemie a laboratorní diagnostiky, 1. lékařská fakulta, Univerzita Karlova v Praze a Všeobecná fakultní nemocnice v Praze, 2005 - 2014
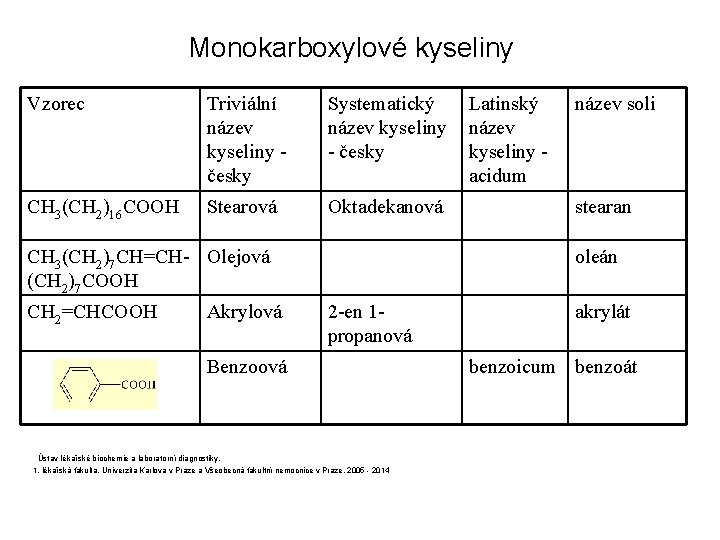
Monokarboxylové kyseliny Vzorec Triviální název kyseliny - česky Systematický Latinský název kyseliny název - česky kyseliny - acidum název soli CH 3(CH 2)16 COOH Stearová Oktadekanová stearan CH 3(CH 2)7 CH=CH- Olejová (CH 2)7 COOH oleán CH 2=CHCOOH Akrylová 2 -en 1 propanová Benzoová benzoicum benzoát Ústav lékařské biochemie a laboratorní diagnostiky, 1. lékařská fakulta, Univerzita Karlova v Praze a Všeobecná fakultní nemocnice v Praze, 2005 - 2014 akrylát
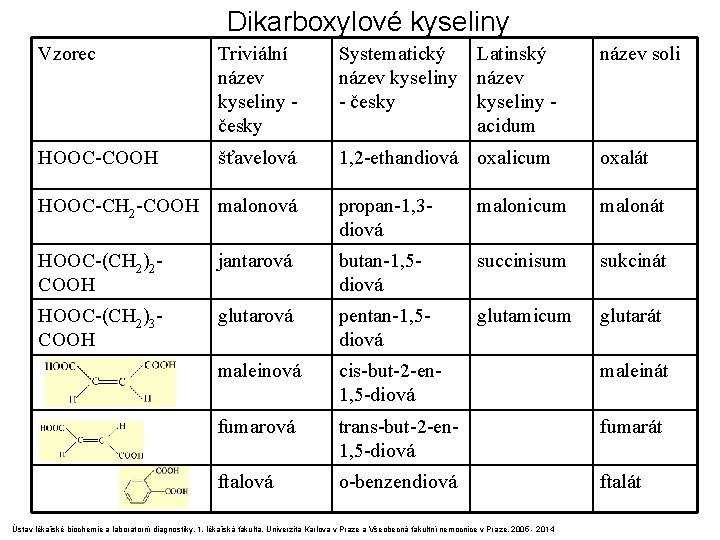
Dikarboxylové kyseliny Vzorec Triviální název kyseliny - česky Systematický Latinský název kyseliny název - česky kyseliny - acidum název soli HOOC-COOH šťavelová 1, 2 -ethandiová oxalicum oxalát HOOC-CH 2 -COOH malonová propan-1, 3 diová malonicum malonát HOOC-(CH 2)2 COOH jantarová butan-1, 5 diová succinisum sukcinát HOOC-(CH 2)3 COOH glutarová pentan-1, 5 diová glutamicum glutarát maleinová cis-but-2 -en 1, 5 -diová maleinát fumarová trans-but-2 -en 1, 5 -diová fumarát ftalová o-benzendiová Ústav lékařské biochemie a laboratorní diagnostiky, 1. lékařská fakulta, Univerzita Karlova v Praze a Všeobecná fakultní nemocnice v Praze, 2005 - 2014 ftalát
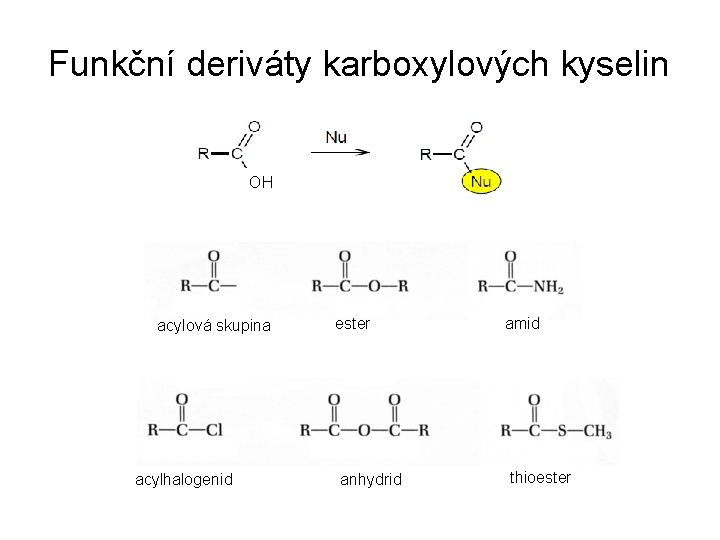
Funkční deriváty karboxylových kyselin OH acylová skupina acylhalogenid ester anhydrid amid thioester
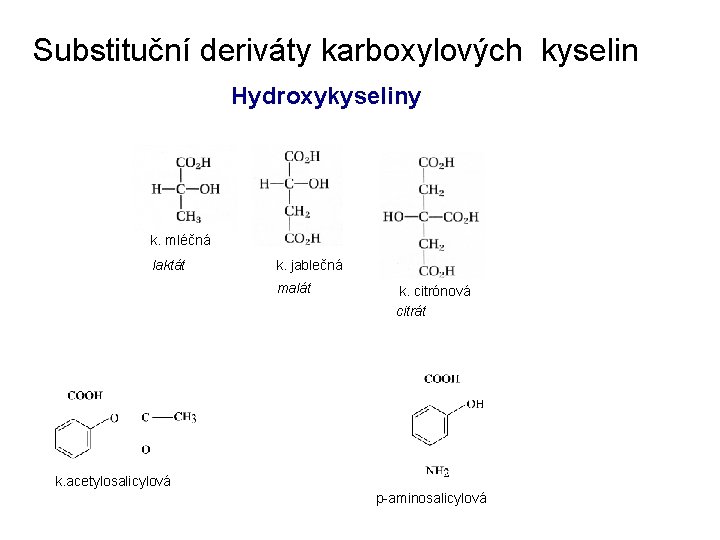
Substituční deriváty karboxylových kyselin Hydroxykyseliny k. mléčná laktát k. jablečná malát k. citrónová citrát k. acetylosalicylová p-aminosalicylová
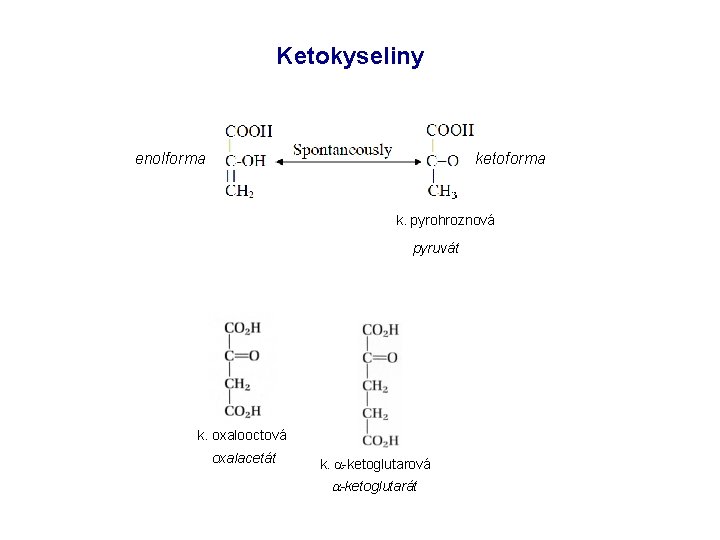
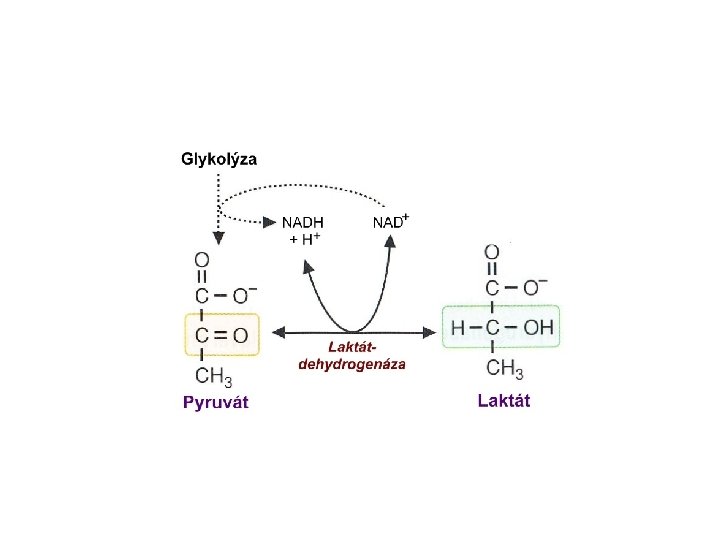
Ketokyseliny enolforma ketoforma k. pyrohroznová pyruvát k. oxalooctová oxalacetát k. a-ketoglutarová a-ketoglutarát

Organické sloučeniny obsahující dusík
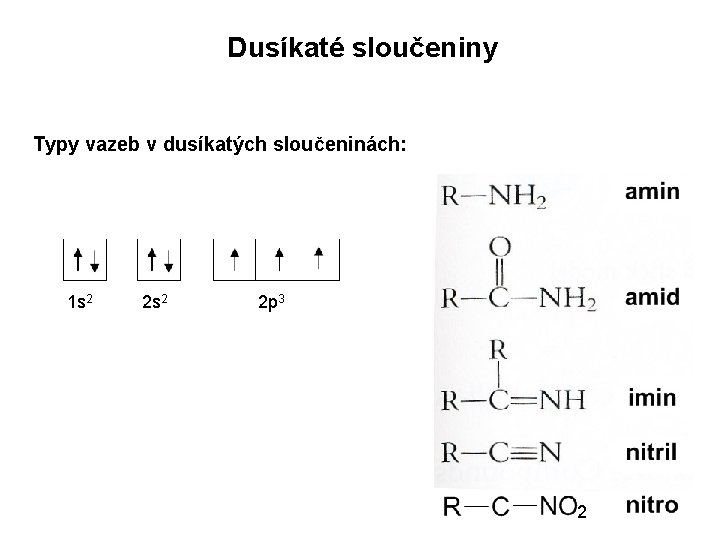
Dusíkaté sloučeniny Typy vazeb v dusíkatých sloučeninách: 1 s 2 2 p 3 2
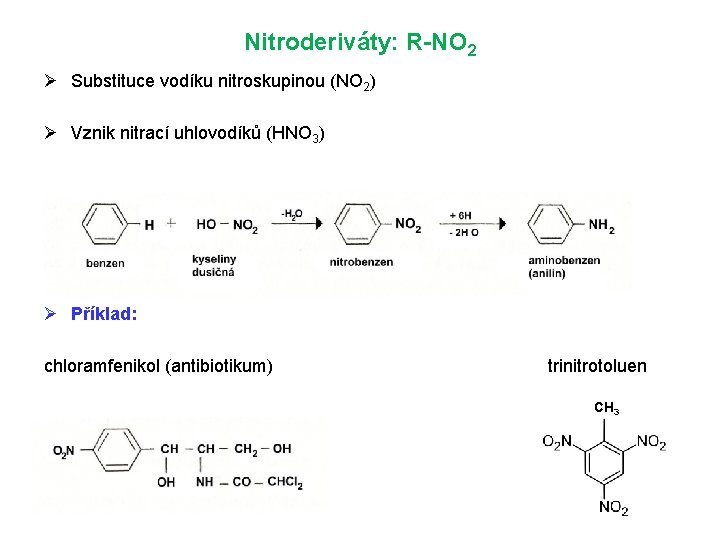
Nitroderiváty: R-NO 2 Ø Substituce vodíku nitroskupinou (NO 2) Ø Vznik nitrací uhlovodíků (HNO 3) Ø Příklad: chloramfenikol (antibiotikum) trinitrotoluen CH 3
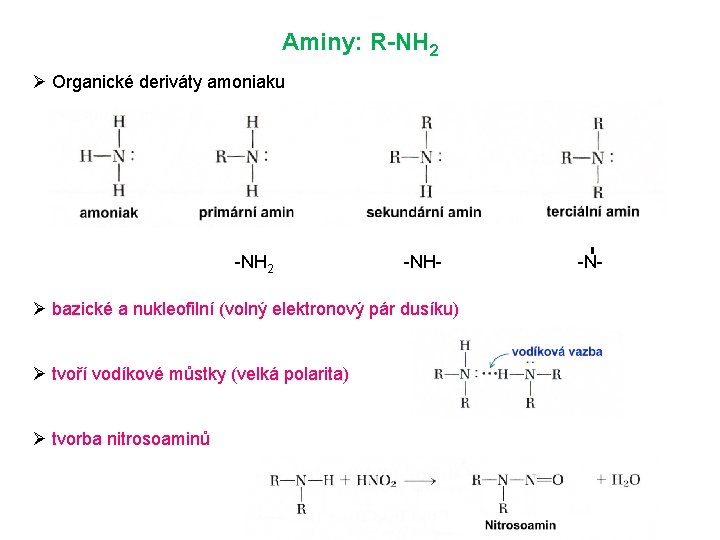
Aminy: R-NH 2 Ø Organické deriváty amoniaku -NH 2 -NH- Ø bazické a nukleofilní (volný elektronový pár dusíku) Ø tvoří vodíkové můstky (velká polarita) Ø tvorba nitrosoaminů -N-

Význam aminů: Nejdůležitější organické zásady Význam v biochemii: Ø kvartérní amoniové báze Ø biogenní aminy Ø aminokyseliny Ø proteiny Ø alkaloidy
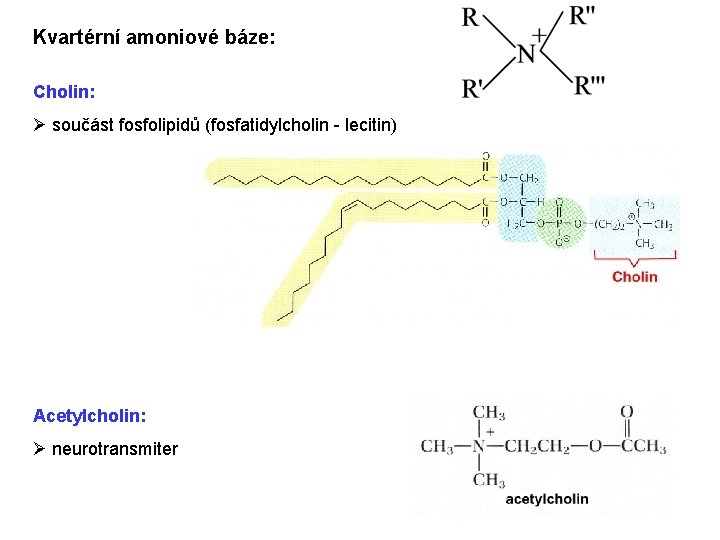
Kvartérní amoniové báze: Cholin: Ø součást fosfolipidů (fosfatidylcholin - lecitin) Acetylcholin: Ø neurotransmiter
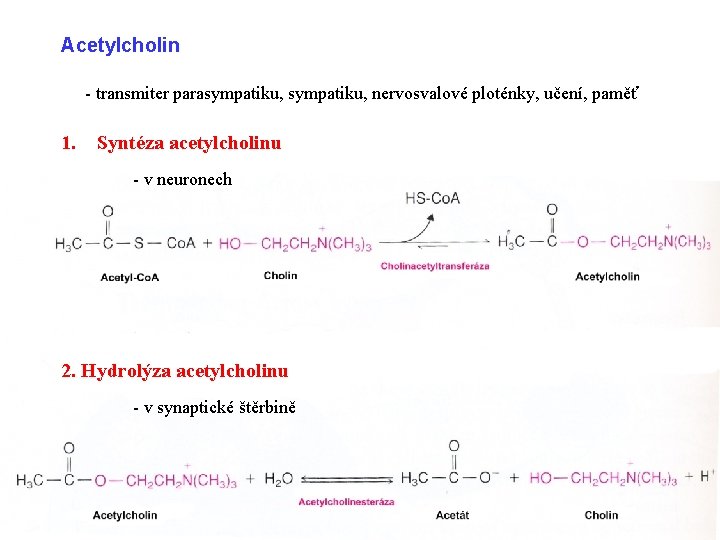
Acetylcholin - transmiter parasympatiku, nervosvalové ploténky, učení, paměť 1. Syntéza acetylcholinu - v neuronech 2. Hydrolýza acetylcholinu - v synaptické štěrbině
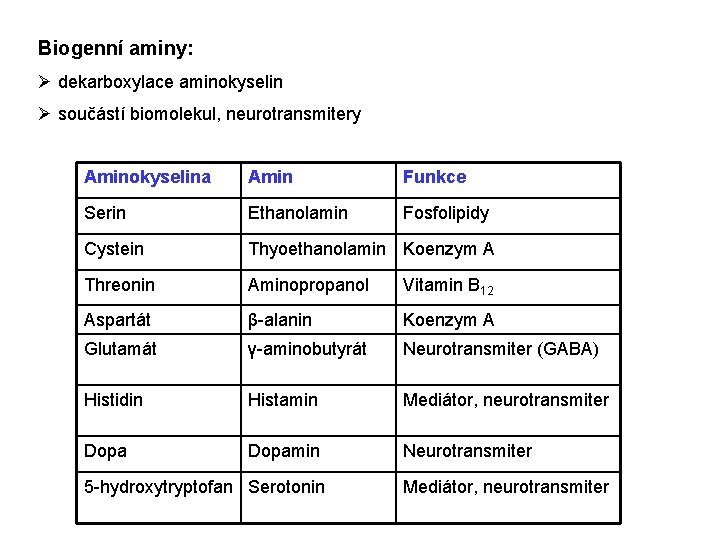
Biogenní aminy: Ø dekarboxylace aminokyselin Ø součástí biomolekul, neurotransmitery Aminokyselina Amin Funkce Serin Ethanolamin Fosfolipidy Cystein Thyoethanolamin Koenzym A Threonin Aminopropanol Vitamin B 12 Aspartát β-alanin Koenzym A Glutamát γ-aminobutyrát Neurotransmiter (GABA) Histidin Histamin Mediátor, neurotransmiter Dopamin Neurotransmiter 5 -hydroxytryptofan Serotonin Mediátor, neurotransmiter
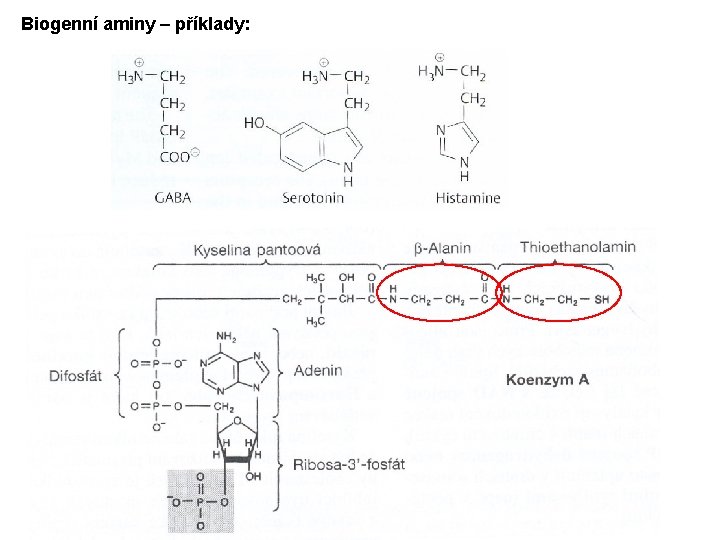
Biogenní aminy – příklady:
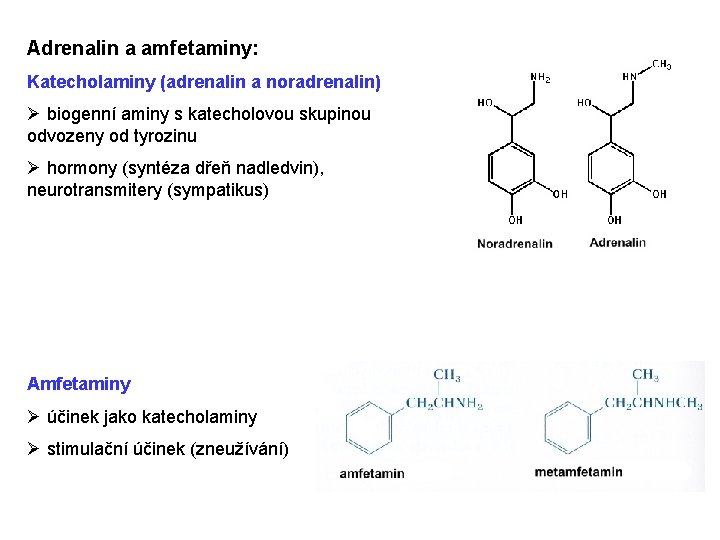
Adrenalin a amfetaminy: Katecholaminy (adrenalin a noradrenalin) Ø biogenní aminy s katecholovou skupinou odvozeny od tyrozinu Ø hormony (syntéza dřeň nadledvin), neurotransmitery (sympatikus) Amfetaminy Ø účinek jako katecholaminy Ø stimulační účinek (zneužívání)
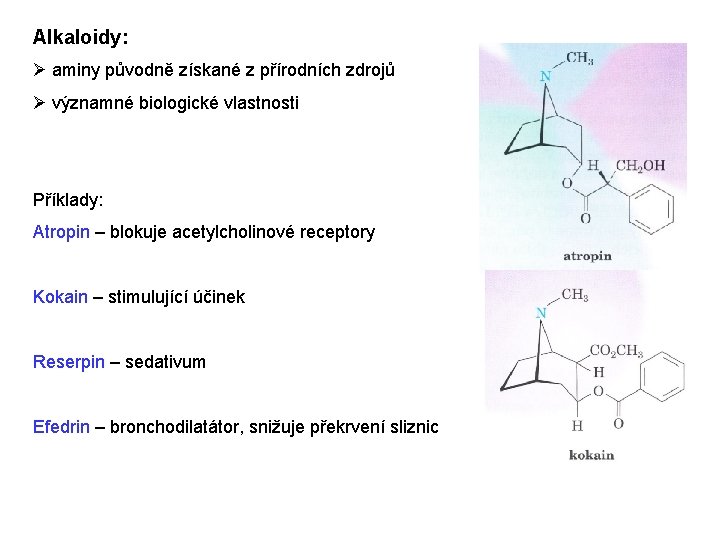
Alkaloidy: Ø aminy původně získané z přírodních zdrojů Ø významné biologické vlastnosti Příklady: Atropin – blokuje acetylcholinové receptory Kokain – stimulující účinek Reserpin – sedativum Efedrin – bronchodilatátor, snižuje překrvení sliznic
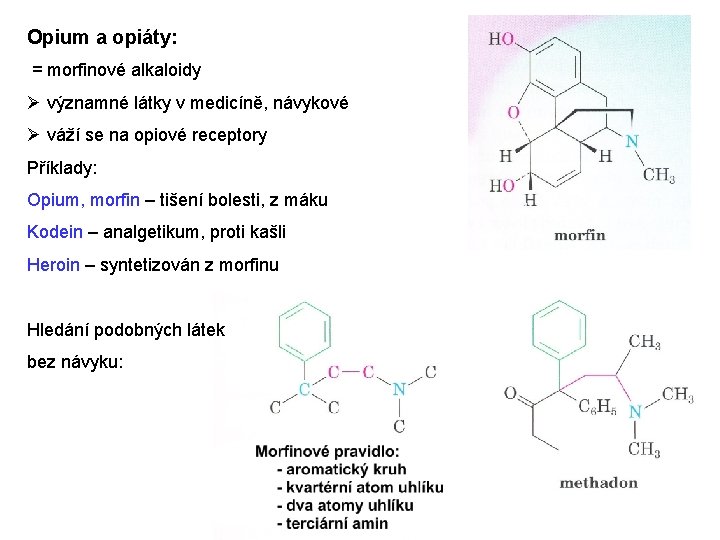
Opium a opiáty: = morfinové alkaloidy Ø významné látky v medicíně, návykové Ø váží se na opiové receptory Příklady: Opium, morfin – tišení bolesti, z máku Kodein – analgetikum, proti kašli Heroin – syntetizován z morfinu Hledání podobných látek bez návyku:
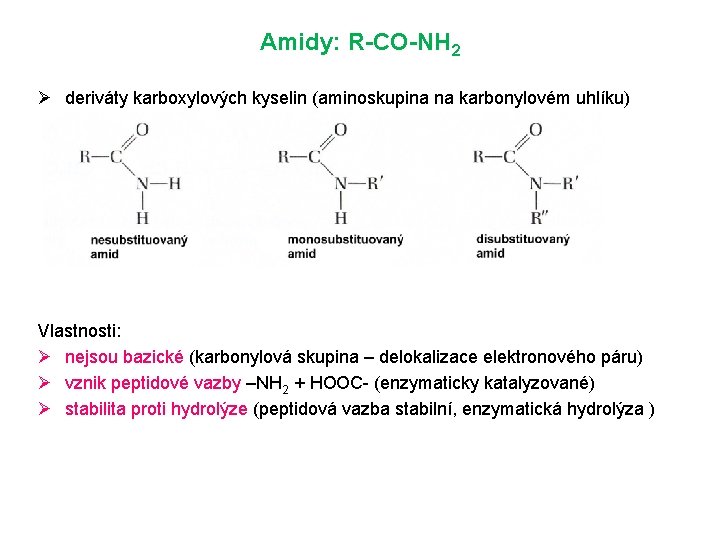
Amidy: R-CO-NH 2 Ø deriváty karboxylových kyselin (aminoskupina na karbonylovém uhlíku) Vlastnosti: Ø nejsou bazické (karbonylová skupina – delokalizace elektronového páru) Ø vznik peptidové vazby –NH 2 + HOOC- (enzymaticky katalyzované) Ø stabilita proti hydrolýze (peptidová vazba stabilní, enzymatická hydrolýza )
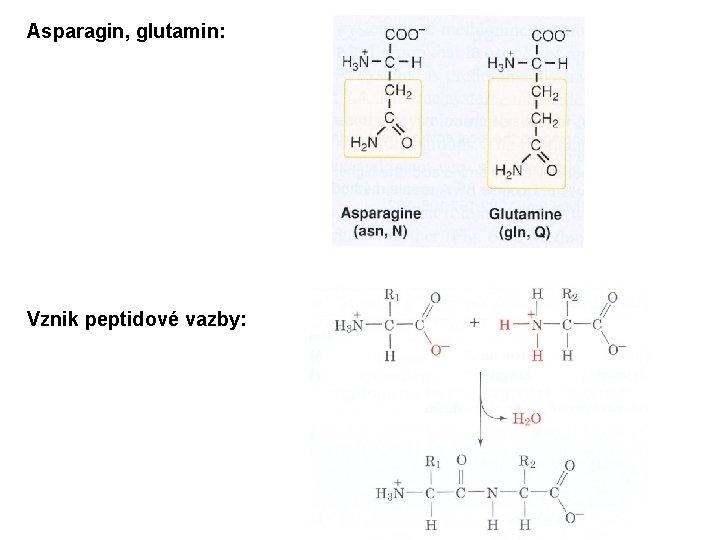
Asparagin, glutamin: Vznik peptidové vazby:
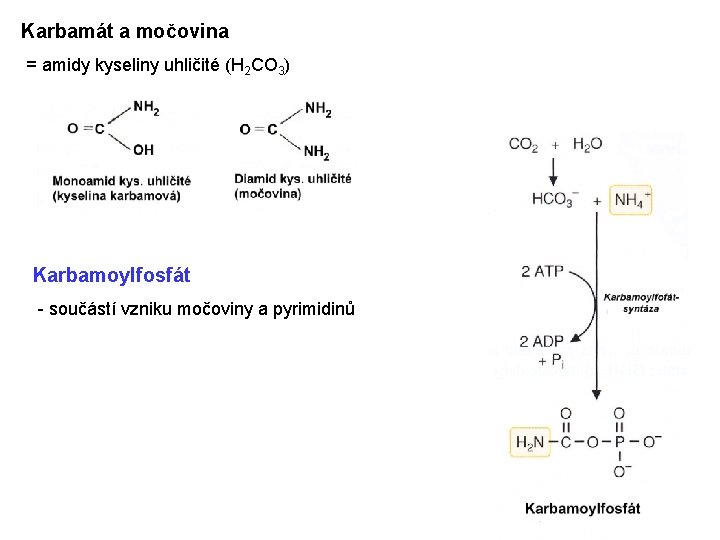
Karbamát a močovina = amidy kyseliny uhličité (H 2 CO 3) Karbamoylfosfát - součástí vzniku močoviny a pyrimidinů
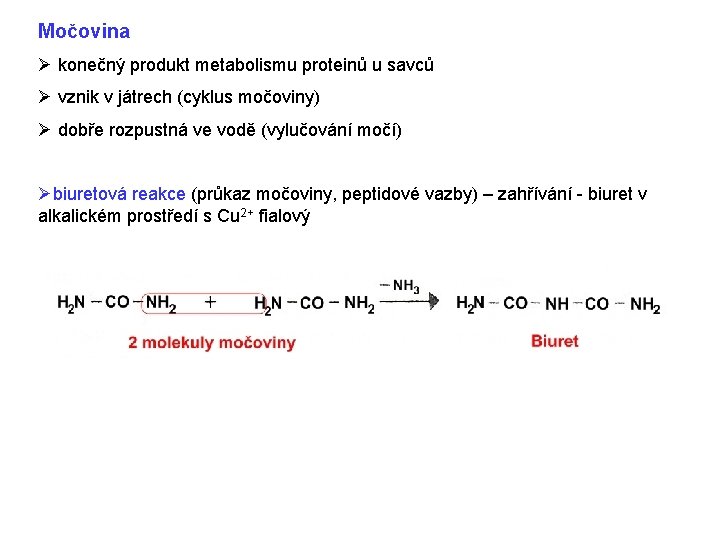
Močovina Ø konečný produkt metabolismu proteinů u savců Ø vznik v játrech (cyklus močoviny) Ø dobře rozpustná ve vodě (vylučování močí) Øbiuretová reakce (průkaz močoviny, peptidové vazby) – zahřívání - biuret v alkalickém prostředí s Cu 2+ fialový
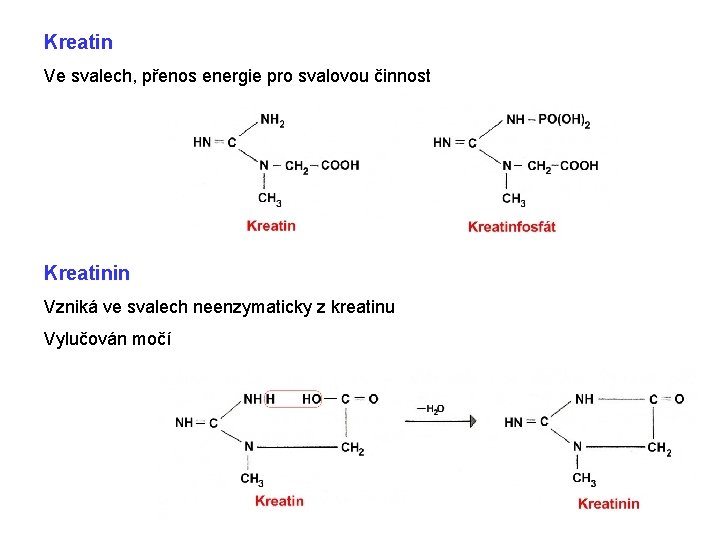
Kreatin Ve svalech, přenos energie pro svalovou činnost Kreatinin Vzniká ve svalech neenzymaticky z kreatinu Vylučován močí
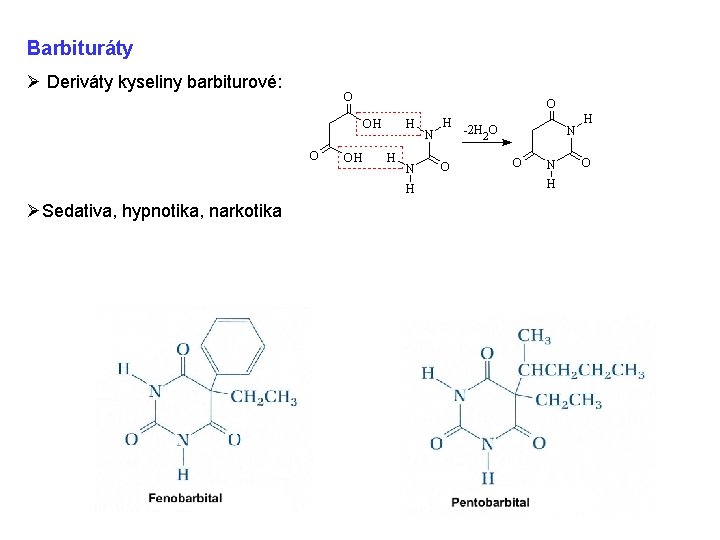
Barbituráty Ø Deriváty kyseliny barbiturové: ØSedativa, hypnotika, narkotika
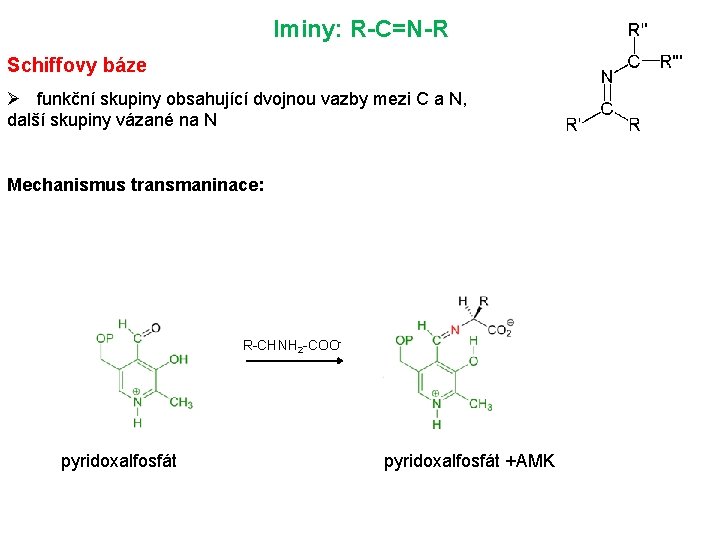
Iminy: R-C=N-R Schiffovy báze Ø funkční skupiny obsahující dvojnou vazby mezi C a N, další skupiny vázané na N Mechanismus transmaninace: R-CHNH 2 -COO- pyridoxalfosfát +AMK

Organické sloučeniny obsahující síru
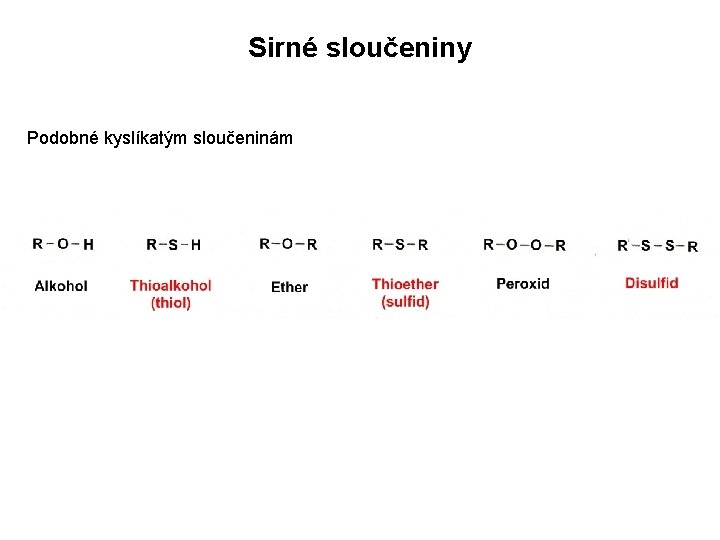
Sirné sloučeniny Podobné kyslíkatým sloučeninám
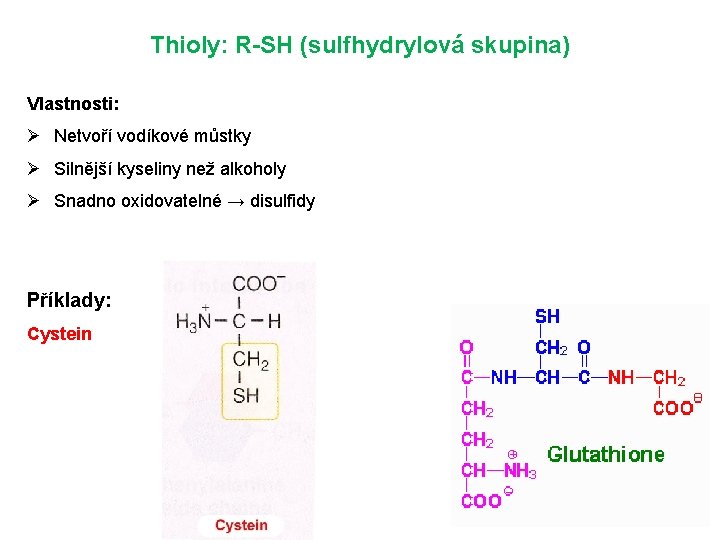
Thioly: R-SH (sulfhydrylová skupina) Vlastnosti: Ø Netvoří vodíkové můstky Ø Silnější kyseliny než alkoholy Ø Snadno oxidovatelné → disulfidy Příklady: Cystein
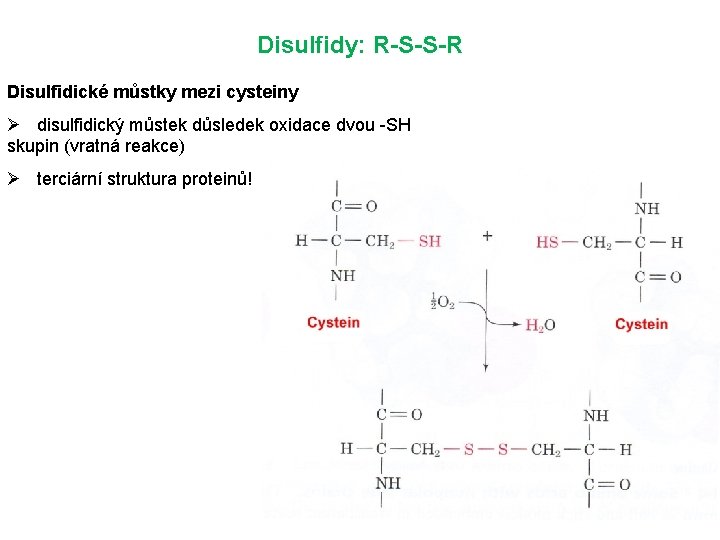
Disulfidy: R-S-S-R Disulfidické můstky mezi cysteiny Ø disulfidický můstek důsledek oxidace dvou -SH skupin (vratná reakce) Ø terciární struktura proteinů!
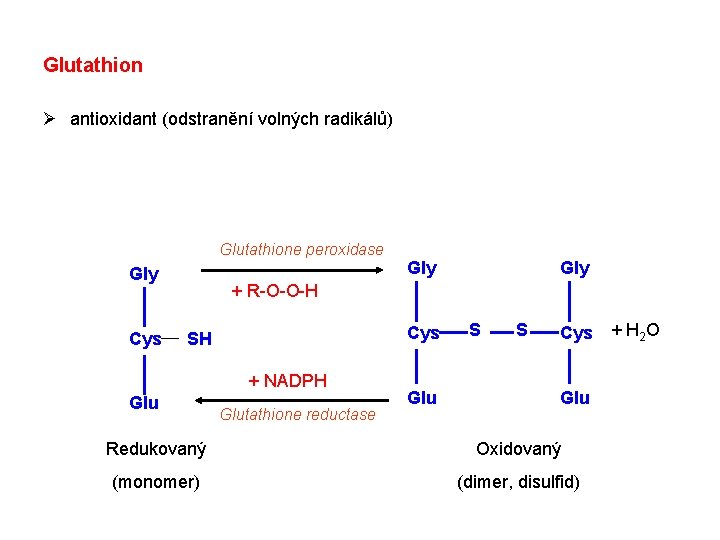
Glutathion Ø antioxidant (odstranění volných radikálů) Glutathione peroxidase Gly Cys Gly + R-O-O-H Cys SH + NADPH Glutathione reductase Glu S S Cys + H 2 O Glu Redukovaný Oxidovaný (monomer) (dimer, disulfid)
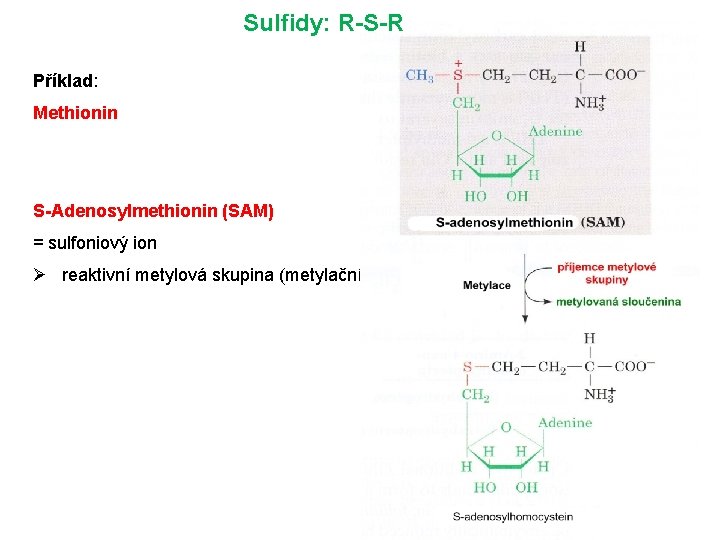
Sulfidy: R-S-R Příklad: Methionin S-Adenosylmethionin (SAM) = sulfoniový ion Ø reaktivní metylová skupina (metylační agens)!
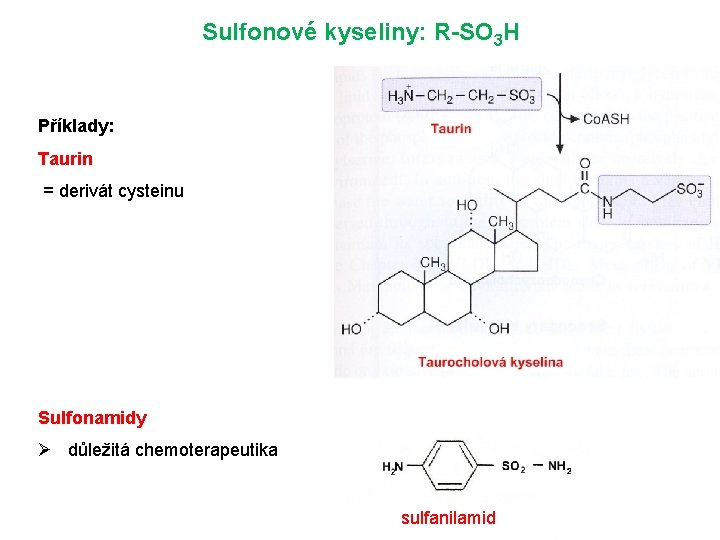
Sulfonové kyseliny: R-SO 3 H Příklady: Taurin = derivát cysteinu Sulfonamidy Ø důležitá chemoterapeutika sulfanilamid

Biologicky významné heterocykly
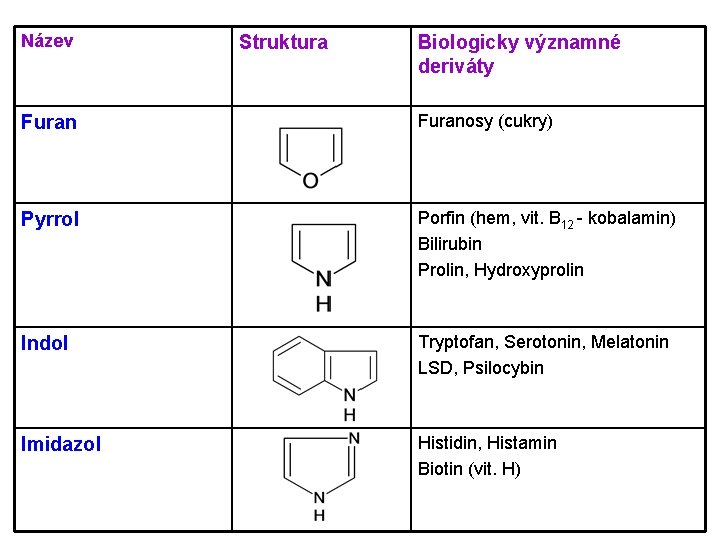
Název Struktura Biologicky významné deriváty Furanosy (cukry) Pyrrol Porfin (hem, vit. B 12 - kobalamin) Bilirubin Prolin, Hydroxyprolin Indol Tryptofan, Serotonin, Melatonin LSD, Psilocybin Imidazol Histidin, Histamin Biotin (vit. H)
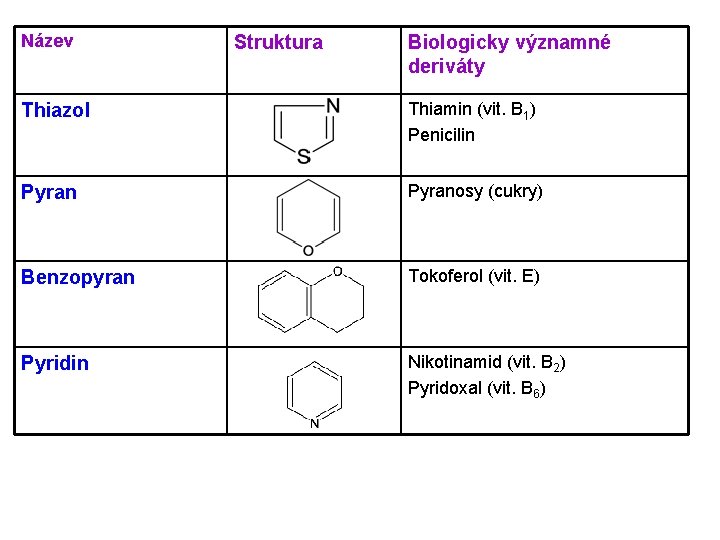
Název Struktura Biologicky významné deriváty Thiazol Thiamin (vit. B 1) Penicilin Pyranosy (cukry) Benzopyran Tokoferol (vit. E) Pyridin Nikotinamid (vit. B 2) Pyridoxal (vit. B 6)
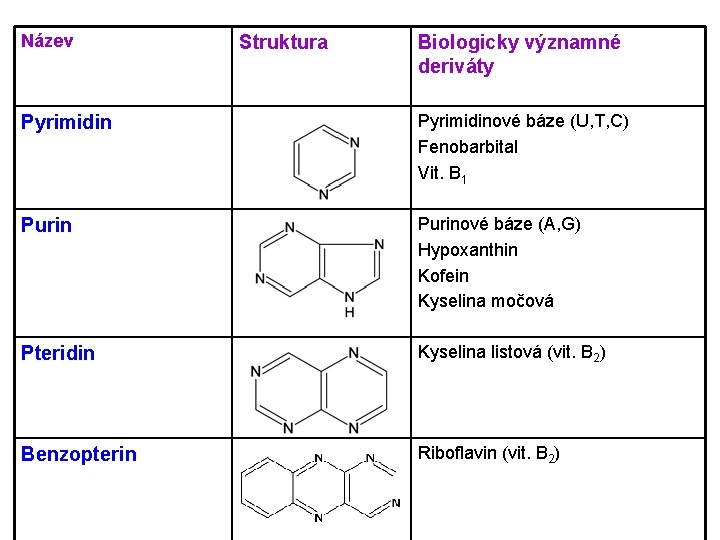
Název Struktura Biologicky významné deriváty Pyrimidinové báze (U, T, C) Fenobarbital Vit. B 1 Purinové báze (A, G) Hypoxanthin Kofein Kyselina močová Pteridin Kyselina listová (vit. B 2) Benzopterin Riboflavin (vit. B 2)
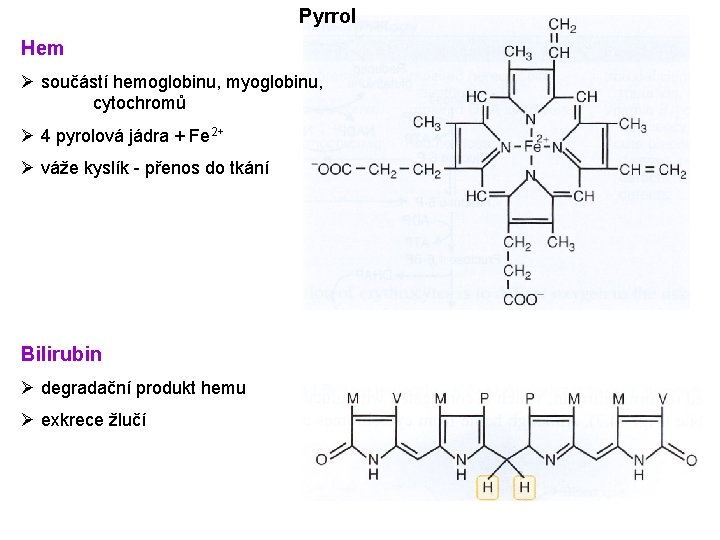
Pyrrol Hem Ø součástí hemoglobinu, myoglobinu, cytochromů Ø 4 pyrolová jádra + Fe 2+ Ø váže kyslík - přenos do tkání Bilirubin Ø degradační produkt hemu Ø exkrece žlučí
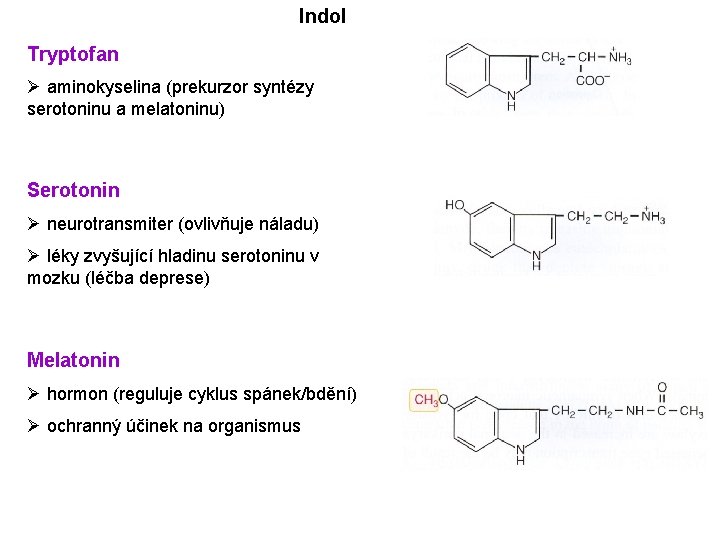
Indol Tryptofan Ø aminokyselina (prekurzor syntézy serotoninu a melatoninu) Serotonin Ø neurotransmiter (ovlivňuje náladu) Ø léky zvyšující hladinu serotoninu v mozku (léčba deprese) Melatonin Ø hormon (reguluje cyklus spánek/bdění) Ø ochranný účinek na organismus
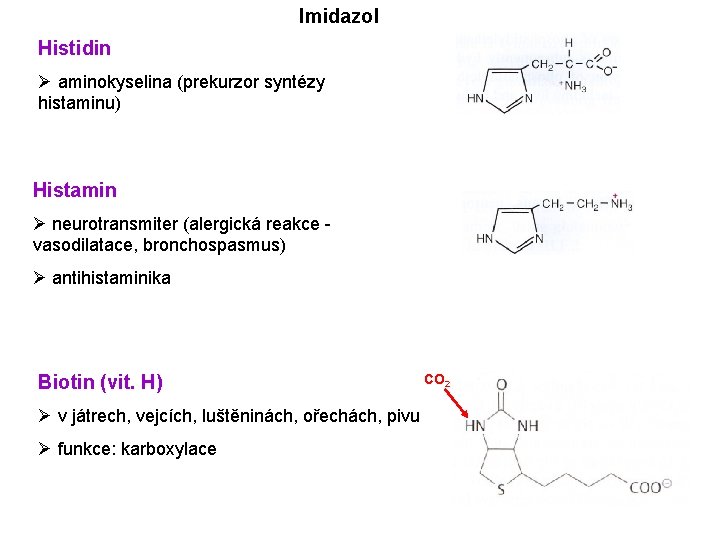
Imidazol Histidin Ø aminokyselina (prekurzor syntézy histaminu) Histamin Ø neurotransmiter (alergická reakce vasodilatace, bronchospasmus) Ø antihistaminika Biotin (vit. H) Ø v játrech, vejcích, luštěninách, ořechách, pivu Ø funkce: karboxylace CO 2
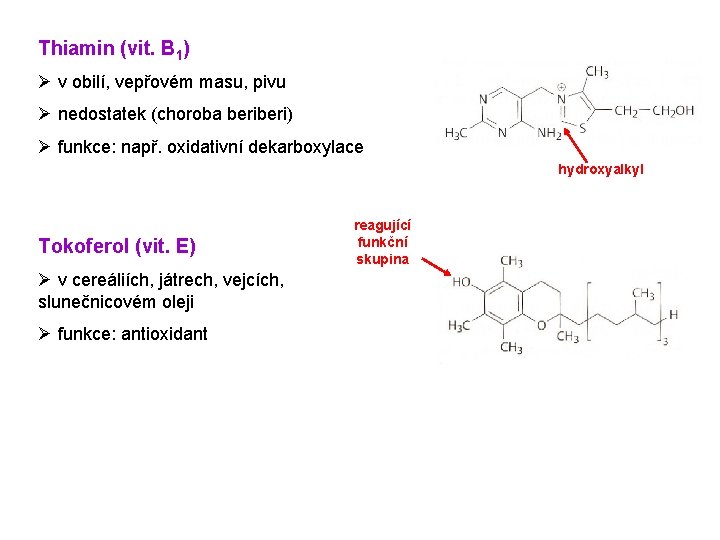
Thiamin (vit. B 1) Ø v obilí, vepřovém masu, pivu Ø nedostatek (choroba beri) Ø funkce: např. oxidativní dekarboxylace hydroxyalkyl Tokoferol (vit. E) Ø v cereáliích, játrech, vejcích, slunečnicovém oleji Ø funkce: antioxidant reagující funkční skupina
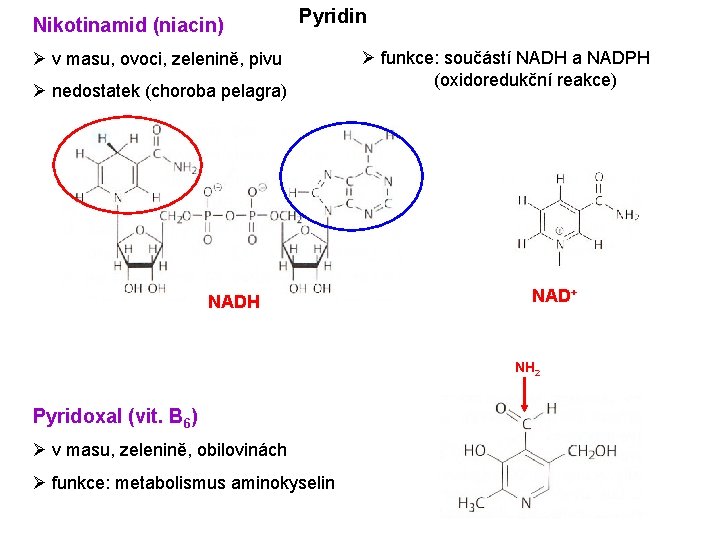
Nikotinamid (niacin) Pyridin Ø v masu, ovoci, zelenině, pivu Ø nedostatek (choroba pelagra) NADH Ø funkce: součástí NADH a NADPH (oxidoredukční reakce) NAD+ NH 2 Pyridoxal (vit. B 6) Ø v masu, zelenině, obilovinách Ø funkce: metabolismus aminokyselin
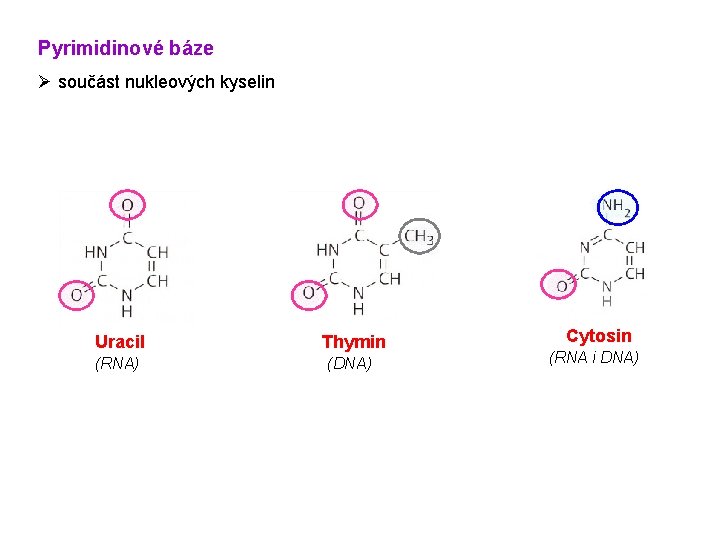
Pyrimidinové báze Ø součást nukleových kyselin Uracil Thymin (RNA) (DNA) Cytosin (RNA i DNA)
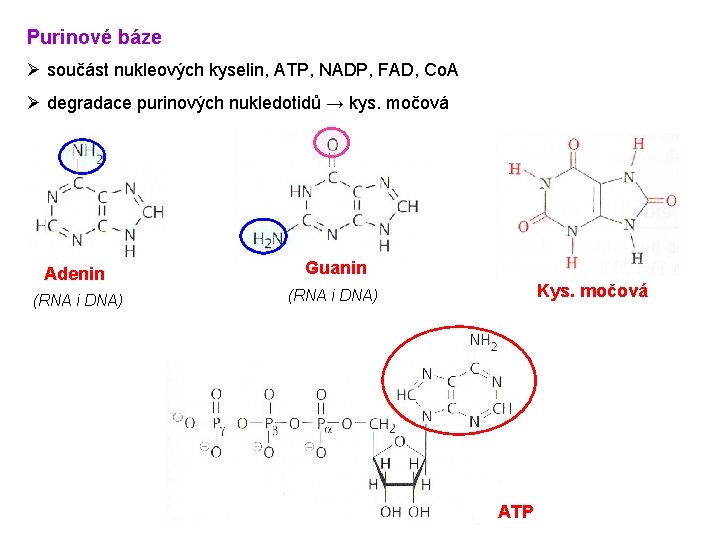
Purinové báze Ø součást nukleových kyselin, ATP, NADP, FAD, Co. A Ø degradace purinových nukledotidů → kys. močová Adenin Guanin (RNA i DNA) Kys. močová ATP
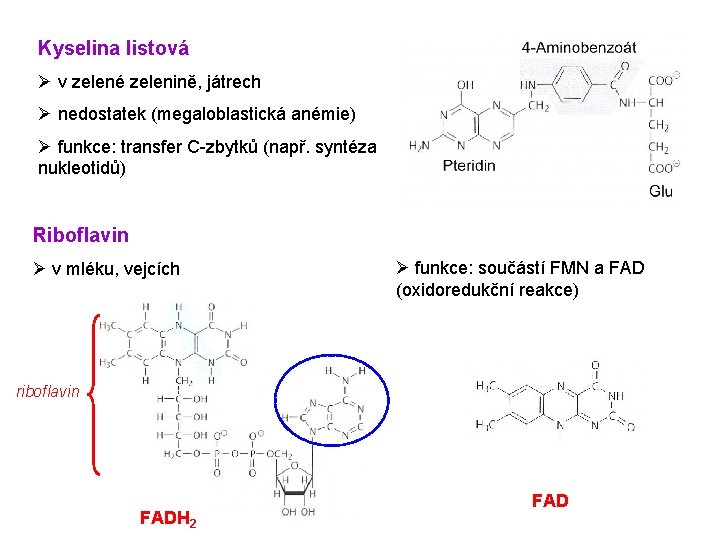
Kyselina listová Ø v zelené zelenině, játrech Ø nedostatek (megaloblastická anémie) Ø funkce: transfer C-zbytků (např. syntéza nukleotidů) Riboflavin Ø v mléku, vejcích Ø funkce: součástí FMN a FAD (oxidoredukční reakce) riboflavin FADH 2 FAD

Děkuji za pozornost
- Slides: 70